Синдром швахмана даймонда по мкб 10
Содержание
- Описание
- Дополнительные факты
- Причины
- Симптомы
- Диагностика
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: Синдром Швахмана-Даймонда.
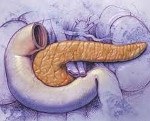
Синдром Швахмана-Даймонда
Описание
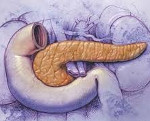
Синдром Швахмана. Даймонда — это генетическая патология, проявляющаяся секреторной недостаточностью поджелудочной железы, костномозговыми нарушениями и серьезными гематологическими изменениями. Первые симптомы (диарея, метеоризм, снижение аппетита, дистрофия, деформация скелета, анемия ) регистрируются на 5-6 месяце во время введения прикорма. Основные диагностические мероприятия: биохимический и общий анализ крови и кала, гормональные исследования, УЗИ, КТ и МРТ органов брюшной полости, рентгенография скелета. Лечение направлено на устранение клинических признаков и поддержание жизнедеятельности.
Дополнительные факты
Синдром Швахмана-Даймонда – редкое генетическое заболевание, для которого характерны нарушение работы поджелудочной железы и дисфункция костного мозга. Болезнь проявляется всесторонней задержкой развития (умственного, психического и физического), отмечена повышенная восприимчивость к инфекциям. Распространенность заболевания составляет 1:50 000 рожденных детей. Синдром несколько чаще встречается у мальчиков. Прогноз крайне неблагоприятный, так как большинство пациентов не доживают до 7 лет.
Впервые патология была описана Bodian и Sheldon в 1964 году у пациентов с врожденной гипоплазией поджелудочной железы, задержкой роста и панцитопенией. В том же году Швахмоном и Даймондом была детально изучена экзокринная панкреатическая недостаточность и дисфункция костного мозга при данном заболевании. Многообразие проявлений синдрома требует согласованного междисциплинарного подхода к лечению патологии с участием специалистов в области гастроэнтерологии, генетики, педиатрии.
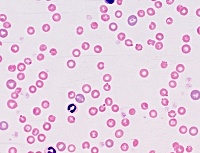
Синдром Швахмана-Даймонда
Причины
Причиной развития синдрома Швахмана-Даймонда является генетическая аномалия. Патология вызвана мутацией одного из участков 7 хромосомы (ген SBDS), она наследуется по аутосомно-рецессивному типу, то есть оба родителя должны передать дефектный ген своему ребенку. Регистрируются и спорадические случаи синдрома Швахмана-Даймонда – в их этиологии важную роль отводят воздействию вирусов паротита и Коксаки на ткани эмбриона. Клинические признаки начинают появляться на 5-6 месяц после рождения.
Хотя точная функция гена SBDS не определена, его мутация вызывает задержку развития; жировое перерождение ткани поджелудочной железы; гипоплазию костного мозга, которая приводит к серьезным гематологическим изменениям.
Симптомы
Клинические признаки синдрома Швахмана-Даймонда появляются после начала введения прикорма (5-6 месяцев). Первый симптом патологии – диарея, а точнее, стеаторея, для которой характерно значительное увеличение доли жира в каловых массах. На фоне нарушения стула снижается аппетит, появляется метеоризм. Эти признаки обусловлены недостаточностью секреторной функции поджелудочной железы. Помимо этого, выявляются и другие эндокринные нарушения, результатом которых является развитие субнанизма – низкорослости. Постепенно развивается дистрофия костной ткани, задерживается физическое и психическое развитие ребенка. У большинства пациентов регистрируется деформация костей, сопровождающаяся беспричинными переломами.
С первого дня жизни ребенка определяется измененная картина крови: снижается количество нейтрофилов (нейтропения), резко сокращается число эритроцитов (анемия) и тромбоцитов (тромбоцитопения), все это сочетается с геморрагическим синдромом (повышенная кровоточивость на фоне нарушения свертываемости). Пациенты подвержены развитию инфекционных заболеваний различных систем организма (органов дыхания, мочевыделительной системы, кожи и пр. ).
Метеоризм. Отсутствие аппетита. Понос (диарея).
Диагностика
Диагностика синдрома Швахмана-Даймонда не представляет трудностей, заподозрить наличие патологии может педиатр при проведении профилактического осмотра и появлении характерных симптомов. Врач тщательно собирает анамнез, выявляет хронические заболевания, а также случаи возникновения синдрома у ближайших родственников. Так как первые признаки связаны с диспепсическими нарушениями, то патологию может заподозрить и гастроэнтеролог.
Чтобы поставить окончательный диагноз, необходимо провести инструментальные и лабораторные методы обследования: анализ кала и крови, гормональные исследования, КТ, МРТ, УЗИ органов брюшной полости, рентгенографию скелета.
Анализ каловых масс выявляет стеаторею, общий анализ крови — нейтропению, тромбоцитопению, анемию, иногда панцитопению – снижение количества всех клеток крови. Биохимический анализ крови показывает состояние обменных процессов, а также концентрацию и свойства ферментов.
КТ, МРТ, УЗИ органов брюшной полости выявляют изменение ткани поджелудочной железы, эти исследования проводят также для исключения других болезней пищеварительной системы. Рентгенография костей определяет степень деформации скелета. После подтверждения диагноза всем пациентам назначается консультация невролога и генетика.
Лечение
Лечение синдрома Швахмана-Даймонда направлено на устранение неблагоприятных симптомов и поддержание жизненно важных функций. Всем пациентам прописывают строгую диету: ограничивают жиры, повышают содержание белков. Обязательна заместительная терапия, восполняющая недостающие ферменты поджелудочной железы. При появлении инфекционных заболеваний выписывают антибактериальные препараты. Также необходимо восстановить показатели картины крови; анемия успешно поддается терапии, другие изменения трудно корректируются. Если развивается тяжелая форма патологии и серьезные гематологические нарушения, проводят химио- и лучевую терапию, трансплантацию костного мозга.
Прогноз синдрома Швахмана-Даймонда крайне неблагоприятный. Согласно статистике, пациенты умирают в 7-10 лет, очень редко они доживают до 20 лет. Это связано с сильным снижением иммунитета и развитием серьезных инфекционных заболеваний. В редких случаях характер течения патологии меняется в сторону улучшения, как правило, постепенно уменьшается секреторная недостаточность, но при этом гематологические нарушения не восстанавливаются.
Основные медуслуги по стандартам лечения | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник

Синдром Швахмана-Даймонда – это генетическая патология, проявляющаяся секреторной недостаточностью поджелудочной железы, костномозговыми нарушениями и серьезными гематологическими изменениями. Первые симптомы (диарея, метеоризм, снижение аппетита, дистрофия, деформация скелета, анемия и т. п.) регистрируются на 5-6 месяце во время введения прикорма. Основные диагностические мероприятия: биохимический и общий анализ крови и кала, гормональные исследования, УЗИ, КТ и МРТ органов брюшной полости, рентгенография скелета. Лечение направлено на устранение клинических признаков и поддержание жизнедеятельности.
Общие сведения
Синдром Швахмана-Даймонда – редкое генетическое заболевание, для которого характерны нарушение работы поджелудочной железы и дисфункция костного мозга. Болезнь проявляется всесторонней задержкой развития (умственного, психического и физического), отмечена повышенная восприимчивость к инфекциям. Распространенность заболевания составляет 1:50 000 рожденных детей. Синдром несколько чаще встречается у мальчиков. Прогноз крайне неблагоприятный, так как большинство пациентов не доживают до 7 лет.
Впервые патология была описана Bodian и Sheldon в 1964 году у пациентов с врожденной гипоплазией поджелудочной железы, задержкой роста и панцитопенией. В том же году Швахмоном и Даймондом была детально изучена экзокринная панкреатическая недостаточность и дисфункция костного мозга при данном заболевании. Многообразие проявлений синдрома требует согласованного междисциплинарного подхода к лечению патологии с участием специалистов в области гастроэнтерологии, генетики, педиатрии.
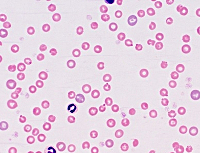
Синдром Швахмана-Даймонда
Причины синдрома Швахмана-Даймонда
Причиной развития синдрома Швахмана-Даймонда является генетическая аномалия. Патология вызвана мутацией одного из участков 7 хромосомы (ген SBDS), она наследуется по аутосомно-рецессивному типу, то есть оба родителя должны передать дефектный ген своему ребенку. Регистрируются и спорадические случаи синдрома Швахмана-Даймонда – в их этиологии важную роль отводят воздействию вирусов паротита и Коксаки на ткани эмбриона. Клинические признаки начинают появляться на 5-6 месяц после рождения.
Хотя точная функция гена SBDS не определена, его мутация вызывает задержку развития; жировое перерождение ткани поджелудочной железы; гипоплазию костного мозга, которая приводит к серьезным гематологическим изменениям.
Симптомы синдрома Швахмана-Даймонда
Клинические признаки синдрома Швахмана-Даймонда появляются после начала введения прикорма (5-6 месяцев). Первый симптом патологии – диарея, а точнее, стеаторея, для которой характерно значительное увеличение доли жира в каловых массах. На фоне нарушения стула снижается аппетит, появляется метеоризм. Эти признаки обусловлены недостаточностью секреторной функции поджелудочной железы. Помимо этого, выявляются и другие эндокринные нарушения, результатом которых является развитие субнанизма – низкорослости. Постепенно развивается дистрофия костной ткани, задерживается физическое и психическое развитие ребенка. У большинства пациентов регистрируется деформация костей, сопровождающаяся беспричинными переломами.
С первого дня жизни ребенка определяется измененная картина крови: снижается количество нейтрофилов (нейтропения), резко сокращается число эритроцитов (анемия) и тромбоцитов (тромбоцитопения), все это сочетается с геморрагическим синдромом (повышенная кровоточивость на фоне нарушения свертываемости). Пациенты подвержены развитию инфекционных заболеваний различных систем организма (органов дыхания, мочевыделительной системы, кожи и пр.).
При легкой форме симптомы, характерные для заболевания, не ярко выражены, при адекватной терапии такие пациенты доживают до 20 лет. При тяжелой форме клинические признаки рано появляются и быстро прогрессируют, любые терапевтические мероприятия не дают положительного эффекта, эти больные погибают очень рано.
Диагностика синдрома Швахмана-Даймонда
Диагностика синдрома Швахмана-Даймонда не представляет трудностей, заподозрить наличие патологии может педиатр при проведении профилактического осмотра и появлении характерных симптомов. Врач тщательно собирает анамнез, выявляет хронические заболевания, а также случаи возникновения синдрома у ближайших родственников. Так как первые признаки связаны с диспепсическими нарушениями, то патологию может заподозрить и гастроэнтеролог.
Чтобы поставить окончательный диагноз, необходимо провести инструментальные и лабораторные методы обследования: анализ кала и крови, гормональные исследования, КТ, МРТ, УЗИ органов брюшной полости, рентгенографию скелета.
Анализ каловых масс выявляет стеаторею, общий анализ крови — нейтропению, тромбоцитопению, анемию, иногда панцитопению – снижение количества всех клеток крови. Биохимический анализ крови показывает состояние обменных процессов, а также концентрацию и свойства ферментов.
КТ, МРТ, УЗИ органов брюшной полости выявляют изменение ткани поджелудочной железы, эти исследования проводят также для исключения других болезней пищеварительной системы. Рентгенография костей определяет степень деформации скелета. После подтверждения диагноза всем пациентам назначается консультация невролога и генетика.
Лечение синдрома Швахмана-Даймонда
Лечение синдрома Швахмана-Даймонда направлено на устранение неблагоприятных симптомов и поддержание жизненно важных функций. Всем пациентам прописывают строгую диету: ограничивают жиры, повышают содержание белков. Обязательна заместительная терапия, восполняющая недостающие ферменты поджелудочной железы. При появлении инфекционных заболеваний выписывают антибактериальные препараты. Также необходимо восстановить показатели картины крови; анемия успешно поддается терапии, другие изменения трудно корректируются. Если развивается тяжелая форма патологии и серьезные гематологические нарушения, проводят химио- и лучевую терапию, трансплантацию костного мозга.
Прогноз синдрома Швахмана-Даймонда крайне неблагоприятный. Согласно статистике, пациенты умирают в 7-10 лет, очень редко они доживают до 20 лет. Это связано с сильным снижением иммунитета и развитием серьезных инфекционных заболеваний. В редких случаях характер течения патологии меняется в сторону улучшения, как правило, постепенно уменьшается секреторная недостаточность, но при этом гематологические нарушения не восстанавливаются.
Источник
Рубрика МКБ-10: D61.0
МКБ-10 / D50-D89 КЛАСС III Болезни крови, кроветворных органов и отдельные нарушения, вовлекающие иммунный механизм / D60-D64 Апластические и другие анемии / D61 Другие апластические анемии
Определение и общие сведения[править]
Анемия Фанкони
Синонимы: панцитопения Фанкони
Анемия Фанкони — является наследственным нарушением репарации ДНК, характеризуется прогрессирующей панцитопенией с недостаточностью костного мозга, разнообразными врожденными пороками развития и предрасположенность к развитию гематологических или солидных опухолей.
Последние определение несущей частоты дали оценку более чем 1/200, с ожидаемой распространенности при рождении, по крайней мере, 1 / 160,000. В некоторых популяциях, несущая частота значительно выше, из-за мутации-основателей. Более 2000 случаев заболевания сообщались в литературе.
Анемия Фанкони, как правило, аутосомно-рецессивное заболевание, но может произойти и Х-сцепленная передача.
Этиология и патогенез[править]
Анемия Фанкони происходит из-за мутаций в генах, участвующих в репарации ДНК и геномной стабильности. Пятнадцать генов, представляющих 15 комплементационных групп были идентифицированы на сегодняшний день.
Клинические проявления[править]
У 2/3 больных, первые признаки анемии Фанкони — врожденные пороки развития, которые могут затрагивать скелет, кожу, мочеполовую и сердечно-легочную сферу, желудочно-кишечный тракт и центральную нервную систему. Аномалии конечностей могут быть односторонними или двусторонними, причем в последнем случае часто асимметричными. Также могут присутствовать низкий рост и вес, микроцефалия и/или микрофтальм. Нередки пигментация кожи и гипоплазия основания большого пальца (возвышения тенара). Почти 20% пациентов имеют пороки развития уха с или без потери слуха. Врожденные пороки развития могут варьироваться в семье. Если врожденные пороки развития не манифестированы, постановка диагноза может быть отложена до наступления отказа костного мозга (BMF), которое происходит в среднем возрасте до 7 лет. Гематологические нарушения могут возникать в более молодом возрасте, реже у взрослых, при этом 90% пациентов отказ костного мозга развивается в возрасте до 40 лет. У пациентов может развиться острый миелоидный лейкоз, которому часто предшествует миелодиспластический синдром. Пациенты также высоко предрасположены к образованию солидных опухолей головы, шеи и аногенитальной области. Маленький рост часто обусловлен гормональными дефектами. Фертильность полность нарушена у мужчин и сильно нарушается у половине женщин. Беременность часто осложняется.
Конституциональная апластическая анемия: Диагностика[править]
Анемию Фанкони можно заподозрить при панцитопении и характерных фенотипических проявлениях. Прогрессирующая апластическая анемия обычно развивается в возрасте старше 1 года, в среднем — в возрасте 7 лет. Макроцитоз наблюдается еще до возникновения цитопении. При подозрении на анемию Фанкони необходим поиск сопутствующих аномалий развития. Диагноз подтверждают усиленным разрушением хромосом под действием диэпоксибутана, митомицина С или других веществ, повреждающих ДНК. Возможна пренатальная диагностика.
Дифференциальный диагноз[править]
Клинические проявления анемии Фальконе совпадают со многими нарушениями мальформации (Дубовица, Секеля, Холта-Орама, Баллера-Герольда, тромбоцитопения с отсутствуем радиальной кости, синдром неймегеновского повреждения, VACTERL ассоциация, врожденный дискератоз.
Диагностика анемии Фальконе более очевидна когда у пациента развивается отказ костного мозга или злокачественные опухоли. Анемию Фальконе следует рассматривать в дифференциальной диагностике всех молодых пациентов с отказом костного мозга неизвестной этиологии.
Следует также рассмотреть другие синдромы с предрасположенностью к новообразованиям (синдром Блума, Ротмунда-Томсона или синдром Вернера) или синдромы, сопровождающиеся панцитопенией (анемия Блекфана-Даймонда, иммунная панцитопения, синдром Пирсона или синдром Швахмана-Даймонда).
Конституциональная апластическая анемия: Лечение[править]
Поддерживающая терапия включает в себя переливание эритроцитов или очищенных тромбоцитов. Единственным средством для лечения гематологических проявлений является пересадка гемопоэтических стволовых клеток. Тем не менее, этот подход несет тенденцию к увеличению риска солидных опухолей. Симптоматическое лечение включает в себя пероральное введение андрогенов, что улучшает показатели крови у некоторых пациентов, в частности, кол-во эритроцитов. Назначение факторов роста кроветворения может быть рассмотрено после проведения аспирации и биопсии костного мозга, которые должны выполняться регулярно во время лечения.
Прогноз
Отказ костного мозга и злокачественные опухоли ухудшают прогноз, сокращая продолжительность жизни.
Профилактика[править]
Прочее[править]
Анемия Блекфена-Даймонда
Синонимы: синдром Аазе, врожденная аплазия эритроцитов, врожденная эритроцитарная аплазия, врожденная гипоплатическая анемия типа Блекфена-Даймонда
Определение и общие сведения
Анемия Блекфена-Даймонда является врожденной арегенеративной и часто макроцитарной анемией с эритробластопенией.
Ежегодная заболеваемость в Европе по оценкам составляет около 1 / 150,000. Оба пола в равной степени подвержены заболеванию и ни в одной этнической группе не было выявлено предрасположенности к врожденной гипопластической анемии.
Анемия Блекфена-Даймонда наследуется как аутосомно-доминантный признак с переменной пенетрацией.
Этиология и патогенез
В настоящее время, вызывающие болезнь мутации выявляются у 40-45% пациентов. Все вовлеченные в патогенез анемии Блекфена-Даймонда гены кодируют белки рибосом, среди них есть как небольшие субъединицы (RPS7, RPS17, RPS19, RPS24 ), так и крупные (RPL5, RPL11, RPL35a). Мутации в RPS19, RPL5 и RPL11 наблюдаются у 25%, 9% и 6,5% пациентов соответственно, в то время как другие гены, отвественны за 1-3% случаев. Единственная очевидная корреляция генотип/фенотип — частые краниофациальные аномалии у носителей мутации RPL5 и RPL11 и наоборот эти аномалии редки у носителей мутации RPS19.
Клинические проявления
Анемия Блекфена-Даймонда обнаруживается в раннем возрасте, как правило, в течение первых 2-х лет жизни, возникновение анемии после 4-х лет очень маловероятно. Первые признаки заболевания — бледность и одышка, особенно во время кормления или во время сосания. Бледность, без органомегалии — признака, указывающего на гемолиз или вовлечением других гемопоэтических клеточных линий. Более половины всех пациентов демонстрируют низкий рост и врожденные аномалии, наиболее часто черепно-лицевые (синдром Пьера-Робина и расщепление нёба), большого пальца и урогенитального тракта. Беременность у женщин-носителей признака несет высокий риск, как для матери, так и для ребенка. Пациенты с анемией Блекфена-Даймонда также имеют более высокий риск лейкемии и новообразований.
Диагностика
У ребенка с анемией и эритробластопенией диагноз может быть поддержан семейной историей (10-20% случаев), сопутствующими пороками развития (40% случаев), а также повышенным уровнем эритроцитарной аденозиндезаминазой, который является частым, но неспецифическим признаком, поскольку также может быть повышена у родственников при отсутствии других симптомов заболевания. Обнаружение болезнетворной мутации имеет диагностическое значение.
Генетическое консультирование и пренатальная диагностика затруднена из-за изменчивости клинических проявлений и того факт, что только 40-45% пациентов имеют мутации в пределах гена RP. В семейных случаях, риск рецидива составляет 50%. Проводить ультразвуковое наблюдение во время беременности рекомендуется во всех случаях.
Дифференциальный диагноз
Дифференциальный диагноз должен включать в себя транзиторную эритробластопению, хронические инфекции парвовируса В19 и другие врожденные анемии.
Лечение
Регулярные переливания крови и долгосрочная терапия кортикостероидами. Лечение должно быть адаптировано к каждому случаю и в зависимости от возраста пациента. Стероиды не следует вводить в течение первого года жизни. Низкий рост, как в рамках синдрома так и из-за связанных с лечением осложнений (стероиды, гемохроматоз), является серьезной проблемой для таких пациентов. Аллогенная трансплантация костного мозга должны быть рассмотрена при резистентности к кортикостероидам, если доступен здоровый и HLA-идентичный сиб.
Прогноз
Прогноз, как правило, хороший. Тем не менее, осложнения лечения и более высокий уровень заболеваемости раком может привести к снижению продолжительности жизни. Тяжесть заболевания зависит от качества и реакции на лечение. Для пациентов, проходящих регулярные переливания, качество жизни явно не страдает.
Синдром Швахмана-Даймонда
Синонимы: недостаточность поджелудочной железы и дисфункция костного мозга, синдром Швахмана, синдром Швахмана-Бодиана-Даймонда
Определение и общие сведения
Синдром Швахмана-Даймонда является редким мультисистемным синдромом, который характеризуется хронической и обычно легкой нейтропенией, экзокринной недостаточностью поджелудочной железы со стеатореей, скелетной дисплазией с низким ростом и повышенным риском развития аплазии костного мозга или лейкозной трансформации.
Во всем мире распространенность оценивается примерно 1/350000 и распространенности при рождении на уровне около 1 / 200.000 живорожденных. Передача аутосомно-рецессивная.
Этиология и патогенез
Синдром Швахмана-Даймонда в 95% случаев вызывается мутаций гена SBDS (7q11.22), кодирующим белок рибосом, участвующий в биогенезе рибосом и других клеточных процессах.
Клинические проявления
Синдром Швахмана-Даймонда имеет переменную клиническую картину, даже внутри одной семьи. Как правило, он проявляется в младенчестве или раннем детстве. Наиболее распространенный симптом — интерметтирующая умеренная нейтропения, сопровождаемая развитием рецидивирующих инфекций. Умеренная анемия и тромбоцитопения также могут наблюдаться у пациентов. Экзокринная недостаточность панкреатической железы приводит к снижению прибавки массы тела, замедлении роста и хронической стеаторее. Участие со строны костной ткани характеризуется замедленным созреванием костей, дисплазией метафизов, впалой грудной клеткой и генерализованной остеопенией. Другие симптомы включают в себя экзему или ихтиоз кожи, аномалии зубнов и психомоторную заторможенность. Умеренный или тяжелый интеллектуальный дефицит (50% пациентов) вызывает трудности в обучении. Гематологические проявления могут быть осложнены аплазией костного мозга, острым миелолейкозом и миелодиспластическим синдромом. В неонатальном периоде патология обычно не наблюдается, но в некоторых случаях сообщалось о панцитопении, респираторным дистрессе и тяжелой спондилометафизарной дисплазии.
Диагностика
Диагноз основывается на клинических, лабораторных и рентгенологических исследованиях. Анализ крови демонстрирует наличие нейтропении (абсолютное количество нейтрофилов <1500 / мл), которая может сопровождаться от легкой до умеренной тромбоцитопенией, умеренной анемией и повышением фетального гемоглобина. Экзокринная недостаточность поджелудочной железы проявляется низкими уровнями поджелудочной изоамилазы и/или трипсиногена, низким уровнем фекальной эластазы в анализе кала, жировой дистрофией на МРТ (МРТ картина может быть нормальной до возраста 5 лет). Рентгенография позволяет обнаружить, как правило в возрасте после 5 лет, — аномалии метафизов и пластин роста. Мазок костного мозга выявляют различную степень с дисгранулопоэза или дисэритропоэза. Диагноз подтверждается с помощью генетического тестирования.
Дифференциальный диагноз
Дифференциальный диагноз включает муковисцидоз, синдром Пирсона, анемию Фанкони, синдром Йохансона-Близзарда, анемию Блекфана-Даймонда, целиакию и аутосомно-рецессивную тяжелую врожденную нейтропению вследствие дефицита G6PC3.
Лечение
Недостаточность поджелудочной железы требует назначения панкреатических ферментов и адаптированной диеты. Антибиотикопрофилактика терапия может быть достаточной, чтобы избежать инфекций; в противном случае, может быть предложен гранулоцитов колониестимулирующий фактор. Тяжелые гематологические осложнения требуют трансплантации гемопоэтических стволовых клеток. Хирургическое вмешательство может быть предложено для скелетных аномалий. Пациенты с трудностями в обучении требуют специальной образовательной поддержки.
Прогноз
Прогноз является переменным. Опасная для жизни осложнения включают аплазию костного мозга и лейкозную трансформацию, а иногда и вирусные инфекции. Около 1/3 пациентов имеют данные осложнение, некоторые из них могут быть успешно купированы трансплантацией костного мозга.
Врожденная амегакариоцитарная тромбоцитопения
Синонимы: врожденная амегакариоцитарная тромбоцитопеническая пурпура
Определение и общие сведения
Врожденная амегакариоцитарная тромбоцитопения является редким наследственным синдромом недостаточности костного мозга, характеризуется изолированным тяжелым уменьшением количества тромбоцитов и мегакариоцитов в первые годы жизни ребенка, которое позже развивается в недостаточность костного мозга с панцитопенией.
Точная распространенность неизвестна, менее чем 100 случаев описано в литературе. Кроме того, заболеваемость может быть недооценена из-за трудной диагностики заболевания. Наследование аутосомно-рецессивное.
Этиология и патогенез
Врожденная амегакариоцитарная тромбоцитопения происходит из-за мутаций в гене MPL (1p34), кодирующем рецептор (с-MPL) тромбопоэтина, экспрессирущий в плюрипотентных гемопоэтических стволовых клетках и в мегакариоцитах. Различные типы мутаций связаны с различными фенотипами патологии. Нонсенс-мутации приводят к полной потере функции рецептора тромбопоэтина — I тип, миссенс мутации ведут к остаточной функции рецептора — тип II. Случаи, без каких-либо дефектов в гене MPL рассматриваются как тип III.
Делеции 21q22 приводят к RUNX1 гаплонедостаточности — развивается вариант амегакариоцитарной тромбоцитопении с различными аномалиями: задержка роста, дефицит слуха, грыжи и трудности кормления.
Клинические проявления
Врожденная амегакариоцитарная тромбоцитопения проявляется с рождения, часто в первый день или, по крайней мере, в течение первого месяца жизни петехиями, пурпурой, желудочно-кишечными или внутричерепными кровоизлияниями, кровоизлияними в легких вследствие наличия изолированной тромбоцитопении и почти полным отсутствием мегакариоцитов в костном мозге. Тип I является тяжелой формой заболевания и характеризуется постоянно низким количеством тромбоцитов и раннем прогрессированием (как правило, в возрасте до 2-х лет) аплазии костного мозга, сопровождаемой панцитопенией. Тип II является более мягкой формой, которая проявляется транзиторным увеличением количества тромбоцитов, более 50×109/л, в течение первого года жизни или позже в возрасте 3-6 лет и не сопровождается развитием панцитопении.
Есть сообщения о случаях сопутствующих дефектов межпредсердной и межжелудочковой перегородок, гипоплазии головного мозга и мозжечка, а также замедления психомоторного развития.
Диагностика
Диагноз основывается на клинических признаках, тромбоцитопении (количество тромбоцитов ниже 50×109/л) с нормальным средним объемом тромбоцитов, значательном повышении уровня тромбопоэтина в сыворотке и отсутствии или малом количестве мегакариоцитов в аспирате костного мозга. Генетическое тестирование может подтвердить диагноз.
Дифференциальный диагноз
Дифференциальный диагноз проводят с идиопатической тромбоцитопенической пурпурой, на поздней стадии с апластической анемией, а также с анемией Фанкони, тромбоцитопенией с отсутствием лучевой кости и синдромом Вискота-Олдрича.
Лечение
Лечение поддерживающее, показаны переливания тромбоцитов. Трансплантация кроветворных стволовых клеток является единственной эффективной лечебной стратегией.
Прогноз
Прогноз неблагоприятный, трилинейная аплазия костного мозга происходит в течение первых лет жизни.
WT конечностно-кровяной синдром
Характеризуется гематологическими аномалиями (анемия Фанкони, лейкоз и лимфомы), которые часто обнаруживаются в детстве. Также присутствуют аномалии развития конечностей и кистей рук: расщепление или гипоплазия большого пальца, кожная синдактилия, дефекты локтевой и лучевой костей. Синдром был описан в нескольких семьях. Передача аутосомно-доминантная.
Синдром атаксии с панцитопенией
Синонимы: атаксия-панцитопения синдром, миелоцеребеллярный синдром
Синдром атаксии с панцитопенией характеризуется мозжечковой атаксией, различной гематологической цитопенией и предрасположенностью к недостаточности костного мозга и миелоидному лейкозу, иногда связан с моносомией 7 пары.
Вызвается миссенс мутацией гена SAMD9L. Наследование аутосомно-доминантное.
Источники (ссылки)[править]
https://www.orpha.net
Am J Hum Genet. 2016 Jun 2; 98(6): 1146–1158.
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
- Гидрокортизон
- Дексаметазон
- Метилпреднизолон
- Преднизолон
Источник
