Синдром с смита лемли опитца
Синдром Смита-Лемли-Опица (SLO) представляет собой нарушение обмена веществ, которое включает в себя несколько различных симптомов, таких как значительно медленный рост, характерные легкие признаки, микроцефалия (измерение головы меньше нормального), умственная отсталость, которая может быть легкой или умеренной, трудности в обучении и проблемы поведение.
Это также сопровождается пороками развития легких, сердца, почек, кишечника и даже половых органов. Кроме того, они могут представлять синдактилию или слияние некоторых пальцев или полидактилию; это означает, что у них более 5 пальцев на ноге или руке.
По-видимому, это связано с отсутствием фермента, который важен для метаболизма холестерина, который приобретается при генетическом наследовании аутосомно-рецессивного паттерна..
Тем не менее, такие проявления, кажется, сильно различаются в зависимости от тяжести заболевания даже в одной семье.
Этот синдром может встречаться в литературе под такими названиями, как: дефицит 7-дегидрохолестерин редуктазы, синдром RSH или синдром SLO.
Немного истории …
В 1964 году педиатры Дэвид Смит, Люк Лемли и Опитц Джон описали 3 пациентов мужского пола с микроцефалией и гипогенитализмом и определили это состояние как RSH по инициалам первоначальных фамилий этих пациентов..
Впоследствии название синдрома было изменено на фамилии первооткрывателей (SLO).
Примерно через 30 лет Tint et al. (1994) обнаружили у 5 пациентов с этим состоянием значительно более низкие концентрации холестерина в крови, но увеличение более чем в 1000 раз уровня 7-дегидрохолестерина. Они увидели, что это увеличение связано с отсутствием фермента, который должен преобразовывать 7-дегидрохолестерин в холестерин.
Позже был идентифицирован ген DHCR7, связанный с этим заболеванием, клонирование в 1998 году (Witsch-Baumgartner & Lanthaler, 2015).
статистика
Синдром Смита-Лемли-Опитца затрагивает приблизительно 1 на 20 000–60 000 живорождений во всем мире. Он действительно может быть унаследован от 1 из 1590 до 13 500 особей, но эта цифра не используется, потому что многие плоды с этим заболеванием умирают до своего рождения (Национальная организация по редким заболеваниям, 2016).
Что касается секса, то он одинаково влияет как на мужчин, так и на женщин, хотя его легче диагностировать у мужчин, поскольку пороки развития половых органов более заметны, чем у женщин. Кроме того, это, кажется, чаще встречается у людей европейского происхождения; особенно из стран, принадлежащих к центральной Европе, таких как Чехия или Словакия. Тем не менее, это очень редко в популяции Африки или Азии.
Причины синдрома Смита-Лемли-Опица
Синдром SLO появляется из-за мутаций в гене DHCR7, присутствующем в хромосоме 11, который отвечает за отправку заказов на производство фермента 7-дегидрохолестерин редуктазы. Это фермент, который модулирует выработку холестерина и будет отсутствовать или очень мало при этом синдроме, что приводит к недостаточной выработке холестерина, что будет препятствовать нормальному росту.
Это оказывает большое влияние, так как холестерин важен для организма. Он состоит из липида, похожего на жир, который получают в основном из продуктов животного происхождения, таких как яичные желтки, молочные продукты, мясо, птица и рыба.
Важно, чтобы эмбрион развивался без затруднений, выполняя важные функции, такие как вклад в структуру мембран клеток и миелина (вещества, которое покрывает клетки мозга). Он также служит для производства гормонов и пищеварительных кислот.
Недостаток фермента 7-дегидрохолестеринредуктазы вызывает накопление в организме компонентов, которые могут быть токсичными для холестерина. Таким образом, мы имеем, с одной стороны, низкий уровень холестерина и в то же время накопление веществ, которые могут быть токсичными для организма; вызывая отсутствие роста, умственную отсталость, физические уродства и проблемы во внутренних органах.
Однако с полной уверенностью не известно, как эти проблемы, связанные с холестерином, приводят к симптоматике синдрома Смита-Лемли-Опитца..
В настоящее время в гене DHCR7 обнаружено более 130 мутаций, связанных с синдромом, фактически существует база данных, которая включает все описанные случаи SLO с ее вариантами, фенотипами и генотипами..
Хотя существует так много возможных мутаций, большинство случаев относится к 5 наиболее частым, а остальные очень редки (Witsch-Baumgartner & Lanthaler, 2015).
Эти мутации в гене DHCR7 наследуются по аутосомно-рецессивному типу, это означает, что человек, представивший синдром, должен был унаследовать мутированный ген от двух родителей. Если вы получите его только от одного из родителей, вы не представите болезнь; но это может быть носитель и передать его в будущем.
Существует 25% риска того, что у двух родителей-носителей есть больной ребенок, в то время как риск того, что ребенок будет носителем, также будет составлять 50% при каждой беременности. С другой стороны, в 25% случаев он может родиться без этих генетических мутаций или быть носителем; все эти данные не зависят от пола ребенка (Национальная организация по редким заболеваниям, 2016 г.).
Имейте в виду, что вероятность рождения детей с генетическим рецессивным расстройством выше, если родители являются близкими родственниками (или родственниками), чем родители, у которых нет таких связей.
Какие симптомы это имеет??
Симптомы варьируются в зависимости от пострадавшего человека, в зависимости от количества холестерина, которое они могут производить.
По словам Хименеса Рамиреса и соавт. (2001), клинические характеристики охватывают несколько аспектов и могут быть очень разнообразными. Как правило, они находятся на лице, конечностях и половых органах; хотя они могут включать другие телесные системы.
Многие из пострадавших имеют типичные признаки аутизма, влияющие на социальное взаимодействие. Если состояние мягкое, можно увидеть только некоторые проблемы в обучении и поведении; но в наиболее серьезных случаях у человека могут быть серьезные нарушения интеллекта и физические отклонения, которые могут привести к смерти.
Есть симптомы, которые могут уже присутствовать с рождения человека, хотя мы будем включать те, которые встречаются на всех этапах жизни:
У более чем 50% пациентов:
— Недостаток физического развития наблюдается после рождения.
— Умственная отсталость (100%).
— Микроцефалия (90%).
— Синдактилия или слияние 2 или 3 пальцев (- Пальпебральный птоз, то есть опущенное верхнее веко (70%).
— Мочевой тракт расположен в отличном месте от нормального у мужчин, так как он может быть в нижней части головки, туловища или сочленении между мошонкой и половым членом. Присутствует в 70% случаев.
— Расщелина неба, которая проявляется в виде удлиненного отверстия в небе (50%).
— Очень маленькая челюсть или микрогнатия.
— Очень маленький язык (микроглоссия).
— Уши низкой имплантации.
— Короткий нос.
— Неполный спуск одного или обоих яичек.
— Гипотония или низкий мышечный тонус.
— Расстройства пищевого поведения.
— Поведенческие расстройства: антисоциальное, саморазрушительное и насильственное поведение. Аутистическое самостимуляционное поведение также проявляется как повторяющиеся движения баланса.
— аутизм.
От 10 до 50% случаев:
— Ранняя катаракта.
— Полидактилия или еще один палец после мизинца.
— Задержка роста в стадии плода.
— Двусмысленные гениталии.
— Пороки сердца.
— Мультикистозная почка.
— Отсутствие почки или обоих при рождении.
— Заболевания печени.
— Гиперплазия надпочечников
— Легочные аномалии.
— Избыточное потоотделение.
— Церебральные нарушения в структурах, расположенных по средней линии, такие как неполное развитие мозолистого тела, перегородки и червя мозжечка.
— Акроцианоз: кожная вазоконстрикция, которая вызывает синеватый цвет в руках и ногах.
— Эквиновар ног.
— Пилорический стеноз (15%)
— Болезнь Гиршпрунга, которая вызывает недостаточную моторику кишечника (15%)
— светочувствительность.
Другие симптомы:
— Ожирение или кома.
— Накопление жидкости в организме плода.
-Изменения в неврологическом развитии.
— Нейропсихиатрические проблемы, которые появляются чаще, когда они достигают зрелого возраста.
— Дыхательная недостаточность из-за проблем с легкими.
— Потеря слуха.
— Изменения в зрении, которые могут сопровождаться косоглазием.
— рвота.
— запор.
— конвульсии.
Как вы можете диагностировать?
Этот синдром возникает из зачатия, даже когда ребенок рождается, симптомы не очень четкие и более тонкие, чем в позднем детстве или в зрелом возрасте; особенно если они являются более легкими формами заболевания. По этой причине в нескольких случаях он обнаруживается поздно.
В любом случае, наиболее обычным является то, что это состояние уже подозревается вскоре после рождения из-за пороков развития, которые оно обычно представляет (Steiner, 2015).
По данным Национальной организации по редким заболеваниям (2016 г.), диагноз основывается на физических обследованиях и анализе крови, который определяет уровень холестерина. Важно, чтобы ребенка оценивали во всех возможных аспектах, связанных с заболеванием, таких как глаза, уши, сердце, скелетные мышцы, гениталии и желудочно-кишечные расстройства..
Что касается анализов крови, субъект с SLO будет иметь высокую концентрацию 7-дегидрохолестерина (7-DHC) в крови (предшественник, который должен трансформироваться ферментом 7-дегидрохолестеринредуктазой для получения холестерина), и очень высокие уровни. низкий уровень холестерина.
Он также может быть обнаружен до рождения с помощью ультразвукового или ультразвукового метода, устройства, которое использует звуковые волны для исследования внутренней части матки беременной женщины. С помощью этой техники можно наблюдать физические деформации этого синдрома.
Другим тестом является амниоцентез, который включает удаление небольшого образца амниотической жидкости (там, где развивается плод) для выявления генетических дефектов. Эту же информацию можно получить, взяв пробу ворсин хориона (CVS), извлекая образец ткани из плаценты..
С другой стороны, молекулярно-генетические тесты могут использоваться для пренатальной диагностики, чтобы наблюдать, есть ли мутации в гене DHCR7, и если это будет представлять болезнь или будет только носителем.
Как протекает заболевание??
К сожалению, большинство более тяжелых случаев SLO умирают вскоре после рождения. Если есть серьезная умственная неспособность, этим людям трудно развить независимую жизнь.
Однако при условии надлежащего медицинского обслуживания и правильного питания эти пациенты могут вести нормальный образ жизни..
Какие есть процедуры?
В настоящее время нет специального лечения синдрома Смита-Лемли-Опитца. Это связано с тем, что биохимическое происхождение заболевания сегодня не известно с абсолютной уверенностью, поскольку холестерин выполняет несколько сложных функций в обмене веществ..
Лечение SLO основано на специфических проблемах, которые встречаются у больного ребенка, и лучше вмешаться на ранней стадии..
Это может быть очень полезно для приема добавок холестерина или увеличения потребления холестерина через диету, чтобы улучшить уровень развития и уменьшить светочувствительность. Иногда в сочетании с желчными кислотами.
В случае непереносимости солнца этим пациентам рекомендуется использовать солнцезащитный крем, солнцезащитные очки и соответствующую одежду при выходе на улицу..
Было показано, что снабжение такими лекарственными средствами, как симвастатин, может снизить тяжесть заболевания. Хотя, поскольку клинический фенотип возникает при недостатке холестерина в эмбриогенезе, его необходимо вводить в это время (Witsch-Baumgartner & Lanthaler, 2015).
С другой стороны, препарат-антагонист токсического предшественника холестерина, который находится в избытке (7-дегидрохолестерин), также может быть использован для предотвращения его увеличения. Витамин Е добавки могут помочь.
Другие виды специфических лекарств могут быть полезны при таких симптомах, как рвота, гастроэзофагеальный рефлюкс или запор.
Операция или брекеты могут быть необходимы, если с этим синдромом связаны физические уродства или проблемы с мышцами, такие как расщелина нёба, пороки сердца, мышечная гипотония или генитальные изменения.
В заключение необходимо продолжить исследования этого синдрома, чтобы разработать более эффективные и специфические методы лечения..
ссылки
- Хименес Рамирес, А.; Вальдивия Альфаро, Р .; Эрнандес Гонсалес, Л .; Леон Корралес, L.; Machín Valero, Y. and Torrecilla, L. (2001). Синдром Смита Лемли Опица. Представление случая с биохимическим диагнозом. Медицинский вестник Эспиритуана, 3 (3).
- Синдром Смита Лемли Опица. (Н.Д.). Получено 6 июля 2016 года от Национальной организации по редким заболеваниям (NORD).
- Синдром Смита-Лемли-Опица. (Н.Д.). Получено 6 июля 2016 г. из Университета Юты, Медицина.
- Синдром Смита-Лемли-Опица. (Н.Д.). Получено 6 июля 2016 г. из Совета.
- Синдром Смита-Лемли-Опица. (5 июля 2016 г.) Получено от Genetics Home Reference.
- Штейнер Р. (1 апреля 2015 г.). Синдром Смита-Лемли-Опица. Получено из Medscape.
- Tint G.S., Irons M., Elias E.R. et al. (1994). Дефектный биосинтез холестерина, связанный с синдромом Смита-Лемли-Опитца. N Engl J Med, 330: 107-113
- Witsch-Baumgartner, M. & Lanthaler, B. (2015). День рождения синдрома: 50-летие синдрома Смита-Лемли-Опица. Европейский журнал генетики человека, 23 (3), 277-278.
Источник
Синдром Смита-Лемли-Опитца — этиология, клиника, диагностикаСиндром Смита-Лемли-Опитца недавно стал объектом пристального внимания неврологов и психиатров из-за отчетливой взаимосвязи с аутистическими проявлениями. Возможно, данное заболевание имеет генетическую природу и тесно связано с аутистическими симптомами (см. ниже). Синдром Смита-Лемли-Опитца (ССЛО) регистрируется с частотой около 1 на 70000 новорожденных. Характерна высокая перинатальная смертность и высокая частота мертворождений. Среди выживших детей не менее чем у 80% отмечаются тяжелые отклонения, а у оставшихся 20% изменения фенотипа выражены умеренно. Синдром Смита-Лемли-Опитца (ССЛО) до сих пор диагностируется на основании типичных клинических признаков. Заболевание вызвано врожденным нарушением постскваленового синтеза холестерина. Нарушение синтеза холестерина при ССЛО вызвано наследственной мутацией гена 3-b-гидроксистерол-d-7 редуктазы (DHCR7). Повреждение гена DHCR7 приводит к нарушению синтеза холестерина и десмостерола, приводящее к повышению уровня 7DHC/8DHC, характерному снижению уровня холестерина и, что особенно важно, дисморфическому развитию. Открытие синдрома Смита-Лемли-Опитца вызвало новые вопросы о роли путей биосинтеза холестерина в развитии человека. В настоящее время у 250 пациентов с синдромом Смита-Лемли-Опитца идентифицирована 121 мутация; разнообразие мутаций обеспечивает различную клиническую выраженность. Для воспроизведения некоторых аномалий развития, характерных для ССЛО, и выяснения патогенеза заболевания, было создано две генетических модели синдрома на мышах. Наиболее характерными проявлениями синдрома наряду с задержкой умственного развития, аутизмом, другими поведенческими нарушениями и гипотонией является необычное строение лица с высоким плоским лбом, вывернутыми вперед ноздрями и микрогнатией, а также аномалии гениталий у мальчиков, включая крипторхизм и (или) гипоспадию, а в крайних случаях—неразвитые мужские гениталии, несмотря на нормальный кариотип XY (Scarbrough et al., 1986). Другие проявления включают аномальное строение ушных раковин, птоз век, эпикант, поперечное возвышение ладони и различные аномалии конечностей и внутренних органов (Opitz et al., 1994). У некоторых пациентов отмечаются припадки, достаточно часто встречается отсутствие аппетита. В течение первого года жизни смертность высокая. Аномалии головного мозга могут включать микроцефалию, гипоплазию лобных долей, аномальное строение извилин и гипоплазию мозжечка. Случаи наиболее выраженного поражения иногда выделяются как ССЛО 2 типа (Curry et al., 1987). Синдром наследуется аутосомно-рецессивным путем. Явное повышение частоты заболевания у мужчин, вероятно, связано с более легкой диагностикой на основании очевидных аномалий половых органов. Концентрация холестерина в плазме очень низкая, в то время как содержание 7-гидрохолестерола повышено, что предполагает дефект фермента, приводящего к разрыву двойной связи гидрохолестерола (Tint et al., 1994). Выживаемость строго коррелирует с более высоким уровнем холестерина плазмы (Tint et al., 1995). Возможна пренатальная диагностика путем определения содержания 7-дегидрохолестерола в амниотической жидкости (Dallaire et al., 1995). Потребление большого количества холестерина может нормализовать его уровень в крови, но необязательно будет клинически эффективно (Ullrich et al., 1996). Нарушения аутистического спектра часто регистрируются у пациентов с синдромом Смита-Лемли-Опитца (Gillberg и Coleman, 2000; Tierney et al., 2001; Sikora et al, 2006). Данные результаты и сообщение о низком уровне холестерина при различных случаях семейного аутизма позволяют предположить, что стериновый обмен может иметь важное значение для подгруппы пациентов с поведенческим синдромом аутизма и что хотя бы теоретически возможно «лечение» холестерином в случаях аутизма с низким уровнем холестерина. — Также рекомендуем «Синдром Смита-Магениса — этиология, клиника, диагностика» Редактор: Искандер Милевски. Дата публикации: 6.12.2018 Оглавление темы «Наследственные синдромы в неврологии.»:
|
Источник
Синдром Смита — Лемли — Опица (синдром SLOS, RSH или дефицит 7-дегидрохолестерол редуктазы) — наследственное заболевание, которое связано с нарушением метаболизма холестерина. Проявляется черепно-лицевыми аномалиями, умственной отсталостью, шестипалостью и другими врожденными неврологическими нарушениями и аномалиями развития.
Общие сведения
В 1964 г. обнаруженный у трех пациентов синдром совместно с генетиком Дж. Опицем описали американский педиатр Д. Смит и бельгийский педиатр Л. Лемли, поэтому заболевание назвали в их честь.
Детальное описание синдрома, сделанное в 1969 г., принадлежит Р. Н. Файн с соавторами — для названия данного синдрома в этом описании использованы первые буквы фамилий первых выявленных больных (синдром RSH).
Заболеванию больше подвержены новорожденные европеоидной расы – частота составляет 1:20 000 — 1:30 000 случаев. С меньшей частотой синдром встречается у представителей азиатской и негроидной расы.
Носителем мутантного гена является каждый тридцатый человек.
Заболеванию больше подвержены мальчики – соотношение со случаями заболевания у девочек составляет 3 к 1.
Формы
В настоящее время некоторыми исследователями выделяются два типа синдрома SLOS:
- к I типу относят заболевание со множественными пороками развития, которое совместимо с жизнью;
- ко II типу относят заболевание, которому свойственен ранний летальный исход.
Разница между данными формами заключается в основном в характере мутации, а не в генетической гетерогенности.
Причины развития
Синдром Смита – Лемли – Опица вызывается мутациями гена DHCR7, который расположен на 11 в регионе q13. 4.
Ген DHCR7 кодирует 7-стеролредуктазу, необходимую для биосинтеза фермента 7-дегидрохолестерол редуктазы. Этот фермент отвечает за конечную стадию производства холестерина – жироподобного воскового вещества, которое производится в организме (80%) и поступает с пищей (20%).
Холестерин:
- при взаимодействии с белками в период эмбрионального развития контролирует раннее развитие мозга, половых органов и конечностей;
- является структурным компонентом клеточных мембран и миелиновых оболочек, которые изолируют нервные клетки;
- участвует в образовании желчных кислот и выработке стероидных гормонов;
- участвует в синтезе витамина D.
В настоящее время у состоящего из 9-ти экзонов (кодирующих синтез белка и несущих наследственную информацию участков) гена DHCR7 выявлено более 120 мутаций, которые вызывают синдром SLOS. Встречаются:
- точечная замена, при которой одно азотистое основание заменяется другим;
- делеции (утрата) небольших участков гена;
- сплайсинговые мутации, при которых образуется ненормальный тип кодирующей наследственную информацию РНК.
Чаще всего мутации наблюдаются на участках 4,6,7,9 – именно с этими экзонами связано до 70% выявленных гетерогенных мутаций, причем 50% случаев заболевания вызвано четырьмя наиболее распространенными мутациями:
- Мутацией сплайсинга IVS8-1 G’-‘C, которая обнаружена в 13 мутантных аллелях. Заключается в изменении последовательности нуклеотидов в ДНК. Вызывает тяжелую форму заболевания, а ее гомозиготная форма – ранний летальный исход. Встречается в 30 % случаев заболевания у лиц европейского происхождения.
- Точечной миссенс-мутацией T93M, распространенной у лиц средиземноморского происхождения. Заключается в мутационном изменении нуклеотидной последовательности ДНК, при котором кодирующий тринуклеотид заменяет аминокислоту треонин в белке на аминокислоту метионин. В результате в плазме крови повышается уровень 7-дегидрохолестерина. Заболевание протекает в легкой форме.
- Мутацией p.W151X, которая наблюдается в 10 мутантных аллелях гена DHCR7. При гомозиготности нонсенс-мутация W151X вызывает летальную форму синдрома SLOS. Заключается в утрате способности кодона (единицы генетического кода) кодировать определенную аминокислоту, благодаря чему белок приобретает новые свойства, инактивируется или деградирует.
- Мутацией c.964-1GC.
Большинство выявленных мутаций гена DHCR7 являются точечными миссенс-мутациями, изменяющими одиночные аминокислоты и снижающими выработку холестерина.
Остальные выявленные мутации являются делециями или инсерциями (вставками) нуклеотидов, которые приводят к производству аномального фермента, устраняя его активность. Без активной 7-дегидрохолестерол редуктазы клетки не способны производить холестерин в достаточном количестве.
В результате в крови и тканях накапливаются потенциально токсичные продукты производства холестерина (уровень 7-дегидрохолестерола повышается в 2000 раз). Сочетание низкого уровня холестерина и накопление сопутствующих веществ вызывает нарушения во многих системах организма.
Тяжесть заболевания зависит от локализации и типа мутации в гене DHCR7.
Болезнь относится к аутосомно-рецессивному типу наследования.
Патогенез
Патогенез заболевания до конца не установлен, но известно, что снижение синтеза 7-дегидрохолестерол редуктазы вызывает существенное повышение в плазме уровня 7-дегидрохолестерола и дефицит холестерина.
Проведенные на крысах эксперименты показали, что избыток 7-дегидрохолестерола в мозге приводит к нарушению процесса обучения, а накопление в эмбрионах оксигенированного 7-дегидрохолестерола вызывает задержку роста.
Недостаток 7-дегидрохолестерол редуктазы вызывает у новорожденных голопрозэнцефалию (неполное разделение эмбрионального переднего мозга), отсутствие гипофиза и аномалии конечностей и гениталий.
Симптомы
Симптоматика синдрома Смита – Лемли – Опитца отличается разнообразием. Легкая форма заболевания сопровождается незначительными умственными и физическими нарушениями, а тяжелые случаи отличаются выраженными физическими пороками развития и летальным исходом в перинатальном возрасте.
Синдром SLOS в 100% случаев отличается:
- низкой массой и длинной тела при рождении;
- узким лбом;
- птозом (опущением век);
- наличием эпикантуса;
- косоглазием;
- микроцефалией и различными деформациями черепа;
- низко расположенными ушными раковинами;
- коротким носом с открытыми ноздрями и широким концом;
- недоразвитием челюсти (микрогнатией) и ее широким альвеолярным краем.
Наблюдается также:
- неправильное строение внешних половых органов – гипоспадия (неправильно расположенное отверстие мочеиспускательного канала, дисплазия крайней плоти, искривление полового члена), крипторхизм (неопущение яичка в мошонку), гипертрофия клитора, невыраженность половых органов;
- односторонняя или двусторонняя постаксиальная полидактилия (шестипалость) кистей или стоп;
- наличие поперечной складки на ладонях;
- наличие Y-образной синдактилии (сращения) II–III пальцев;
- укороченный III палец на руках;
- вальгусная стопа.
Встречаются также другие виды синдактилии или отсутствие (недоразвитие) одного или нескольких пальцев, вывих бедра, кифоз, сколиоз, наличие шейных ребер, тонкие ребра или их отсутствие.
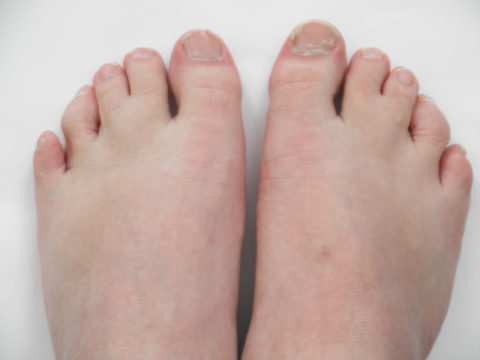
 Синдактилия пальцев ног при синдроме Смита — Лемли — Опица
Синдактилия пальцев ног при синдроме Смита — Лемли — Опица
Синдром SLOS во многих случаях сопровождается:
- врожденными пороками сердца;
- аномалиями почек;
- эпилепсией;
- тугоухостью и катарактой;
- увеличением или уменьшением долей легкого;
- сужением привратника (отдел желудка);
- гастроэзофагеальной рефлюксной болезнью;
- аномалией развития толстой кишки;
- голопрозэнцефалией;
- наличием расщелины неба;
- тяжелыми нарушениями сна;
- повышенной возбудимостью, проявлениями агрессии;
- пониженным мышечным тонусом.
В большинстве случаев заболевание сопровождается отставанием в умственном развитии, а у половины больных диагностируют наличие аутизма.
К симптомам перинатального периода относят:
- воротниковый отек (больше чем 3 мм) в I триместре;
- специфические деформации у плода, которые обнаружены во II триместре при помощи УЗИ;
- маловодие.
Диагностика
Для постановки диагноза заболевания используются:
- Клинические данные.
- Данные биохимического анализа крови. Определение уровня холестерина в крови не является достоверным методом (у 10 % больных этот уровень соответствует норме), поэтому используется определение уровня 7-дегидрохолестерола в тканях или в плазме крови.
В сомнительных случаях диагноз подтверждается ДНК-диагностикой, анализом фермента 7-дегидрохолестерин редуктазы или анализом биосинтеза стерина в культуре клеток.
Пренатальная диагностика включает:
- биопсию ворсинчатого хориона, которая проводится на 10-й полной неделе вынашивания и позволяет определить уровень стеролов в ворсинах хориона;
- амниоцентез, при котором определяют уровень 7-дегидрохолестерина в амниотической жидкости;
- кордоцентез, который проводится не раньше 18 полных недель вынашивания и позволяет исследовать уровень холестерина в пуповинной крови.
Возможна также диагностика по УЗИ при характерных пороках развития плода.
Лечение
Эффективного лечения синдрома Смита – Лемли – Опитца в настоящее время не существует.
Проводится:
- Хирургическое лечение аномалий развития (дефектов конечностей и др.).
- Поддерживающая терапия, которая заключается в использовании пищевого холестерина. Пищевой холестерин поступает в организм больного либо в виде продуктов с богатым содержанием холестерина (яичных желтков и др.), либо в виде водной или масляной суспензии, либо в кристаллической форме. Обычно препаратом выбора является порошок Cholesterol Module, позволяющий точно рассчитывать дозу и свести к минимуму негативные последствия холестериновой диеты (запоры, рвота).
Источник
