Синдром с пороком сердца перегородки
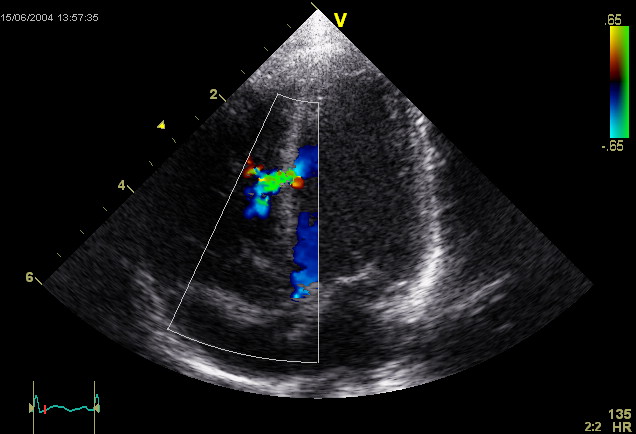
Дефект межпредсердной перегородки – врожденная аномалия сердца, характеризующаяся наличием открытого сообщения между правым и левым предсердиями. Дефект межпредсердной перегородки проявляется одышкой, повышенной утомляемостью, отставанием в физическом развитии, сердцебиением, бледностью кожи, шумами в сердце, наличием «сердечного горба», частыми респираторными заболеваниями. Дефект межпредсердной перегородки диагностируется с учетом данных ЭКГ, ФКГ, ЭхоКС, катетеризации полостей сердца, атриографии, ангиопульмонографии. При дефекте межпредсердной перегородки производится его ушивание, пластика или рентгенэндоваскулярная окклюзия.
Дефект межпредсердной перегородки
Дефект межпредсердной перегородки (ДМПП) – одно или несколько отверстий в перегородке, разделяющей левую и правую предсердные полости, наличие которых обуславливает патологический сброс крови, нарушение внутрисердечной и системной гемодинамики. В кардиологии дефект межпредсердной перегородки встречается у 5-15% лиц с врожденными пороками сердца, при этом в 2 раза чаще диагностируется у женщин.
Наряду с дефектами межжелудочковой перегородки, коарктацией аорты, открытым артериальным протоком, дефект межпредсердной перегородки входит в число наиболее часто встречающихся врожденных пороков сердца. Дефект межпредсердной перегородки может являться изолированным врожденным пороком сердца или сочетаться с другими внутрисердечными аномалиями: дефектом межжелудочковой перегородки, аномальным дренажем легочных вен, митральной или трикуспидальной недостаточностью.
Причины дефекта межпредсердной перегородки
Формирование дефекта связано с недоразвитием первичной или вторичной межпредсердной перегородки и эндокардиальных валиков в эмбриональном периоде. К нарушению органогенеза могут приводить генетические, физические, экологические и инфекционные факторы.
Риск развития дефекта межпредсердной перегородки у будущего ребенка существенно выше в тех семьях, где есть родственники с врожденными пороками сердца. Описаны случаи семейных дефектов межпредсердной перегородки в сочетании с атриовентрикулярной блокадой или с недоразвитием костей кисти (синдромом Холта-Орама).
Кроме наследственной обусловленности, к возникновению дефекта межпредсердной перегородки, могут приводить вирусные заболевания беременной (краснуха, ветряная оспа, герпес, сифилис и др.), сахарный диабет и другие эндокринопатии, прием некоторых медикаментов и алкоголя во время беременности, производственные вредности, ионизирующая радиация, гестационные осложнения (токсикозы, угроза выкидыша и др.).
Особенности гемодинамики при дефекте межпредсердной перегородки
В силу разницы давления в левом и правом предсердиях, при дефекте межпредсердной перегородки происходит артериовенозное шунтирование крови слева направо. Величина сброса крови зависит от размеров межпредсердного сообщения, соотношения сопротивления атриовентрикулярных отверстий, пластического сопротивления и объема заполнения желудочков сердца.
Лево-правое шунтирование крови сопровождается увеличением наполняемости малого круга кровообращения, возрастанием объемной нагрузки правого предсердия и усилением работы правого желудочка. Ввиду несоответствия между площадью клапанного отверстия легочной артерии и объемом выброса из правого желудочка, происходит развитие относительного стеноза легочной артерии.
Длительная гиперволемия малого круга кровообращения постепенно приводит к развитию легочной гипертензии. Это наблюдается только тогда, когда легочный кровоток превышает норму в 3 и более раза. Легочная гипертензия при дефекте межпредсердной перегородки обычно развивается у детей старше 15 лет, при поздних склеротических изменениях легочных сосудов. Тяжелая легочная гипертензия вызывает правожелудочковую недостаточность и смену шунта, что проявляется вначале транзиторным веноартериальным сбросом (при физической нагрузке, натуживании, кашле и др.), а затем и стойким, сопровождающимся постоянным цианозом в покое (синдром Эйзенменгера).
Классификация дефектов межпредсердной перегородки
Дефекты межпредсердной перегородки различаются по количеству, размерам и расположению отверстий.
С учетом степени и характера недоразвития первичной и вторичной межпредсердных перегородок соответственно выделяют первичные, вторичные дефекты, а также полное отсутствие межпредсердной перегородки, обусловливающее общее, единственное предсердие (трехкамерное сердце).
К первичным ДМПП относят случаи недоразвития первичной межпредсердной перегородки с сохранением первичного межпредсердного сообщения. В большинстве случаев они сочетаются с расщеплением створок двух- и трехстворчатого клапанов, открытым атриовентрикулярным каналом. Первичный дефект межпредсердной перегородки, как правило, характеризуется большим размером (3-5 см) и локализуется в нижней части перегородки над предсердно-желудочковыми клапанами и не имеет нижнего края.
Вторичные ДМПП образованы недоразвитием вторичной перегородки. Обычно они имеют небольшие размеры (1-2 см) и располагаются в центре межпредсердной перегородки или в области устьев полых вен. Вторичные дефекты межпредсердной перегородки часто сочетаются с аномальным впадением легочных вен в правое предсердие. При этом типе порока межпредсердная перегородка сохранена в своей нижней части.
Встречаются комбинированные дефекты межпредсердной перегородки (первичный и вторичный, ДМПП в сочетании с дефектом венозного синуса). Также дефект межпредсердной перегородки может входить в структуру сложных ВПС (триады и пентады Фалло) или сочетаться с тяжелыми сердечными пороками — аномалией Эбштейна, гипоплазией камер сердца, транспозицией магистральных сосудов.
Формирование общего (единственного) предсердия связано с недоразвитием или полным отсутствием первичной и вторичной перегородок и наличием большого дефекта, занимающего площадь всей межпредсердной перегородки. Структура стенок и оба предсердных ушка при этом сохранены. Трехкамерное сердце может сочетаться с аномалиями атриовентрикулярных клапанов, а также с аспленией.
Одним из вариантов межпредсердной коммуникации является открытое овальное окно, обусловленное недоразвитием собственного клапана овального отверстия или его дефектом. Однако ввиду того, что открытое овальное отверстие не является истинным дефектом перегородки, связанным с недостаточностью ее ткани, данная аномалия не может быть причислена к дефектам межпредсердной перегородки.
Симптомы дефекта межпредсердной перегородки
Дефекты межпредсердной перегородки могут протекать с длительной гемодинамической компенсацией, а их клиника отличается значительным разнообразием. Выраженность симптоматики определяется величиной и локализацией дефекта, длительностью существования ВПС и развитием вторичных осложнений. На первом месяце жизни единственным проявлением дефекта межпредсердной перегородки обычно служит транзиторный цианоз при плаче и беспокойстве, что обычно связывается с перинатальной энцефалопатией.
При дефектах межпредсердной перегородки средних и больших размеров симптоматика проявляется уже в первые 3-4 мес. или к концу первого года жизни и характеризуется стойкой бледностью кожных покровов, тахикардией, умеренным отставанием в физическом развитии, недостаточным приростом массы тела. Для детей с дефектами межпредсердной перегородки типично частое возникновение респираторных заболеваний — рецидивирующих бронхитов, пневмоний, протекающих с длительным влажным кашлем, стойкой одышкой, обильными влажными хрипами и др., обусловленными гиперволемией малого круга кровообращения. У детей первого десятилетия жизни отмечаются частые головокружения, склонность к обморокам, быстрая утомляемость и одышка при физической нагрузке.
Небольшие дефекты межпредсердной перегородки (до 10-15 мм) не вызывают нарушения физического развития детей и характерных жалоб, поэтому первые клинические признаки порока могут развиться лишь на втором-третьем десятилетии жизни. Легочная гипертензия и сердечная недостаточность при дефекте межпредсердной перегородки формируются примерно к 20 годам, когда возникает цианоз, аритмии, редко – кровохарканье.
Диагностика дефекта межпредсердной перегородки
При объективном обследовании пациента с дефектом межпредсердной перегородки выявляется бледность кожных покровов, «сердечный горб», умеренное отставание в росте и весе. Перкуторно определяется увеличение границ сердца влево и вправо; при аускультации слева от грудины во II-III межреберьях выслушивается умеренно интенсивный систолический шум, который в отличие от дефекта межжелудочковой перегородки или стеноза легочной артерии, никогда не бывает грубым. Над легочной артерией выявляется расщепление II тона и акцентирование его легочного компонента. Аускультативные данные подтверждаются при проведении фонокардиографии.
При вторичных дефектах межпредсердной перегородки ЭКГ-изменения отражают перегрузку правых отделов сердца. Могут регистрироваться неполная блокада правой ножки пучка Гиса, АВ-блокады, синдром слабости синусового узла. Рентгенография органов грудной клетки позволяет увидеть усиление легочного рисунка, выбухание ствола легочной артерии, увеличение тени сердца вследствие гипертрофии правого предсердия и желудочка. При рентгеноскопии обнаруживается специфичный признак дефекта межпредсердной перегородки — усиленная пульсация корней легких.
ЭхоКГ-исследование с цветным допплеровским картированием выявляет лево-правый сброс крови, наличие дефекта межпредсердной перегородки, позволяет определить его величину и локализацию. При зондировании полостей сердца обнаруживается повышение давления и насыщения крови кислородом в правых отделах сердца и легочной артерии. В случае диагностических трудностей обследование дополняется атриографией, вентрикулографией, флебографией яремных вен, ангиопульмонографией, МРТ сердца.
Дефект межпредсердной перегородки следует дифференцировать от дефекта межжелудочковой перегородки, открытого артериального протока, митральной недостаточности, изолированного стеноза легочной артерии, триады Фалло, аномального впадения легочных вен в правое предсердие.
Лечение дефекта межпредсердной перегородки
Лечение дефектов межпредсердной перегородки только хирургическое. Показаниями к кардиохирургической операции служит выявление гемодинамически значимого артериовенозного сброса крови. Оптимальный возраст для коррекции порока у детей — от 1 до 12 лет. Хирургическое лечение противопоказано при высокой легочной гипертензии с веноартериальным сбросом крови, обусловленной склеротическими изменениями легочных сосудов.
При дефектах межпредсердной перегородки прибегают к различным способам их закрытия: ушиванию, пластике с помощью перикардиального лоскута или синтетической заплаты в условиях гипотермии и ИК. Рентгенэндоваскулярная окклюзия дефекта межпредсердной перегородки позволяет закрывать отверстия не более 20 мм.
Хирургическая коррекция дефектов межпредсердной перегородки сопровождается хорошими отдаленными результатами: у 80-90% больных отмечается нормализации гемодинамики и отсутствие жалоб.
Прогноз дефекта межпредсердной перегородки
Малые дефекты межпредсердной перегородки совместимы с жизнью и могут обнаруживаться даже в пожилом возрасте. У некоторых больных с небольшим дефектом межпредсердной перегородки возможно спонтанное закрытие отверстия в течение первых 5-ти лет жизни. Продолжительность жизни лиц с большими дефектами межпредсердной перегородки при естественном течении порока составляет в среднем 35-40 лет. Гибель пациентов может наступить от правожелудочковой сердечной недостаточности, нарушений ритма и проводимости сердца (пароксизмальной тахикардии, мерцательной аритмии и др.), реже — от легочной гипертензии высокой степени.
Пациенты с дефектами межпредсердной перегородки (оперированные и неоперированные) должны находиться под наблюдением кардиолога и кардиохирурга.
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 4 апреля 2018;
проверки требует 1 правка.
Дефект межжелудочковой перегородки
Дефект межжелудочковой перегородки (ДМЖП) — врожденный порок сердца, характеризующийся наличием дефекта между правым и левым желудочками сердца.
Эпидемиология[править | править код]
Дефект межжелудочковой перегородки (ДМЖП) — встречается наиболее часто, причём как в изолированном виде, так и в составе многих других пороков сердца. Среди ВПС частота данного порока варьирует от 27,7 до 42 %.[3] Одинаково часто встречается как у мальчиков, так и у девочек. Существуют данные об аутосомно-доминантном и рецессивном типах наследования. В 3,3 % случаев у прямых родственников больных с ДМЖП также обнаруживают этот порок.[4]
Классификация[править | править код]
В межжелудочковой перегородке выделяют 3 отдела: верхняя часть — мембранозная, прилегает к центральному фиброзному телу, средняя часть — мышечная, и нижняя — трабекулярная. Соответственно этим отделам называют и дефекты межжелудочковой перегородки, однако большинство из них имеют перимембранозную локализацию (до 80 %). На долю мышечных ДМЖП приходится 20 %[3][5].
По размерам дефекты подразделяют на большие, средние и малые. Для правильной оценки величины дефекта его размер надо сравнивать с диаметром аорты. Мелкие дефекты размером 1-2 мм, расположенные в мышечной части межжелудочковой перегородки, называются болезнью Толочинова-Роже. Вследствие хорошей аускультативной картины и отсутствия гемодинамических нарушений для их характеристики уместно выражение: «много шума из ничего». Отдельно выделяют множественные большие дефекты межжелудочковой перегородки, по типу «швейцарского сыра», имеющие неблагоприятное прогностическое значение[5].
Гемодинамика[править | править код]
Внутрисердечные гемодинамические нарушения при ДМЖП начинают формироваться спустя некоторое время после рождения, как правило, на 3—5 сутки жизни.[6]
В раннем неонатальном периоде шум в сердце может отсутствовать вследствие одинакового давления в правом и левом желудочках из-за так называемой неонатальной легочной гипертензии. Постепенное падение давления в системе легочной артерии и в правом желудочке создаёт разность (градиент) давлений между желудочками, вследствие чего появляется сброс крови слева направо (из области высокого давления в область низкого давления).
[7][8]
Дополнительный объём крови, поступающий в правый желудочек и легочную артерию, приводит к переполнению сосудов малого круга кровообращения, где развивается лёгочная гипертензия.
Выделяют три стадии легочной гипертензии по В. И. Бураковскому.
- Застой крови (гиперволемическая стадия легочной гипертензии) может приводить к отёку легких, частому присоединению инфекции, развитию пневмоний, манифестирующих в ранние сроки жизни, имеющих тяжелое течение и плохо поддающихся лечению. Если с гиперволемией не удается справиться консервативными методами, в таких случаях проводят паллиативную операцию — сужение легочной артерии по Мюллеру. Суть операции заключается в создании временного искусственного стеноза легочной артерии, который препятствует попаданию в МКК избыточного количества крови. Однако повышенная нагрузка, падающая при этом на правый желудочек, диктует в дальнейшем (спустя 3—6 месяцев) необходимость проведения радикальной операции.[9]
- При естественном течении порока со временем в сосудах малого круга кровообращения срабатывает рефлекс Китаева (спазмирование в ответ на перерастяжение), что приводит к развитию переходной стадии лёгочной гипертензии. В этот период ребёнок перестает болеть, становится более активным, начинает прибавлять в весе. Стабильное состояние пациента в эту фазу является лучшим периодом для проведения радикальной операции.[9] Давление в легочной артерии (и соответственно в правом желудочке) в эту фазу колеблется в пределах от 30 до 70 мм рт. ст. Аускультативная картина характеризуется уменьшением интенсивности шума при появлении акцента II тона над лёгочной артерией.[5]
- В дальнейшем, если хирургическая коррекция ВПС не проводится, начинают формироваться процессы склерозирования сосудов легких (высокая легочная гипертензия — синдром Эйзенменгера). Этот патологический процесс не имеет обратного развития и приводит к значительному повышению давления в легочной артерии (иногда до 100—120 мм рт. ст.).[5]
Аускультативно можно выслушать резко выраженный акцент II тона над легочной артерией («металлический» оттенок).[10]
Систолический шум становится слабо-интенсивным, а в некоторых случаях может совсем отсутствовать. На этом фоне можно зафиксировать появление нового диастолического шума, обусловленного недостаточностью клапанов лёгочной артерии (шум Грехема-Стилла).[10] В клинической картине заболевания отмечается множество патологических признаков: сердечный «горб», расширение границ относительной сердечной тупости, больше вправо. Над легкими выслушиваются участки ослабленного и жесткого дыхания, могут встречаться свистящие хрипы. Самым характерным признаком синдрома Эйзенменгера является постепенное нарастание цианоза, — сначала периферического, а в дальнейшем и диффузного. Это происходит вследствие перекрестного сброса крови в области дефекта межжелудочковой перегородки, который при превышении давления в правом желудочке становится право-левым, то есть меняет своё направление. Наличие у пациента третьей стадии легочной гипертензии может стать основным мотивом отказа кардиохирургов от проведения операции.[6]
Клиническая картина[править | править код]
Клиническая картина при ДМЖП заключается в симптомокомплексе сердечной недостаточности, развивающейся, как правило, на 1-3 месяцах жизни (в зависимости от размеров дефекта).[8]
Кроме признаков сердечной недостаточности ДМЖП может манифестировать ранними и тяжелыми пневмониями. При осмотре ребёнка можно выявить тахикардию и одышку, расширение границ относительной сердечной тупости, смещение верхушечного толчка вниз и влево. В ряде случаев определяется симптом «кошачьего мурлыканья». Систолический шум, как правило, интенсивный, выслушивается над всей областью сердца, хорошо проводится на правую сторону грудной клетки и на спину с максимальной интенсивностью в IV межреберье слева от грудины. При пальпации живота определяется гепатомегалия и спленомегалия. Изменения периферической пульсации не характерны. У детей с ДМЖП как правило быстро развивается гипертрофия.
Диагностика[править | править код]
Диагностика любого порока сердца складывается из рентгенологического исследования органов грудной полости, электрокардиографии и двухмерной допплерэхокардиографии.
При рентгенологическом исследовании органов грудной клетки описывают форму сердца и состояние легочного рисунка, определяют размер кардио-торакального индекса (КТИ). Все эти показатели имеют свои особенности при разных степенях лёгочной гипертензии. В первой, гиперволемической стадии, выявляется сглаженность талии и погруженность верхушки сердца в диафрагму, увеличение КТИ. Со стороны легочного рисунка отмечается его усиление, нечеткость, размытость. Крайней степенью гиперволемии в лёгких является отёк лёгких. В переходной стадии лёгочной гипертензии отмечается нормализация лёгочного рисунка, некоторая стабилизация размеров КТИ. Для склеротической стадии лёгочной гипертензии характерно значительное увеличение размеров сердца, причем в основном за счёт правых отделов, увеличение правого предсердия (формирование прямого атрио-вазального угла), выбухание дуги лёгочной артерии (индекс Мура более 50 %), приподнятость верхушки сердца, которая образует с диафрагмой острый угол. Со стороны лёгочного рисунка часто описывается симптом «обрубленного дерева»: яркие, чёткие, увеличенные корни, на фоне которых лёгочный рисунок прослеживается только до определённого уровня. На периферии имеет место признаки эмфиземы. Грудная клетка имеет вздутую форму, ход ребер горизонтальный, диафрагма уплощена, стоит низко.[9]
ЭКГ имеет свои закономерности, тесно связанные с фазой течения ВПС и степенью лёгочной гипертензии. Сначала выявляются признаки перегрузки левого желудочка — повышение его активности, затем развитие его гипертрофии. С течением времени присоединяются признаки перегрузки и гипертрофии правых отделов сердца — как предсердия, так и желудочка, — это свидетельствует о высокой лёгочной гипертензии. Электрическая ось сердца всегда отклонена вправо. Могут встречаться нарушения проводимости — от признаков неполной блокады правой ножки пучка Гиса до полной атрио-вентрикулярной блокады.[10]
При допплер-ЭхоКГ уточняется место расположения дефекта, его размер, определяется давление в правом желудочке и лёгочной артерии. В первой стадии лёгочной гипертензии давление в ПЖ не превышает 30 мм.рт.ст., во второй стадии — от 30 до 70 мм.рт.ст., в третьей — более 70 мм.рт.ст.[6]
Лечение[править | править код]
Лечение данного порока подразумевает консервативную терапию сердечной недостаточности и хирургическую коррекцию порока сердца. Консервативное лечение складывается из препаратов инотропной поддержки (симпатомиметики, сердечные гликозиды), мочегонных препаратов, кардиотрофиков.[8]
В случаях высокой легочной гипертензии назначаются ингибиторы ангиотензинпревращающего фермента — капотен или каптоприл.
Оперативные вмешательства подразделяются на паллиативные операции (в случае ДМЖП — операция суживания лёгочной артерии по Мюллеру) и радикальную коррекцию порока — пластика дефекта межжелудочковой перегородки заплатой из листков перикарда в условиях искусственного кровообращения, кардиоплегии и гипотермии.[5]
Примечания[править | править код]
- ↑ Disease Ontology release 2019-05-13 — 2019-05-13 — 2019.
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 Шарыкин. Врожденные пороки сердца. — Теремок, 2005. — 384 с.
- ↑ https://www.mma.ru/article/id34653 Дефект межжелудочковой перегородкм. Медицинская энциклопедия ММА
- ↑ 1 2 3 4 5 Прахов А.В. Неонатальная кардиология. — НГМА, 2008. — 388 с.
- ↑ 1 2 3 Банкл Г. Врожденные пороки сердца и крупных сосудов. — 1980. — 312 с.
- ↑ Вишневский А.А., Галанкин Н.К. Врожденные пороки сердца и крупных сосудов. — 1962. — 210 с.
- ↑ 1 2 3 Белозеров Ю.М. Детская кардиология. — МЕДпресс-информ, 2004. — 600 с.
- ↑ 1 2 3 Белоконь Н.А., Подзолков В.П. Врожденные пороки сердца. — 1991. — 352 с.
- ↑ 1 2 3 Василенко В.Х.,Фельдман С.Б., Могилевский Э.Б. Пороки сердца. — 1983. — 366 с.
Ссылки[править | править код]
- Форум родителей детей с врожденными пороками сердца
- Об эффективности хирургической коррекции дефекта межжелудочковой перегородки у детей первого года жизни
- ДМЖП — библиотека медакадемии
Литература[править | править код]
- 1.Банкл Г. Врожденные пороки сердца и крупных сосудов. — 1980. — 312 с.
- 2. Белозеров Ю.М. Детская кардиология. — МЕДпресс-информ, 2004. — 600 с.
- 3. Белоконь Н.А., Подзолков В.П. Врожденные пороки сердца. — 1991. — 352 с.
- 4. Василенко В.Х.,Фельдман С.Б., Могилевский Э.Б. Пороки сердца. — 1983. — 366 с.
- 5. Вишневский А.А., Галанкин Н.К. Врожденные пороки сердца и крупных сосудов. — 1962. — 210 с.
- 6. Имре Литтманн, Рене Фоно. Врожденные пороки сердца и крупных сосудов. — 1954. — 232 с.
- 7. Прахов А.В. Неонатальная кардиология. — НГМА, 2008. — 388 с.
- 8. Шарыкин. Врожденные пороки сердца. — Теремок, 2005. — 384 с.
Источник
