Синдром ригидного человека что это
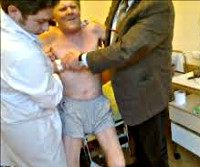

Синдром «ригидного человека» — редкое неврологическое заболевание неясного генеза, проявляющееся постоянным тоническим напряжением мышц (ригидностью) и отдельными болезненными спазмами, ограничивающими подвижность пациента. Диагностируется синдром «ригидного человека» по типичной клинической картине и данным электрофизиологических исследований, при исключении прочей патологии, способной вызывать ригидность. Лечение симптоматическое. Традиционно применяются бензодиазепины и баклофен. Альтернативными методами являются плазмаферез, глюкокортикостероидная терапия, внутримышечное введение ботулотоксина, лечение иммуноглобулином.
Общие сведения
Синдром «ригидного человека» (СРЧ) — редкая неврологическая патология, клинически проявляющаяся мышечной ригидностью и спазмами. Ригидностью мышц называется их постоянное тоническое напряжение. Следствием ригидности является скованность и ограничение произвольных и непроизвольных двигательных актов. При синдроме «ригидного человека» ригидность преобладает в аксиальных (идущих вдоль позвоночника) мышцах и проксимальных мышцах конечностей. При этом тонус мышц-разгибателей выше, чем сгибателей, что придает больному характерный внешний вид с необычайно прямой и даже выгнутой спиной, выраженным поясничным прогибом, развернутыми назад плечами и несколько запрокинутой головой. Впервые синдром «ригидного человека» был подробно описан в 1956 г. американскими врачами-неврологами Мершем и Вольтманом, в честь которых он носит название синдром Мерша-Вольтмана. Статистика распространенности синдрома в настоящее время не собрана, в виду его большой редкости.

Синдром «ригидного человека»
Причины синдрома «ригидного человека»
В этиопатогенезе синдрома многое остается неясным. Клинические исследования, проводимые специалистами в области неврологии, показали, что базовым патогенетическим субстратом патологии выступает повышенная возбудимость двигательных нейронов, локализующихся в передних рогах спинного мозга. Предположительно, это обусловлено дисфункцией ГАМКергической системы, оказывающей тормозное воздействие на мотонейроны ЦНС. Данная гипотеза подтверждается низким содержанием ГАМК в цереброспинальной жидкости пациентов с СРЧ и наблюдающейся у них антиспастической эффективностью ГАМКергических и антиадренергических фармпрепаратов.
В 1966 г. была изложена аутоиммунная теория этиологии синдрома. В 1988 г. у пациентов, имеющих синдром «ригидного человека», в цереброспинальной жидкости и в крови были найдены антитела к глутаматдекарбоксилазе — ферменту, катализирующему синтез ГАМК из глутаминовой кислоты и концентрирующемуся в окончаниях ГАМКергических нейронов. Однако дальнейшие исследования показали, что такие антитела в цереброспинальной жидкости имеются лишь у 68% пациентов с СРЧ, а в крови — только у 60%. Следует отметить идентичность клинической картины у пациентов с антителами и без них.
Неясен остается вопрос патогенетической роли выявленных антител к гутаматдекарбоксилазе: являются ли они непосредственной причиной дисфункции мотонейронов или только ее следствием. Наряду с указанными антителами синдром «ригидного человека» зачастую сопровождается наличием других антител: к клеткам щитовидной железы, эпителию желудка, инсулин-продуцирующим клеткам поджелудочной железы, антимитохондриальных и антинуклеарных антител.
Симптомы синдрома «ригидного человека»
Заболевание может дебютировать в любом возрасте, но чаще всего манифестация происходит в третью и четвертую декады жизни. Типично постепенное развитие. Как правило, первыми симптомами выступают преходящее напряжение (ригидность) и боли в мышцах спины, шеи и живота. Затем ригидность приобретает постоянный характер, на ее фоне возникают периодические интенсивные спазмы мышц. В течение нескольких месяцев в процесс вовлекаются мышцы проксимальных отделов рук и ног. У 25% пациентов наблюдается спазмы мимической мускулатуры, приводящие к гипомимии или непроизвольным движениям (например, вытягиванию губ при спазме круговой мышцы рта); поражение дистальных мышц (чаще мышц голеней).
Преобладание ригидности в мышцах-разгибателях приводит к переразгибанию спины, формированию выраженного поясничного лордоза, постоянному приподнятому положению плеч и некоторому запрокидыванию головы. Вследствие тонического состояния мышц живота формируется «доскообразный живот». Характерна походка «заводной куклы» с медленными, с трудом осуществляемыми мелкими шагами. В тяжелых случаях резко страдает подвижность пациентов: они не могут самостоятельно сесть на стул или встать с него, одеться, наклониться, повернуть голову. При этом конечности кажутся плотно сросшимися с туловищем и двигаются вместе с ним единым блоком. Если синдром «ригидного человека» сопровождается поражением дыхательной мускулатуры, то у пациентов даже при незначительной физической нагрузке возникает дыхательная недостаточность.
На фоне перманентной ригидности наблюдаются отдельные мышечные спазмы. Они могут иметь спонтанный, акционный или рефлекторный характер. Акционные спазмы провоцируются движением, рефлекторные — вариабельными внешними воздействиями (прикосновением, холодом, натуживанием, эмоциональной реакцией и т. п.). Наиболее часто спастические сокращения происходят в мышцах спины и ног. Длительность спазмов варьирует от нескольких секунд до десятков минут. В отдельных случаях сила сокращения мышц при спазме бывает настолько велика, что приводит к вывиху или перелому. При спазме дыхательных мышц и мышц гортани возникают расстройства ритма дыхания. Генерализованный характер спазма обуславливает падение больного. Зачастую спазмы протекают с острой болью, которая по окончании спазма приобретает тупой мозжащий характер. В 75% спазмы сочетаются с эмоциональными (тревога, дисфория) и вегетативными (тахикардия, гипергидроз, мидриаз, подъем АД) симптомами.
Интенсивность ригидности и мышечных спазмов варьирует в течение дня. Типично их исчезновение в состоянии сна. В отдельных случаях наблюдается спастический статус (частые интенсивные спазмы), угрожающий развитием тяжелой аритмии, сердечной недостаточности, грубых дыхательных расстройств, ДВС-синдрома, шока.
Диагностика синдрома «ригидного человека»
Трудности диагностики СРЧ связаны с его редкой встречаемостью и необходимостью исключить все другие возможные причины ригидности. В ходе осмотра невролог обращает внимание на отсутствие какой-либо неврологической симптоматики, кроме мышечной ригидности и повышения сухожильных рефлексов. Дифференцировать синдром «ригидного человека» следует от сирингомиелии, спинального инсульта, опухоли спинного мозга, миелита, торсионной дистонии, миотонии, болезни Паркинсона.
Основным параклиническим методом диагностики выступает ЭФИ нервно-мышечной системы. Электронейрография не выявляет нарушений проведения импульсов по нервным стволам. Электромиография обнаруживает постоянную активность мышечных двигательных единиц, сохраняющуюся, когда пациент пытается расслабить мышцу или напрягает мышцы-антагонисты. При этом форма потенциалов действия не изменена. Воздействие внешних раздражителей (электростимуляции, шума, прикосновения) приводит к усилению ЭМГ-активности, провоцирует одновременное сокращение мышц-антагонистов. Характерно исчезновение мышечной ригидности при введении диазепама или миорелаксантов, блокаде периферического нерва.
Биопсия мышц может выявлять атрофические и фиброзные изменения мышечных волокон, которые могут быть следствием ишемии, развивающейся в результате продолжительных интенсивных сокращений. С целью выявления сопутствующей патологии проводятся лабораторные анализы, исследование цереброспинальной жидкости, МРТ головного мозга, КТ или МРТ позвоночника. У пациентов, имеющих синдром «ригидного человека», зачастую диагностируются и другие заболевания: витилиго, ретинопатия, пернициозная анемия, гипотиреоз и др. По различным данным 30-50% пациентов имеют сахарный диабет I типа.
Лечение и прогноз синдрома «ригидного человека»
Проводимая терапия направлена на купирование спазмов и ригидности. Хороший эффект достигается при применении бензодиазепинов (диазепама, клоназепама). Лечение стартует с минимальной дозы, принимаемой 1-2 раза в сутки. Затем происходит наращивание дозировки с разделением суточной дозы на 3-4 приема. При достижении эффекта в виде отсутствия спазмов и уменьшения ригидности дозу препарата перестают повышать. Типичной для пациентов является хорошая переносимость больших дозировок бензодиазепинов. Однако у ряда больных достигнуть эффективной лечебной дозы не получается из-за сильного седативного действия препаратов. В таких случаях назначается баклофен — агонист ГАМК-рецепторов. Он может назначаться в комбинации с бензодиазепинами, что позволяет достигнуть лечебного эффекта при более низких дозировках препаратов. В тяжелых случаях производится интратекальная инфузия баклофена при помощи имплантированной помпы.
В случаях неэффективности или непереносимости указанного выше лечения препаратами выбора становятся вальпроаты, тиагабин, вигабатрин. Возможно введение ботулотоксина в околопозвоночные мышцы. Уменьшению ригидности способствует коррекция сопутствующей патологии (гипотиреоза, сахарного диабета и пр.). На основе аутоиммунной этиопатогенетической гипотезы СРЧ были разработаны иммунотерапевтические методы лечения. Однако их эффективность различна у разных пациентов. Хорошо зарекомендовали себя комбинация плазмафереза и глюкокортикостероидов, внутривенное введение иммуноглобулина. Неэффективность всех указанных лечебных методик является показанием к назначению цитостатической терапии.
Синдром «ригидного человека» имеет серьезный прогноз. Характерно медленное прогрессирование. У ряда пациентов удается стабилизировать состояние и сохранить возможность самообслуживания путем симптоматической терапии, у других — ригидность прогрессирует и, не смотря на осуществляемое лечение, по прошествии нескольких лет делает их постельными больными. Обездвиженность ведет к возникновению застойной пневмонии, являющейся в большинстве случаев причиной смертельного исхода. У некоторых пациентов причиной летального исхода становятся тяжелые вегетативные расстройства или диабетическая кома.
Источник
Синдром ригидного человека — СРЧ (stiff person syndrome) — представляет собой достаточно редкое и часто сложно диагностируемое иммунозависимое заболевание центральной нервной системы, характеризующееся прогрессирующей мышечной ригидностью, нарушениями ходьбы и болезненными спазмами в аксиальных мышцах и конечностях (с одновременным сокращением мышц-агонистов и антагонистов), которые могут провоцироваться внешними стимулами, а также постоянной непроизвольной активностью двигательных единиц, выявляемой при нейро-физиологическом обследовании (впервые данное заболевание было описано F. Moersch и H. Woltman у 14 пациентов в 1956 г., в связи с чем существует еще одно его название — синдром Мерша-Вольтмана).
Частота встречаемости СРЧ в настоящее время оценивается как один случай на миллион населения. Возраст манифестации варьирует в пределах 13 — 81 лет (средний возраст 46 лет), однако описаны редкие случаи дебюта в детском и даже младенческом возрасте. Среди пациентов преобладают женщины (2/3).
[1] Ведущим признаком СРЧ является ригидность, начинающаяся обычно с тораколюмбальных параспинальных мышц, в среднем на четвертом десятилетии жизни без каких-либо видимых провоцирующих факторов, и распространяющаяся на проксимальную мускулатуру конечностей и мышцы живота. В конечном итоге у пациентов формируются ригидная «роботоподобная» походка и поясничный гиперлордоз, возникают ограничения наклонов туловища и самостоятельной ходьбы. [2] Вторым патогномоничным для СРЧ признаком являются болезненные мышечные спазмы, которые часто возникают внезапно и могут приводить к падениям. Выраженность ригидности и спазмов флюктуирует, провоцируется внешними физическими и эмоциональными стимулами, холодом, интеркуррентными инфекциями.
СРЧ имеет разную клиническую феноменологию, выделяют [1] «синдром ригидной конечности», [2] СРЧ с миоклонусом (jerking stiff persone syndrome), [3] СРЧ, ассоциированный с эпилепсией и дистонией, [4] СРЧ с нейроофтальмологическими проявлениями — аутоиммунной ретинопатией, [5] церебеллярную форму СРЧ с атаксией и дисметрией, а также [6] прогрессирующей энцефаломиелит с ригидностью и миоклонусом (progressive encephalomyelitis with rigidity and myoclonus) — крайне редкий вариант СРЧ с поражением серого вещества мозга, стволовыми симптомами и выраженной дизавтономией. Обратите внимание: СРЧ c другими неврологическими проявлениями, помимо мышечных ригидности и спазмов (эпилепсия, стволовые знаки, дизавтономия и т.п.), иногда называют СРЧ-плюс синдромы.
СРЧ считается аутоиммунным заболеванием. Эффекты ГАМК-ергической нейротрансмиссии ингибируются в результате взаимодействия специфических антител c глутаматдекарбоксилазой — ГДК (от англ. glutamate decarboxylase) — фермента, участвующего в синтезе g-аминомасляной кислоты, а также с пресинаптическими и постсинаптическими протеинами, в результате нарушается функция тормозных нейронов головного и спинного мозга.
Обратите внимание! Выделяют следующие три патогенетических формы СРЧ: [1] классическую аутоиммунную (часто ассоциированную с другими аутоиммунными заболеваниями), [2] паранеопластическую (ассоциированную с мелкоклеточным раком легких, раком груди, лимфомами и другими онкопроцессами) и [3] СРЧ-плюс синдромы.
Наиболее часто при СРЧ выявляются антитела к ГДК, которая представлена в двух изоформах — 65 кДа (ГДК65) и 67 кДа (ГДК67). СРЧ обычно ассоциирован с антителами к ГДК65 (анти-ГДК65). Анти-ГДК65 связаны со множеством неврологических (СРЧ и его подвиды, лимбический энцефалит, эпилепсия, мозжечковая атаксия) и неневрологических (сахарный диабет типа 1, диффузный токсический зоб и зоб Хашимото, пернициозная анемия) патологий. Многие из этих соматических заболеваний, особенно часто сахарный диабет типа 1, поскольку ГДК экспрессируют клетки поджелудочной железы, выявляются у пациентов с СРЧ. По последним данным, около 80% больных с СРЧ имеют анти-ГДК65 и около 60% — анти-ГДК67. При СРЧ, особенно при паранеопластическом его варианте, выявляются антитела и к другим ассоциированным с рецептором g-аминомасляной кислоты протеинам – амфифизину и гефирину, а также к рецептору глицина.
читайте также пост: Лимбический энцефалит (на laesus-de-liro.livejournal.com) [читать]
Нарушение ГАМК-ергической нейротрансмиссии лежит в основе клинической картины СРЧ — постоянной активности двигательных единиц, формирующей непрерывные одновременные сокращения мышц-агонистов и антагонистов (мышечную ригидность), повышенной чувствительности к внешним стимулам, гиперэкплексии, дизавтономии, нейропсихиатрических проявлений синдрома (тревожность, беспокойство, депрессия, фобии, панические атаки). При игольчатой электромиографии у пациентов с СРЧ выявляется постоянная активность двигательных единиц в отсутствие произвольного сокращения мышцы, которая исчезает при введении диазепама.
При морфологическом исследовании биоптатов мышечной ткани в случаях СРЧ не выявляется какой-либо патологии, либо могут обнаруживаться неспецифические изменения в виде атрофии, фиброза, дегенерации и регенерации, иногда отека и инфильтрации мышечных волокон, которые связывают с ишемией, вызванной интенсивными длительными мышечными сокращениями.
Таким образом, были сформулированы диагностические критерии СРЧ (M.Dalakas, 2009):
[1] наличие мышечной ригидности в аксиальных параспинальных мышцах и мускулатуре живота, приводящей к поясничному гиперлордозу;
[2] наличие мышечных спазмов, провоцируемых тактильными и эмоциональными стимулами;
[3] отсутствие другого неврологического заболевания, могущего объяснить эти симптомы;
[4] постоянная активность двигательных единиц по данным электромиографии;
[5] выявление специфических антител по данным иммуногистохимии и радиоиммунного анализа.
Поскольку патогенез СРЧ включает в себя аутоиммунный компонент и нарушение ГАМК-ергической нейротрансмиссии, то в лечении используется воздействие на оба этих компонента. Активно применяются иммуносупрессивная и иммуно-модулирующая терапия: глюкокортикоиды (преднизолон или Метипред), цитостатики (азатиоприн, циклофосфамид), внутривенные иммуноглобулины, курсы плазмафереза. На ГАМК-ергическую трансмиссию наилучшим образом при СРЧ влияет диазепам в крайне высоких дозах — до 75 мг/сут. Интересно, что пациенты с СРЧ хорошо переносят такие высокие дозировки диазепама. Применяют также баклофен (до 75 мг/сут), антиконвульсанты (Финлепсин, вальпроаты). Как правило, эффект лечения достигается от совместного применения иммуносупрессивной терапии и препаратов, усиливающих ГАМК-ергическую нейротрансмиссию.
Прогноз при СРЧ сложный. Большинство больных инвалидизируются на фоне нарастающей ригидности, теряют способность к самостоятельному передвижению, в том числе и из-за болезненных мышечных спазмов, возникающих при любом движении. Паранеопластический СРЧ и СРЧ с выраженной дизавтономией могут стать причиной гибели пациента.
Подробнее о синдроме СРЧ в следующих источниках:
по материалам статьи «Синдром ригидного человека с миоклонусом и дизавтономией: описание случая А.В. Сердюк, Е.А. Ковражкина (Портал Consilium Medicum: журнал «Неврология и ревматология«» (Прил.) 2017; №09 : 65-68) [читать];
статья «Спектр неврологических синдромов, ассоциированных с антителами к глутамат-декарбоксилазе» М.Ю. Краснов, Э.В. Павлов, М.В. Ершова, С.Л. Тимербаева, С.Н. Иллариошкин; ФГБНУ «Научный центр неврологии», Москва (журнал «Анналы клинической и экспериментальной неврологии» №4 2015) [читать];
статья «Синдром ригидного человека с глазодвигательными и мозжечковыми нарушениями» Н.Н. Яхно, В.В. Голубева, Ю.В. Мозолевский, О.Е. Зиновьева, Э.А. Катушкина, Б.С. Шенкман, И.Н. Чистяков, З.А. Подлубная, И.М. Вихлянцев; Клиника нервных болезней им. А.Я. Кожевникова ММА имени И.М. Сеченова, Москва; Институт медикобиологических проблем РАН, Москва; Институт теоретической и экспериментальной биофизики РАН, Москва (журнал «Анналы клинической и экспериментальной неврологии» №4, 2007) [читать];
статья «Синдром ригидного человека с дебютом в грудном возрасте» С.А. Мальмберг, Е.Л. Дадали, Д.Б. Жумаханов, А.Х. Джаксыбаева; Кафедра клинической физиологии и функциональной диагностики Института повышения квалификации ФМБА России, Москва; ФГБУЗ «Центральная детская клиническая больница» ФМБА России; ФГБНУ «Медико-генетический научный центр», Москва; Национальный научный центр материнства и детства; Республика Казахстан, Астана (журнал «Нервно-мышечные болезни» №2, 2015) [читать]
Источник
