Синдром раздраженного кишечника клинический случай
Синдром раздраженного кишечника (СРК) — первая функциональная патология, описана впервые в 1849 г. Cumming. C позиций понимания нормальной и патологической физиологии, существовавшей в то время, ученые не могли объяснить наличие у одного и того же пациента нарушений стула в виде поноса и запора. За прошедшие 150 лет наука продвинулась, но большое количество вопросов осталось, особенно в отношении группы функциональных заболеваний, в том числе и СРК.
М.Ф.Осипенко
ГБОУ ВПО Новосибирский государственный медицинский университет Минздрава России
Синдром раздраженного кишечника (СРК) — первая функциональная патология, описана впервые в 1849 г. Cumming. C позиций понимания нормальной и патологической физиологии, существовавшей в то время, ученые не могли объяснить наличие у одного и того же пациента нарушений стула в виде поноса и запора. За прошедшие 150 лет наука продвинулась, но большое количество вопросов осталось, особенно в отношении группы функциональных заболеваний, в том числе и СРК.
Клинический случай
На прием обратилась пациентка 36 лет, менеджер по профессии. Образованный человек, пристально следящий за своим здоровьем. Ее беспокоили абдоминальные боли, сочетающиеся с нарушением стула, — неустойчивый, временами совсем неоформленный, учащенный по утрам. Изредка — чувство переполнения в эпигастрии после съеденной необильной пищи. Временами — подташнивание без рвоты. Симптомы усиливаются несколько раз в неделю, особенно в рабочие дни. Боли в мышцах, пояснице, спонтанно возникающие, тазовые боли, постоянное чувство разбитости и усталости. Состояние ухудшается перед менструациями за 3–5 дней. Отмечаются колебания массы тела. Пациентка планировала беременность и хотела убедиться в том, что симптоматика не угрожает ее жизни и вынашиванию беременности, желала получить рекомендации как улучшить качество жизни.
Из анамнеза: больна около 5 лет после перенесенной острой лямблиозной инфекции с лихорадкой и длительным периодом восстановления. Многократно лечилась от «дисбактериоза», дважды у нее обнаружены лямблии в кале, получала противопаразитарную терапию. В связи с тазовыми болями многократно исключали гинекологическую патологию.
Инструментальное обследование: фиброэзофагога стродуоденоскопия (ФЭГДС) без патологии. Ультразвуковое исследование: лабильный перегиб желчного пузыря.
Получала разные препараты (спазмолитики, смекта, антибиотики и др.). Эффект был неустойчивый. С подросткового возраста выставлялся диагноз «вегето-сосудистая дистония». Периодически перед выходом на учебу в школе и институте сильные приступы тошноты. У родственников (матери, младшей сестры) — вегето-сосудистая дистония.
При объективном исследовании: болезненность в местах прикрепления сухожилий конечностей, чувствительная пальпация толстой кишки, небольшое вздутие живота.
Диагноз: СРК с преобладанием диареи, постинфекционный СРК (ПИ-СРК). Функциональная диспепсия. Фибромиалгия. Хроническая тазовая боль (рис. 1).
К факторам, предрасполагающим развитию ПИ-СРК, относятся:
- бактериальная инфекция, протозойная инфекция, гельминты чаще, чем вирусы;
- длительность течения соответствующей инфекции;
- курение;
- наличие поражения слизистой кишечника;
- женский пол;
- депрессия, ипохондрия;
- назначение антибактериальных препаратов;
- возраст моложе 60 лет.
Если рассматривать данный клинический случай с позиции предрасполагающих к развитию ПИ-СРК факторов, то у пациентки имеют место: протозойная инфекция длительного, рецидивирующего течения, женский пол, молодой возраст.
Рис. 1. Варианты СРК.

Подтверждение диагноза является непростой задачей. Еще 20 лет назад врачи были твердо уверены, что функциональная патология — это диагноз исключения, для постановки которого требовалось исключение всех нозологических форм. В настоящее время в мире доминирует концепция, что в случае четкого соответствия критериям, в том числе и с учетом длительности, вероятность СРК как самостоятельной нозологической формы составляет 90% (92–98%). Исключениями являются ситуации, в которых помимо полного соответствия критериям нет симптомов «тревоги». В приведенном клиническом случае у пациентки не было ни одного симптома «тревоги», присутствовали небольшие колебания массы тела, которые были отчетливо связаны с психоэмоциональными ситуациями. При отсутствии симптомов тревоги необходимо исключить те основные заболевания, которые могут иметь схожую картину с СРК. В качестве скрининга рекомендуется: С-реактивный белок, гормоны щитовидной железы, исследование на целиакию, кал на яйца глист.
При доминирующей стойкой диарее следует исключить инфекцию Clostridium difficile, глютеновую энтеропатию; при отягощенной наследственности (воспалительные, опухолевые заболевания кишечника) проводится колоноскопия с биопсией с целью исключения органических заболеваний, в том числе и микроскопического колита.
Пациентке были проведены обследования: гормоны щитовидной железы, антитела к эндомизию и трансглутаминазе, общий уровень иммуноглобулина A + ФЭГДС с биопсией из двенадцатиперстной кишки, С реактивный белок, тест на C. difficile, кальпротектин, панкреатическая эластаза.
Проведенные анализы не подтвердили наличия у пациентки другой патологии, что позволило оставить первоначальный диагноз.
Основы терапии СРК
Ключевым моментом в терапии СРК являются правильные отношения «врач—пациент». Не следует обнадеживать пациента с функциональной патологией полным излечением, на данном этапе сделать этого врач не в состоянии. Пациента можно успокоить, что данное заболевание не представляет угрозы для жизни и ее продолжительности и существуют эффективные лекарственные средства, позволяющие добиться улучшения или длительной ремиссии.
Необходимо подчеркнуть хроническую причину симптомов: в 75% болезнь длится 5 лет и более. Существенным компонентом терапии СРК является дополнительная альтернативная медицина: когнитивная гипнотерапия, релаксационные методики, динамическая психотерапия, акупунктура/»прижигание» болевых активных точек с воздействием через систему эндогенных нейротрансмиттеров, физическая активность, йога, использование ряда лекарственных препаратов (алоэ, мятное масло, пробиотические препараты).
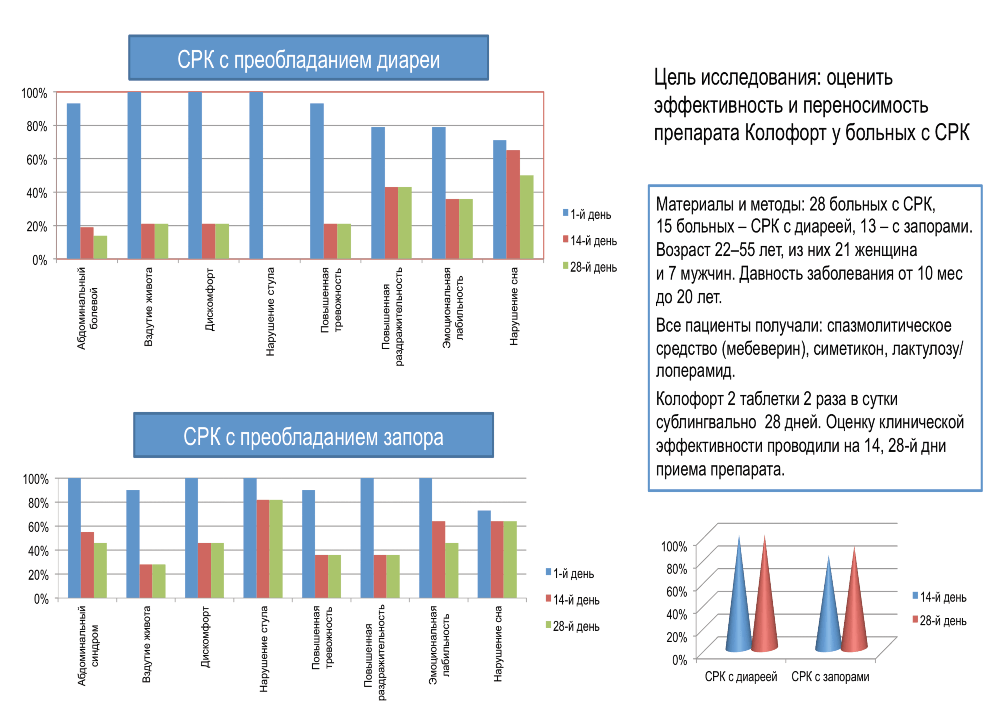
В рамках новых подходов к терапии СРК обращает на себя внимание применение препарата Колофорт. Более 15 доклинических исследований препарата и его компонентов было проведено in vitro, in vivo, ex vivo в России, Франции, Бельгии. На моделях животных современными методами было показано деликатное действие Колофорта и на иммунное воспаление, и на функциональную активность рецепторов гистамина, и на серотонинергические рецепторы, представлена спазмолитическая активность препарата. Также было показано, что препарат обладает противоотечным и анальгетическим действием. Нами был проведен небольшой пилотный проект, включивший 28 пациентов с СРК, продемонстрировавший хорошую эффективность и переносимость препарата в большей степени у пациентов с СРК с диареей (рис. 2).
Рис. 2. Пилотный проект.

Руководствуясь этими данными, мы рекомендовали пациентке Колофорт по 2 таблетки 2 раза в день в течение 1 мес.
Важным аспектом терапии становится питание:
- Ограничение определенных продуктов в случае установления выявления четкой связи между их употреблением и усугублением симптомов.
- Ограничение жира улучшает течение СРК.
- Ограничение углеводов (ферментируемые олиго-, ди- и моносахариды и полиолы — FODMAPs) — фруктанты, галактаны, лактоза, фруктоза, сорбитол, ксилитол, маннитол и т.д. — диета 1-й линии при СРК.
Следует исключить из рациона: артишоки, свеклу, капусту, грибы, лук, чеснок, кукурузу, редис, сельдерей, яблоки, абрикосы, вишню, черешню, нектарины, персики, груши, виноград, манго, арбуз, сухие фрукты, соки фруктовые, мед, сорбитол, маннитол, молоко, сыры, масло по переносимости.
При назначении питания следует учитывать наличие лактазной недостаточности.
Новые данные появились по применению спазмолитиков у этих больных. По результатам исследования рекомендовано использование спазмолитиков по тре бованию в те дни, когда пациентов беспокоит абдоминальная боль.
Терапия диарейного синдрома заключается в выявлении стрессора, провоцирующего гастроколитический рефлекс. Назначают для купирования диареи лоперамид, холестирамин и др.
Применение антидепрессантов также показало высокую эффективность в лечении пациентов с СРК.
Терапия, назначенная пациентке:
- Разъяснение сути болезни.
- Физическая активность.
- Колофорт по 2 таблетки 2 раза в день 1 мес.
- FODMAPs free-питание.
- Спазмолитики, смекта при необходимости в режиме «по требованию».
- Психотерапевтическая помощь.
Через месяц у больной была отмечена положительная динамика: пациентка спокойна, большая часть симптомов была купирована.
В настоящее время в мире разрабатывается большое количество новых молекул, предназначенных для терапии СРК, что позволяет и врачам и пациентам смотреть в будущее с оптимизмом.
Таким образом, в ходе симпозиума «Новое лекарственное средство. Синдром раздраженного кишечника: новые ответы на старые вопросы» были представлены современные концепции этиологии, патогенеза и терапии заболевания. Все докладчики были единодушны во мнении, что на сегодняшний день доказано наличие иммуно-воспалительных изменений при СРК, это ставит под сомнение функциональную природу заболевания. Кроме того, активную роль в формировании патогенеза СРК играют психологические и стрессовые факторы. Многоуровневый механизм формирования симптомов у пациентов с СРК предполагает комплексный патогенетический подход к его терапии. Колофорт — единственный комбинированный лекарственный препарат для лечения СРК, который воздействует на ключевые звенья патогенеза СРК, что клинически проявляется снижением интенсивности абдоминальной боли, коррекцией моторно-эвакуаторной дисфункции, анксиолитическим и антидепрессивным действием, а также снижением висцеральной гиперчувствительности. Колофорт рекомендован для лечения пациентов с разными вариантами СРК, что позволяет эффективно контролировать заболевание вне зависимости от его клинических проявлений.
Источник
Случай из практики
В отделение гастроэнтерологии в плановом порядке поступила женщина 29 лет, которую беспокоят упорные запоры до 4–5 сут. Задержка стула сопровождается нарастанием ощущения тяжести в нижних отделах живота, вздутия живота, переходящего в эпизоды кишечной колики. После дефекации все абдоминальные симптомы полностью разрешаются.
В отделение гастроэнтерологии в плановом порядке поступила женщина 29 лет, которую беспокоят упорные запоры до 4–5 сут. Задержка стула сопровождается нарастанием ощущения тяжести в нижних отделах живота, вздутия живота, переходящего в эпизоды кишечной колики. После дефекации все абдоминальные симптомы полностью разрешаются.
Жалобы на проблемы со стулом отмечались еще с детства, в 15 лет рентгенологически была выявлена долихосигма, неоднократно лечилась и обследовалась стационарно, но добиться положительной динамики опорожнения кишки не удалось. Для регуляции стула пациентка использовала обогащение рациона пищевыми волокнами, свечи с глицерином, клизмы. Более 10 лет наблюдается невропатологами с диагнозом «неврастения», получает нейротропное лечение.
Ухудшение состояния стала отмечать полгода назад, когда пыталась регулировать массу тела ограничительной диетой (на текущий момент индекс массы тела – 16 кг/м2 при нижней границе нормы 18,5 кг/м2).
При обследовании выявлены перетяжка в шейке желчного пузыря, поверхностный гастрит с явлениями гастростаза и дуодено–гастрального рефлюкса. Уровень тиреоидных гормонов в нормальных пределах. Бариевая клизма подтвердила наличие долихосигмы, также отмечается значительное опущение поперечно–ободочной кишки, после попытки опорожнения барий сохраняется как в правой, так и в левой половине ободочной кишки.
При общении обращают на себя внимание высокий уровень тревожности пациентки и заметная эмоциональная лабильность. При оценке с помощью вопросника IBSQoL (36 вопросов) выявлено снижение качества жизни до 72,3%, индекс тяжести ВЕSТ – 42,1%, что свидетельствует о серьезной тяжести заболевания.
Сбор диетологического анамнеза выявил избыточное среднесуточное потребление белка – 114,2 г/сут. (оптимально 75 г/сут.), потребление жира составило 64,4 г/сут. при сниженном потреблении углеводов – 67 г/сут. (оптимально – 300 г/сут.), содержание пищевых волокон в рационе – 11 г/сут., калорийность – 1305 ккал/сут. (фактический расход энергии – 2253 ккал/сут.).
При применении водородно–метанового дыхательного теста с лактулозой выявлен избыточный рост метаногенной флоры (пик метана – 72 ррм).
Исследование функциональной активности аноректальной зоны выявило снижение выносливости (17 с при норме от 25 с) при длительном сокращении сфинктера, снижение кашлевого и ректоанального ингибиторного рефлекса. При баллонной оценке рецепторного аппарата выявлено снижение чувствительности – первое ощущение возникло при 40 мл наполнения (норма – 20 мл), хотя ощущение первого позыва осталось в нормальных пределах – 110 мл. Полученные результаты свидетельствуют о серьезном нарушении работы нервно–мышечного аппарата кишки.
Больная консультирована психотерапевтом, который диагностировал астено–депрессивное состояние, произведена коррекция психотропной терапии.
Представленный случай интересен тем, что у данной пациентки совмещается значительное количество различных факторов, патогенетически значимых в рамках синдрома раздраженного кишечника (СРК) с запорами. Помимо явлений висцеральной гиперчувствительности, встречающейся наиболее часто у пациентов с СРК, в данном случае присоединение депрессии и избыточного роста метаногенной флоры на фоне нерационально построенного питания усилило выраженность задержки стула. Подобное сочетание патогенетических механизмов плохо поддается лечению по общепринятым стандартам и вызывает трудности ведения таких пациентов у врачей первичного звена: пациенты обращаются к ним снова и снова, а как помочь в случае, когда привычные лекарственные средства не работают, врач не знает – пациент становится «трудным».
Проблема
СРК является представителем функциональных заболеваний кишечника с очень широкой распространенностью среди населения развитых стран. Согласно определению Римских критериев III пересмотра, для СРК характерно наличие абдоминальной боли/дискомфорта, имеющих связь с нарушениями опорожнения кишечника. Пациенты с СРК очень часто страдают от внекишечных проявлений – нарушения сна, тревоги, депрессии, дизурии [3].
По современным представлениям в основе патогенеза СРК – наличие висцеральной гиперчувствительности, нарушение сигнального взаимодействия по оси кишка – мозг, воспаление/иммунная активация слизистой оболочки кишки из–за изменения состава микрофлоры кишечника, проявления психосоциального стресса на фоне когнитивных особенностей индивида [3]. Для клинициста в первую очередь важно исключить наличие у пациента признаков органической патологии, снять с помощью разъяснения тревожную настороженность в отношении онкологических и иных заболеваний с плохим прогнозом.
Врачу первичного звена сложно установить, какая из составляющих патогенеза СРК определяет состояние пациента в каждом конкретном случае. Общепринятой практикой ведения СРК является использование средств, направленных на нейтрализацию основного кишечного симптома, – антидиарейных препаратов, спазмолитиков, прокинетиков, разного рода слабительных и психотропных средств и т.д. При этом некоторые пациенты могут оставаться резистентными к лечению даже при назначении до 4 препаратов одновременно [2]. Новейшие серотонинергические препараты демонстрируют высокую эффективность при лечении СРК, но из–за нерешенных проблем с безопасностью их применения и переносимостью, а также высокой стоимости появления их в арсенале врача в ближайшее время ожидать не стоит [3].
Еще одна проблема состоит в том, что больными СРК из–за особенностей восприятия (тревожное ожидание) применение нескольких медицинских препаратов может восприниматься негативно – как попытка врача скрыть тяжесть болезни. Они рассуждают так: если болезнь, как утверждается, протекает доброкачественно, то зачем мне назначили такое количество таблеток? В то же время такие пациенты охотно применяют лекарственные травы для облегчения своих симптомов. Возможно, клиническая эффективность многокомпонентных препаратов растительного происхождения послужит достаточным основанием для их использования в целях многоцелевой терапии таких многофакторных заболеваний, как СРК.
В последние 5 лет осуществлен значительный прорыв в отношении понимания специфических механизмов действия веществ растительного происхождения, важных для устранения симптомов функциональной диспепсии [3]. Установлено, что значительное число трав и специй способны активировать катионные каналы семейства ТRР (Transient Receptor Potential), которые расположены в мембране чувствительных нервов по всему телу, обеспечивают способность первичного восприятия термических, химических и механических стимулов, в том числе отвечают за висцеральные ощущения и боль [4]. Экстракты трав могут избирательно активировать или блокировать ТRP–каналы, что объясняет синергические эффекты травяных сборов и служит обоснованием их терапевтического потенциала. К настоящему времени наиболее изученными в лечении заболеваний ЖКТ являются фитофармацевтический Иберогаст и масло перечной мяты [3].
Иберогаст – торговая марка препарата STW5 – фиксированной комбинации экстрактов иберийки горькой (Iberis amara), дягиля лекарственного (Angelica аrchangelica), ромашки аптечной (Matricaria chamomilla), тмина обыкновенного (Carum carvi), расторопши пятнистой (Silybum marianum), мелиссы лекарственной (Melissa officinalis), мяты перечной (Mentha piperita), чистотела майского (Chelidonium majus), солодки голой (Glycyrrhiza glabra). В клинических испытаниях STW5 продемонстрировал эффективность в устранении симптомов функциональной диспепсии и СРК за счет влияния на моторную, секреторную функции ЖКТ и коррекции гиперчувствительности за счет потенцирования эффектов входящих в состав препарата компонентов (табл. 1) [7].
Специфичность действия на моторику обусловлена возможностью компонентов Иберогаста селективно ингибировать 5–НТ4–серотонировые и М3–мускариновые рецепторы, а также связываться с рецепторами аденозина А2а при относительно низком сродстве к рецепторам серотонина 5–НТ3 [5]. Особенностями взаимодействия с рецепторами и различными типами ионных каналов объясняется регион–специфичное действие препарата, например расслабление дна и тела желудка при одновременном стимулировании фазовых сокращений антральной мускулатуры. В тонкой кишке Иберогаст способствует устранению спазма, стимулированного такими медиаторами, как ацетилхолин, гистамин, простагландин F2ά, субстанция Р, эффект опосредован ингибированием потенциала действия и волн медленных сокращений в подвздошной кишке, а в толстой кишке наблюдается подавление быстрых и медленных ингибиторных потенциалов перехода [1]. Наличие в составе препарата Иберогаст экстракта иберийки горькой позволяет добиться роста тонуса в атоничной подвздошной кишке [3]. В целом совокупность этих эффектов на моторику кишки позволяет характеризовать Иберогаст как препарат, нормализующий тонус кишечной стенки [1].
Важным механизмом устранения диспептических и кишечных симптомов является изменение активности чувствительных нервных окончаний кишечной стенки. Назначение Иберогаста внутрь снижает чувствительность подвздошной кишки к механическому растяжению, серотонину и брадикинину [3]. Доказана способность компонентов препарата (мята, тмин) связываться с рецепторами TPRV3 и TPRМ8, отвечающими за восприятие боли в органах ЖКТ [4]. В препаратах толстой кишки человека Иберогаст посредством прямого действия компонентов на хлорные каналы влияет на секрецию слизи кишечным эпителием [5].
Воспалительные изменения минимальной степени выраженности – важный патогенетический фактор функциональных заболеваний ЖКТ. Иберогаст обладает доказанным противовоспалительным эффектом, устраняющим индуцированные декстран натрия сульфатом (dextransodiumsulfate, DSS) или тринитробензенсульфонатом (trinitrobenzenesulfonate, TNBS) колиты, причем протективное действие сопоставимо с эффективностью сульфосалазина [7]. Противовоспалительное действие Иберогаста заключается в снижении экспрессии ФНОα, стимуляции ИЛ–10, антиоксидантной активности, которая может потенцировать противовоспалительные эффекты [6,7]. Таким образом, Иберогаст имеет достаточно серьезную доказательную базу для использования в качестве препарата патогенетической терапии СРК.
Тактика лечения и ее обоснование
С учетом продолжительного анамнеза заболевания пациентка нуждается в длительном курсе антидепрессантов, которые, помимо замещения нейромедиаторов, могут оказывать эффект фактора роста нервных клеток, что способствует восстановлению нейронных цепей управления эмоциональной сферой. Принимая во внимание наличие задержки стула у пациентки, мы назначили селективный ингибитор обратного захвата серотонина эсциталопрам в дозе 10 мг в утренние часы. У данной пациентки сформировался порочный круг, когда восприятие имеющихся кишечных симптомов служит источником тревоги, поэтому одновременно с антидепрессивными препаратами, которые должны смягчить тревожную настороженность пациентки, применялся Иберогаст в стандартной дозе 20 капель х 3 р./сут. для устранения моторных нарушений кишечной деятельности и явлений висцеральной гиперчувствительности.
На фоне назначенного основного варианта стандартной диеты и указанной терапии с 3–го дня лечения наблюдалось снижение интенсивности имеющихся жалоб (тяжести внизу живота), на 5–й день терапии появился спонтанный стул с неполным опорожнением (3–й день после ирригоскопии), с 10–го дня опорожнение кишечника стало полным, отмечена положительная динамика эмоционального состояния. Об улучшении состояния свидетельствовали показатели качества жизни: по вопроснику IBSQoL качество жизни повысилось до 84,5%, индекс тяжести BEST снизился до 28%. Контроль аноректальной манометрии, выполненный через 12 дней, выявил восстановление нормальной величины порога возбуждения аноректальной зоны – при проведении баллонной пробы первое ощущение возникло при 20 мл наполнения, отмечен рост выносливости (22 с) при длительном сокращении сфинктера.
Устранение симптомов и улучшение общего самочувствия пациентки можно было бы приписать влиянию психотропной терапии, а не эффектам компонентов Иберогаста, но, как известно [8], начало проявления эффектов антидепрессантов наступает, самое раннее, через 2 нед. от начала лечения, а в данном случае мы наблюдали положительную динамику симптомов уже с 3–го дня терапии, что подтверждает эффективность именно Иберогаста и хорошо согласуется с результатами клинических и экспериментальных исследований.
Учитывая наличие избыточного роста бактерий в тонкой кишке, кажется оправданным назначение препаратов с антибактериальным действием, но это назначение было отложено на 2–й этап терапии, так как имеется достаточно высокая вероятность разрешения избыточного роста на фоне нормализации моторики кишки. Если в домашних условиях не наступит полная нормализация опорожнения кишечника в течение 2–х мес., то проведение мероприятий по подавлению метаногенной флоры будет вполне оправданным. Весьма перспективным представляется использование в лечении СРК с избыточным ростом бактерий в тонкой кишке комбинации Иберогаста как прокинетика с пробиотиком, например S. boulardii. Однако в данной ситуации, когда основные жалобы разрешились при применении сочетания антидепрессанта и Иберогаста, принято решение отказаться от добавления пробиотика ввиду того, что начало приема такого препарата часто сопровождается усилением урчания и газообразования в кишечнике, что может повлиять на уровень тревожности пациентки и подорвать ее доверие к назначенной схеме лечения из–за возвращения некоторых симптомов.
Литература
1. Ammon H.P.T., Kelber O., Okpanyi S.N. Spasmolytic and tonic effect of Iberogast (STW5) in intestinal smooth muscle // Phytomedicine. 2006. Vol. 13. P. 67–74.
2. Brierly S.M., Kelber O. Use of natural products in gastrointestinal therapies // Current Opinion in Pharmacology. 2011. Vol. 11. P. 604–611.
3. Chang F.Y., Lu C.L. Treatment of Irritable Bowel Syndrome using complementary and alternative medicine // J Chin Med Assoc. 2009. Vol. 72. № 6. Р. 294–299.
4. Holzer P. Transient receptor potential (TRP) channels as drug targets for diseases of the digestive system // Pharmacology & Therapeutics. 2011. Vol. 131. P. 142–170.
5. Simmen U., Kelber O., Okpanyi S.N. et al. Binding of STW5 (Iberogast) and its components to intestinal 5–HT, muscarinic M3 and opioid receptors // Phytomedicine 2006. Vol. 13. P. 51–55.
6. Wagner H. Multitarget therapy – the future of treatment for more than just functional dyspepsia // Phytomedicine. 2006. Vol. 13. P. 122–129.
7. Wegener T., Wagner H. The active components and the pharmacological multi–target principle of STW 5 (Iberogast) // Phytomedicine 2006. Vol. 13. P. 20–35.
8. Изнак А.Ф., Поздеева Е.А., Изнак Е.В. «Чистые» стереоизомеры – новое направление повышения эффективности антидепрессантов (обзор литературы) // Сonsilium medicum. Обозрение психиатрии и медицинской психологии им. В.М. Бехтерева. 2008. № 1. С. 8–13.
Источник
