Синдром поражения клубочков у детей

Поражение клубочков почек детей. Патогенез гломерулонефрита
Патология клубочков может быть следствием генетических и иммунологических причин, а также нарушений свертываемости крови. К генетическим причинам относятся:
1) мутация генов, кодирующих белки клубочков, интерстиция или канальцевого эпителия;
2) мутация регуляторных генов, контролирующих транскрипцию ДНК;
3) нарушение посттранскрипционных модификаций РНК;
4) нарушение посттрансляционных модификаций белков.
Наиболее часто имеют место иммунные повреждения клубочков, приводящие к гломерулонефриту, который одновременно является и генетической формой ряда заболеваний, и гистопатологическим термином, означающим воспаление клубочковых капилляров. Признаки гломерулонефрита, вызванного иммунологическими нарушениями, включают:
1) морфологические и иммунопатологические проявления, сходные с таковыми при экспериментальном иммунном гломерулонефрите;
2) отложение в клубочках иммуноглобулинов и компонентов комплемента;
3) изменения комплемента в сыворотке крови или присутствие в ней аутоантител (например, к базальной мембране клубочков).
Существует, по-видимому, два основных механизма иммунных повреждений почечных клубочков:
1) отложение в них иммунных комплексов (антиген-антитело) и
2) взаимодействие антител с местными антигенами in situ.
В последнем случае антиген может быть как собственным нормальным компонентом клубочков (например, неколлагеновый домен (NC-1) коллагена IV типа — предполагаемый антиген при нефрите У человека, обусловленном антителами к базальной мембране клубочков), так и откладывающимся в них веществом.
При заболеваниях, обусловленных отложением иммунных комплексов, антитела образуются и связываются с антигенами, которые обычно находятся вне почек. Иммунные комплексы накапливаются в почках и активируют систему комплемента, приводя к повреждению почечной ткани. Экспериментальные исследования показывают, что такие комплексы образуются в крови и лишь откладываются в почках. Однократное внутривенное введение кроликам бычьего сывороточного альбумина приводит к развитию у животных острой сывороточной болезни.
Через 1 нед. после введения у кроликов вырабатываются антитела к бычьему сывороточному альбумину, причем антиген остается в крови в высокой концентрации. Попадающие в кровь антитела формируют иммунные комплексы с антигеном. Пока количество антигена в крови превышает количество антител (избыток антигена), эти комплексы имеют небольшие размеры и остаются растворенными в крови. Тем не менее они откладываются в почечных клубочках. Процесс отложения иммунных комплексов в почках зависит от особенностей комплексов (их концентрации, заряда и размера) и самих клубочков (способности мезангиальной ткани к захвату комплексов, отрицательного заряда капиллярной стенки), гидродинамических сил и влияния различных медиаторов (ангиотензин II, простагландины).
Отложение иммунных комплексов в клубочках приводит к развитию у кроликов острого пролиферативного гломерулонефрита. Методом прямой иммунофлюоресценции на стенках клубочковых капилляров обнаруживают гранулярные (комковатые) отложения, содержащие иммуноглобулины и компоненты комплемента. Под электронным микроскопом видно, что эти отложения располагаются на эпителиальной стороне базальной мембраны клубочков и в мезангии. Через несколько дней в кровь попадает дополнительное количество антител, несвязанный антиген в конце концов исчезает из крови, гломерулонефрит стихает. У кроликов комплемент не принимает участия в поражении капилляров; оно обусловлено в основном притоком макрофагов. Однако на других экспериментальных моделях установлено участие комплемента в повреждении капилляров.
Примером взаимодействия антител с антигеном in situ служит антительный гломерулонефрит, при котором антитела реагируют с антигенами самой базальной мембраны клубочков. Иммуногистоло-гические исследования обнаруживают при этом отложения иммуноглобулинов и комплемента в виде непрерывной полосы на базальной мембране, как при синдроме Гудпасчера и некоторых типах быстро прогрессирующего гломерулонефрита.
Воспалительная реакция, развивающаяся после иммунного повреждения, может быть обусловлена активацией нескольких механизмов. Важнейшим среди них является система комплемента, которая может активироваться иммунными комплексами по классическому пути или полисахаридами и эндотоксином по альтернативному (пропердиновому). Оба эти пути сходятся в точке образования компонента С3, после чего одна и та же последовательность реакций приводит к лизису клеточных мембран. Главные повреждающие продукты образуются после активации компонента С3. К ним относятся анафилатоксин (стимулирующий сократительные белки сосудистой стенки и увеличивающий ее проницаемость) и хемотаксические факторы (С5а), которые привлекают нейтрофилы и, вероятно, макрофаги к месту активации комплемента. Эти клетки выделяют вещества, прямо действующие на сосудистую стенку и базальную мембрану.
Система свертывания крови может активироваться непосредственно после повреждения эндотелиальных клеток (при котором обнажается тромбогенный субэндотелиальный слой и запускается каскад соответствующих реакций) или опосредованно через активацию комплемента. Отложения фибрина обнаруживаются как в самих клубочковых капиллярах, так и в боуменовом пространстве в форме полулуний. Активация процессов свертывания крови может стимулировать образование кининов, которые, в свою очередь, обладают хемотаксическими и анафилатоксиноподобными свойствами.
— Вернуться в оглавление раздела «физиология человека»
Оглавление темы «Заболевания детей»:
- Врожденные невропатии у детей. Диагностика
- Семейная вегетативная дисфункция — синдром Райли-Дея у детей. Причины
- Диагностика семейной вегетативной дисфункции — синдрома Райли-Дея. Лечение
- Врожденная нечувствительность к боли и ангидроз. Рефлекторная симпатическая дистрофия
- Синдром Гийена-Барре у детей: восходящий паралич Ландри и синдром Миллера-Фишера
- Диагностика и лечение синдрома Гийена-Барре у детей. Прогноз
- Паралич Белла у детей. Диагностика и лечение
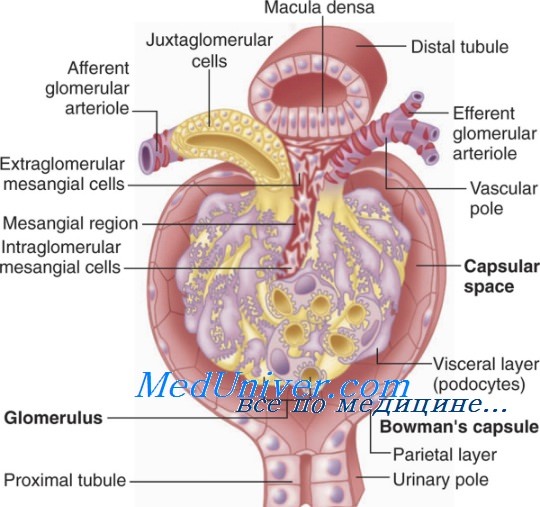
- Анатомия почечных клубочков. Строение
- Клубочковая фильтрация в почках. Механизмы
- Поражение клубочков почек детей. Патогенез гломерулонефрита
Источник
Почечная недостаточность»
ЦЕЛЬ ЗАНЯТИЯ
Ознакомить студентов с основными синдромами поражения мочевой системы, с диагностикой различных вариантов нарушения функции почек.
АННОТАЦИЯ
Формирование синдромного поражения при изменениях со стороны мочевой системы представляет большие трудности. Это вызвано тесной связью различных отделов мочевой системы друг с другом. Изолированность поражения трудно выделить и более правильно следует говорить о преимущественном поражении того или иного отдела. Также стоит отметить тот факт, что при диагностике поражения мочевой системы приходится в основном ориентироваться на лабораторную диагностику, так как физикальные данные чаще всего появляются на более поздних стадиях.
С точки зрения клинических проявлений все многообразие патологии мочевой системы удобно разделить на поражение нефрона и поражение мочевыводящих путей. В поражении нефрона выделяют синдром поражения клубочков и поражение канальцев, в котором, в свою очередь можно отметить синдром поражения проксимальных канальцев и синдром поражения дистальных канальцев. При поражении мочевыводящих путей выделяется синдром поражения верхних мочевыводящих путей и синдром поражения нижних мочевыводящих путей.
Синдром поражения клубочков
Поражение клубочков, прежде всего, связано с нарушением проницаемости базальной мембраны, как в стороны уменьшения, так и в сторону повышения этой проницаемости. Поражение базальной мембраны может быть связано с отложением иммунных комплексов, кровоизлиянием в клубочек. Клинические проявления определяются типом повреждения клубочков, размером повреждения, тяжестью течения, темпом прогрессирования, а также рядом других факторов (возраст, состояние питания и другие).
Для синдрома поражения клубочков наиболее характерны такие экстраренальные проявления, как отеки и гипертензия.
Нарушение гомеостаза в первую очередь характеризуется нарушением азотистого обмена — повышением в крови уровня мочевины, креатинина. Клинически для азотемии характерны изменения со стороны кожных покровов — сухость, мацерация. Вследствие внепочечного выделения продуктов азотистого обмена отмечается и характерный запах от больного.
Из ренальных проявлений следует отметить различную степень эритроцитурии вплоть до макрогематурии (моча имеет вид «мясных помоев»), протеинурию, цилиндрурию, снижение диуреза – нарушение мочеобразования по типу олигурии. При обследовании помимо азотемии выявляется гипопротеинемия, нарушение фильтрационной способности почек.
При поражении канальцев на первый план выступают проявления нарушения гомеостаза и, в первую очередь, электролитные нарушения. При этом следует помнить, что проксимальный каналец играет ведущую роль в реабсорбции профильтровавшихся низкомолекулярных веществ, растворенных в плазме (от 50 до 100% для отдельных веществ). Петля Генле и дистальный каналец осуществляют в большей степени реабсорбируют главные ионы и в меньшей степени воду. При этом, нижние отделы нефрона осуществляют тонкую регуляцию большинства веществ.
Нарушения функций канальцев могут быть первичные (врожденные или наследственные тубулопатии) и вторичные. При первичных поражениях канальцев возможно отставание в росте, полиурия с раннего возраста, жажда, рвота, запоры; снижение сопротивляемости к инфекциям. Выражены признаки интоксикации. Потери калия ведут к появлению признаков гипокалиемии: мышечная гипотония, гипорефлексия, понижение артериального давления. При ряде тубулопатий (фосфат-диабет) отмечается нарушение структуры костей, деформация конечностей.
Наpушения функций канальцев могут быть втоpичными – напpимеp, пpи отpавлении свинцом, действии некотоpых лекаpственных сpедств и токсинов.
Синдром поражения проксимальных канальцев
Нарушения гомеостаза при поражении проксимальных канальцев связаны с нарушением механизмов клубочкового-канальцевого равновесия и почечного порога реабсорбции. Оба механизма чрезвычайно стабильны и изолированное поражение проксимальных канальцев определяется, как правило, только при врожденной патологии. Клиническая симптоматика может широко варьировать от бессимптомной до ярко выраженных проявлений.
Наиболее характерными лабораторными признаками поражения проксимальных канальцев являются глюкозурия, аминоацидурия, селективная протеинурия (альбуминурия), нарушение фосфорно-кальциевого обмена (рахит).
Глюкозурия приводит к многообразным проявлениям нарушения углеводного обмена.
Аминоацидурия приводит к задержке развития. Довольно быстро присоединяется нефролитиаз.
Нарушение фосфорно–кальциевого баланса сопровождается гипофосфатемией, нарушением структуры костей, деформацией скелета.
При поражении проксимальных канальцев возможно развитие ацидоза вследствие нарушения реабсорбции гидрокарбонатов, что приводит к гипербикарбонатурии, гиперхлоремии.
Собственно говоря, практически мы уже очертили круг дополнительных методов исследования – это биохимическое исследование крови и мочи на предмет электролитных сдвигов, количественное определение аминокислот в крови и моче методами хроматографии и электрофореза, определение клиренса глюкозы.
Синдром поражения дистальных канальцев
Нарушения гомеостаза при поражении дистальных канальцев связаны с низкой чувствительности рецепторов канальцевого эпителия к антидиуретическому гормону и/или альдостерону, что приводит к изменениям концентрационной функции почек и водно-электролитным расстройствам. Дефект ацидогенетической функции дистальных канальцев вызывает нарушение секреции и экскреции Н+ и развитие ацидоза.
Проявлением нарушения концентрационной функции является полиурия, гипостенурия, изостенурия.
Электролитные расстройства в первую очередь касаются натрия (гипонатриемия), кальция (гипокальциемия), калия (сначала гипо-, а затем гиперкалиемия). Имеет значение и нарушение других электролитов – магния, фосфора, цинка.
Соответственно и клиническая картина в основном связана с экстраренальными проявлениями — изменения со стороны кожи, легких, желудочно-кишечного тракта, сердечно-сосудистой системы, костно-мышечной системы.
Диагностика поражения этого отдела нефрона возможна при проведении проб с водной нагрузкой, нагрузочных проб с фуросемидом и хлористым аммонием, определению ацидоаммониогенеза, исследованию экскреции электролитов с мочой.
Наряду с традиционным подходом, когда выделяется отдельный сегмент нефрона и на нем сосредоточены диагностические и терапевтические усилия, существует и другой подход, предлагаемый профессором A. Vander, – фокусирование внимания на судьбе отдельного вещества, перемещающегося по нефрону.
Проиллюстрируем это на примере уратов. У детей повышение концентрации мочевой кислоты в крови имеет место при нервно-артритическом диатезе. У взрослых повышение в плазме мочевой кислоты может вызвать подагру.
Мочевая кислота находится в плазме в форме ионизированных уратов, не связанных с белками и легко фильтрующихся. В проксимальном отделе нефрона они активно секретируются и здесь же осуществляется их реабсорбция. В норме скорость реабсорбции гораздо выше, чем секреции. Поэтому с мочой выводится лишь часть профильтровавшихся уратов. Но секреция уратов является и механизмом регулирования их концентрации в плазме. При увеличении количества уратов в плазме из-за более активного образования увеличивается секреция в проксимальных канальцах и нарастает выделение их с мочой.
Следовательно, в каждом клиническом случае у пациента с повышением концентрации мочевой кислоты в плазме или подагрой важно определить, какие факторы, или их сочетания являются ведущими в генезе патологического процесса — снижение фильтрации уратов из-за уменьшении скорости клубочковой фильтрации; избыточная реабсорбция или недостаточная их секреция.

Источник
Синдром острого поражения клубочков проявляется нарушением мочеотделения (олигурия, анурия) и патологическими изменениями мочи (протеинурия, гематурия, цилиндрурия, эпителиальные клетки и липоиды, нередко лейкоцитурия).
Олигурия является одним из ранних и частых симптомов острого гломерулонефрита и проявляется почти одновременно с головной болью, болью в пояснице и гипертонией. Диурез может уменьшаться до 80—100 мл в сутки при очень высоком удельном весе мочи (1040— 1050 и более). В отдельных случаях наступает кратковременная анурия.
Олигурия, анурия — следствие экстраренальной задержки жидкости в организме и отчасти нарушения фильтрационной функции клубочков. Она исчезает на 4—6-й день после назначения постельного режима.
Боль в пояснице (симптом Пастернацкого) объясняют гиперемией почек и растяжением их капсулы. Явления дизурии (частые и болезненные мочеиспускания) при остром гломерулонефрите редки и непродолжительны. Они встречаются в основном у детей раннего возраста (до 3—5 лет), а также у детей при осложнении гломерулонефрита пиелоциститом или циститом.
Протеинурия — постоянный симптом острого гломерулонефрита. Уровень белка в моче колеблется от следов до 30%о и выше. Более высокие показатели белка в моче наблюдаются у детей до 5 лет. Белок мочи, как и белок сыворотки крови, состоит из альбуминовых и глобулиновых фракций, поэтому в настоящее время общепринятым считается происхождение протеинурии из крови. Проникновение белка в мочу обусловлено повреждением подоцитов эпителиальных клеток клубочковых капилляров, базальных мембран и эндотелия.
Гематурия — один из важнейших и характерных признаков острого гломерулонефрита, имеющих большее диагностическое значение. В большинстве случаев это микрогематурия (число выщелоченных эритроцитов не превышает 20—40 экземпляров в поле зрения). Механизм гематурии объясняют проникновением эритроцитов через поврежденную стенку капилляров клубочка в связи с ее повышенной проницаемостью.
Лейкоцитурия при остром гломерулонефрите — нередкое явление. Интенсивность ее более выражена у детей дошкольного возраста. Происхождение лейкоцитурии связывают с аутоиммунными процессами, разыгрывающимися в почечной паренхиме. В случаях пиурии на фоне клиники гломерулонефрита при большом содержании эпителия почек и лоханок речь идет об островоспалительном генезе.
Цилиндрурия. В осадке мочи находят гиалиновые, зернистые, реже эпителиальные цилиндры. Цилиндры состоят из свернувшихся белковых масс, перерожденного эпителия канальцев и реже из форменных элементов крови. Наличие эритроцитных цилиндров во многих случаях является диагностическим признаком острого гломерулонефрита. Эпителиальные цилиндры и липоиды обнаруживаются чаще при тяжелом течении заболевания.
Существенную помощь в ранней диагностике острого гломерулонефрита, назначении патогенетической терапии и в прогнозе оказывают показатели азотистых веществ в крови и моче и состояние функции почек.
Показатели свободной пробы, или пробы по Зимницкому, очень ценны. Они обнаруживают в отдельных порциях малое количество мочи высокого удельного веса. Содержание остаточного азота в крови непостоянно и бывает нормальным или несколько повышенным (50— 70 мг%). Повышение остаточного азота в крови происходит за счет мочевины и в меньшей степени за счет креатинина и аминокислот. Параллельно, как правило, повышается уровень мочевины крови. Весьма характерно для выраженной формы острого гломерулонефрита уменьшение клубочковой фильтрации до 30—40 мл/мин (норма 80—120 мл/мин] и очищение крови от мочевины (ниже 50% при норме 50—150%).
Ранняя стадия заболевания часто сопровождается гиперхлоремией и нарушением кислотно-щелочного равновесия с уменьшением щелочного резерва.
Источник
Предклубочковые функциональные нарушения почек. Клубочковый синдром.
Предклубочковые функциональные нарушения имеют некоторые общие черты с клубочковыми нарушениями, так как они могут привести к уменьшению клубочкового кровотока. Прежде всего это приводит к артериальной гипертонии. Поразительно, что кровоток нарушается, как правило, не настолько значительно, чтобы наступило недостаточное выведение шлаков. Остаточный азот, следовательно, повышен лишь в очень небольшом числе случаев, т. е. больной с общими сосудистыми нарушениями обычно не доживает до уремической фазы. Смерть наступает раньше от других осложнений (главным образом от кровоизлияния в мозг, сердечной недостаточности).
Однако имеются также случаи с длительным повышением остаточного азота. Кратковременное повышение (терминальное) остаточного азота при злокачественном нефросклерозе Фара (Fahr) является правилом. Протеинурия, гематурия и отеки при чистом прегломерулярном функциональном нарушении не наблюдаются. Поэтому отсутствие их имеет большое дифференциально-диагностическое значение.
Клубочковый синдром характеризуется следующими признаками.
1. Повышенная проницаемость клубочков:
а) гематурия;
б) протеинурия.
2. Уменьшение клубочкового кровотока и недостаточное выведение ультрафильтрата:
а) задержка:
1) шлаковых продуктов белкового обмена — остаточного азота — азотемия;
2) фосфатов — гиперфосфатемия;
3) электролитов — гиперкалиемия, а также задержка натрия и хлора;
4) воды — отек;
б) артериальная гипертония (вследствие повышенного образования ренина в ответ на недостаточный кровоток);
в) олигурия до степени анурии.
Эти симптомы не при всех болезненных состояниях клубочков выражены в одинаковой степени, что ведет к различным клиническим проявлениям.
Канальцевые (тубулярные) синдромы у взрослых встречаются обычно в менее чистой форме, чем у детей. Так, если у детей могут наблюдаться такие нарушения функции проксимальных канальцев, как почечная глюкозурия и гипо- и гиперфосфатемия, в основе чего лежит недостаток ферментов, то у взрослых мы практически находим лишь почечный диабет и как следствие сильно повышенной канальцевой активности псевдогипопаратиреоидизм (Олбрайт), протекающий с гиперфосфатемией.
Синдром Фанкони (глюкозурия, фосфатурия, аминоацидурия) в юношеском возрасте встречается очень редко.
Синдром поражения дистальных отделов канальцев может быть подразделен на острый и хронический. Дистальные отделы канальцев значительно больше подвержены экзогенным повреждениям, так как вследствие концентрации мочи в этом отделе вещества осаждаются гораздо легче и повреждают тем самым канальцы. Кроме того, из-за своего положения на границе между корковым и мозговым веществом эти отделы канальцев менее защищены от восходящих почечных инфекций, а также межуточного отека и фиброза.
Острый тубулярный синдром [нефроз-нижнего нефрона (lower nephron nephrosis) американских авторов] характеризуется в первую очередь олигурией, которая может перейти в анурию, и сопровождается шоковым состоянием. Этот синдром ренальной аноксии встречается после обширных размозжений тканей (crush syndrom), переливаний несовместимой крови, быстрого распада форменных элементов крови, при ожогах, после приема плохо растворимых сульфаниламидов. Белки, гемоглобин и сульфаниламиды выводятся при этих состояниях клубочками и повреждают дистальные отделы канальцев.
— Также рекомендуем «Подостро-хронический дистальный тубулярный синдром. Заболевания с повреждением клубочков почек.»
Оглавление темы «Заболевания почек.»:
1. Двусторонние заболевания почек. Болезни почек.
2. Предклубочковые функциональные нарушения почек. Клубочковый синдром.
3. Подостро-хронический дистальный тубулярный синдром. Заболевания с повреждением клубочков почек.
4. Нефрозы. Липоидный нефроз. Нефротический синдром.
5. Диффузный геморрагический гломерулонефрит. Клиника диффузного гломерулонефрита.
6. Течение диффузного гломерулонефрита. Прогрессирующий хронический гломерулонефрит.
7. Поражения канальцев почек. Обессоливающий нефрит.
8. Межуточный нефрит. Хронический межуточный нефрит.
9. Восходящий пиелонефрит. Почечная недостаточность вследствие затрудненного оттока мочи.
10. Оценка состояния функции почек. Удельный вес мочи.
Источник
