Синдром линча и колоректальный рак
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 мая 2018;
проверки требуют 22 правки.
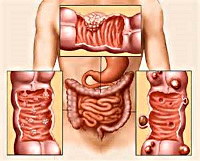
Злокачественное новообразование толстого кишечника — злокачественная опухоль толстой кишки и её придатка — червеобразного отростка.
Вследствие неточного перевода английского термина (англ. colorectal cancer) часто обобщённую группу таких опухолей называют упрощённо колоректальным раком, хотя в русском языке это более узкий термин (не включающий в себя, в частности, лимфому толстого кишечника); английский же термин охватывает также и рак прямой кишки.
Эпидемиология[править | править код]
Каждый год, по данным Груздевой Е.С., в мире выявляется более 600 тысяч новых случаев рака толстой кишки. В России заболеваемость составляет около 50 тысяч новых случаев в год. Далеко не все случаи колоректального рака выявляются даже на поздней стадии, показатель составляет не более 70 %.
Этиология[править | править код]
Рак толстой кишки — полиэтиологическое заболевание, то есть может иметь под собой множество причин. К ним относятся: генетические факторы, факторы внешней среды (включая питание, канцерогены), воспалительный процесс в кишечнике.
Хотя генетика колоректального рака остается до конца не раскрытой, последние исследования показывают её большое значение в развитии болезни. Так, наследственная мутация в гене APC (англ.)русск. является причиной семейного аденоматозного полипоза (англ.)русск., при котором у пациента имеется почти 100 % вероятность развития рака толстой кишки к возрасту 40 лет[1].
В возникновении колоректального рака прослеживается два пути: из обычных аденом, начинающийся с мутации гена APC (модель Fearon-Vogelstein) и по «зубчатому пути», который отличается уникальным генетическим профилем и морфологическими характеристиками уже на начальных этапах развития образований. Такие образования занимают от 7-9 %. Риск развития рака из них составляет 7,5-15 %. Предшественниками эпителиальных образований являются очаги абберантных крипт. Около 20 % колоректального рака продемонстрировали распространенные дефекты в метилировании ДНК (так называемый CIMP-положительный профиль), мутации в онкогенах BRAF (KRAS), микросателлитную нестабильность, и многие из них могут возникнуть в рамках зубчатых образований и определяют их морфологическое строение. Зубчатый полипозный синдром так же имеет специфические генетические изменения, связанные с биаллельной мутацией гена MUTYH. Риск развития колоректального рака при этом синдроме очень высок и может составлять более 50 %, возможно наличие синхронных или метахронных раковых опухолей. Они, как правило, сопровождаются MSI-H и представлены зубчатой морфологией. Понимание эпигенетического пути и молекулярных особенностей зубчатых поражений дает представление об их клинической значимости и обеспечивает доказательства, необходимые для лечения и наблюдения пациентов с этим заболеванием.
Синдром Линча (англ.)русск. (наследственный рак толстой кишки без полипоза) также связан с высоким риском возникновения рака толстой кишки в возрасте до 50 лет. В отличие от семейного аденоматозного полипоза, при синдроме Линча чаще страдает проксимальный отдел толстой кишки. Пациенты с данным синдромом также подвержены высокому риску развития рака яичников и тела матки в молодом возрасте. Синдром обусловлен ошибками репликации в генах hMLH1, hMSH2, hMSH6, hPMS1, hPMS2 и, возможно, других, ещё не известных[2][3][4].
Факторы риска[править | править код]
- Диетические — употребление пищи, бедной клетчаткой и богатой твердыми животными жирами.
- Употребление алкоголя[5].
- Ожирение.
- Курение[6].
- Воспалительные заболевания кишечника.
По результатам исследования, опубликованным в Журнале Клинической Онкологии (Journal of Clinical Oncology), курильщики с раком толстого кишечника имеют в два раза более высокий риск смерти по сравнению с некурящими людьми[7].
Также была проведена работа, опубликованная в журнале Gut (The BMJ journals), результаты которой свидетельствуют, что длительное применение антибиотиков в молодом и среднем возрасте увеличивает риск появления колоректальных аденом, склонных к малигнизации[8]. Ученые исследовали связь между длительной антибиотикотерапией (более 2 месяцев) в возрасте 20-39 лет и 40-59 лет с развитием аденоматозных полипов. Все участники прошли колоноскопию, по результатам которой было выявлено, что у 1195 из 16642 участников обнаружены колоректальные аденомы. Проведя анализ доступных данных, исследователи заключили, что применение антибиотиков более 2 месяцев у лиц в возрасте 20-39 лет приводит к риску возрастания полипов на 36 %, а в возрасте 20-59 лет — на 69 %. Высокий риск перехода аденомы в злокачественную опухоль был подтвержден многочисленными исследованиями. Риск развития рака прямой и ободочной кишки у лиц с аденоматозными полипами в 3-5 раз выше, чем у обычной популяции.
Диагностика[править | править код]
- Колоноскопия с биопсией
- Ирригоскопия
- СКТ органов малого таза, брюшной полости
- УЗИ ОБП, ОМТ
Прогноз[править | править код]
По причине поздней диагностики летальность от этого заболевания довольно высока и достигает 40 % в течение года с момента выявления болезни.
Наиболее частым органом, в который метастазирует колоректальный рак, является печень. Это обусловлено особенностями венозного оттока от кишечника, который осуществляется через систему воротной вены печени. По данным некоторых авторов, наличие метастазов в печени при колоректальном раке достигает 50 % (Curtiss, 1995).
Другим частым меcтом рецидива колоректального рака является брюшина. Перитонеальный канцероматоз выявляется примерно у 10% пациентов с только что установленным диагнозом. В случае рецидива, брюшина поражается примерно в 60% изолированно, либо вместе с печенью.
По данным Viganò пятилетняя выживаемость у пациентов с метастазами колоректального рака в печени без специфического лечения не превышает 2 %, а медиана выживаемости колеблется в пределах 6,6—10 мес[9].
В настоящее время смертность после резекций печени по поводу метастазов колоректального рака составляет менее 6 %, а в крупных специализированных клиниках менее 3 %[10].
Лечение[править | править код]
Большинство пациентов с установленным раком толстой кишки является кандидатами на операцию. Суть операции заключается в удалении части толстой кишки, несущей опухоль, и лимфоузлов, в которых могут быть обнаружены метастазы.
Послеоперационное гистологическое исследование обязательно во всех случаях. Во время него оценивается удаленный орган: сохранность мезоректальной или мезоколической фасций, уровень инвазии опухоли, количество лимфатических узлов в препарате и сколько из них поражены метастазами, расстояние от опухоли до края резекции.
Химиотерапия (FOLFIRI и др.).
Химиотерапия в сочетании с кетогенной диетой в одном исследовании на малом числе пациентов показала чуть более хорошие результаты[11][значимость факта?]
Примечания[править | править код]
- ↑ Tomislav Dragovich, MD, PhD. Colon Cancer (англ.). Medscape. Дата обращения 8 октября 2015.
- ↑ Lengauer C., Kinzler K. W., Vogelstein B. Genetic instabilities in human cancers //Nature. — 1998. — Т. 396. — №. 6712. — С. 643—649.
- ↑ Lynch H. T. et al. Etiology, natural history, management and molecular genetics of hereditary nonpolyposis colorectal cancer (Lynch syndromes): genetic counseling implications //Cancer Epidemiology Biomarkers & Prevention. — 1997. — Т. 6. — №. 12. — С. 987—991.
- ↑ Angioli R. et al. Hereditary and sporadic ovarian cancer: genetic testing and clinical implications (review) //International journal of oncology. — 1998. — Т. 12. — №. 5. — С. 1029—1063.
- ↑ Колоректальный рак. www.euro.who.int (5 февраля 2018). Дата обращения 5 февраля 2018.
- ↑ Модифицируемые факторы риска развития рака. // Факторы риска развития рака. Пер. с англ. Н. Д. Фирсова(2017).
- ↑ Люди с раком толстого кишечника, которые курят, имеют вдвое более высокий риск смерти. Euroonco.ru. Дата обращения 25 марта 2015.
- ↑ Long-term use of antibiotics and risk of colorectal adenoma Длительное применение антибиотиков и риск колоректальной аденомы
- ↑ Viganò L., Ferrero A., Lo Tesoriere R., Capussotti L. Liver surgery for colorectal metastases: results after 10 years of follow-up. Long-term survivors, late recurrences, and prognostic role of morbidity // Ann Surg Oncol, 2008, 15 (9). — P. 2458—2464. Epub 2008 May 8.
- ↑ Wang X., Hershman D. L., Abrams J. A., Feingold D., Grann V. R., Jacobson J. S., Neugut A. I. Predictors of survival after hepatic resection among patients with colorectal liver metastasis // British Journal of Cancer, 2007, 97 (12). — P. 1606—1612. Epub 2007 Dec 11.
- ↑ Kenji Furukawa, Kyosuke Shigematus, Yoshie Iwase, Wakako Mikami, Hiroko Hoshi. Clinical effects of one year of chemotherapy with a modified medium-chain triglyceride ketogenic diet on the recurrence of stage IV colon cancer. // Journal of Clinical Oncology. — 2018-05-20. — Т. 36, вып. 15_suppl. — С. e15709–e15709. — ISSN 0732-183X. — doi:10.1200/JCO.2018.36.15_suppl.e15709.
Ссылки[править | править код]
- Предраковые заболевания толстой и прямой кишки
- Побочное следствие от потери гена ТР53 при колоректальном раке подсказало новую стратегию его лечения
Источник
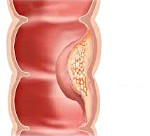
Синдром Линча – наследственное заболевание, сопровождающееся развитием злокачественных новообразований в толстом кишечнике. Клинические проявления аналогичны другим видам колоректального рака. Отличительными особенностями являются раннее начало, высокая частота первично-множественных опухолей и преимущественное поражение правых отделов толстого кишечника. При синдроме Линча-II колоректальный рак сочетается с внекишечными злокачественными неоплазиями. Диагноз выставляется с учетом семейного анамнеза, иммуногистохимических тестов, колоноскопии, ирригоскопии, биопсии и других исследований. Лечение – операции, химиотерапия.

Общие сведения
Синдром Линча (наследственный неполипозный колоректальный рак) – генетически обусловленное заболевание, при котором наблюдается развитие злокачественных опухолей толстого кишечника. Передается по аутосомно-доминантному типу. Составляет около 3% от общего количества случаев колоректального рака. В 30% случаев при синдроме Линча отмечается возникновение синхронных или метахронных неоплазий. В ряде случаев новообразования толстой кишки сочетаются с онкологическими поражениями яичников, матки, мочевого пузыря, почечной лоханки, мочеточника, желудка, желчных путей и тонкого кишечника.
Риск развития онкологического заболевания у больных синдромом Линча с подтвержденной генетической мутацией колеблется от 30 до 80%. Отличительной особенностью является раннее начало заболевания. Злокачественные опухоли при синдроме Линча обычно диагностируются в возрасте до 50 лет, на 10-15 лет раньше, чем в среднем по популяции. Средний возраст появления первых симптомов составляет 44 года. Около 70% неоплазий локализуются в правой половине толстого кишечника. Лечение проводят специалисты в сфере онкологии, абдоминальной хирургии и гастроэнтерологии.

Синдром Линча
Причины развития и классификация синдрома Линча
Причиной развития являются мутации генов, ответственных за ошибки репарации ДНК: PMS2, MSH6, MSH2 и MLH1. Возможно сочетание нескольких мутаций с соответствующим увеличением риска возникновения злокачественных новообразований. Выявляется аутосомно-доминантный характер наследования. Обычно у больных с синдромом Линча диагностируются слизистые аденокарциномы или перстневидно-клеточный рак. Для опухолей характерен низкий уровень дифференцировки клеток при редком метастазировании, хорошем ответе на терапию и относительно благоприятном прогнозе.
Различают два типа заболевания: синдром Линча-I и синдром Линча-II. Первый вариант протекает без внекишечных проявлений, единственным признаком заболевания является раннее развитие множественных неоплазий толстого кишечника при отсутствии предшествующего полипоза. При синдроме Линча-II наблюдается сочетание аденокарцином толстой кишки и злокачественных опухолей других локализаций. Обычно страдают внутренние женские половые органы, возможно также поражение вышележащих отделов пищеварительного тракта. Вероятность развития рака эндометрия при синдроме Линча-II составляет от 30 до 60%, риск возникновения новообразований других локализаций – 10-15%.
Симптомы синдрома Линча
До появления злокачественных опухолей толстого кишечника симптоматика отсутствует. При развитии неоплазий клинические проявления соответствуют ненаследственному колоректальному раку. Наблюдаются боли, нарушения аппетита, расстройства стула, слабость и анемия. Из-за высокого расположения новообразований кровь в кале при синдроме Линча визуально обычно не определяется. Выраженность и характер болевого синдрома существенно варьируют. Обычно пациенты жалуются на ноющие либо тянущие боли слабой или средней интенсивности. Реже у больных синдромом Линча возникает кратковременная приступообразная боль, напоминающая боли при остром холецистите или остром аппендиците.
При пальпации достаточно крупных опухолей определяются малоподвижные узлы плотно- или мягкоэластической консистенции. При прогрессировании злокачественного новообразования у больных синдромом Линча выявляются симптомы интоксикации, возникшие из-за распада неоплазии, и явления кишечной непроходимости, обусловленные препятствием прохождению каловых масс по кишечнику. При отдаленном метастазировании наблюдаются нарушения функций соответствующих органов. Отмечаются выраженная слабость, эмоциональная лабильность, склонность к депрессиям, повышение температуры и прогрессирующее истощение.
Симптомы опухолей других локализаций при синдроме Линча также соответствуют ненаследственным формам онкологических поражений тех или иных органов. Рак эндометрия и рак яичников на начальных стадиях могут протекать бессимптомно. В последующем при раке эндометрия наблюдаются боли, кровянистые, серозные или серозно-сукровичные выделения. При распространении новообразования на соседние органы возникают расстройства дефекации и мочеиспускания. Для рака яичников характерны ощущение дискомфорта, увеличение живота, нарушения менструального цикла и т. д.
Диагностика синдрома Линча
До появления злокачественных новообразований синдром Линча диагностируют на основании семейной истории и данных генетических исследований. Из-за незначительной распространенности в популяции проведение всеобщих скрининговых обследований считается нецелесообразным, генетические анализы выполняют только при выявлении соответствующего семейного анамнеза. Анамнестическими критериями синдрома Линча являются наличие гистологически подтвержденных карцином толстого кишечника у трех или более близких родственников, являющихся представителями двух или более поколений, а также один или несколько случаев начала заболевания в возрасте младше 50 лет.
Для обнаружения характерных для синдрома Линча генетических мутаций используют иммуноферментные исследования и тест на микросателлитную нестабильность. При появлении клинических признаков заболевания пациентов с синдромом Линча направляют на ирригоскопию и колоноскопию. Выполняют анализ кала на скрытую кровь. Осуществляют УЗИ, КТ или МРТ брюшной полости. План обследования больных синдромом Линча с подозрением на злокачественные опухоли женских половых органов и верхних отделов ЖКТ составляют с учетом установленных стандартов для неоплазий соответствующих локализаций. Перечень исследований при подозрении на отдаленное метастазирование определяют с учетом предположительного расположения вторичных очагов.
Лечение и профилактика при синдроме Линча
Всех пациентов с подтвержденной наследственной мутацией рассматривают, как представителей группы риска. Больным с синдромом Линча необходимо пожизненное диспансерное наблюдение, включающее в себя регулярные осмотры онколога и гастроэнтеролога, проведение колоноскопии 1 раз в 1-2 года, начиная с 25 лет, фиброгастродуоденоскопии и УЗИ брюшной полости – 1 раз в 1-2 года, начиная с 30 лет. Женщинам с синдромом Линча проводят регулярные гинекологические осмотры. Инструментальные обследования назначают 1 раз в 1-2 года, начиная с 30 лет.
При возникновении злокачественной опухоли толстого кишечника предпочтительным вариантом для больных синдромом Линча является субтотальная колэктомия. Это хирургическое вмешательство позволяет увеличить продолжительность жизни и обеспечивает более благоприятный прогноз по сравнению с частичной резекцией толстой кишки. Учитывая влияние удаления значительной части толстого кишечника на качество жизни пациентов, решение о проведении подобной операции принимают после подробного разъяснения последствий вмешательства. Вопрос о целесообразности химиотерапии при синдроме Линча пока остается дискутабельным, хотя некоторые исследователи указывают на достаточно высокую эффективность иринотекана.
Синдром Линча — лечение в Москве
Источник
Синдром Линча — обусловленное генетической мутацией состояние, проявляющееся значительно более частым развитием злокачественных новообразований в некоторых органах, чаще всего в толстой кишке и матке. Как правило, проявления синдрома наследуются из поколения в поколение, что помогает выявлению носителей неблагоприятной мутации и принятию мер по раннему распознаванию злокачественного процесса.
Причина развития синдрома
Причины развития большинства спорадических злокачественных новообразований недостаточно изучены, чуть лучше дело обстоит с наследуемыми из поколения в поколения карциномами.
В начале прошлого века американский морфолог Альфред Уотин нашёл семью немецких эмигрантов, где в каждом поколении были больные раком, чаще толстой кишки, а иногда матки и желудка. Довести исследование до логического завершения не получилось из-за смерти учёного.
Через полвека и ныне здравствующий американский онколог Генри Линч среди своих пациентов нашёл две семьи в каждом поколении имевшие больных раком толстой кишки, причём опухоль у большинства возникала в молодом возрасте. Позже выяснилось, что у всех больных была мутация в одном из генов MMR, отвечающих за сборку ДНК после случайных поломок.
Каждый ребенок от больного родителя получал одну нормальную нить ДНК и вторую с «испорченным» геном — такой тип передачи называется аутосомно-доминантным, отчего в каждом поколении семьи обязательно появлялись онкологические больные.
Как показали последующие исследования, мутантные гены значительно увеличивали скорость малигнизации, если кишечный полип до рака в среднем «растёт» от 10 до 15 лет, то при генетическом сбое на это требуется меньше 3 лет.
Запись
на консультацию
круглосуточно
Какие варианты заболевания встречаются?
На основании клинических проявлений были выделены варианты наследственного заболевания:
- Синдром Линча I — у молодых членов семьи развивается только рак толстого кишечника.
- Синдром Линча II — кроме рака кишки возникают и другие злокачественные опухоли.
- Болезнь Мюир-Торре — толстокишечный рак сочетается с множественными доброкачественными и злокачественными кожными новообразованиями, исходящими из сальных желез и волосяных фолликулов.
- Истинный синдром Тюрко — колоректальный рак и злокачественная опухоль головного мозга — глиобластома.
Ассоциированные с синдромом Линча опухоли
Самое частое проявление генетического дефекта — колоректальный рак (КРР), из всех кишечных карцином 3–5% связаны с синдром Линча. Риск развития опухоли очень высок и достигает 75%, причём инициация злокачественного заболевания чаще всего случается до 50-летия.
Высока вероятность развития рака тела матки, но почти вдвое ниже КРР. Эндометрий при синдроме поражается много раньше, чем в общей популяции, и в большинстве случаев сопровождает вхождение женщины в климактерический период.
Много меньше, но выше популяционного риск, возникновения рака яичников, карциномы желудка и мужской мочевыделительной системы, злокачественных опухолей головного мозга.
Нет однозначных доказательств повышения вероятности при мутации в генах MMR карцином молочной, предстательной и поджелудочной желез.
Нечасто у носителей генетической мутации в коже возникают похожие на шелушащиеся бородавки кератоакантомы и «кофейные» пятна.
Диагностика синдрома Линча
Первоначально носителей генетической мутации выявляют по медицинской истории семьи, где в разных поколениях было хотя бы три раковых больных. Методика опроса по «Амстердамским критериям II» выясняет у кого с учётом степени кровного родства и в каком возрасте выявляли злокачественные новообразования. Чувствительность методики невысока, дополнительные критерии Bethesda улучшают результаты опроса, но таким способом не удается выявить более четверти наследников синдрома.
Сегодня для диагностики наследственного заболевания используют специальные компьютерные программы. Окончательный диагноз выставляется после молекулярно-генетического исследования, обнаруживающего мутации в генах. Генетику необходимо выполнить и всем кровным родственникам больного, чтобы наблюдать их и вовремя обнаружить рак.
Положительных по генетическим мутациям пациентов с 30–35 лет регулярно обследуют:
- Женщинам ежегодно выполняется гинекологический осмотр с УЗИ и берут кровь на онкомаркер СА-125;
- Мужчины каждый год сдают анализ мочи;
- Вне зависимости от половой принадлежности каждые 2–3 года выполняется гастроскопия и анализы на хеликобактерную инфекцию, которую необходимо лечить.
Зачем нужен анализ на микросателлитную нестабильность?
Важный анализ при кишечной карциноме — выявление микросателлитов ДНК в опухолевых клетках, результат определяет прогноз заболевания и влияет на выбор лечения. Микросателлитная нестабильность (МСН, MSI) коррелирует с распространенностью кишечной карциномы, так при II стадии обнаруживается у каждого пятого, при IV — у каждого 25 больного.
В нормальной клетке регулярно случаются поломки ДНК, но легко устраняются, поэтому нить ДНК остается «как прежде». Мутация генов репарации может приводить к образованию в разорванной ДНК ни единственной правильной «заплатки», а множества дефектных «заплаток», составленных из обрывков разной длины, но из одной и той же «ткани» нуклеиновых кислот — это и есть микросателлиты.
При небольшой опухоли МСН выступает маркером хорошего прогноза и позволяет отказаться от профилактической химиотерапии, при запущенном заболевании — всё ровно наоборот. При выявлении микросателлитной нестабильности в клетках обычного спорадического рака в схему химиотерапии включают платиновые производные, в исследованиях отмечена высокая результативность иммуноонкологических препаратов.
При подозрении на наследственное заболевание, но отрицательных Амстердамских критериях у выходцев семейных кланов, часто сталкивающихся со злокачественными заболеваниями, обнаружение микросателлитной нестабильности позволяет установить синдром Линча. Нестабильности микросателлитов не обязательна для клеток обычной карциномы, но практически не бывает синдрома Линча без МНС, поэтому при известных исторических семейных обстоятельствах она признаётся маркером генетической патологии.
Особенности кишечной карциномы при наследственной патологии
При синдроме Линча значительно ускорено развитие рака из полипа, из-за чего болезнь развивается не в преддверии 70-летия, как при обычном злокачественном процессе, а в возрасте «чуть за» 40 лет. Курение и избыточный вес мужчины тоже повышают скорость малигнизации полипов.
Поражаются преимущественно правые отделы кишечника, что совсем не характерно для спорадического рака, как правило, такая локализация отмечается только у каждого третьего больного. Генетические опухоли часто высокой степени злокачественности и нередко с метастазами в лимфоузлах, но выживаемость пациентов выше, чем при спорадическом КРР.
При синдроме после оперативного лечения высока вероятность появления опухоли в другом отделе кишечника и с течением времени рецидивов всё больше.
Стандартная тактика лечения таких пациентов не разработана, в некоторых случаях рассматривается больший объём оперативного вмешательства, но всё очень индивидуально.
Профилактика развития злокачественных новообразований
Профилактика колоректального рака — своевременное удаление полипов, клинические исследования показали, что при синдроме Линча прием аспирина несколько снижает скорость малигнизации. В отношении других злокачественных процессов меры профилактики не разработаны, основной упор делается на регулярные обследования на протяжении всей жизни.
Самое разумное для носителей мутации не просто проходить регулярное обследование в районной поликлинике, а непременно в онкологическом учреждении, где знают все «болевые точки» таких пациентов и могут предложить превентивное лечение.
Запись
на консультацию
круглосуточно
Список литературы:
- Burn J., Bishop T., Mecklin J.P. et al./Effect of aspirin or resistant starch on colorectal neoplasia in the Lynch syndrome//N Engl J Med 2008; 359
- Giardiello F.M., Allen J.I.; Axilbund J.E. et al./Guidelines and Management of Linch Syndrome: A Consensus Statement by the us Multi-Society Task Force on Colorectal Cancer// Disease of the colon and rectum; 2014, V57
- Hampel H., Frankel W.L., Martin E. et al./Screening for the Lynch syndrome (hereditary non polyposis colorectal cancer)//N Engl J Med 2005; 352
- Kastrinos F./Inherited Colorectal Cancer Syndrome// Cancer J; 2011, V17
- Pérez-Cabornero L., Infante M., Velasco E., et al./ Genotype-phenotype correlation in MMR mutation-positive families with Lynch syndrome//Intern J of Colorectal Disease; 2013, V28
- Piñol V, Castells A, Andreu M et al./Accuracy of the revised Bethesda guidelines, microsatellite instability, and immunohistochemistry for the identification of patients with hereditary non polyposis colorectal cancer// JAMA 2005; 293
- Umar A, Boland CR, Terdiman JP et al./Revised Bethesda guidelines for hereditary non polyposis colorectal cancer (Lynch syndrome) and microsatellite instability//J Natl Cancer Inst 2004; 96
Источник
