Синдром эванса фишера код мкб

Синдром Фишера-Эванса (ФЭС)- это заболевание, сочетающее в себе аутоиммунную анемию гемолитического вида и тромбоцитопению.
 ФЭС является редким диагнозом, хотя точная частота неизвестна.
ФЭС является редким диагнозом, хотя точная частота неизвестна.
Впервые французские исследователи сообщили о выявлении семи детей с ФЭС из 164 случаев ITP и 15 случаев АИГА.
Перед вами фрагмент клинической рекомендации из Медицинской экспертной системы Консилиум. Развернуть рекомендацию полностью вы можете в системе. Если вы не подписчик, воспользуйтесь пробным доступом.
Никакой гендерной, этнической специфичности не было отмечено. Средний возраст на презентации колебался от 5 до 7 лет, общий возрастной диапазон – 0–2 и 6–26 лет.
В трех крупных клиниках во Франции ФЭС диагностирован у 36 детей за 1990–2002 годы, средний возраст 5 лет.
Количество детей с ФЭС составляет от 10 до 24,9 процента среди пациентов с аутоиммунной гемолитической анемией и тромбоцитопенией.
↯
Больше статей в журнале
«Заместитель главного врача»
Активировать доступ
Диагнозы по МКБ
D69.3 Идиопатическая тромбоцитопеническая пурпура
За последние годы появились работы о роли трипептидил пептидазы (tripeptidyl peptidase II) (TPP2).
Дефицит TPP2 выявляется при ФЭС и предрасположенности к вирусным инфекциям. ТРР2 блокирует пролиферацию Т-клеток и продолжительность жизни лимфоцитов.
Би-аллельные мутации ТТР2 обусловливают раннее развитие ФЭС.
Примерно в 50 процентах случаев ФЭС ассоциируется с аутоиммунопатологическими процессами, иммунодефицитными, лимфопролиферативными состояниями.
Жалобы и анамнез
Чаще болезнь начинается исподволь: больные жалуются на боли в суставах, животе, субфебрильную температуру.
Позднее присоединяются умеренная слабость и одышка, на коже обнаруживаются геморрагии (экхимозы, петехии), кровоизлияния в слизистую оболочку рта, конъюнктиву, наблюдаются носовые и маточные кровотечения.
Проявления геморрагического синдрома: внутренние и наружные кровотечения, кровоизлияния могут предшествовать появлению клинических и лабораторных признаков иммунного гемолиза. В некоторых случаях гемолиз начинается раньше.
У ряда больных анемия и тромбоцитопения выявляются одновременно.
Тромбоцитопения может развиться через несколько лет после спленэктомии, выполненной по поводу аутоиммунной гемолитической анемии, при этом признаки гемолиза могут отсутствовать.
Физикальное обследование
В ходе общеклинического осмотра обращает на себя внимание проявление геморрагического, анемического синдромов. Значимых изменений со стороны внутренних органов нет.
Единичные авторы описывают незначительную спленомегалию. Клиническая картина характеризуется анемией, высоким ретикулоцитозом и непрямой гипербилирубинемией, сочетающимися с тромбоцитопенией, то есть симптомами, свойственными аутоиммунной гемолитической анемии и тромбоцитопенической пурпуре.
Проявления геморрагического синдрома представлены обильными гематомами, профузными носовыми, маточными кровотечениями, множественными разнокалиберными геморрагиями на слизистых и кожных покровах.
Реабилитация и амбулаторное лечение
Срок диспансерного наблюдения даже у пациентов, достигших полной клинико-иммунологической ремиссии, – не менее 10 лет с учетом высокого риска рецидивирования и развития иных проявлений иммунопатологических процессов.
Вакцинация по индивидуальному графику в соответствии с рекомендациями для пациентов с первичными имммунодефицитными состояниями.
Педиатрические пациенты с аутоиммунными мультилинейными цитопениями после завершения диагностики, коррекции основного симптомокомплекса нуждаются в динамическом наблюдении с целью профилактики рецидивов и диагностики вторых лимфопролиферативных синдромов, других первичных иммунодефицитов и аутоиммунных заболеваний.
На фоне длительного течения ФЭС описано развитие Т-клеточной лимфомы, вовлечение в патологический процесс других органов – почек, щитовидной железы.
Развитие международного регистра для таких пациентов необходимо, чтобы улучшить понимание их сложной естественной истории.
Профилактика и диспансерное наблюдение
Специфическая профилактика ФЭС не разработана. К рекомендациям общего характера относится элиминация/ограничение действия эндогенных и экзогенных неблагоприятных факторов, стимулирующих иммунопатологические реакции организма.

Алгоритмы лечения, протоколы первичного приема, новые формы ИДС, памятки для пациентов и врачей — читайте и скачивайте материалы на www.provrach.ru
Источник
Фишера-Эванса синдром (J. A. Fisher; R. S. Evans, совр. американский врач; синдром; син. синдром Эванса) — сочетание аутоиммунной гемолитической анемии с аутоиммунной тромбоцитопенией.
Заболевание впервые описал Фишер в 1947 г. и предположил иммунный генез анемии и тромбоцитопении. Эванс и сотр. в 1951 г. более подробно описали клинику аутоиммунной гемолитической анемии (см.), сочетающейся с аутоиммунной тромбоцитопенией (см.). Выделяют симптоматическую и идиопатическую форму Фишера-Эванса синдрома.
Симптоматическая форма наблюдается при хроническом гепатите, системной красной волчанке, хроническом лимфолейкозе, лимфоме, саркоме, лимфогранулематозе, ревматоидном артрите, туберкулезе и др. В редких случаях синдром является первым проявлением этих заболеваний. При идиопатической форме установить связь гемолиза и тромбоцитопении с каким-либо другим патологическим процессом не удается.
В основе патогенеза лежит повышенное разрушение эритроцитов и тромбоцитов вследствие фиксации на их поверхности белков иммуноглобулиновой природы — аутоантител (см.). Антиэритроцитарные антитела чаще являются неполными тепловыми агглютининами (см. Агглютинация) и принадлежат к иммуноглобулинам (см.) различных классов (G, реже — M или A). Они специфически связываются с антигенами системы резус (см. Группы крови); в нек-рых случаях направлены против антигенов других систем. Специфичность антитромбоцитарного иммуноглобулина класса G (антител) не установлена, однако доказано, что его содержание на поверхности эритроцитов по сравнению с нормой увеличено. Разрушение эритроцитов и тромбоцитов осуществляется преимущественно в селезенке, иногда в печени и костном мозге. В связи с этим продуцирование кроветворных клеток в костном мозге увеличено, в миелограмме (см.) отмечается увеличение содержания эритроидных клеток и мегакариоцитов (см. Кроветворение).
Клиническая картина характеризуется анемией, высоким ретикулоцитозом и непрямой гипербилирубинемией, сочетающимися с тромбоцитопенией, т. е. симптомами, свойственными аутоиммунной гемолитической анемии (см.) и тромбоцитопенической пурпуре (см. Пурпура тромбоцитопеническая). Чаще болезнь начинается исподволь; больные жалуются на боли в суставах, животе, субфебрильную температуру. Позднее присоединяется умеренная слабость и одышка, на коже обнаруживаются геморрагии (экхимозы, петехии), кровоизлияния в слизистую оболочку рта, конъюнктиву, наблюдаются носовые и маточные кровотечения. Геморрагический синдром (внутренние и наружные кровотечения, кровоизлияния) может предшествовать появлению клин, и лаб. признаков иммунного гемолиза (см.). В нек-рых случаях гемолиз начинается раньше. У ряда больных анемия и тромбоцитопения выявляются одновременно. Тромбоцитопения может развиться через несколько лет после спленэктомии (см.), выполненной по поводу аутоиммунной гемолитической анемии, при этом признаки гемолиза могут отсутствовать.
Диагноз устанавливают на основании клин, картины и прямой пробы Кумбса (см. Кумбса реакция), подтверждающей аутоиммунный характер гемолиза. Отрицательные результаты пробы Кумбса не исключают наличия у больного иммунного гемолиза, т. к. при усилении гемолиза значительная часть нагруженных антителами эритроцитов разрушается. Установить гемолиз помогает также обнаружение повышенного содержания в крови ретикулоцитов, укорочения продолжительности жизни эритроцитов, увеличения клеток эритроидного ряда в костном мозге. При выявлении тромбоцитопении и повышенного (или нормального) количества мегакариоцитов в костном мозге диагностируют тромбоцитолиз (процесс распада тромбоцитов). Иммунный характер тромбоцнтопении подтверждает предложенный Диксоном (R. Dixon) и Россе (W. Rosse) количественный метод определения иммуноглобулинов класса G на поверхности тромбоцитов; при Фишера-Эванса синдроме их содержание на поверхности тромбоцитов повышено.
Лечение проводят глюкокортикоидными гормонами; при отсутствии эффекта производят спленэктомию (см.). Если после операции выраженный гемолиз и (или) тромбоцитолиз рецидивируют, назначают цитостатические препараты (азатиоприн, циклофосфан, винкристин), обычно их комбинируют с глюкокортикоидными гормонами. Детям при отсутствии жизненных показаний назначения цитостатических препаратов следует избегать. При тяжелой анемии, угрожающей жизни больного, показаны трансфузии эритроцитной массы или многократно отмытых эритроцитов, подобранных индивидуально с помощью непрямой пробы Кумбса. Переливание тромбоцитной массы не оказывает эффекта, т. к. донорские клетки быстро разрушаются.
Прогноз часто неблагоприятный. При Фишера-Эванса синдроме нередко наблюдаются тяжелые гемолитические кризы (см.), сильные кровотечения (см.), обусловленные дефицитом тромбоцитов. Нередки осложнения, связанные с необходимостью длительного применения глюкокортикоидных гормонов и цитостатических препаратов.
При Фишера-Эванса синдроме следует уделять особое внимание профилактике рецидивов гемолиза и (или) тромбоцитолиза при возникновении инфекционных болезней, в особенности вирусных (в нек-рых случаях назначают небольшие дозы глюкокортикоидных гормонов). Больные должны избегать инсоляции; исключается прием препаратов, блокирующих функцию тромбоцитов (напр., препаратов салициловой кислоты).
Библиогр.: Идельсон Л. И., Дицковский Н. А. и Ермильченко Г. В. Гемолитические анемии, М., 1975, библиогр.; Руководство по гематологии, под ред. А. И. Воробьева и Ю. И. Лорие, М., 1979; Савченко В. Г. и Идельсон Л. И. Применение метода Диксона и Россе для количественного определения иммуноглобулинов на поверхности тромбоцитов при тромбоцитопенической пурпуре, Пробл. гематол. и перелив, крови, т. 26, № 7, с. 49, 1981; Dixon R., R osse W. а. Ebbert L. Quantitative determination of antibody in idiopathic thrombocytopenic purpura, New Engl. J. Med., v. 292, p. 230, 1975; Evans R. S. a. o. Primary thrombocytopenic purpura and acquired hemolytic anemia, evidence for a common etiology, Arch, intern. Med., v. 87, p. 48, 1951; Pirofsky B. Autoimmunization and the autoimmune hemolytic anemias, Baltimore, 1969; Progress in hematology, ed. by E. B. Brown a. С. V. Moore, v. 6, p. 82, N. Y.— L., 1969.
В. Г. Савченко.
Источник: Большая Медицинская Энциклопедия (БМЭ), под редакцией Петровского Б.В., 3-е издание
Рекомендуемые статьи
Источник
Что такое синдром Фишера-Эванса?
Синдром Фишера-Эванса (сокр. СФЭ) или синдром Эванса — редкое заболевание, при котором иммунная система организма вырабатывает антитела, которые ошибочно разрушают эритроциты, тромбоциты, а иногда и некоторые лейкоциты, известные как нейтрофилы. Это приводит к аномально низкому уровню этих кровяных клеток в организме (цитопении).
Преждевременное разрушение эритроцитов (гемолиз) известна как аутоиммунная гемолитическая анемия или АИГА. Тромбоцитопения относится к низким уровням тромбоцитов (идиопатическая тромбоцитопения пурпура или ИТП в данном случае). Нейтропения означает низкий уровень некоторых лейкоцитов, известных как нейтрофилы. Синдром Эванса определяется как ассоциация АИГА наряду с ИТП; нейтропения встречается реже. В некоторых случаях аутоиммунное разрушение этих кровяных клеток происходит одновременно (вместе); однако в большинстве случаев сначала развивается одно состояние, а затем другое (последовательно).
Симптомы и тяжесть синдрома Фишера-Эванса могут сильно различаться у разных людей. Синдром Эванса потенциально может вызвать тяжелые, угрожающие жизни осложнения. СФЭ может проявляться сам по себе как первичное (идиопатическое) заболевание или в сочетании с другими аутоиммунными заболеваниями или лимфопролиферативными расстройствами как вторичное заболевание. (Лимфопролиферативные расстройства характеризуются перепроизводством лейкоцитов). Различие между первичным и вторичным СФЭ имеет большое значение, так как это влияет на лечение.
СФЭ в медицинской литературе был впервые описан доктором Фишером (J.A. Fisher) в 1947 г., затем более подробно в 1951 году доктор Роберт Эванс и его коллеги описали клинику аутоиммунной гемолитической анемии, сочетающейся с аутоиммунной тромбоцитопенией. В течение многих лет расстройство считалось случайным возникновением АИГА с тромбоцитопенией и/или нейтропенией. Тем не менее, исследователи теперь считают, что расстройство представляет собой отчетливое состояние, характеризующееся хроническим, глубоким (больше, чем в случае только ИТП или АИГА) состоянием нарушения иммунной системы (дисрегуляция).
Признаки и симптомы
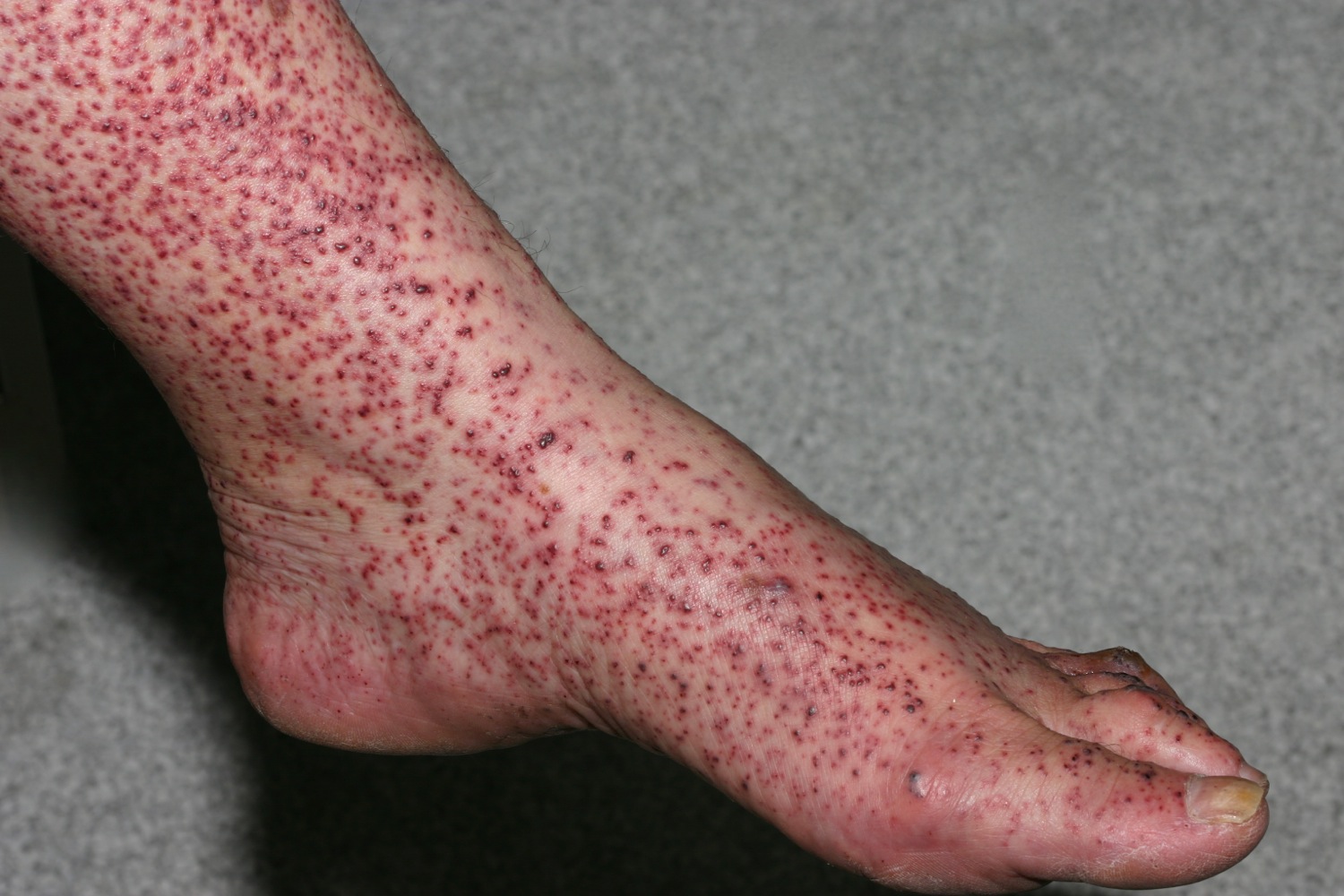
Симптомы и тяжесть синдрома Фишера-Эванса могут сильно варьироваться от одного человека к другому, а также от начала, течения и продолжительности расстройства. У большинства людей наблюдается хроническое течение с периодами ухудшения симптомов (обострения) и ремиссий, обычно вызванных временным лечением. Большинство симптомов вызвано низким уровнем специфических клеток крови в организме. Эти клетки крови выполняют определенные функции. Эритроциты доставляют кислород в организм и удаляют углекислый газ, тромбоциты помогают свертывать кровь, чтобы остановить кровопотерю, а лейкоциты помогают бороться с инфекцией.
Некоторые люди с СФЭ могут сначала столкнуться с ускоренным разрушением эритроцитов быстрее, чем организм может заменить их. Низкий уровень циркулирующих эритроцитов, состояние известное как анемия, может вызывать различные симптомы, включая:
- усталость;
- бледный цвет кожи;
- головокружение;
- одышку;
- темную мочу;
- учащенное сердцебиение (тахикардия).
У некоторых людей может развиться пожелтение кожи и особенно склеры глаз (желтуха).
Другие люди могут сначала страдать от низкого уровня тромбоцитов, состояния известного как тромбоцитопения. Тромбоцитопения может вызывать крошечные красноватые или пурпурные пятна на коже (петехии), большее пурпурное обесцвечивание на коже, вызванное кровотечением из разорванных кровеносных сосудов в подкожную клетчатку (экхимоз), и пурпуры, сыпь, состоящие из пурпурных пятен, вызванных внутренними кровотечениями из небольших кровеносных сосудов. Пострадавшие люди могут быть более подвержены ушибам после минимальной травмы и самопроизвольным кровотечениям из слизистых оболочек.
Низкий уровень лейкоцитов, состояние известное как нейтропения, встречается реже у людей с синдромом Фишера-Эванса, чем анемия или тромбоцитопения. Люди с нейтропенией могут быть подвержены рецидивирующим инфекциям. Общие симптомы могут включать:
- лихорадку;
- общее ощущение плохого самочувствия (недомогание);
- язвы на слизистых оболочках рта.
Дополнительные симптомы, которые могут возникнуть у людей с синдромом Фишера-Эванса, включают увеличение лимфатических узлов, селезенки и печени. Эти признаки могут приходить и уходить или, в некоторых случаях, могут происходить только во время острых эпизодов.
Слишком часто пациенты с синдромом Эванса могут не реагировать на лечение (рефрактерный синдром Эванса) и в конечном итоге их состояние может прогрессировать, вызывая опасные для жизни осложнения, включая сепсис, тяжелые кровотечения (кровоизлияния) и значительные сердечно-сосудистые проблемы, включая сердечную недостаточность.
Причины и факторы риска
Точная, основная причина синдрома Фишера-Эванса неизвестна. СФЭ является аутоиммунным заболеванием. Она возникает, когда иммунная система вырабатывает антитела, которые по ошибке атакуют здоровые ткани, в частности, эритроциты, тромбоциты и иногда определенные лейкоциты.
Иммунная система обычно реагирует на чужеродные вещества, вырабатывая специализированные белки, называемые антителами. Антитела работают, уничтожая посторонние вещества напрямую или покрывая их веществом, которое помечает их для разрушения лейкоцитами. Когда антитела нацелены на здоровые ткани, их можно назвать аутоантителами. Исследователи полагают, что запускающее событие (такое как инфекция или основное расстройство) может побудить иммунную систему вырабатывать аутоантитела при синдроме Эванса.
СФЭ может возникнуть в сочетании с другим расстройством в качестве вторичного состояния. Вторичный синдром Эванса может быть связан с другими расстройствами, включая аутоиммунный лимфопролиферативный синдром (АЛПС), красную волчанку, антифосфолипидный синдром, синдром Шегрена, общий вариабельный иммунодефицит, дефицит IgA, некоторые лимфомы и хронический лимфолейкоз.
Затронутые группы населения
Частота возникновения и распространенность СФЭ неизвестна. Расстройство может затрагивать детей и взрослых.
Близкие по симптомам расстройства
Симптомы следующих расстройств могут быть похожи на симптомы синдрома Эванса. Сравнения могут быть полезны для дифференциальной диагностики.
Несколько различных расстройств могут характеризоваться наличием как гемолитической анемии, так и тромбоцитопении. Эти расстройства включают:
- пароксизмальную ночную гемоглобинурию (ПНГ);
- приобретенную тромботическую тромбоцитопеническую пурпуру (ПТТП);
- гемолитико-уремический синдром (ГУС);
- синдром Казабаха-Мерритта (СКМ).
Аутоиммунный лимфопролиферативный синдром (АЛПС) является редким генетическим заболеванием, который по симптомам напоминает СФЭ. Характерным признаком АЛПС является наличие аномально большого количества лейкоцитов, называемых лимфоцитами, которые могут накапливаться в лимфатических узлах, печени и селезенке, вызывая увеличение этих органов. АЛПС может привести к симптомам, схожим с синдромом Фишера-Эванса, особенно к анемии, тромбоцитопении и нейтропении. У большинства людей с АЛПС имеется мутация члена суперсемейства генов рецепторов фактора некроза опухоли (TNFRSF6), также называемого CD95 или Fas. Точная связь между этими расстройствами, если таковые имеются, до конца не выяснена. Считается, что примерно половина детей с диагнозом синдрома Эванса может иметь основную АЛПС в качестве причины из-за неспособности аутореактивных клеток пройти нормальную запрограммированную гибель клеток (апоптоз). Пересечение АЛПС и СФЭ у взрослых менее очевидно.
Диагностика
Диагноз СФЭ основан на выявлении характерных симптомов, детальной истории болезни, тщательной клинической оценке и разнообразных специализированных тестах. Никакой конкретный тест не является убедительным для СФЭ, и диагноз ставится после исключения других возможных диагнозов. В частности, диагноз синдрома Эванса может быть поставлен, когда аутоиммунная гемолитическая анемия (с положительным прямым тестом Кумбса) и тромбоцитопения (ИТП) возникают у одного и того же пациента, даже если не в одно и то же время.
— Клиническое тестирование и обследование.
Лабораторные исследования включают общий анализ крови (ОАК), который может выявить низкий уровень эритроцитов, тромбоцитов и лейкоцитов. Другой анализ крови, известный как прямой тест на антиглобулин, используется, чтобы определить, является ли количество определенных антител выше нормального. Разнообразные тесты могут применяться для исключения других состояний. Такие тесты могут включать биопсию костного мозга, дополнительные анализы на антитела и компьютерную томографию (КТ) грудной клетки, живота и таза.
Некоторые врачи рекомендуют обследовать детей с СФЭ на АЛПС из-за высокой распространенности этих двух расстройств, возникающих вместе. Скрининг включает тестирование на наличие двойных отрицательных Т-клеток (ДНТ) с помощью проточной цитометрии, присутствие которых свидетельствует о АЛПС.
Стандартные методы лечения
Лекарств от синдрома Эванса нет, и лечение часто является сложной задачей. Лечение направлено на конкретные симптомы, которые проявляются у каждого больного. Лечение может потребовать скоординированных усилий команды специалистов. Педиатрам, хирургам, гематологам, гематологам-педиатрам, иммунологам, ревматологам и другим медицинским работникам может потребоваться систематическое и всестороннее планирование лечения заболевания у ребенка.
Большинство пострадавших людей нуждаются в лечении, хотя в редких случаях сообщалось о спонтанной ремиссии. Для лечения людей с СФЭ использовался целый ряд различных методов лечения, и их эффективность среди больных людей сильно варьировала. Некоторые люди имеют длительные ремиссии расстройства; другие испытывают хронические проблемы без ремиссии.
Следовательно, конкретные терапевтические процедуры и вмешательства могут варьироваться в зависимости от многочисленных факторов, таких как тяжесть заболевания; уровень клеток крови; наличие или отсутствие определенных симптомов; возраст человека и общее состояние здоровья; и/или других факторов. Решения, касающиеся использования конкретных схем приема лекарств и/или других видов лечения, должны приниматься врачами и другими членами команды здравоохранения при тщательной консультации с пациентом на основе особенностей его случая; тщательное обсуждение потенциальных выгод и рисков, включая возможные побочные эффекты и долгосрочные последствия; предпочтения пациента; и другие соответствующие факторы.
Терапия первой линии для синдрома Фишера-Эванса часто состоит из кортикостероидов, таких как преднизолон. Кортикостероиды помогают подавить иммунную систему и уменьшить выработку аутоантител. Первоначальные результаты часто эффективны.
Внутривенная терапия иммуноглобулином (ВВИГ) также использовалась, чтобы лечить людей с СФЭ. ВВИГ терапия модифицирует деятельность иммунной системы. ВВИГ представляет собой раствор, содержащий антитела, взятые у здоровых людей и доставленные непосредственно в вену больного.
Хирургическое удаление селезенки (спленэктомия) использовалось для лечения некоторых людей с СФЭ. Большинство сообщений являются неубедительными и анекдотичными, и эффективность процедуры трудно определить из-за одновременного (сопутствующего) использования других методов лечения, таких как лекарства. Спленэктомия обычно предназначена для лиц, которые не реагируют на другие терапевтические варианты (рефрактерный синдром Эванса). У детей спленэктомия редко приводит к длительной ремиссии симптомов. У взрослых эффективность варьируется, и симптомы обычно возвращаются в какой-то момент. Поэтому, как правило, спленэктомия откладывается как можно дольше, и делается все возможное, чтобы не выполнить процедуру.
Во время острого эпизода переливание крови и/или тромбоцитов может быть необходимо для устранения симптомов. Тем не менее, следует избегать использования переливаний крови или тромбоцитов.
В настоящее время изучаются новые методы лечения синдрома Эванса. Ритуксимаб является высокоэффективным средством лечения пациентов с СФЭ. Ритуксимаб классифицируется как моноклональное антитело или биологическая терапия — лекарства, которые действуют как антитела, но искусственно созданы в лаборатории. Первоначальные исследования показали, что препарат в целом безопасен и эффективен. Преимущества ритуксимаба в том, что он позволяет избежать серьезной иммуносупрессии и побочных эффектов, связанных с другими иммунодепрессантами. Недостатком является то, что в случаях СФЭ, в котором причиной является АЛПС, представляется вероятным, что будет развиваться гипогаммаглобулинемия, которая может сохраняться у пациентов, получавших ритуксимаб. Гипогаммаглобулинемия — состояние, при котором иммунная система организма не вырабатывает достаточного количества антител, в результате чего больные могут быть подвержены бактериальным инфекциям и, в меньшей степени, некоторым вирусным инфекциям.
В небольшой серии пациентов с синдромом Эванса были изучены дополнительные препараты. Следующим агентом, который, по-видимому, является относительно эффективным при заболевании, является микофенолата мофетил.
Препараты могут использоваться отдельно или в комбинации (многоагентная терапия) в качестве терапии второй линии у больных с СФЭ, которые не отвечают на кортикостероиды или ВВИГ терапию. Необходимы дополнительные исследования для определения долгосрочной безопасности и эффективности этих потенциальных методов лечения больных с синдромом Фишера-Эванса.
Прогноз
Долгосрочные перспективы для людей с синдромом Эванса могут варьироваться. У некоторых людей, страдающих СФЭ, могут наблюдаться периоды длительной ремиссии, в течение которых признаки и симптомы заболевания исчезают или становятся менее выраженными. Другие имеют хронические проблемы без ремиссий.
Больные с синдромом Фишера-Эванса редко справляются без лечения. Даже при лечении реакция на терапию может быть переменной и часто разочаровывающей. Часто встречаются случаи тромбоцитопении и анемии, а также эпизоды кровоизлияний (кровотечений) и серьезных инфекций. У людей с заболеванием больше склонности к развитию других аутоиммунных заболеваний. СФЭ иногда приводит к летальному исходу, поэтому важно тщательное наблюдение врача, знакомого с этим заболеванием.
Источник
