Синдром холестаза у новорожденных клинические рекомендации

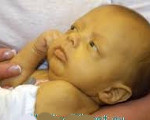
Холестаз новорожденного – это патологическое состояние, которое характеризуется нарушением секреции желчи, приводит к гипербилирубинемии и желтухе. Клинические проявления включают субиктеричность склер, пожелтение слизистых оболочек и кожи, гепатомегалию, задержку в физическом развитии, гиповитаминозы А, D, K, E. Диагностика холестаза новорожденного заключается в выявлении основного заболевания, лабораторной оценке работы печени, УЗИ, гепатобилиарном сканировании и биопсии печени. Лечение зависит от этиологического фактора и подразумевает рациональное питание, введение в рацион легкоусвояемых жиров, витаминотерапию или оперативное вмешательство.
Общие сведения
Холестаз новорожденного – это гетерогенное состояние в педиатрии и неонатологии, которое проявляется нарушением выведения желчи с дальнейшим развитием гипербилирубинемии. Точную распространенность патологии установить тяжело, поскольку это состояние зачастую включают в структуру основного заболевания. Терапевтическая тактика и прогноз для жизни ребенка зависят от этиологического фактора холестаза новорожденного. Как правило, устранение ведущей патологии ведет к купированию холестатического синдрома. В тяжелых случаях может требоваться пересадка печени.
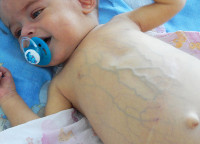
Холестаз новорожденного
Причины
Все этиологические факторы холестаза новорожденного разделяют на внепеченочные и внутрипеченочные. Последняя группа включает в себя нарушения инфекционного, метаболического, генетического, аллоимунного или токсического происхождения.
- К инфекционным причинам относятся так называемые TORCH-инфекции: токсоплазмоз, краснуха, ЦМВ, герпес-вирус, сифилис, гепатит В и другие.
- Спровоцировать холестаз новорожденного могут такие нарушения метаболизма, как галактоземия, муковисцидоз, тирозинемия, недостаточность α1-антитрипсина.
- Генетическими факторами являются синдром Алажиля, кистозный фиброз, прогрессирующий семейный внутрипеченочный холестаз и др.
- Гестационное аллоиммунное поражение печени развивается при трансплацентарном прохождении материнских IgG в организм ребенка. Это вызывает активацию системы комплемента, которая способна повреждать гепатоциты.
- Длительное парентеральное вскармливание у тяжело недоношенных детей и наличие синдрома короткой кишки относятся к токсическим причинам холестаза новорожденного.
Перечень внепеченочных факторов развития холестаза новорожденного включает в себя все нарушения, которые ухудшают отток желчи из печени. Наиболее распространенная причина – атрезия желчевыводящих путей. Чаще всего наблюдается у недоношенных детей. Иногда, помимо внепеченочного билиарного тракта, поражаются и внутрипеченочные желчные протоки. Точная этиология данного состояния неизвестна. Предположительно, развитие билиарной атрезии вызывают инфекционные заболевания матери во время беременности.
Патогенез
Пусковым механизмом появления клинических симптомов при холестазе новорожденного является нарушение экскреции прямого билирубина, провоцирующее повышение его уровня в крови – гипербилирубинемию. Это приводит к дефициту желчных кислот в системном кровотоке. Так как они отвечают за всасывание и транспорт жиров и жирорастворимых витаминов (А, D, K, E) в организме ребенка возникает их дефицит. Результатом становится недостаточная прибавка массы тела, гиповитаминозы, задержка физического и психомоторного развития.
Симптомы холестаза новорожденного
Клиника холестаза новорожденного развивается на протяжении первых 10-14 дней жизни ребенка. Первичные проявления – беспокойство, снижение аппетита, недостаточная прибавка массы тела и роста. Почти сразу возникает субиктеричность склер и слизистых оболочек, при дальнейшем нарастании гипербилирубинемии отмечается желтушность кожных покровов.
На этом фоне моча приобретает коричневый оттенок, а кал становится бесцветным (ахолическим). Постепенно увеличивается печень, что проявляется незначительным увеличением живота. Также при холестазе новорожденного отмечается хронический зуд, клинические проявления гиповитаминозов А, D, K, E.
Осложнения
При дальнейшем прогрессировании основного заболевания, приводящего к фиброзу печени, развивается портальная гипертензия. Она, в свою очередь, становится причиной асцита и кровотечений из варикозно расширенных вен пищевода. Исход варьируется от длительного доброкачественного течения до быстрого развития печеночной недостаточности и цирроза с летальным исходом уже на первом году жизни.
Диагностика
Диагностика холестаза новорожденного включает в себя сбор анамнестических данных, физикальное обследование ребенка, лабораторные и инструментальные методы исследования. При опросе родителей педиатр или неонатолог обращают внимание на все возможные этиологические факторы: заболевания матери во время беременности, генетические патологии, врожденные аномалии развития ребенка. При физикальном осмотре определяется дефицит массы тела и роста, желтушность склер, слизистых оболочек и кожи, гепатомегалия. Подтверждающая диагностика:
- Лабораторные тесты. В биохимическом анализе крови выявляется гипербилирубинемия за счет прямой фракции, диспротеинемия. Возможно повышение трансаминаз – АлТ и АсТ. Характерные признаки холестаза новорожденного – ахолический, богатый на жиры кал и насыщенная уробилином моча. С целью исключения TORCH-инфекций проводится ИФА и бактериальный посев мочи. Также используются тесты на метаболические нарушения или генетические аномалии, которые могут вызывать развитие холестаза новорожденных – анализы на содержание NaCl в поте, галактозы в моче, уровень α1-антитрипсина в крови.
- Эхография. Первый этап – ультразвуковое исследование органов брюшной полости. Оно позволяет выявить гепатомегалию, аномалии строения желчного пузыря и желчевыводящих протоков. Далее выполняется УЗ-сканирование печени для оценки экскреции желчи на всех уровнях билиарного тракта – от внутрипеченочных протоков до двенадцатиперстной кишки.
- Биопсия печени. При невозможности подтвердить диагноз данными методами показана биопсия печени. При неонатальном холестазе гистологический анализ биоптата может выявить увеличенные портальные триады, пролиферацию и фиброзирование желчных протоков при атрезии желчевыводящий путей, гигантские полиядерные клетки при врожденном гепатите и др. При подозрении на аллоиммунное происхождение холестаза новорожденного определяется большое количество железа в гепатоцитах или тканях губ.
Лечение холестаза новорожденного
Консервативная терапия
Терапия при холестазе новорожденного включает в себя несколько моментов: полноценное лечение основного заболевания, насыщение рациона ребенка витаминами А, D, K, E и среднецепочечными жирными кислотами, применение урсодезоксихолевой кислоты. Большое количество витаминов возмещает их недостаточное всасывание в кишечнике. Среднецепочечные жирные кислоты способны всасываться в кровоток даже в условиях дефицита желчных солей при холестазе новорожденного, тем самым компенсируя дефицит триглицеридов в организме. Урсодезоксихолевая кислота является гепатопротектором и желчегонным средством, стимулирующим работу печени и желчевыводящих путей и купирующим гипербилирубинемию.
При подозрении на аллоиммунное происхождение холестаза новорожденного (даже при неподтвержденном диагнозе) показано введение внутривенных иммуноглобулинов или обменное переливание крови.
Хирургическое лечение
При подтвержденной атрезии желчевыводящих путей уже на 1-2 месяце жизни проводится портоэнтеростомия по методу Касаи. Данная операция значительно улучшает показатель выживаемости, однако в будущем приводит к частым рецидивирующим холангитам, стойкому холестазу и задержке в психофизическом развитии. На фоне быстро развивающегося цирроза печени необходима трансплантация органа.
Прогноз и профилактика
Прогноз при холестазе новорожденного напрямую зависит от основного заболевания и эффективности терапевтических мероприятий. При атрезии желчевыводящих путей и отсутствии раннего хирургического вмешательства быстро развивается печеночная недостаточность. Далее это состояние трансформируется в цирроз с нарастающей гипертензией в системе воротной вены уже на первых месяцах жизни ребенка. Смерть наступает, как правило, в возрасте 10-12 месяцев. Инфекционные и метаболические причины холестаза новорожденного могут иметь как доброкачественный прогноз, так и быстро прогрессирующее течение. Аллоиммунное поражение печени на фоне отсутствия раннего лечения в большинстве случаев завершается летальным исходом.
Профилактика холестаза новорожденного включает в себя антенатальную охрану плода, медико-генетическое консультирование семейных пар и планирование беременности, регулярное посещение женской консультации, полноценное прохождение всех необходимых анализов и исследований. Данные меры позволяют оценить риск развития генетических заболеваний еще до начала беременности и выявить опасные заболевания уже на ранних сроках.
Источник
Рекомендации:
1. Диагноз холестатического ЛПП может быть установлен по повышению уровня ЩФ>2N или АЛТ/ЩФ <2 и наличию временной связи между приемом препарата и появлением клинической симптоматики, а также при исключении других причин холестаза (III/С1). Проведение биопсии печени необязательно (III/С2).
2. Рекомендуется прекращение приема препарата и тщательное наблюдение за клинической симптоматикой и биохимическими показателями (III/С2). Применение УДХК и кортикостероидов для терапии ЛПП может быть успешно, но отсутствует доказательная база в виде контролируемых исследований (III/С2).
10.Холестаз во время беременности.
10.1.Внутрипеченочный холестаз беременных (ВХБ).
ВХБ представляет собой обратимую форму холестаза и характеризуется (1) интенсивным кожным зудом, возникающим в большинстве случаев во втором или третьем триместрах беременности; (2) повышением уровня АЛТ и желчных кислот натощак и (3) спонтанным разрешением всех симптомов в течение 4-6 недель после родов. Клиническое значение ВХБ заключается в потенциальном риске для плода (спонтанные или ятрогенные преждевременные роды, асфиксия во время родов, внутриутробная смертность)¸хотя по данным последних исследований уровень перинатальной смертности (9/1000) сопоставим с таковым среди общей популяции. Зуд, особенно сильный по ночам, влияет на качество жизни матери. Довольно редко при ВХБ возникают стеаторея и послеродовые кровотечения вследствие дефицита витамина К.
Патогенез ВХБ многофакторный, включает генетические, гормональные факторы, а также воздействие факторов окружающей среды.
Для установления диагноза ВХБ необходимо наличие кожного зуда (который не может быть объяснен другими причинами) и повышение уровня желчных кислот в сыворотке крови ≥11мкмоль/л. Редко может наблюдаться изолированное повышение сывороточного уровня желчных кислот, у большинства пациенток также повышается уровень АЛТ. Уровень желчных кислот – самый чувствительный маркер холестаза беременных, он может повышаться до изменения других печеночных проб. Вероятность осложнений для плода существенно повышается при раннем начале ВХБ (до 33 недели беременности) и повышении уровня желчных кислот >40 мкмоль/л. Уровень gГТ может быть повышен при мутациях гена АВСВ4. В 10-15% случаев наблюдается легкая желтуха за счет конъюгированного билирубина. Проведение биопсии печени не требуется.
В случаях раннего или атипичного дебюта ВХБ необходимо проводить дифференциальную диагностику с преэклампсией и острой жировой печенью беременных (Таблица 6).
Таблица 6
Характеристика внутрипеченочного холестаза беременных, синдрома HELLP и острой жировой печени беременных
Внутрипеченочный холестаз беременных | HELLP синдром | Острая жировая печень беременных | |
% | 0.1-1,0 | 0,2-0,6 | 0,005-0,01 |
Триместр | (2 или) 3 | 3 и после родов | 3 или после родов |
Наследственная отягощенность | Часто | Нет | Редко |
Наличие преэклампсии | Нет | Да | 50% |
Типичные клинические признаки | Зуд, увеличение АЛТ/АСТ, уровня желчных кислот натощак | Гемолиз, увеличение уровня печеночных проб, тромбоцитопения (часто<50000/мкл) | Печеночная недостаточность с умеренной желтухой, коагулопатия, энцефалопатия, гипогликемия |
Повышение уровня АЛТ | Умеренное до 10-20 N | Умеренное до 10-20 N | 5-15N |
Билирубин | <5 мг/дл (<85 мкмоль/л) | В большинстве случаев <5 мг/дл (<85 мкмоль/л) | Часто <5 мг/дл (<85 мкмоль/л) |
Инструментальные методы исследования | Норма | Инфаркты печени, гематомы | Жировая инфильтрация |
Материнская смертность (%) | 1-25 | 7-18 | |
Фетальная/перинатальная смертность (%) | 0,4-1,4 | 11 | 9-23 |
Рецидив при последующих беременностях (%) | 45-70 | 4-19 | 20-70 (при наличии мутаций 3-гидроксиацил-коэнзим А дегидрогеназы |
Если после родов симптоматика не разрешается, следует думать о других хронических болезнях печени: ПБЦ, ПСХ, дефиците АВСВ4 или хроническом гепатите С, при которых кожный зуд может появиться на последних неделях беременности.
В 10% случаев во время беременности могут появиться камни в желчном пузыре или билиарный сладж, яркая симптоматика наблюдается у 1,2% из этих пациенток. Диагноз основывается на анализе клинической картины, повышении уровня печеночных проб, данных УЗИ. При возникновении обструктивного холестаза в результате закупорки камнем общего желчного протока или ухудшении течения панкреатита следует выполнить ЭРХПГ, сфинктеротомию и экстракцию камня под прикрытием антибиотиков (ампициллин). Для наркоза в небольших дозах могут использоваться меперидин, пропофол, фентанил и мидозолам.
10.2. Применение лекарственных препаратов при лечении холестатических заболеваний печени во время беременности.
В случае неактивного или малоактивного холестатического заболевания печени у женщин детородного возраста возможна неосложненная беременность без обострения заболевания печени. У больных АИГ или перекрестным синдромом ПБЦ/АИГ возможно обострение заболевания во время беременности или после родов.
УДХК. При холестатических заболеваниях разрешается применение УДХК во втором и третьем триместрах беременности. Ни у матерей, ни у новорожденных не зафиксировано побочных эффектов применения УДХК. Для применения во время грудного вскармливания УДХК не одобрена, в то же время следует отметить, что препарат практически безопасен для ребенка, поскольку в грудном молоке не обнаружено значительное содержание УДХК.
Кортикостероиды. Использование преднизолона безопасно во время беременности и лактации, однако при применении в первом триместре беременности увеличивается риск развития расщелины неба (волчья губа) у детей.
Азатиоприн. Применение азатиоприна безопасно во время беременности, в то же время в исследованиях на животных описан тератогенный эффект препарата. Риски и выгода терапии азатиоприном должны в деталях обсуждаться с пациенткой. В грудное молоко азатиоприн проникает в очень небольших количествах, однако возможность грудного вскармливания также должна решаться индивидуально.
Рекомендации:
1. Диагноз ВХБ устанавливается на основании появления зуда во время беременности, повышения уровня АЛТ и желчных кислот натощак в сыворотке крови и исключения других причин зуда и нарушения функции печени (ШШ-2/C2). Диагноз считается подтвержденным после нормализации печеночных проб после родов.
2. Женщин с ВХБ следует информировать о возможности преждевременных родов (II-2/В1). Специальное наблюдение за плодом не рекомендуется (III/С2). Прием УДХК уменьшает выраженность зуда и улучшает печеночные пробы (I/В1), нет достаточных данных о защитном действии препарата в отношении развития осложнений у плода (II-1/С2). При удлинении протромбинового времени следует назначать витамин К (III/С2). Время родоразрешения следует обсуждать в каждом конкретном случае (II-2/С2).
3. Для лечения клинически манифестных холестатических заболеваний печени у беременных можно использовать УДХК во втором и третьем триместрах (I/В1). Для лечение АИГ во время беременности следует использовать преднизолон (возможна комбинация с азатиоприном) для предотвращения обострения заболевания, что может иметь более значимые негативные последствия для исхода беременности, чем потенциальный риск применения лекарств (III/С2).
4. При появлении клиники холелитиаза при беременности следует выполнить эндоскопическую сфинктеротомию и удаление камня (II-3/В1). Даже в первом триместре беременности рентгеновское исследование нельзя считать абсолютно противопоказанным (III/С2). При бессимптомное течении желчнокаменной болезни холецистэктомию следует выполнить после родов (III/С2).
10. Внепеченочные проявления холестаза.
11.1. Зуд.
Кожный зуд может быть симптомом холестаза любой этиологии. Патогенез зуда до настоящего времени не расшифрован. В терминальных стадиях заболеваний печени зуд может ослабевать. Нет достаточной доказательной базы, что УДХК уменьшает зуд при холестазе, за исключением случаев ВХБ. Как препарат первой линии для купирования зуда широко используют холестирамин. В ряде случаев проблемой может стать плохая переносимость препарата из-за его вкуса, что можно решить добавлением фруктового сока. Следует иметь ввиду, что УДХК следует принимать не раньше, чем через 4 часа после приема холестирамина, чтобы предотвратить ее связывание и снижение эффективности.
Препаратом второй линии для купирования зуда служит агонист прегнанового Х рецептора рифампицин. Есть данные о его двухлетнем эффективном применении. У 12% больных с холестазом на фоне приема рифампицина описано развитие лекарственного гепатита через 2-3 месяца приема. Поэтому важно начинать лечение с малых доз, тщательно мониторируя печеночные пробы перед увеличением дозы.
К препаратам третьей линии относят антагонисты опиоидов. Их применение ограничивают реакции, напоминающие синдром отмены.
Есть данные об эффективном применении сертралина (механизм действия не ясен). Не рекомендуется использование антигистаминных средств (отсутствие эффекта), ондансетрона (ограниченная эффективность) и фенобарбитала (выраженные побочные эффекты).
При резистентном к терапии зуде описаны случаи позитивного эффекта от применения экстракорпорального альбуминового диализа, плазмафереза и дренирование желчных протоков. Последним средством лечения зуда может выступать трансплантация печени.
Рекомендации (Рис.2):
1. Терапия первой линии – холестирамин 4 г до 4 раз в день (II-2/В1). Следует разнести прием холестирамина и других лекарств по меньшей мере на 4 часа (II-3/В1).
2. Терапия второй линии – рифампицин в стартовой дозе 150 мг, при тщательном наблюдении за печеночными пробами можно увеличить дозу максимально до 600 мг/день (I/А1).
3. Терапия третьей линии – налтрексон per os в дозе 50 мг/день (стартовая доза 25 мг) (I/В1). Следует рассматривать возможность применения этого препарата только при неэффективности или непереносимости холестирамина (или других ионообменных смол) и рифампицина (III/С1).
4. Терапия четвертой линии – сертралин при неэффективности вышеуказанных препаратов (II-2/С2).
5. При неэффективности всех перечисленных препаратов возможно направление пациентов в специализированные центры для проведения экстракорпорального альбуминового диализа, плазмафереза или дренирования желчных протоков (III/С2).
6. Если все вышеперечисленные лекарства и методы оказываются неэффективными, возможно выполнение трансплантации печени (III/С1).
11.2. Слабость.
Слабость – характерный симптом ПБЦ, выраженность ее не коррелирует с тяжестью заболевания печени. Прежде чем отнести данный симптом к проявлениям ПБЦ следует исключить другие возможные причины, в том числе АИГ.
Рекомендации:
1. Необходимо исключить гипотиреоз, анемию, диабет, депрессию, побочное действие лекарств и пр. (III/С2).
2. Следует минимизировать провоцирующие слабость факторы (избыток антигипертензивных препаратов, нарушение сна вследствие употребления кофе в вечерние часы) (III/С2). Важна психологическая поддержка.
3. Для купирования слабости не показано проведение трансплантации печени (если к этому нет других показаний) (III/С1).
11.3. Остеопороз.
Рекомендации:
1. У всех больных с холестазом следует оценить риск развития остеопороза, обращая особое внимание на устранимые факторы риска и советы по модификации образа жизни (III/С2).
2. При установлении диагноза хронического холестатического заболевания печени необходимо выполнить денситометрию (III/С2). Повторное исследование проводят ежегодно в зависимости от выраженности холестаза и индивидуальных факторов риска (III/С2).
3. Рекомендуется применение кальция (1000-1200 мг/день) и витамина D (400-800 МЕ/день) у всех больных холестатическими заболеваниями печени, хотя это положение не имеет достаточной доказательной базы (III/С2).
4. Если при денситометрии Т<-2,5 или имел место патологический перелом (I/В1) необходимо назначить алендронат или другие бифосфонаты, при Т<-1,5 назначение этих препаратов желательно (III/С2).
11.4. Жирорастворимые витамины.
Рекомендации:
1. Всем больным с холестазом следует назначать препараты кальция и витамин D перорально в качестве составной части программы по предупреждению остеопороза (III/С2).
2. В случаях выраженного холестаза при наличии стеатореи или доказанном низком уровне жирорастворимых витаминов следует назначить витамины А, Е и К per os (III/С2).
3. Парентеральное назначение витамина К показано профилактически перед проведением инвазивных процедур в случаях выраженного холестаза и при возникновении кровотечения (II-2/С1).
11.5 Варикозно расширенные вены пищевода и гепатоцеллюлярная карцинома.
Как и при других хронических болезнях печени, при холестатических заболеваниях развиваются варикозно расширенные вены пищевода и гепатоцеллюлярная карцинома. Программы скрининга, профилактики и лечения аналогичны таковым при других заболеваниях печени. Независимые факторы риска развития варикозно расширенных вен у больных ПБЦ: уровень тромбоцитов <200000/мм, уровень сывороточного альбумина <40 г/л и сывороточного билирубина >20 мкмоль/л.
Рисунок 1. Алгоритм диагностики холестатических заболеваний печени у взрослых пациентов.
Рисунок 2. Подходы к терапии кожного зуда при холестазе.
| Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 |
Источник
