Синдром хатчинсона гилфорда детская прогерия

Прогери́я (др.-греч. προσ- — сверх, γέρων — старик) — один из редчайших генетических дефектов. При прогерии возникают изменения кожи и внутренних органов, которые обусловлены преждевременным старением организма. Классифицируют детскую прогерию (синдром Гетчинсона (Хатчинсона) — Гилфорда) и прогерию взрослых (синдром Вернера).
Британский врач Джонатан Хатчинсон в 1886 г. впервые описал случай преждевременного старения у шестилетнего мальчика, которое проявлялось атрофией кожи и её придатков[1][2]. В дальнейшем его соотечественник и коллега Гастингс Гилфорд, изучив клинико-морфологические особенности этой патологии, ввел термин «прогерия».[2] Прогерию взрослых описал немецкий врач Карл Вильгельм Отто Вернер, который еще будучи студентом-медиком наблюдал этот синдром у четырех сиблингов в возрасте около 30 лет и задокументировал эти наблюдения в кандидатской диссертации в 1904 году.
В мире зафиксировано не более 350 случаев прогерии, в числе которых 11-летняя Адалия Роуз (Adalia Rose), 17-летняя Хейли Окинс, 16-летняя Ашанти Элиотт-Смит, а также 18-летняя Онталаметсе Фалатсе (Ontlametse Phalatse) из городка Хеброн неподалеку от Йоханнесбурга, являющаяся единственной больной прогерией представительницей негроидной расы. Широкую известность в мире получили страдавший прогерией и скончавшийся 5 июня 2011 года Леон Бота, диджей и исполнитель xип-хопa, который вел видеоблог на YouTube[3], а также американский мотивационный спикер Сэм Бернс, умерший 10 января 2014 года в возрасте 17 лет.
У детей[править | править код]
Причина детской прогерии — мутации гена LMNA, кодирующего ламин А. Ламины — белки, из которых выстроен особый слой оболочки клеточного ядра. В большинстве случаев прогерия встречается спорадически, в нескольких семьях зарегистрирована у сибсов, в том числе от кровнородственных браков, что свидетельствует о возможности аутосомно-рецессивного типа наследования. В клетках кожи больных обнаружены нарушения репарации ДНК и клонирования фибробластов, а также атрофические изменения эпидермиса и дермы, исчезновение подкожной клетчатки.
Хотя детская прогерия может быть врождённой, у большинства больных клинические признаки проявляются обычно на 2—3-м году жизни. Резко замедляется рост ребёнка, отмечаются атрофические изменения дермы, подкожной клетчатки, особенно на лице, конечностях. Кожа истончается, становится сухой, морщинистой, на туловище могут быть склеродермоподобные очаги, участки гиперпигментации. Сквозь истонченную кожу просвечивают вены. Внешний вид больного: большая голова, лобные бугры выступают над маленьким заостренным («птичьим») лицом с клювовидным носом, нижняя челюсть недоразвита. Наблюдаются также атрофия мышц, дистрофические процессы в зубах, волосах и ногтях; отмечаются изменения костно-суставного аппарата, миокарда, гипоплазия половых органов, нарушение жирового обмена, помутнение хрусталика, атеросклероз.
Средняя продолжительность жизни при детской прогерии — 13 лет. Большинство источников указывают возраст смерти от 7 до 27 лет, при этом случаи достижения совершеннолетия очень редки. Известны только два случая пациентов, переживших 27-летний рубеж — японец, описанный Огихарой и другими в 1986 году и проживший 45 лет [4] и Тиффани Ведекинд которой 41 год и она считается самой пожилой из всех пациентов, у которых диагностировали синдром «Бенджамина Баттона».
У взрослых[править | править код]
Прогерия взрослых имеет аутосомно-рецессивный тип наследования. Дефектный ген — WRN (ген АТФ-зависимой хеликазы). Предполагается связь процесса с нарушением репарации ДНК, обмена соединительной ткани.
Гистологическая картина: уплощение эпидермиса, гомогенизация и склероз соединительной ткани, атрофия подкожной клетчатки с замещением её соединительнотканными волокнами. Клинически заболевание проявляется в период полового созревания. Отмечаются замедленный рост, симптомы гипогонадизма. Обычно на третьем десятилетии жизни у больного седеют и выпадают волосы, развивается катаракта, постепенно истончается кожа и атрофируется подкожная клетчатка на лице и конечностях, вследствие чего руки и особенно ноги становятся тонкими. Появляются очаги склеродермоподобного уплотнения, дисхромии, наиболее выраженные в дистальных отделах конечностей и на лице, что наряду с тонким клювовидным носом, суженным ротовым отверстием придает ему маскообразность. На местах, подвергающихся давлению, развиваются гиперкератоз, хронические плохо заживающие трофические язвы. Обнаруживаются остеопороз, метастатическая кальцификация мягких тканей, реже остеомиелит. Часто наблюдается сахарный диабет, признаки которого, как и симптомы раннего генерализованного атеросклероза, обычно выявляются у больных в возрасте 30—40 лет; возможны злокачественные новообразования (например, рак кожи, саркома, аденокарцинома).
Диагноз устанавливают на основании клинической картины. Дифференциальный диагноз проводят с врожденной пойкилодермией, склеродермией. Лечение симптоматическое, в основном направлено на профилактику атеросклеротических осложнений, устранение сахарного диабета, трофических язв. Оно проводится терапевтом, эндокринологом или другим специалистом в зависимости от превалирующих клинических симптомов. Прогноз для выздоровления неблагоприятный; большинство больных погибает от атеросклеротических осложнений и злокачественных новообразований. Профилактика не разработана.
Старение[править | править код]
Установлено, что тяжёлая форма прогерии человека (синдром Хатчинсона — Гилфорда) связана с молекулярными изменениями, характерными для нормального старения, среди них геномная нестабильность, уменьшение длины теломер и нарушение гомеостаза стволовых клеток. Эти данные вместе с генетическими исследованиями продолжительности жизни привели к гипотезе, согласно которой при синдромах прогерии ускоряется ряд патологических изменений, которые, как правило, управляют обычным процессом старения[5].
Примечания[править | править код]
Литература[править | править код]
- Фёдорова Е. В. О врождённой прогерии. — 1980. — Т. 4. — С. 66. — (Педиатрия).
Источник
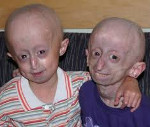
Прогерия – редкое генетическое заболевание, характеризующееся преждевременным старением организма, соответствующими изменениями внутренних органов. Проявляется гиперпигментацией, истончением и утратой эластичности кожи, поседением и выпадением волос, увеличением размеров черепа, уменьшением его лицевой части, экзофтальмом, развитием атеросклероза сосудов, инфаркта и фиброза миокарда, остеопороза, сахарного диабета, формированием злокачественных опухолей. Диагностика основана на сборе клинических данных, лабораторном исследовании ДНК. Лечение направлено на устранение симптомов заболевания: профилактику и терапию атеросклероза, инфаркта миокарда, диабета, остеопороза, рака.
Общие сведения
Термин «прогерия» в переводе с древнегреческого языка означает «преждевременное старение». Детская форма прогерии называется синдромом Хатчинсона-Гилфорда согласно фамилиям исследователей, которые впервые независимо друг от друга описали данную патологию: британский врач Дж. Хатчинсон – в 1889 году, его соотечественник Х. Гилфорд – в 1897 году. Взрослая форма носит название «синдром Вернера», так как в 1904 году немецкий врач О. Вернер первым официально наблюдал симптомы старения у подростков 14-19 лет. Оба варианта болезни являются крайне редкими. Распространенность детской прогерии составляет 1 случай на 7-8 млн. человек, с момента начала исследований патологии выявлено около 150 больных детей. Взрослая прогерия встречается чаще, средние эпидемиологические показатели – 1 больной на 100 тыс. населения.

Прогерия
Причины прогерии
В основе заболевания лежит генетическая мутация. Причиной детского типа прогерии является дефект гена LMNA, который кодирует особый белок ламин A, выстраивающий оболочку ядра клетки. Как правило, мутация происходит спорадически – во время созревания половых клеток у родителей или при зачатии. Однако исследователи выявили несколько случаев патологии у родных братьев и сестер, часть из которых входила в семьи с близкородственными браками. Это свидетельствует о возможности наследования мутации по аутосомно-рецессивному типу (родители являются носителями дефектного гена, но не болеют и способны к деторождению).
Прогерия взрослых – наследственное заболевание. Оно развивается при наличии дефекта в гене RECQL2, который ответственен за производство белка WRN, поддерживающего стабильность генома, целостность и структуру ДНК. Передача мутации происходит аутосомно-рецессивным способом, болезнь проявляется у людей, получивших два дефектных гена в одной аллели (от матери и от отца).
Патогенез
При детском варианте прогерии генетический дефект приводит к нарушению синтеза структурно правильного белка ламина А, образующего внутренний каркас ядерной оболочки. В результате мутации налаживается производство укороченного белка-предшественника преламина А, а строение созревшего конечного белка отличается от нормального. Молекулы белка встраиваются в ядерную мембрану, изменяют ее форму и повышают хрупкость. Ядро не может сохранять свою целостность, клетка гибнет раньше времени.
При болезни Вернера возникает недостаточность WRN-белка, определяется генетически детерминированная нестабильность хромосом. Их структура очень часто изменяется спонтанно или под воздействием некоторых факторов. В итоге ухудшается способность клеток к делению, пролиферативный потенциал становится в 3-5 раз меньше, чем должен быть в норме. В 10 раз увеличивается частота спонтанных мутаций, аномально укорачиваются теломеры – концевые участки хромосом, защищающие гены от повреждений.
Симптомы прогерии
Прогерия Хатчинсона дебютирует после периода нормального развития в возрасте от 6 месяцев до 2 лет. Изменяется внешность детей: замедляется рост, увеличиваются размеры черепа, но лицевая часть остается маленькой, нижняя челюсть – недоразвитой. Формируется клювовидный тонкий нос и экзофтальм (выпячивание глаз). Тотально выпадают волосы – на голове и теле, ресницы и брови. При алопеции разрушаются волосяные фолликулы, поэтому дальнейший рост волос становится невозможным. На волосистой части головы выбухают вены. Дерма и подкожная клетчатка подвергаются атрофическим изменениям: кожа истончается, иссушается, покрывается морщинами. Развивается липодистрофия – заметное снижение количества подкожного жира. Относительно сохранным он остается на щеках и лобке.
На туловище образуются склеродермоподобные очаги – уплотнения в нижней части живота, на ягодицах и бедрах. На открытых участках кожи появляются пигментные пятна. Ногти недоразвитые, ломкие, утолщенные, округло выпуклые – имеют форму «часовых стекол». К 2 годам развивается фиброз органов и околосуставных тканей. Пассивные движения в локтевых и коленных суставах ограничены (контрактуры), формируется характерное положение костей ног – «поза всадника». Скелет подвергается гипоплазии, дисплазии и дегенеративным изменениям. Молочные и постоянные зубы прорезываются с опозданием, частично отсутствуют, скученные, искривленные, подвержены кариесу. К 5-6 годам диагностируется атеросклероз сосудов, сердечные шумы, гипертрофия левого желудочка, помутнение хрусталика, резистентность к инсулину. Половые органы остаются недоразвитыми. Уровень умственного развития обычно выше, чем у сверстников.
Клинические проявления синдрома Вернера обнаруживаются с 14 до 18 лет. Подросток начинает отставать в росте, его волосы седеют и выпадают. К 20 годам пациенты лысеют. Кожа лица и конечностей бледнеет, истончается, натягивается. Под ней видна сеть кровеносных сосудов. Мышечная и жировая ткани атрофируются, руки и ноги становятся непропорционально тонкими, кожа над суставными выступами изъязвляется. К 30 годам появляется катаракта, голос слабеет и хрипнет, на ногах образуются язвы, на подошвах – мозоли, сосудистые звездочки, кератоз. Внешний вид пациентов специфичен: низкий рост, лунообразное лицо, выступающий подбородок, суженное ротовое отверстие, псевдоэкзофтальм.
Сальные и потовые железы атрофируются. Костно-суставные изменения включают метастатическую кальцификацию, явления генерализованного остеопороза, эрозивных остеоартритов, ограниченную подвижность и деформацию пальцев рук, сгибательные контрактуры, боли в конечностях, артрит и остеомиелит. Отмечаются атеросклеротические изменения сосудов, медленно прогрессирует катаракта, снижаются интеллектуальные способности. После 30 лет проявляются эндокринные заболевания – сахарный диабет, гипогонадизм, тиреопатии. У 5-10% больных обнаруживаются злокачественные опухоли различных органов, костей и кожи. Причиной смерти становится онкопатология или тяжелое сердечно-сосудистое заболевание.
Диагностика
Диагноз прогерии устанавливается на основании клинико-анамнестических данных. В зависимости от имеющейся симптоматики в диагностике могут принимать участие эндокринологи, неврологи, дерматологи, терапевты, врачи-генетики. Детскую и взрослую прогерию необходимо дифференцировать с системной склеродермией, пойкилодермией, синдромом Ротмунда-Томсона, синдромом Видемана-Раутенштрауха. К основным методам обследования больных относятся:
- Опрос. В ходе беседы врачи уточняют время появления симптомов, их выраженность, степень физической и социальной дезадаптации, наличие периода обычного развития (6-24 месяца при детской форме, 14-20 лет – при взрослой). Собирают данные семейного и генеалогического анамнеза, выявляя генетическую патологию или ее отсутствие в роду.
- Осмотр. Специалисты оценивают неврологический статус, пассивную и активную подвижность суставов, костные деформации, состояние кожи и подкожной клетчатки, сохранность зрения, интеллектуальных функций. Пациенты могут быть направлены на инструментальные исследования: рентгенографию костей, УЗИ и МР-томографии органов, ЭКГ, офтальмоскопию.
- Биогенетическое исследование. Выполняется анализ генетического материала методом секвенирования ДНК. Исследуются участки генов, дефекты в которых приводят к развитию прогерии. У пациентов с детской и взрослой формой болезни обнаруживаются мутации в гомозиготном и компаунд-гетерозиготном состоянии.
Лечение прогерии
Специфические методы терапии прогерии не разработаны. Медицинская помощь пациентам заключается в облегчении симптомов болезни. Проводится лечение атеросклероза, остеопороза, остеомиелита, катаракты, диабета, патологий сердца и онкологических заболеваний. Известен случай, когда состояние больного заметно улучшилось на несколько лет после операции трансплантации сердца.
Научные исследования ведутся в области генной инженерии – совершаются попытки выделить мутационный ген из ДНК и заменить его здоровым. Параллельно разрабатывается метод этиотропной терапии. Ученые из Швеции нашли способ нейтрализации дефектных молекул ламина A, которые проникают в мембрану клеточных ядер и способствуют гибели клетки. Положительные результаты получены на экспериментах с мышечной тканью крыс, на людях препарат пока не опробован. В США с 2012 года ведется изучение эффективности применения ингибитора фарнезилтрансферазы (лекарственного средства, разработанного для лечения рака). После терапии дети из экспериментальной группы чувствовали себя лучше, повысилась жесткость и эластичность артерий, плотность костей, снизились случаи транзиторных ишемических атак, сердечных патологий, утраты зрения и слуха. Продолжительность жизни увеличилась на 1,6-6 лет.
Прогноз и профилактика
В среднем больные детской прогерией доживают до 13 лет, зарегистрированы случаи смерти в 7 и 27 лет. Продолжительность жизни при взрослом типе заболевания составляет 30-40 лет. Причиной летального исхода становятся атеросклеротические осложнения и злокачественные новообразования. Профилактические меры отсутствуют. Предупредить рождение больного ребенка можно при наследственном характере болезни – при синдроме Вернера, в отдельных случаях синдрома Хатчинсона, когда патология выявлена в семье, будущие родители отнесены к группе высокого риска. Таким парам назначается медико-генетическое консультирование.
Источник
«Глядя на это обрюзгшее лицо, ввалившиеся глаза и дряблую кожу, вряд ли можно подумать, что это ребенок. Однако это так». Историю 5-летнего Байезида Хосейна, который живет на юге Бангладеш, знают многие. Мальчик страдает от редкого генетического заболевания – прогерии, при котором тело и организм стареют в восемь раз быстрее обычного. Начинается все с атрофии мышц, дистрофических процессов в зубах, волосах и ногтях, изменений в костно-суставном аппарате, заканчивается этот процесс атеросклерозом, инсультом и злокачественными опухолями. Как мы видим, у прогерии совсем не обнадеживающие симптомы, которые перерастают в смертельно опасные болезни. Поэтому таких пациентов всегда ждет фатальный исход. Но можно ли им облегчить мучения и даже продлить жизнь? Или, быть может, ученые уже находятся в шаге от создания лекарства от этого нарушения? Расскажем в сегодняшней статье.
Детская прогерия, или синдром Гетчинсона (Хатчинсона) – Гилфорда
Впервые недуг, при котором организм преждевременно стареет, был выявлен и описан в 1889 году Дж. Хатчинсоном и независимо от него в 1897 году – Х. Гилфордом. В их честь и назвали синдром, проявляющийся в детском возрасте.
Несмотря на то что прогерия – заболевание достаточно редкое (лишь у одного из 7 млн новорожденных его диагностируют), за всю историю наблюдений за этим недугом в мире зафиксировано уже более 150 случаев. При рождении дети выглядят абсолютно здоровыми, первые признаки ускоренного старения начинают проявляться у малышей в возрасте 10-24 месяцев.
Причиной болезни является мутация гена LMNA, он производит белок преламин А, образующий уникальную белковую сеть – внутренний каркас ядерной оболочки. Итог — клетки теряют способность нормально делиться.
Исследуя больных, генетики также обнаружили нарушения в репарации (восстановительной функции) ДНК, клонировании фибробластов (основных клеток соединительной ткани) и исчезновение подкожной клетчатки.
Как правило, прогерия – это ненаследственное заболевание, и случаи его развития единичны, но есть и исключения. В нескольких семьях зарегистрирована такая мутация у детей-сибсов — потомков близкородственных родителей. И это свидетельствует о возможности аутосомно-рецессивного типа наследования, который проявляется уже у людей во взрослом возрасте. К слову, случается это с одним из 200 000 человек.
Прогерия у взрослых, или синдром Вернера
Еще в 1904 году немецкий врач Отто Вернер заметил резкие изменения во внешнем виде и состоянии у людей 14-18 лет. Он и открыл синдром, который связан с резкой потерей в весе, отставанием в росте, появлением седины и постепенным облысением.
Все эти превращения подростка в старичка связаны с дефектом гена WRN (ген АТФ-зависимой хеликазы). Роль продуцируемого им белка WRN состоит в том, чтобы поддерживать геномную стабильность и сохранять структуру и целостность ДНК человека. Мутация же со временем нарушает экспрессию генов, ДНК теряет возможность восстановления, что и является причиной преждевременного старения.
В отличие от маленьких пациентов, которые не отстают, а где-то даже превосходят своих сверстников в умственном развитии, у взрослых наблюдается противоположный эффект, т.к. прогерия начинает пагубно влиять и на их интеллектуальные способности.
Около 10% больных к сорока годам сталкиваются с такими страшными заболеваниями, как саркома, рак молочной железы, астроцитома, меланома. Развивается онкология на фоне сахарного диабета и нарушения функций паращитовидных желез. Поэтому средняя продолжительность жизни людей с синдромом Вернера – 30-40 лет.
Craig Whitehead / Unsplash.com
Первое в мире лечение прогерии. Американские ученые испытали уникальный препарат
На данный момент прогерия считается неизлечимой болезнью. Жизнь людей, имеющих синдром Гетчинсона (Хатчинсона) – Гилфорда, обрывается в возрасте 7-13 лет, но есть единичные случаи, когда пациенты доживали до 20, и даже 27 лет. И все это благодаря какому-никакому лечению.
Однако специалистов из Фонда исследований прогерии (PRF) и детской больницы Бостона не устраивала такая статистика. В 2012 г. они начали первые в мире клинические испытания препарата, способного помочь быстро стареющим детям. И, как сообщает EurekAlert!, они в этом деле преуспели.
Изучение больных прогерией растянулось на 2,5 года. Ученые пригласили к участию 28 детей из 16 различных стран мира, у 75% из которых была диагностирована болезнь. Дети приезжали в Бостон каждые четыре месяца и проходили полное медицинское обследование.
В течение всего времени испытуемым дважды в день давали специальный препарат ингибитора фарнезилтрансферазы (FTI), который изначально разрабатывался для лечения рака. Команда исследователей оценивала динамику веса, жесткость артерий (параметр для риска инфаркта и инсульта), а также жесткость и плотность костей (параметр риска остеопороза).
В итоге каждый ребенок чувствовал себя значительно лучше. Дети стали набирать вес, наблюдались улучшения в структуре костей, а самое главное – в сердечно-сосудистой системе.
Как отмечают медики, результаты этого исследования являются весьма обнадеживающими. В дальнейшем планируется продолжить изучение препаратов FTI и их эффекта, что даст дополнительную информацию о сердечно-сосудистых заболеваниях и нормальном процессе старения.
«Результаты этого испытания обнадеживают нашу семью. Мы с волнением и надеждой думаем о будущем Меган. Мы благодарны Фонду исследования прогерии и всем врачам за их стремление помочь моей дочери и всем детям, больным прогерией», – говорит Сэнди Найбор, мать 12-летней Меган, которая участвовала в клинических испытаниях.
Прогерия в культуре и жизни
Уж поверьте мне, никогда не поздно или, в моём случае, никогда не рано быть тем, кем хочешь быть. Нет временных рамок – начни, когда захочешь. Ты можешь измениться или остаться прежним – для этого нет каких-то правил. Мы можем сделать лучший или худший выбор, надеюсь, ты сделаешь лучший.
Этот монолог взят из фильма Дэвида Финчера «Загадочная история Бенджамина Баттона», который базируется на сюжете одноименного рассказа Фрэнсиса Скотта Фицджеральда.
С самого рождения герой этой известной истории был изгоем, т.к. с младенчества имел внешность и состояние здоровья 80-летнего человека: у него были морщины по всему телу и атрофированные ноги. Однако время идет, а Бенджамин, напротив, не стареет, а молодеет. С мужчиной происходит много различных перипетий, и, конечно, в его жизни случается любовь.
Однако, как бы ни любил зритель хорошие финалы, здесь его не случается. Баттон, прожив целую жизнь, в итоге превращается в младенца с маразмом и тихо умирает во сне.
В реальной жизни не бывает таких чудес, и больные прогерией никогда не становятся молодыми. Но, несмотря на свой недуг, такие люди не перестают быть счастливыми. В частности, Леон Бота – южноафриканский художник, музыкант и диджей – известен миру не только своей творческой деятельностью, а также тем, что со страшным заболеванием смог прожить до 26 лет.
Прогерию Леону диагностировали в возрасте 4 лет, но болезнь не сломала ему жизнь. Этот человек любил наслаждаться каждой минутой, хотя и осознавал, что скорая кончина неизбежна. Так, например, в январе 2007 года мужчина организовал свою первую персональную художественную выставку в Дурбанвиле, темой которой стала хип-хоп культура как образ жизни. Отметим, что таких показов у «молодого» человека было несколько.
Бота занимался также диджеингом и тёрнтейблизмом (разновидность диджеинга) и под псевдонимом DJ Solarize выступал в известных клубах. Кроме того, он сотрудничал с южноафриканской группой Die Antwoord и снялся в их видеоклипе на песню Enter the Ninja.
Но, к сожалению, прогерия не щадит никого. Поэтому 5 июня 2011 г. Бота умер от эмболии легочной артерии – патологическое состояние, когда часть сгустка крови (эмбол), оторвавшаяся от первичного места своего образования (часто, ноги или руки), перемещается по кровеносным сосудам и закупоривает просвет легочной артерии.
Сегодня ученые во всех странах мира изучают это загадочное заболевание. Из списка смертельных они хотят перенести его в список трудноизлечимых. Стоит отметить, что в этом направлении наука уже достигла огромных результатов. Однако остается множество вопросов, в которых необходимо разобраться, а именно: каковы сходства и различия частных случаев прогерии и нормального старения организма, как связаны между собой генетические причины синдрома Вернера и Гетчинсона (Хатчинсона) – Гилфорда и как противостоять ускоренному старению организма. Возможно, спустя некоторое время, найдутся ответы, и специалистам удастся предупредить развитие болезни, тем самым они смогут продлить жизнь больным прогерией людям.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Источник
