Синдром гудпасчера код по мкб

Содержание
- Описание
- Дополнительные факты
- Причины
- Симптомы
- Диагностика
- Лечение
- Прогноз
Названия
Название: Синдром Гудпасчера.
Синдром Гудпасчера
Описание
Синдром Гудпасчера. Аутоиммунная патология, характеризующаяся образованием аутоантител к базальным мембранам почечных клубочков и легочных альвеол. Клинически синдром Гудпасчера проявляется рецидивирующими легочными кровотечениями, прогрессирующим гломерулонефритом и почечной недостаточностью. Диагноз синдрома Гудпасчера подтверждается выявлением антител к базальной мембране клубочков (Anti GBM), данными биопсии почек и легких, рентгенологического исследования легких. Лечение синдрома Гудпасчера включает иммуносупрессивную терапию (глюкокортикостероиды, цитостатики), плазмаферез, по показаниям – гемодиализ, трансплантацию почек.
Дополнительные факты
Синдром Гудпасчера — иммуно-воспалительное поражение капилляров почек и легких, протекающее с развитием гломерулонефрита и геморрагического пневмонита. Впервые признаки данной патологии были описаны в 1919 г. Американским патофизиологом Э. У. Гудпасчером, за что болезнь и была названа его именем. В ревматологии синдром Гудпасчера относится к системным васкулитам и нередко обозначается как «геморрагический легочно-почечный синдром», «геморрагическая пневмония с гломерулонефритом», «идиопатический гемосидероз легких с нефритом». Частота развития синдрома Гудпасчера составляет 1 случай на 1 млн. Населения. Отмечается два возрастных пика заболеваемости – в 20-30 лет и 50-60 лет; болеют преимущественно мужчины. При отсутствии лечения синдрома Гудпасчера летальность среди пациентов достигает 75-90%.
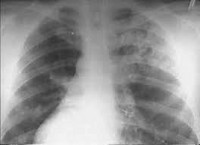
Синдром Гудпасчера
Причины
Этиологические механизмы заболевания достоверно не определены. Клинические наблюдения указывают на связь развития синдрома Гудпасчера с перенесенной вирусной инфекцией (гриппом, вирусным гепатитом А и тд ), приемом лекарственных препаратов (карбимазола, пеницилламина), производственными вредностями (вдыханием паров органических растворителей, лаков, бензина), переохлаждением, курением. Отмечена генетическая предрасположенность к данному синдрому у лиц–носителей HLA-DRwl5, HLA-DR4 и HLA-DRB1 аллелей. Описаны семейные случаи синдрома Гудпасчера.
Под воздействием того или иного этиологического фактора, в результате изменения толерантности иммунной системы, в организме начинается выработка аутоантител к базальным мембранам легочных альвеол и почечных клубочков. Предполагается, что в роли аутоантигена выступает структурный компонент а-3 цепи коллагена IV типа, присутствующий в базальных мембранах легочных и почечных капилляров. Сформировавшиеся антитела (GВМ-антитела) в присутствии С3-комплемента связываются с антигенами; образовавшиеся иммунные комплексы откладываются вдоль базальных мембран, индуцируя иммуно-воспалительное поражение почечных клубочков (гломерулонефрит) и альвеол (альвеолит). В развитии аутоиммунного воспаления большая роль принадлежит активации клеточных элементов (Т-лимфоцитов, эндотелиоцитов, моноцитов, альвеолярных макрофагов, полиморфноядерных лейкоцитов), цитокинов (инсулиноподобного, тромбоцитарного факторов роста, факторов некроза опухоли, интерлейкина-1), свободных радикалов, протеолитических ферментов и других факторов, повреждающих почечную и легочную ткань.
Патоморфологическими субстратами синдрома Гудпасчера служат геморрагический некротизирующий альвеолит и нефрозонефрит. При гистологическом исследовании почечной ткани обнаруживается пролиферативно-мембранозный, пролиферативный или некротизирующий гломерулонефрит, склероз клубочков и фиброз почечной паренхимы. Морфологическое исследование легочной ткани выявляет капиллярит межальвеолярных перегородок, легочные инфильтраты, гемосидероз, пневмосклероз.
Симптомы
Выделяют три варианта клинического течения синдрома Гудпасчера: злокачественный, умеренный и медленный. Для злокачественного течения характерны рецидивирующая геморрагическая пневмония и стремительно прогрессирующий гломерулонефрит. При втором типе легочно-почечный синдром развивается медленнее и выражен умеренно. При третьем варианте синдрома Гудпасчера преобладают явления гломерулонефрита и ХПН; легочные проявления развиваются поздно.
Злокачественный вариант синдрома Гудпасчера дебютирует легочным кровотечением и острой почечной недостаточностью, требующими проведения интенсивной терапии (устранения водно-электролитных нарушений, возмещения кровопотери, ингаляций кислорода, ИВЛ, гемодиализа или перитонеального диализа). В других случаях заболевание может начинаться с общих симптомов: субфебрилитета, недомогания, похудания. Иногда появлению жалоб предшествует перенесенная ОРВИ. Из специфических симптомов обычно первыми развиваются признаки поражения легких — кашель, прогрессирующая одышка, цианоз, боль в грудной клетке, рецидивирующее кровохарканье или легочное кровотечение. Поражение легких при синдроме Гудпасчера нередко осложняется сердечной астмой и отеком легких.
Боль в грудной клетке. Кашель. Кровохарканье. Лейкоцитоз. Недомогание. Одышка. Увеличение СОЭ.
Диагностика
При осмотре пациентов с синдромом Гудпасчера обращает на себя внимание бледность кожных покровов, пастозность или отеки лица. В легких выслушиваются сухие и влажные хрипы, количество которых увеличивается в момент кровохарканья и после него. В общем анализе крови обнаруживается гипохромная анемия, анизоцитоз, пойкилоцитоз, лейкоцитоз, резкое увеличение СОЭ. Для общего анализа мочи характерна протеинурия, цилиндрурия, эритроцитурия; проба по Зимницкому выявляет изогипостенурию. В биохимическом анализе крови определяется нарастание уровня креатинина, мочевины, серомукоида; снижение концентрации железа. Для синдрома Гудпасчера типично обнаружение большого количества эритроцитов, сидерофагов и гемосидерина в общем анализе мокроты.
Наиболее чувствительным и специфичным методом диагностики синдрома Гудпасчера служит определение антител к базальной мембране клубочков (Anti-GBM) с помощью ИФА или РИА. На рентгенограммах легких выявляются множественные очаговые тени. Морфологическое подтверждение синдрома Гудпасчера основывается на данных биопсии легких и почек. Вспомогательное значение имеют результаты инструментальной диагностики: спирометрии, УЗИ почек, ЭКГ, ЭхоКГ.
В рамках проведения диагностических мероприятий необходимо исключить рак легких, туберкулез, бронхоэктазы, идиопатический гемосидероз легких, системную красную волчанку, узелковый периартериит, геморрагический васкулит, синдром Черджа-Стросс, гранулематоз Вегенера, микроскопический полиангиит, криоглобулинемию. Диагностика и лечение синдрома Гудпасчера должны проводиться совместными усилиями специалистов — ревматологов, пульмонологов, нефрологов.
Лечение
В остром периоде синдрома Гудпасчера показано назначение пульс-терапии метилпреднизолоном или комбинированной пульс-терапии (метилпреднизолон+циклофосфан) с последующим переводом на поддерживающую терапию после достижения клинико-лабораторной и рентгенологической ремиссии. С целью элиминации циркулирующих иммунных комплексов проводится плазмаферез. Симптоматическая терапия синдрома Гудпасчера включает переливания эритроцитарной массы и плазмы крови, назначение препаратов железа. При развитии терминальной почечной недостаточности применяются сеансы гемодиализа. Возможно выполнение нефрэктомии с последующей трансплантацией почки, однако это не исключает рецидива некротизирующего гломерулонефрита в трансплантате.
Прогноз
Течение синдрома Гудпасчера неуклонно прогрессирующее; прогноз – мало обнадеживающий. Гибель пациентов происходит, как правило, вследствие профузных легочных кровотечений, тяжелой почечной или дыхательной недостаточности. При злокачественном варианте летальный исход наступает в считанные недели. В остальных случаях средняя продолжительность жизни колеблется от нескольких месяцев до 1-3 лет. В литературе описаны единичные спонтанные ремиссии синдрома Гудпасчера.
Источник
- Описание
- Причины
- Симптомы (признаки)
- Диагностика
- Лечение
Краткое описание
Синдром Гудпасчера — аутоиммунное заболевание, характеризующееся присутствием АТ к коллагену типа IV c a — 3 — цепью (Гудпасчера Аг). Указанный Аг входит в состав базальной мембраны почечных клубочков и альвеолярной мембраны, поэтому основными клиническими проявлениями синдрома Гудпасчера выступают лёгочное кровотечение и прогрессирующий гломерулонефрит. Статистические данные. Распространённость: 0,5 на 1 000 000. Возраст: 5–40 лет. Преобладающий пол — мужской (6:1).
Код по международной классификации болезней МКБ-10:
- M31.0 Гиперчувствительный ангиит
Причины
Этиология неизвестна. К факторам риска относят: курение, респираторную инфекцию, контакт с летучими углеводородами.
Генетические аспекты. Выявлена ассоциация с HLA DRw2.
Патоморфология • Почки •• Эпителиальноклеточные полулуния •• Сморщивание почечных клубочков •• Интерстициальный воспалительный экссудат • Лёгкие •• Внутриальвеолярные кровоизлияния •• Макрофаги, нагруженные гемосидерином •• Фиброз межальвеолярных перегородок.
Симптомы (признаки)
Клиническая картина • Поражение лёгких (опережает поражение почек на несколько недель или месяцев); варьирует от небольшой одышки до повторных лёгочных кровотечений с развитием дыхательной недостаточности • Быстропрогрессирующий гломерулонефрит с развитием почечной недостаточности • Артериальная гипертензия (20%) • Гриппоподобный синдром: лихорадка, миалгии, артралгии, слабость.
Диагностика
Лабораторные данные • ОАК •• гипохромная ЖДА • ОАМ •• микрогематурия •• протеинурия, не достигающая нефротического порога • АТ против Аг базальной мембраны клубочков почек (радиоиммунный метод или метод непрямой иммунофлюоресценции) • Перинуклеарные антинейтрофильные АТ.
Инструментальные данные • Биопсия почек — отложения иммуноглобулинов и комплемента в базальной мембране клубочков, экстракапиллярные полулуния в 50% клубочков • Рентгенография органов грудной клетки — летучие асимметричные облаковидные инфильтраты; деструкция лёгких не характерна.
Дифференциальная диагностика • Гранулематоз Вегенера протекает с деструкцией лёгочной ткани и поражением верхних дыхательных путей • Микроскопический полиангиит, помимо лёгочного и почечного синдромов, имеет и другие (множественный мононеврит, кожные изменения) • Тромбоз почечных вен и ТЭЛА (острое развитие, отсутствие иммунологической активности) • Быстропрогрессирующий гломерулонефрит, осложнённый отёком лёгких.
Лечение
ЛЕЧЕНИЕ
Общая тактика предполагает сочетание плазмафереза, активной иммунодепрессивной терапии и методов коррекции почечной функции. Диета соответствует диете при почечной недостаточности.
Лекарственное лечение • ГК •• Пульс — терапия метилпреднизолоном 30 мг/кг/сут в/в капельно в течение 20–30 мин 3 дня подряд •• Преднизолон после пульс — терапии в дозе 2 мг/кг внутрь до клинического эффекта с постепенным снижением дозы: до 1,75 мг/кг в течение 1 мес, 1,5 мг/кг в течение 3 мес, далее каждую дозу назначают по 6 мес (1,25–1,0–0,75–0,5–0,25 мг/кг), далее каждую дозу назначают по 12 мес (0,125–0,0625 мг/кг). Больным старше 60 лет дозу следует снизить на 25%.
• Цитотоксические иммунодепрессанты применяют в комбинации с ГК •• Циклофосфамид 2–3 мг/кг/сут •• Азатиоприн 1–2мг/кг/сут. Примечания: дозу препарата следует уменьшить на 50% при снижении СКФ до 10 мл/мин; необходим контроль за количеством лейкоцитов и тромбоцитов крови.
Немедикаментозная терапия • Плазмаферез ежедневно или через день в сочетании с иммунодепрессивной терапии в течение 1–2 нед • Гемодиализ — при развитии почечной недостаточности.
Хирургическое лечение • Трансплантация почки в терминальной стадии ХПН. Рецидива заболевания в трансплантате не наблюдают, если перед операцией в крови не обнаруживались АТ к базальной мембране клубочков.
Прогноз неблагоприятен, если на момент постановки диагноза (до начала лечения) уже имеются признаки почечной недостаточности.
Синоним. Синдром лёгочно — почечный наследственный.
МКБ-10 • M31.0 Гиперчувствительный ангиит
Источник
Медицинский эксперт статьи

х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Синдром Гудпасчера, обусловленный наличием специфических антител к базальной мембране капилляров клубочков и/или альвеол, проявляется лёгочными кровотечениями и быстропрогрессирующим гломерулонефритом.
 [1], [2], [3], [4]
[1], [2], [3], [4]
Код по МКБ-10
M31.0 Гиперчувствительный ангиит
Эпидемиология
Заболевание синдром Гудпасчера было впервые описано в 1919 г. E.W. Goodpasture у 18-летнего юноши с массивным лёгочным кровотечением и острой почечной недостаточности, умершего во время эпидемии гриппа.
Заболеваемость синдромом Гудпасчера в Европе не превышает 1 случай на 2 000 000 населения. Доля синдрома Гудпасчера среди всех типов гломерулонефрита составляет 1-5%, а в структуре причин экстракапиллярного гломерулонефрита с полулуниями — 10-20%. Хотя заболевание распространено повсеместно, чаще оно развивается у представителей европеоидной расы. Синдром Гудпасчера может возникать у людей любого возраста. Первый пик заболеваемости отмечают в возрасте 20-30 лет, при этом страдают преимущественно мужчины, у которых имеются признаки как почечного, так и лёгочного поражения. Вторая волна заболеваемости приходится на возраст старше 50-60 лет, причём мужчины и женщины болеют с одинаковой частотой.
 [5], [6], [7], [8]
[5], [6], [7], [8]
Причины синдрома Гудпасчера
Причины синдрома Гудпасчера не известны.
- Развитие синдрома Гудпасчера связывают с вирусной инфекцией, в частности с вирусом гриппа A2.
- Факторы внешней среды, вероятно, играют роль триггеров в развитии заболевания: имеются сообщения о возникновении синдрома Гудпасчера после контакта с бензином, органическими растворителями, использовании некоторых препаратов (пеницилламин). Независимо от роли факторов внешней среды в развитии аутоиммунного процесса, они имеют важное значение в возникновении повреждения лёгких: известно, что лёгочные кровотечения развиваются в основном у курильщиков.
- В последние 10 лет появились описания развития синдрома Гудпасчера после ударноволновой литотрипсии и обструкции мочеточника.
- Механизмы выработки антител к базальной мембране капилляров клубочков неизвестны, однако этому может способствовать генетическая предрасположенность. Установлена связь между развитием синдрома Гудпасчера с антигенами HLA класса DR (HLA-DR15 и HLA-DR4).
Синдром Гудпасчера — классический пример аутоиммунной болезни с антительным механизмом развития. В патогенезе ключевую роль играют антитела к базальной мембране капилляров клубочков.
- Мишенью этих антител служит неколлагеновый домен 3-й цепи коллагена IV типа базальной мембраны клубочков («антиген Гудпасчера», NCI 3IV).
- Коллаген IV типа обнаружен только в составе базальных мембран. Известно, что он состоит из 6 типов цепей: а1-а6. В большинстве базальных мембран разных органов преобладают а1- и а2-цепи, тогда как в базальной мембране клубочков — цепи а3, а4 и а5. Каждая цепь коллагена IV типа состоит из центрального коллагенового домена, N-терминального коллагенового участка (7S-домен) и неколлагенового С-терминального домена (NCI-домен). Три а-цепи коллагена IV типа образуют мономерную структуру, которая связывается со своими NC1-доменами дисульфидными связями.
- При синдроме Гудпасчера AT к базальной мембране капилляров клубочков направлены против NC1-домена а3-цепи коллагена IV типа (NCI 3IV-AT). Этот антиген кроме базальных мембран почек и лёгких обнаружен в других базальных мембранах: капилляров сетчатки, улитки, хориоидального сплетения головного мозга.
- Связывание антител к базальной мембране капилляров клубочков со своими мишенями в гломерулярных и альвеолярных мембранах сопровождается активацией комплемента и вызывает выраженное тканевое повреждение.
- В последнее время в патогенезе нефрита, ассоциированного с антителами к базальной мембране капилляров клубочков, существенную роль отводят также активации клеточных механизмов иммунитета.
 [9], [10], [11]
[9], [10], [11]
Патогенез
Поражение почек при синдроме Гудпасчера морфологически представлено картиной фокального сегментарного некротизирующего гломерулонефрита.
- Уже на ранней стадии болезни в клубочках выявляют сегментарный некроз сосудистых петель, массивную инфильтрацию лейкоцитами, разрывы базальной мембраны клубочков.
- Вслед за этим происходит интенсивное образование полулуний, состоящих из эпителиальных клеток капсулы и макрофагов. Важной отличительной особенностью нефрита, ассоциированного с антителами к базальной мембране капилляров клубочков, при синдроме Гудпасчера является то, что все полулуния одновременно находятся в одной стадии эволюции (эпителиальной) в отличие от других вариантов быстропрогрессирующего гломерулонефрита, при которых эпителиальные полулуния в биоптатах сочетаются с фиброзными.
- По мере прогрессирования болезни в патологический процесс могут вовлекаться все клубочки (диффузный гломерулонефрит) с тотальным некрозом капиллярных петель, что быстро приводит к распространённому нефросклерозу и терминальной почечной недостаточности.
Интерстициальные изменения обычно сочетаются с гломерулярными и представлены воспалительной инфильтрацией интерстиция, которая может развиться в результате повреждающего действия антител к базальной мембране канальцев. В последующем происходит развитие интерстициального фиброза. При иммунофлюоресцентной микроскопии выявляют линейный тип свечения IgG на базальной мембране клубочков в сочетании с линейным свечением СЗ-компонента комплемента у 60-70% больных. Нефрит, ассоциированный с антителами к базальной мембране капилляров клубочков, при синдроме Гудпасчера относят к I типу быстропрогрессирующего гломерулонефрит по классификации R. Glassock (1997).
 [12], [13], [14], [15], [16]
[12], [13], [14], [15], [16]
Симптомы синдрома Гудпасчера
Синдром Гудпасчера может начинаться с появления неспецифических симптомов (общая слабость, недомогание, лихорадка, артралгия, потеря массы тела), менее выраженных по сравнению с аналогичными симптомами при системных васкулитах. Уже в дебюте болезни возможны признаки анемии даже при отсутствии кровохарканья. Однако основные симптомы синдрома Гудпасчера — это прогрессирующая почечная недостаточность вследствие быстропрогрессирующего гломерулонефрита и лёгочные кровотечения.
Поражение лёгких
Кровохарканье — первый симптом синдрома Гудпасчера почти у 70% пациентов, который, как правило, появляется на несколько месяцев раньше признаков поражения почек. В настоящее время отмечают некоторое снижение частоты лёгочных кровотечений, что, как полагают, служит следствием сокращения распространённости курения. Одновременно с кровохарканьем больных беспокоят одышка, кашель.
Выраженность кровохарканья при синдроме Гудпасчера не коррелирует с интенсивностью лёгочного кровотечения, которое может развиться внезапно и привести к смерти больного в течение нескольких часов. В случае лёгочного кровотечения отмечают быстрое развитие дыхательной недостаточности с нарастающими одышкой и цианозом. При аускультации лёгких выслушивают крепитацию в базальных отделах, иногда бронхиальное дыхание. Как персистирующее кровохарканье, так и лёгочное кровотечение приводит к развитию постгеморрагической железодефицитной анемии. Быстрое уменьшение содержания гемоглобина в крови даже при незначительном кровохарканье позволяет диагностировать лёгочное кровотечение. При рентгенологическом исследовании выявляют очаговые или диффузные инфильтраты в базальных и центральных отделах обоих лёгких, расположенные, как правило, симметрично. Обычно инфильтраты исчезают в течение 48 ч, однако часто поражение лёгких осложняется развитием отёка легких или вторичной инфекции, что находит отражение в рентгенологической картине. После купирования острого эпизода интерстициальный фиброз лёгких обычно не развивается.
 [17], [18]
[17], [18]
Поражение почек
Поражение почек при синдроме Гудпасчера может быть изолированным, однако чаще оно сочетается с лёгочным кровотечением. В последнем случае симптомы гломерулонефрита появляются через несколько недель после лёгочного дебюта болезни. Гломерулонефрит проявляется либо микрогематурией с умеренной протеинурией, не превышающей 2-3 г/сут, либо остронефритическим синдромом. Нефротический синдром и артериальная гипертензия при синдроме Гудпасчера развиваются редко. В большинстве случаев заболевание сразу приобретает быстро прогрессирующее течение с развитием олигурическои почечной недостаточности в течение ближайших недель после появления первых симптомов гломерулонефрита. Олигурия при синдроме Гудпасчера служит неблагоприятным прогностическим признаком. Прогрессирование почечной недостаточности у таких пациентов обусловлено также лёгочным кровотечением с гипоксией, анемией, гипергидратацией и присоединением вторичной инфекции.
Диагностика синдрома Гудпасчера
Лабораторная диагностика синдрома Гудпасчера
Наиболее характерные лабораторные симптомы синдрома Гудпасчера — железодефицитная анемия и наличие сидерофагов в мокроте. При лабораторном исследовании обнаруживают также лейкоцитоз и увеличение СОЭ.
Диагностическим признаком болезни синдрома Гудпасчера является обнаружение антител к базальной мембране капилляров клубочков в крови с помощью иммуноферментного анализа.
 [19], [20], [21], [22]
[19], [20], [21], [22]
Какие анализы необходимы?
Дифференциальная диагностика
Синдром Гудпасчера должен быть заподозрен в первую очередь клинически: сочетание поражения лёгких и почек у молодого человека без признаков системного заболевания делает этот диагноз весьма вероятным. Сложности с установлением диагноза «синдром Гудпасчера» могут возникнуть при поражении почек, опережающем поражение лёгких. Однако даже при отсутствии симптомов лёгочного кровотечения наличие быстропрогрессирующего гломерулонефрита без каких-либо признаков системного заболевания, скорее всего, указывает на синдром Гудпасчера. Подтверждением этого диагноза служат антитела к базальной мембране капилляров клубочков в крови и линейное свечение IgG, чаще в сочетании с СЗ-компонентом комплемента на базальной мембране клубочков в биоптате почки.
Дифференциальная диагностика синдрома Гудпасчера проводится прежде всего с системными васкулитами, в клинической картине которых центральное место занимает лёгочно-почечный синдром. Выраженность лёгочных кровотечений при наличии быстропрогрессирующего гломерулонефрита особенно сближает клиническую картину синдрома Гудпасчера и микроскопического полиангиита. Трудности дифференциальной диагностики в этих ситуациях усугубляются тем, что почти у 10% пациентов с ANCA-ассоциированными васкулитами, у большинства из которых определяют бета-ANCA (антитела против миелопероксидазы), обнаруживают также циркулирующие антитела к базальной мембране капилляров клубочков в сыворотке крови. У таких больных течение заболевания больше напоминает васкулит, чем болезнь, связанную с наличием антител к базальной мембране капилляров клубочков, с лучшим ответом на лечение.
 [23], [24], [25], [26], [27], [28], [29], [30], [31], [32]
[23], [24], [25], [26], [27], [28], [29], [30], [31], [32]
Лечение синдрома Гудпасчера
Лечение синдрома Гудпасчера требует применения глюкокортикоидов и цитостатических препаратов в комбинации с сеансами плазмафереза.
- При концентрации креатинина в крови менее 600 мкмоль/л назначают преднизолон внутрь в дозе 1 мг/кг массы тела в сутки и циклофосфамид в дозе 2-3 мг/кг массы тела в сутки. По достижении стабильного клинического эффекта дозу преднизолона постепенно снижают в течение последующих 12 нед, а циклофосфамид полностью отменяют через 10 нед лечения. Терапию иммуносупрессивными препаратами сочетают с интенсивным плазмаферезом, который проводят ежедневно. В случае риска развития лёгочного кровотечения часть удалённой плазмы замещают свежезамороженной плазмой. Стабильный эффект развивается после проведения 10-14 сеансов плазмафереза. Такой режим лечения синдрома Гудпасчера позволяет добиться улучшения функции почек почти у 80% больных, причём снижение азотемии начинается уже через несколько суток после начала плазмафереза.
- При содержании креатинина в крови более 600 мкмоль/л агрессивная терапия малоэффективна и улучшение функции почек возможно лишь у небольшого числа больных с недавней историей заболевания, бурным прогрессированием (в течение 1-2 нед) и наличием в биоптате почки потенциально обратимых изменений. В этих ситуациях основную терапию проводят в сочетании с сеансами гемодиализа.
В случае развития обострений синдрома Гудпасчера применяют тот же терапевтический режим, что и в дебюте болезни.
Данные о трансплантации почки у пациентов с синдромом Гудпасчера немногочисленны. Принимая во внимание тот факт, что после трансплантации возможно усиление продукции антител к базальной мембране капилляров клубочков, рекомендуется при синдроме Гудпасчера выполнять её не ранее чем через 6 мес после исчезновения антител из циркуляции. Всем пациентам с пересаженной почкой следует проводить тщательное мониторирование, включающее кроме контроля гематурии и концентрации креатинина определение титра антител к базальной мембране капилляров клубочков в динамике. Рецидив нефрита, ассоциированного с антителами к базальной мембране капилляров клубочков, в трансплантате наблюдают в 1-12% случаев.
Прогноз
При несвоевременной диагностике синдрома Гудпасчера, влекущей за собой отсрочку начала лечения, прогноз у пациентов с синдромом Гудпасчера неблагоприятный. В этих случаях больные умирают от фульминантного лёгочного кровотечения или быстро наступившей уремии.
Раннее лечение синдрома Гудпасчера, направленное на удаление антител к базальной мембране капилляров клубочков из крови и подавление их продукции (при применении плазмафереза в комбинации с назначением глюкокортикоидов и цитостатиков), может привести к купированию острого эпизода болезни. Однако концентрация креатинина в крови, превышающая 600 мкмоль/л в момент установления диагноза, служит неблагоприятным в отношении почечного прогноза фактором даже при отсутствии лёгочного кровотечения. У таких больных, как правило, развивается необратимая хроническая почечная недостаточность, несмотря на активную иммуносупрессивную терапию.
При синдроме Гудпасчера возможны ранние рецидивы почечно-лёгочного синдрома, развивающиеся в тех случаях, когда основные клинические признаки болезни уже были подавлены с помощью глюкокортикоидов и иммуносупрессирующих препаратов, а титр антител к базальной мембране капилляров клубочков в крови ещё не стал нормальным. У таких пациентов прекращение сеансов плазмафереза или, чаще, присоединение интеркуррентной инфекции может спровоцировать новый рост титров антител к базальной мембране капилляров клубочков и развитие клинической симптоматики. Обострения синдрома Гудпасчера после адекватного лечения первого эпизода описаны, однако развиваются крайне редко и возникают через многие годы от начала болезни спонтанно или после перенесённой инфекции. Поскольку в этих случаях установление диагноза «синдром Гудпасчера» трудностей не вызывает, лечение начинают раньше и исход лучше, чем при первом эпизоде болезни.
Несмотря на применение в настоящее время агрессивной иммунодепрессивной терапии, смертность в остром периоде синдрома Гудпасчера варьирует от 10 до 40%.
 [33], [34]
[33], [34]
Источник
