Синдром гистиоцитов цвета морской волны


Болезнь Ниманна-Пика – это редкое наследственное заболевание, характеризующееся накоплением липидов в различных органах и тканях, что приводит к нарушению их функций. Отличительной особенностью является выраженный клинический полиморфизм. Наиболее частыми считаются очаговые неврологические симптомы, задержка нервно-психического развития, гепато- и спленомегалия. В диагностике используется определение активности специфических ферментов, гистологические исследования, церебральная томография, молекулярно-генетический анализ. Для лечения применяются симптоматическую, субстрат-редуцирующую терапию.
Общие сведения
Болезнь Ниманна-Пика (БНП, сфингомиелиноз, сфингомиелиновый липидоз) относится к группе лизосомных болезней накопления. Впервые нозология была описана немецким педиатром А. Ниманном в 1914 г., в 1930 г. немецкий патологоанатом Л. Пик опубликовал патоморфологические данные. Выделяют 3 типа заболевания, различающиеся по патогенезу, эпидемиологии, характеру течения. Распространенность типов А и B среди общей популяции составляет 1 случай на 250 000 человек, типа С – 1 на 120-150 000 населения. У евреев-ашкенази тип А встречается намного чаще, по разным данным 1:40 000-1:100 000.
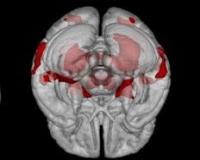
Болезнь Ниманна-Пика
Причины
В основе возникновения всех разновидностей болезни Ниманна-Пика лежат генетические мутации. Типы А и B вызваны мутацией гена SMPD-I, расположенного в локусе 11p15.4-p15.1. Это ген кодирует энзим кислую сфингомиелиназу. Причиной типа С являются мутации генов NPC1 (локус 18q11-q12) и NPC2 (локус 14q24). Данные гены кодируют белки-переносчики, участвующие в транспорте холестерина и других липидов внутри клетки. Патология наследуется по аутосомно-рецессивному типу.
Патогенез
Механизмы развития заболевания на патогенетическом уровне при разных типах болезни Ниманна-Пика несколько различаются. В результате генетической мутации при БНП-А возникает практически полная недостаточность кислой сфингомиелиназы, что ведет к быстрому накоплению сфинголипидов в ЦНС и других внутренних органах.
Это сопровождается стремительным развитием грубой неврологической симптоматики и летальным исходом уже в раннем детском возрасте. Другая разновидность мутации того же гена при типе B вызывает лишь 20%-е снижение функциональной активности сфингомиелиназы. Поэтому отложение липидов происходит преимущественно в клетках ретикулоэндотелиальной системы (печень, селезенка).
При болезни Ниманна-Пика типа С из-за нарушения работы белков-транспортеров в клетках накапливаются разные классы липидов – неэстерифицированный холестерин, сфингомиелин, гликосфинголипиды. Поражается нервная система, внутренние органы. Агрегации холестерина вызывают вторичное снижение активности сфингомиелиназы за счет подавления ее синтеза.
Классификация
В клинической практике выделяются 3 основные разновидности БНП:
- Тип А (классический инфантильный). Самая тяжелая форма. Характеризуется ранним началом, прогрессирующим течением, быстрым наступлением смерти.
- Тип B (висцеральный). Типично более умеренное течение, поздний дебют. Неврологические симптомы практически отсутствуют.
- Тип С. Наиболее распространенный вид с крайне разнообразной симптоматикой. В зависимости от возраста начала манифестации подразделяется на следующие формы:
- неонатальная – до 3 месяцев;
- ранняя младенческая – от 3 месяцев до 2 лет;
- поздняя младенческая – от 2 до 6 лет;
- юношеская (ювенильная) – от 6 до 15 лет;
- взрослая – старше 15 лет.
Симптомы болезни Нимана-Пика
Тип А
Первые признаки появляются почти с самого рождения – это увеличение печени, селезенки, лимфоузлов. С 4-6 месяцев у ребенка снижается аппетит, присоединяются тошнота, рвота. Такие базовые навыки, как способность удерживать голову, ходьба, речь, значительно задерживаются. На втором году жизни формируется спастичность мышц. При глубоком нейродегенеративном поражении головного мозга развиваются нарушение дыхания и сердцебиения, что является основной причиной смерти.
Тип В
Для данной разновидности неврологические симптомы не характерны. Основные симптомы – гепатоспленомегалия, генерализованная лимфаденопатия, частые респираторные инфекции. Поражение дыхательной системы несет наибольшую угрозу для жизни. Инфильтрация альвеол приводит к формированию интерстициальной патологии легких к 20-25 годам, поэтому пациенты испытывают серьезные проблемы с дыханием.
Тип С
Данный тип болезни Ниманна-Пика отличается широким спектром клинических симптомов. Наиболее часто заболевание дебютирует с 7-12 лет. Помимо задержки общего развития имеется снижение общего мышечного тонуса, нарушение походки, координации движений, часто возникают падения. Специфичным неврологическим признаком является ограничение движения глаз при взгляде вверх и вниз.
Еще одним патогномоничным, но редким симптомом считается геластическая катаплексия – внезапная потеря мышечного тонуса в ногах, руках или шее, которая провоцируется эмоциями, например смехом. Ребенок испытывает затруднения при произношении слов или звуков, речь становится невнятной, неразборчивой. Возможны непроизвольные болезненные спазмы мышц лица или кистей рук. Вследствие нарушенного глотания часто возникают поперхивания при приеме пищи.
Нередко происходят тонико-клонические, генерализованные эпилептические припадки. У ребенка значительно ухудшается способность к обучению, запоминанию, быстро утрачиваются недавно приобретенные навыки. У 25% пациентов встречаются острые психозы с галлюцинациями. Иногда отмечаются депрессия, биполярное, обсессивно-компульсивное расстройство (ОКР). Из симптомов поражения внутренних органов характерна гепатоспленомегалия с холестазом.
Осложнения
Для заболевания характерно большое количество осложнений. К наиболее опасным относятся остановка дыхательной или сердечной деятельности вследствие поражения глубинных структур головного мозга. При неонатальной форме БНП типа С быстро прогрессирует печеночная, дыхательная недостаточность, высока вероятность развития водянки плода.
Из-за снижения тонуса мышц глотки возможно попадание пищи в дыхательные пути (аспирация). Инфильтраты в легких способствуют возникновению пневмоний, увеличению давления в сосудах малого круга кровообращения, формированию легочного сердца (правожелудочковой сердечной недостаточности). Отложение липидов в печеночной ткани может привести к циррозу печени.
Диагностика
Курацией больных с БНП занимаются врачи-педиатры, неврологи. При физикальном обследовании важен неврологический осмотр – оценка мышечного тонуса, сухожильных рефлексов, мозжечковых проб. Дифференцировать болезнь Ниманна-Пика необходимо с болезнью Гоше, Тея-Сакса, Вильсона-Коновалова. Для уточнения диагноза назначаются дополнительные методы исследования:
- Рутинные лабораторные исследования. В АОК часто отмечается снижение количества тромбоцитов, реже – гемоглобина, эритроцитов, лейкоцитов. В биохимическом анализе крови обнаруживается увеличение концентрации печеночных трансаминаз (АЛТ, АСТ), билирубина, холестерина.
- Специфические лабораторные тесты. При типах А, B БНП в лейкоцитах выявляется уменьшение уровня кислой сфингомиелиназы. При типе С в крови резко повышены активность хитотриозидазы, содержание продуктов окисления холестерина – 7-кетостерола, холестан-3,5,6-триола.
- Томографические методы. На КТ или МРТ головного мозга визуализируется атрофия коры больших полушарий и мозжечка, истончение мозолистого тела, умеренное расширение желудочков.
- Гистологические исследования. При окраске биоптата кожи филипином наблюдаются интенсивно светящиеся области, сконцентрированные вокруг ядер, которые представляют собой скопления неэстерифицированного холестерина. В аспирате костного мозга отмечается инфильтрация пенистыми клетками (клетками Ниманна-Пика), лазурные гистиоциты.
- ДНК-диагностика. Самый точный метод исследования, позволяющий достоверно подтвердить болезнь Ниманна-Пика – молекулярно-генетическое тестирование, при котором определяются мутации генов SMPD-1, NPC-1, NPC-2.
Лечение болезни Ниманна-Пика
Консервативная терапия
Всем пациентам показана обязательная госпитализация в стационар. Специфическая терапия БНП-А и БНП-В пока не разработана, проводится только симптоматическое лечение. Для прерывания начального звена патогенеза БНП-С назначается субстрат-редуцирующая терапия – препарат миглустат, блокирующий начальные этапы синтеза гликосфинголипидов.
Таким образом значительно уменьшается накопление сфинголипидов в тканях. Благодаря приему миглустата удается добиться замедления прогрессирования и регресса неврологической симптоматики. Препараты для симптоматической терапии всех видов болезни Ниманна-Пика следующие:
- Противосудорожные. Для предупреждения эпилептических припадков назначаются антиконвульсанты – карбамазепин, вальпроевая кислота, ламотриджин.
- Психотропные. С целью коррекции психических расстройств применяются нейролептики (хлорпротиксен), селективные ингибиторы обратного захвата серотонина (флуоксетин).
- Холиноблокаторы и миорелаксанты. Пациентам с дистонией и мышечными спазмами целесообразно использование биперидена, баклофена, тизанидина.
- Желчегонные. Для борьбы с внутрипеченочным холестазом эффективным препаратом является урсодезоксихолевая кислота.
- Антидиарейные ЛС и спазмолитики. При развитии диспепсических симптомов на фоне приема миглустата дополнительно назначается лоперамид, дротаверин.
- Статины. Для снижения уровня холестерина в крови применяется аторвастатин или розувастатин.
Хирургическое лечение
Оперативные вмешательства оказались успешными только в случае болезни Ниманна-Пика-В. Трансплантация стволовых клеток костного мозга у части пациентов позволяет уменьшить степень висцеральных симптомов – гепатоспленомегалии, интерстициального поражения легких. При гиперспленизме с панцитопенией выполняется спленэктомия. Развитие цирроза печени с тяжелой печеночной недостаточностью служит показанием к пересадке печени.
Экспериментальное лечение
Продолжаются исследования по поиску эффективных методов лечения болезни Ниманна-Пика. При экспериментах на лабораторных мышах под влиянием генной терапии в клетках повышалась активность сфингомиелиназы. В настоящее время на стадии клинических испытаний находится препарат 2-гидроксипропил-бетациклодекстрин и заместительная ферментотерапия БНП типа В.
Паллиативное лечение
На позднем этапе заболевания с запущенным нейродегенеративным процессом применяются меры по облегчению состояния больного. При выраженном нарушении глотания может возникнуть необходимость в зондовом питании или наложении гастростомы для того, чтобы обеспечить пациента достаточным количеством питательных веществ и жидкости.
Прогноз и профилактика
В большинстве случаев прогноз для жизни при болезни Ниманна-Пика неблагоприятный. Относительно доброкачественным считается тип В, при котором не затрагивается нервная система. При типе А продолжительность жизни составляет 1-4 года, при типе C – около 10-20 лет с момента постановки диагноза. Наиболее частыми причинами смерти выступают поражения мозговых структур, регулирующих дыхательную и сердечную деятельность.
Реже летальный исход наступает от тяжелых инфекций дыхательных путей, печеночной недостаточности. Основным методом первичной профилактики является пренатальная диагностика на ранних сроках беременности. В ворсинах хориона молекулярно-генетическими тестами определяется наличие мутаций NPC1, NPC2, SMPD-1; в амниоцитах исследуется активность сфингомиелиназы.
Источник
Применение более агрессивной комбинированной полихимиотерапии существенно улучшает прогноз у больных с ходжкинской лимфомой с поражением печени, осложнённым желтухой. Лечение такое же, как при IV стадии заболевания, независимо от наличия желтухи. Аналогичным образом больным с идиопатическим холестазом проводят лечение, соответствующее таковому при лимфоме. При отсутствии эффекта от курса МОРР-терапии проводят лечение по протоколу ABVD. При сохранении желтухи некоторое улучшение можно получить от локального облучения в умеренных дозах.
При обструкции внепеченочных жёлчных путей проводят дистанционную лучевую терапию. При необходимости производят эндоскопическое или чрескожное стентирование общего печёночного или жёлчною протока.
Если причиной желтухи является лекарственная токсичность, можно изменить терапию или снизить дозы.
Лечение неходжкинской лимфомы, осложнённой желтухой, аналогично лечению при болезни Ходжкина.
При первичной лимфоме печени проводят химиотерапию, реже выполняют лобэктомию.
Лимфосаркома
Узлы лимфосаркомы можно обнаружить в печени, особенно в портальных трактах. Макроскопически они напоминают метастазы карциномы. Печень может также вовлекаться в процесс при гигантоклеточной фолликулярной лимфоме.
Множественная миелома
Поражение печени может наблюдаться при плазмоклеточной миеломе; при этом отмечается инфильтрация синусоидов и портальных трактов плазматическими клетками. В результате сопутствующего амилоидоза возможно поражение печёночных артериол.
Ангиоиммунобластная лимфаденопатия
Это заболевание напоминает болезнь Ходжкина. В печени отмечается полиморфная инфильтрация портальных зон (лимфоцитами, плазматическими и бластными клетками) без гистиоцитов или клеток Рид-Штернберга.
Внекостномозговое кроветворение
Примитивные ретикулярные клетки печёночных синусоидов и портальных трактов обладают способностью созревать во взрослые эритроциты, лейкоциты или тромбоциты. Если стимул к регенерации крови достаточно сильный, эта функция может активироваться. У взрослых это встречается редко, в то время как у младенца с анемией миелоидная метаплазия в печени — явление частое. У взрослого человека она наблюдается при замещении или инфильтрации костного мозга и особенно при множественной миеломе, метастатической карциноме костей, миелофиброзе, миелосклерозе и при мраморной болезни костей Альберс-Шёнберга. Внекостномозговой гемопоэз осложняет все состояния, сочетающиеся с лейкоэритробластной анемией.
Удачным примером такого состояния является миелофиброз или миелосклероз, когда отмечается увеличенная печень с гладким плотным краем. Селезёнка значительно увеличена, а её удаление приводит к ещё большему увеличению размеров печени, повышению уровня билирубина и активности ЩФ и ГГТП в сыворотке часто при отсутствии повышения активности сывороточных трансаминаз. Смертность после спленэктомии составляет 10-20%; иногда она вызвана нарушением функции печени вследствие усиления внекостномозгового кроветворения.
Асцит наблюдается у небольшого числа больных с внекостномозговым кроветворением и может быть следствием портальной гипертензии или появления их перитонеальных очагов экстрамедуллярного кроветворения после спленэктомии.
Гистологическая картина
Гистиоцитоз, вызванный пролиферацией клеток Лангерханса (гистиоцитоз X)
В основе этого редкого заболевания лежат пролиферация и агрегация клеток Лангерханса в ретикулоэндотелиальной системе. При электронно-микроскопическом исследовании выявляют трёхслойные палочковидные структуры (гранулы Бирбека) в клетках, содержащих также нейроспецифический белок S-100. Это заболевание включает в себя несколько нозологических единиц, имеющих общие симптомы: эозинофильную гранулёму, протекающую с поражением костей; болезнь Хенда-Шюллера-Крисчена, для которой характерны эндокринные нарушения, поражение кожи; болезнь Леттерера-Сиве диссеминированного типа, проявляющуюся поражением лёгких, костного мозга, кожи, лимфатических узлов, селезёнки, печени. Механизм поражения печени неизвестен. Холестаз обусловлен склерозирующим холангитом с поражением внутрипеченочных протоков или пролиферацией гистиоцитарных клеток в перипортальных зонах. Поражение печени наблюдается у трети больных. Возможно развитие портальной гипертензии и кровотечения из варикозно-расширенных вен пищевода. Печёночная недостаточность, обусловленная билиарным циррозом, встречается редко. Трансплантация печени даёт хорошие результаты. При наблюдении за больными в течение 7 лет после операции рецидивы заболевания отсутствовали.
Болезни накопления липидов
Липидозы — болезни, сопровождающиеся отложением в клетках ретикулоэндотелиальной системы больших количеств липидов. Классификация этих болезней основывается на типе накапливаемого липида: холестерина при ксантоматозе, цереброзида при болезни Гоше, сфингомиелина при болезни Ниманна-Пика.
Первичный и вторичный ксантоматоз
Холестерин в основном накапливается в коже, сухожильных влагалищах, костях и кровеносных сосудах. Печень поражается редко, однако в печёночной ткани могут выявляться изолированные очаги холестеринсодержащих пенистых гистиоцитов. Исследование печени не имеет диагностического значения.
Болезнь накопления эфиров холестерина
Это редкое заболевание связано с недостаточностью кислой гидролазы эфиров холестерина и имеет относительно доброкачественное течение; наследование происходит по рецессивному типу. Характерна бессимптомная гепатоспленомегалия. Печень оранжевого цвета, с избытком эфиров холестерина и нейтрального жира в гепатоцитах. Отмечается также септальный фиброз.
Болезнь Гоше
Это редкое заболевание, наследуемое по аутосомно-рецессивному типу, впервые описано в 1882 г.; встречается в основном у евреев-ашкенази. Является самой частой лизосомальной болезнью накопления, обусловленной дефицитом в лизосомах фермента 13-глюкоцереброзидазы. Указанный дефицит приводит к накоплению субстрата этого фермента в клетках ретикулоэндотелиальной системы всего организма, особенно в клетках печени, костного мозга и селезёнки.
Существует 3 типа заболевания:
- Тип 1 (наблюдается у взрослых, имеет хроническое течение) не сопровождается нейронопатией — самый мягкий и наиболее частый (среди евреев-ашкенази 1:500-2000) тип болезни. Центральная нервная система не поражается.
- Тип 2 (страдают дети, острое течение с поражением нейронов) встречается редко. Кроме висцеральных поражений, отмечается массивное фатальное поражение нервной системы. Дети погибают в младенческом возрасте.
- Тип 3 (ювенильный, имеет подострое течение с поражением нейронов) встречается также редко. Характеризуется постепенным и неравномерным вовлечением нервной системы.
Полиморфизм заболевания обусловлен разнообразием мутаций в структурном гене глюкоцереброзидазы на хромосоме 1, хотя различная по тяжести болезнь может наблюдаться и внутри одного специфического генотипа. Ключевая роль в степени повреждения отводится макрофагальной реакции в ответ на накопление глюкоцереброзида, но механизмы её неизвестны. Однако полный анализ специфических мутаций гена позволяет предсказать клиническое течение заболевания при выявленных генотипах.
Электронно-микроскопическое исследование. Накапливающийся 13-глюкоцереброзид, образующийся из распадающихся клеточных мембран, выпадает в осадок в лизосомах и образует длинные (20-40 мм) трубочки, которые видны при световой микроскопии. Сходные клетки могут обнаруживаться при хроническом миелолейкозе и миеломной болезни, при которых ускорен метаболизм β-глюкоцереброзида.
Хроническая форма у взрослых (тип 1)
Это наиболее часто встречающийся тип болезни. В большинстве случаев болезнь выявляется в возрасте до 30 лет и имеет постепенное начало. Течение хроническое. Диагноз может быть впервые установлен в пожилом возрасте.
Клиническая картина разнообразна и проявляется необъяснимой гепатоспленомегалией (особенно у детей), спонтанными переломами костей или болями в костях и лихорадкой. Возможны также геморрагический диатез и неспецифическая анемия.
К клиническим признакам заболевания относят также пигментацию, которая может быть диффузной или очаговой; при этом кожа имеет рыжевато-коричневый цвет. На нижних конечностях может быть симметричная свинцово-серая пигментация за счёт отложения меланина. На конъюнктиве выявляются жёлтые пингвекулы.
Селезёнка огромных размеров, печень умеренно увеличена, гладкая и плотная. Поверхностные лимфатические узлы обычно не поражаются.
Поражение печени часто сопровождается фиброзом и нарушением функциональных печёночных проб. Активность ЩФ часто повышена, иногда возрастает активность трансаминаз. Могут развиться цирроз и асцит. Портальная гипертензия нередко осложняется кровотечением из варикозно-расширенных вен пищевода.
Рентгенография костей. Длинные трубчатые кости, особенно дистальные отделы бедренной кости, расширены настолько, что имеющееся в норме сужение в надмыщелковой области исчезает. Картина при этом напоминает колбочку Эрленмейера.
В мазках костного мозга можно видеть клетки Гоше, имеющие диагностическое значение.
Аспирационную биопсию печени следует производить при отрицательных результатах стернальной пункции. Поражение печени носит диффузный характер.
Изменения периферической крови. При диффузном поражении костного мозга отмечается лейко-эритробластическая картина. Напротив, лейкопения и тромбоцитопения с увеличением времени кровотечения могут сопровождаться лишь умеренной гипохромной микроцитарной анемией.
Диагноз устанавливают на основании определения активности β-глюкоцереброзидазы в смеси мононуклеарных клеток, получаемых из венозной крови.
Изменения биохимических показателей. Активность ЩФ часто повышена. Иногда возрастает активность трансаминаз. Уровень сывороточного холестерина нормальный.
Лечение
Раньше специфической терапии этой болезни не существовало. Однако в последнее время была доказана клиническая эффективность внутривенных введений модифицированной плацентарной глюкоцереброзидазы, легли козилированной для избирательного захвата маннозовым лецитином на макрофагах. При этом отмечаются уменьшение размеров селезёнки и печени и улучшение гематологических показателей. Клинического эффекта удалось добиться, используя меньшие дозы, чем применялись ранее, что позволяет снизить стоимость лечения.
При чрезвычайно больших размерах селезёнки, а в ряде случаев при тромбоцитопении или приобретённой гемолитической анемии производят спленэктомию или резекцию селезёнки. Полное удаление селезёнки приводит к более агрессивному поражению костей и повышению риска возникновения злокачественных опухолей. В будущем успешная заместительная ферментная терапия устранит необходимость хирургического вмешательства.
При декомпенсированном циррозе производят трансплантацию печени. Она не устраняет метаболический дефект, и для оценки степени повторного накопления липидов печени необходимо длительное наблюдение. Производят также ТКМ, однако её риск существенно выше, чем при проведении заместительной ферментной терапии.
Острая форма у младенцев (тип 2)
Острая форма болезни проявляется в первые 6 мес жизни. Дети обычно умирают, не достигнув 2-летнего возраста. При рождении ребёнок выглядит здоровым. Затем развиваются поражение головного мозга, прогрессирующая кахексия и нарушение психического развития. Увеличиваются размеры печени и селезёнки, могут пальпироваться также поверхностные лимфатические узлы.
При аутопсии выявляют клетки Гоше в ретикулоэндотелиальной системе. Однако они не обнаруживаются в головном мозге, и патогенез его поражения остаётся неясным.
Болезнь Ниманна-Пика
Это редкое семейное заболевание наследуется по аутосомно-рецессивному типу и встречается главным образом у евреев. Болезнь обусловлена дефицитом фермента сфингомиелиназы в лизосомах клеток ретикулоэндотелиальной системы, что приводит к накоплению сфингомиелина в лизосомах. Преимущественно поражаются печень и селезёнка.
Болезнь Нимана-Пика типа А (острая нейронопатическая форма) встречается у детей, которые погибают, не достигнув 2-летнего возраста. Заболевание начинается в первые 3 мес жизни и проявляется анорексией, уменьшением массы тела и задержкой роста. Печень и селезёнка увеличены, кожа становится восковидной и приобретает жёлто-коричневую окраску на открытых частях тела. Поверхностные лимфатические узлы увеличены. В лёгких возникают инфильтраты. Отмечаются слепота, глухота и психические нарушения.
На глазном дне выявляют вишнёво-красные пятна, появляющиеся вследствие дегенерации сетчатки в области макулы.
Анализ периферической крови выявляет микроцитарную анемию, а на более поздних стадиях могут обнаруживаться пенистые клетки Ниманна-Пика.
Заболевание может впервые проявиться перемежающееся холестатической желтухой новорождённых. По мере развития ребёнка появляются неврологические расстройства.
Болезнь Ниманна-Пика типа В (хроническая форма, протекающая без поражения нервной системы) проявляется холестазом новорождённых, который разрешается спонтанно. Цирроз развивается постепенно и может привести к развитию портальной гипертензии, асцита и печёночной недостаточности. Описаны случаи успешной трансплантации печени, произведённой в связи с печёночной недостаточностью. Хотя на протяжении 10-месячного наблюдения не было выявлено никаких признаков отложения липидов в печени, для оценки результата в отношении метаболических нарушений требуется более длительное время.
Диагноз устанавливается на основании пункции костного мозга, которая выявляет характерные клетки Ниманна-Пика, или на основании сниженного уровня сфингомиелиназы в лейкоцитах.
Трансплантация костного мозга производилась у больных с ранним проявлением тяжёлого поражения печени; предварительные результаты оказались обещающими. Отмечено снижение содержания сфингомиелина в печени, селезёнке и костном мозге.
Синдром гистиоцитов цвета морской волны
Подобное состояние проявляется наличием в костном мозге и ретикулоэндотелиальных клетках печени гистиоцитов, приобретающих при окраске по Райту или Гимзе цвет морской волны. В клетках содержатся отложения фосфосфинголипидов и глюкосфинголипидов. Отмечается увеличение размеров печени и селезёнки. Прогноз заболевания обычно благоприятный, хотя описаны случаи развития у этих больных тромбоцитопении и цирроза печени. Возможно, это состояние является одним из вариантов болезни Ниманна-Пика у взрослых.
Источник
