Синдром джервелла ланге нильсена лечение
Медицинская статья опубликована в рубрике: Кардиология, ЛОР, СИНДРОМЫ | Декабрь 9th, 2013
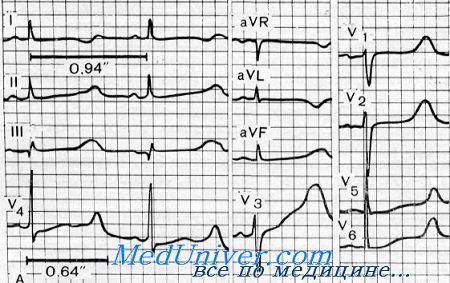
 В 1957 г. Жервелл совместно с Ланге Нильсеном описали синдром, характеризующийся постоянным сочетанием врожденной глухоты, с приступами синкопы и характерными электрокардио графическими изменениями.
В 1957 г. Жервелл совместно с Ланге Нильсеном описали синдром, характеризующийся постоянным сочетанием врожденной глухоты, с приступами синкопы и характерными электрокардио графическими изменениями.
Синдром Жервелла Ланге Нильсена — генетическая аномалия с семейным характером, поражающая оба пола.
Этиопатогенез синдрома Жервелла Ланге Нильсена.
Не существует предположения, которое объяснило бы одновременное нарушение слуха и миокарда. Предположения тех, кто придерживается единого мнения, объясняет аномалию сердца гипокалиемией, а глухоту — нарушением кровоснабжения всего слухового аппарата.
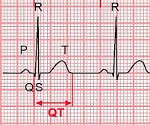
Удлинение интервала Q — Т обусловлено нарушением реполяризации (с неуточненной этиологией), с переменчивой интенсивностью от одного дня к другому, определяя такое же переменчивое изменение интервала Q — Т.
Сердечное синкопе объясняется, как приступ типа Адамса-Стокса, или как приступ венечной ишемии. Смерть, наступившая при этих синкопах, может быть вызвана бесконечным удлинением интервала Q—Т, полной предсердно-желудочковой диссоциацией или фибрилляцией желудочков. Следует подчеркнуть, что синкопе появляются все реже и реже, по мере развития ребенка.
Синдром встречается, как у взрослых, так и у детей; по Fraser, представляет приблизительно 1% всех случаев врожденной глухонемоты. Наследственная передача происходит рецессивным образом, вероятно, как результат палеотропического эффекта аномального гена у гомозигот с полным клиническим проявлением; у гетерозигот синдром проявляется только удлинением интервала Q—T.
Симптоматология синдрома Жервелла Ланге Нильсена.
Врожденная глухота — всегда присутствует; она двусторонняя, обусловливая глухонемоту маленького ребенка. Глухота перцепторного типа, не затрагивает низкие звуки.
Приступы синкопе — повторные, вызываемые обыкновенно волнениями, холодом или даже без видимой причины, продолжаются несколько секунд и внезапно прекращаются.
Во время синкопы у больных отмечается:
- бледность;
- тахикардия;
- полипное;
- больной стонет, теряет или нет сознание;
- иногда появляются судороги.
Несколько минут после прекращения синкопе, у больного затуманенное сознание, затем постепенно приходит в нормальное состояние.
Диагностика синдрома Жервелла Ланге Нильсена.
Электрокардиографические характерные изменения заключаются в:
— патологическом удлинении интервала Q—Т (представляя постоянные и значительные электрокардиографические изменения). В сравнении с нормальным пределом этого интервала (0,31 секунды) величины, встречающиеся у больных, всегда намного выше (в среднем они колеблются между 0,40 и 0,55 секунд при сердечном ритме выше 90/мин).
Фонокардиограмма показывает, что длительность электрической систолы всегда больше механической:
- изменения волны Т очень разнообразна: отрицательная волна, положительная и двухфазная;
- комплекс QRS и интервал Р — Q — всегда нормальные.
Непостоянно добавляется и гипохромная анемия, умеренной интенсивности.
Течение и прогноз синдрома Жервелла Ланге Нильсена.
Течение, как и дальнейший прогноз, неблагоприятные. Смерть ребенка может произойти во время приступа синкопе, тем более, что часто приступ синкопе диагностируется, как приступ эпилепсии и лечат его, как таковой, лишая, таким образом, больного соответствующей экстренной терапии.
Лечение синдрома Жервелла Ланге Нильсена
а) Лечебное:
- экстренное назначение (если диагноз был уточнен) дигиталиса в 1% растворе, 5—6 капель в день, 5 дней в неделю (с еженедельным 2-х дневным перерывом во избежание накопления дигиталиса в миокарде), в течение 3—4 недель. Применением дигиталиса можно избежать смерти во время синкоп, укорачивая и нормализируя интервал Q — R, в отличие от хинидина, который способствует его удлинению (отсюда вытекает абсолютное противопоказание хинидина при приступах синкопе);
- хлористый калий в дозе от 0,5—1 г/день перорально;
- успокаивающие (диазепам).
б) Профилактическое:
- электрокардиографическое исследование всех новорожденных и грудных детей, страдающих судорогами и состоянием синкопе;
- внимание при дифференциальном диагнозе приступа синкопе, который ошибочно может быть принят за приступ эпилепсии; от своевременного и правильного диагноза зависит жизнь больного.
Источник
Синдром Жервелла и Ланге-Нильсена. Кардиоаудиторный или сурдокардиальный синдромJervell и Lange-Nielsen описали синдром глубокой врожденной нейросенсорной глухоты с патологией ЭКГ, характеризующейся удлинением интервала Q—Т, обморочными приступами и иногда внезапной необъяснимой смертью в детском возрасте. Впоследствии синдром был изучен многими авторами (Lcvine, Woodworth, Fraser, Froggatt, James, Jervell, Thingstad, Endsjo, Lisker, Finkelstein, Kallfelz, Sanchez Cascos et al., van Bruggen et al., Fauchier et al., Athanasiou, Weiner). Fraser, Froggatt и Murphy установили его частоту, составляющую от 3 до 4 случаев на 1 млн. рождений. Кроме того, они определили, что синдром может составлять до 1% среди наследственной глухоты. Однако Sanchez Cascos с сотр. нашли только один случай среди 511 глухонемых детей. Fay с соавт. обнаружили одного больного с этим синдромом среди 1100 глухих детей. Кроме того, 4 больных страдали обмороками без удлинения интервала Q—Т, а у 5 больных отмечалось удлинение интервала Q—Т без обмороков. Орган слуха. У всех больных отмечалась врожденная двусторонняя глубокая нейросенсорная глухота. Лабораторные данные. Изменения ЭКГ характеризовались удлинением интервала Q—Т с широкой T-волной, которая могла быть вертикальной, зазубренной, двухфазной или перевернутой. Степень удлинения интервала Q—Т варьировала как внутри одной семьи, так и между разными семьями, но почти всегда превышала 0,5 с (при максимуме 0,4 с В норме). Так как интервал Q—Т удлиняется в зависимости от скорости сердечных сокращений, существует простая формула для определения его величины (Ljting): Q—T= (RRX0,2) +0,18±0,04. В нескольких случаях была обнаружена легкая гипохромная анемия (Jervell, Langc-Nielsen, Fraser, Froggatt, James, Jervell et al., Lamy et al, Kallfelz). Патология. Описаны многочисленные результаты вскрытия. При макроскопическом и гистологическом исследовании сердца в большей части случаев патологии не обнаружили. Специальное исследование проводящей системы сердца показало выраженное сужение главной ветви артерии синусового узла, в результате чего развивался инфаркт узла (Friedmann et al.). Fraser, Froggatt и James обнаружили, что в сердце этих больных отсутствует нормальная гликогенсодержащая перинуклеарная зона в волокнах Пуркинье.
Изменения височной кости описаны Friedmann с соавт.. Наиболее уникальным изменением являлось накопление ПАСК-положительных глыбок гиалина в атрофичной сосудистой полоске. Отмечалась почти полная дегенерация кортиева органа с утратой чувствительных клеток. Покровная мембрана была сморщенной или втянутой, а рейснерова мембрана была сращена с основной мембраной, практически облитсрируя улитковый ход. Чувствительный эпителий утрикулюса и саккулюса был атрофичным, а гребешок дезорганизованным. Отмечалась умеренная утрата нервных клеток спирального узла. Наследственность. Синдром отчетливо наследуется по аутосомно-рецессивному типу. Часто встречаются кровнородственные браки между родителями (Fraser, Froggatt, Murphy, Lamy et al., Sanchez Cascos et al.). У гетерозигот может наблюдаться умеренное удлинение интервала Q—Т (Fraser, Froggatt и Murphy). Предполагают, что заболевание наследуется сцепленно с Rh-фактором (Friedmann, Fraser, Froggatt). Диагноз. Описаны некоторые изменения ЭКГ (такие, как удлинение интервала Q—Т) без глухоты (Johansson, Jorming, van der Straaten, Bruins, Singer et al.). В этих случаях также наблюдались внезапная смерть и/или приступы потери сознания. Однако патология в этих семьях наследовалась по доминантному типу. Jervell описал еще один доминантно наследующийся синдром множественных экстрасистол с приступами фибрилляции желудочков, но с нормальным интервалом Q—Т. Отмечается определенное сходство настоящего заболевания с изменениями, наблюдающимися при синдроме Рефсума. При обоих синдромах выражены нейросенсорная глухота, нарушения сердечной проводимости с удлинением интервала Q—Т и аномальной Т-волной и иногда наступает внезапная смерть. Однако при синдроме Рефсума глухота выявляется в зрелом возрасте и, кроме того, в сыворотке крови повышен уровень фитановой кислоты. Обморочные приступы при синдроме Ланге-Нильсена могут быть ошибочно диагностированы как эпилептические припадки. Однако ЭЭГ нормальна, в то время как ЭКГ резко изменена. Кроме того, после обморочных состояний у детей не развивается глубокого оглушения. Отмечено несколько атипичных случаев. Mathews с соавт. сообщили об аутосомно-доминантной форме с легкой высокочастотной глухотой. Глухота и сердечная патология могут наследоваться как независимые доминантные признаки. Furlancllo с сотр. и Athanasiou и Muller-Seydlitz также описали доминантную форму заболевания у взрослых с легким дефектом слуха. Предполагают также, что в этих семьях имелся синдром «LEOPARD». Читатель, конечно, помнит, что причиной удлинения интервала Q—Т могут служить: гипокалиемия, гипокальциемия, гипомагниемия и введение квинидина и фенотиазина. Прогноз. С возрастом отмечается незначительное прогрессирование дефекта слуха. У больных может наблюдаться различное число обморочных приступов. Примерно в половине случаев больные погибают к 15-летнему возрасту. Было выявлено несколько больных в возрасте старше 21 года. Выводы. Главными чертами этого синдрома являются: — Также рекомендуем «Ушная-зубная или отодентальная дисплазия. Липодистрофия лица, плеч и кисты костей с глухотой» Оглавление темы «Генетические болезни с глухотой»:
|
Источник
Джервелл и Ланге-Нильсена синдром ( JLNS ) представляет собой тип длинного интервала QT синдрома , связанного с тяжелой, двусторонней нейросенсорной потерей слуха . Длинный QT синдром приводит к сердечной мышце , чтобы занять больше времени , чем обычно , чтобы перезарядить между ударами. При отсутствии лечения нерегулярных сердцебиения, называемые аритмии , могут привести к обмороку , судорогам или внезапной смерти. Впервые он был описан Антон Джервелл и Фред Ланге-Нильсена в 1957 году.
Симптомы и признаки
Симптомы этого заболевания являются:
- Врожденная глухота
- синкопа
- Приступы
- Сердцебиение
- Внезапная сердечная смерть
Клинические признаки:
- Продолжительное QTc на ЭКГ
- Двусторонняя нейросенсорная глухота
генетика
Джервелл и Ланге-Нильсена синдром вызывается мутациями в KCNE1 и Kcnq1 генов. Белки , полученные этими двумя генами работают вместе , чтобы сформировать канал калия , который транспортирует положительно заряженный калия ионов из клеток , который называется медленной задержкой выпрямитель тока калия. Движение ионов калия через эти каналы имеет решающее значение для поддержания нормальных функций внутреннего уха и сердечной мышцы. JLNS является аутосомно — рецессивным расстройством означает , что две копии генетической мутации необходима для получения полного синдрома. Мутации в одних и тех же генах могут производить более мягкую Романо-Уорд форму длительного интервала QT синдрома , если только одна копии генетической мутации по наследству.
Около 90% случаев Джервелл и синдрома Ланге-Нильсена вызваны мутациями в Kcnq1 гена, что приводит к Джервелл и Ланге-Нильсена синдром 1 -го типа (JLNS1). KCNE1 мутации ответственны за оставшиеся 10% случаев, в результате чего Джервелл и Ланге-Нильсена синдром 2 -го типа (JLNS2). Мутации в этих генах изменяют обычную структуру и функцию калиевых каналов или предотвратить сборку нормальных каналов. Эти изменения нарушают поток ионов калия во внутреннем ухе и в сердечной мышце, что приводит к потере слуха и нерегулярного ритма сердца характеристики Джервелл и Ланге-Нильсена синдрома.
| Тип | OMIM | Ген | Заметки |
| JLNS1 | 192500 | KCNQ1 | Кодирует альфа-субъединицу медленного задержанного канала выпрямителя калия К V 7.1 , несущей калий ток I Ks . |
| JLNS2 | 176261 | KCNE1 | Зашифровывает норка, калиевые каналы β-субъединица. |
диагностика
Тесты, используемые может быть —
- ЭКГ
- холтеровское мониторирование
- Сердечный Мониторинг событий
- Слуховые тесты
- Генетическое тестирование
- Электролит тесты
- Имплантируемый регистратор петли (ILR) Мониторинг
- Стресс-тестирование ЭКГ / беговая дорожка ЭКГ
лечение
JLNS пациентов с Kcnq1 мутации особенно подвержены патологическим удлинением интервала QT, который предрасполагает их к эпизодам пуантах де пуантах и внезапной сердечной смерти . В связи с этим, если пациент имел синкопальных или история сердца, имплантируемый дефибриллятор сердца должны быть использованы в дополнение к бета — блокаторов , таких как пропранолол .
эпидемиология
Джервеллы и синдром Ланге-Нильсен влияют , по оценкам , один в 166000 до 625000 детей, и отвечают за менее чем 10% от всех случаев длительного интервала QT синдрома. Он имеет значительно более высокий уровень в Норвегии и Швеции на до одного в 200.000.
Рекомендации
внешняя ссылка
Эта статья включает в себя публичный текст домена из американской Национальной медицинской библиотеки
- запись GeneReview / NIH / UW на Джервелл и Lange-Nielsen синдром
Источник

Синдром удлиненного интервала QT – генетически гетерогенное наследственное состояние, характеризующееся нарушением структуры и функциональности некоторых ионных каналов кардиомиоцитов. Выраженность проявлений патологии колеблется в очень широких пределах – от практически бессимптомного течения (выявляются только электрокардиологические признаки) до тяжелой глухоты, обмороков и аритмий. Определение синдрома удлиненного интервала QT производится на основании данных электрокардиологических исследований и молекулярно-генетических анализов. Лечение зависит от формы патологии и может включать в себя постоянный или курсовой прием бета-андреноблокаторов, препаратов магния и калия, а также установку дефибриллятора-кардиовертера.
Общие сведения
Синдром удлиненного интервала QT – группа кардиологических расстройств генетической природы, при которых нарушается прохождение ионных токов в кардиомиоцитах, что способно приводить к аритмиям, обморокам и внезапной сердечной смерти. Впервые подобное состояние было выявлено в 1957 году норвежскими врачами А. Джервеллом и Ф. Ланге-Нильсеном, которые описали сочетание у больного врожденной глухоты, синкопальных приступов и удлинения интервала QT. Несколько позже, в 1962-64 годах были выявлены схожие симптомы у пациентов, имеющих нормальный слух – такие случаи были описаны независимо друг от друга К. Романо и О. Уорд.
Это, а также дальнейшие открытия определили разделение синдрома удлиненного интервала QT на два клинических варианта – Романо-Уорда и Джервелла-Ланге-Нильсена. Первый наследуется по аутосомно-доминантному механизму, его частота в популяции составляет 1 случай на 5 000 населения. Встречаемость синдрома удлиненного интервала QT типа Джервелла-Ланге-Нильсена колеблется в пределах 1-6:1 000 000, он характеризуется аутосомно-доминантным путем наследования и более выраженными проявлениями. По некоторым данным, все формы синдрома удлиненного интервала QT ответственны за треть случаев внезапной сердечной смерти и около 20% внезапной младенческой смерти.
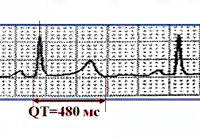
Синдром удлиненного интервала QT
Причины и классификация
В настоящее время удалось идентифицировать 12 генов, мутации в которых приводят к развитию синдрома удлиненного интервала QT, все они кодируют те или иные белки, входящие в состав ионных каналов кардиомиоцитов, отвечающих за натриевый или калиевый ионный ток. Удалось также найти причины различий в клиническом течении этого заболевания. Аутосомно-доминантный синдром Романо-Уорда обусловлен мутацией только одного гена и поэтому может протекать бессимптомно или, как минимум, с отсутствием нарушений слуха. При типе Джервелла-Ланге-Нильсена имеется дефект двух генов – этот вариант, помимо кардиологических симптомов, всегда сопровождается двухсторонней нейросенсорной глухотой. На сегодняшний день известно, мутации каких генов обуславливают развитие синдрома удлиненного интервала QT:
- Синдром удлиненного интервала QT тип 1 (LQT1) обусловлен мутацией гена KCNQ1, расположенного на 11-й хромосоме. Дефекты этого гена наиболее часто выявляются при наличии данного заболевания. Он кодирует последовательность альфа-субъединицы одной из разновидностей калиевых каналов кардиомиоцитов (lKs)
- Синдром удлиненного интервала QT тип 2 (LQT2) вызывается дефектами в гене KCNH2, который локализован на 7-й хромосоме и кодирует аминокислотную последовательность белка – альфа-субъединицы другого типа калиевых каналов (lKr).
- Синдром удлиненного интервала QT тип 3 (LQT3) обусловлен мутацией гена SCN5A, расположенного на 3-й хромосоме. В отличие от предыдущих вариантов патологии, при этом нарушается работа натриевых каналов кардиомиоцитов, так как данный ген кодирует последовательность альфа-субъединицы натриевого канала (lNa).
- Синдром удлиненного интервала QT тип 4 (LQT4) – достаточно редкий вариант состояния, вызванный мутацией гена ANK2, который расположен на 4-й хромосоме. Продуктом его экспрессии является белок анкирин В, который в организме человека участвует в стабилизации структуры микротрубочек миоцитов, а также выделяется в клетках нейроглии и сетчатки глаза.
- Синдром удлиненного интервала QT тип 5 (LQT5) – разновидность заболевания, которая обусловлена дефектом в гене KCNE1, локализованном на 21-й хромосоме. Он кодирует один из белков ионных каналов – бета-субъединицу калиевых каналов типа lKs.
- Синдром удлиненного интервала QT типа 6 (LQT6) вызывается мутацией в гене KCNE2, расположенного также на 21-й хромосоме. Продуктом его экспрессии является бета-субъединица калиевых каналов типа lKr.
- Синдром удлиненного интервала QT типа 7 (LQT7, другое название – синдром Андерсена, в честь педиатра Е. Д. Андерсена, описавшего это заболевание в 70-х годах) обусловлен дефектом гена KCNJ2, который локализуется на 17-й хромосоме. Как и в случае предыдущих вариантов патологии, этот ген кодирует одну из белковых цепей калиевых каналов.
- Синдром удлиненного интервала QT типа 8 (LQT8, другое название – синдром Тимоти, в честь К. Тимоти, описавшей это заболевание) вызван мутацией гена CACNA1C, который располагается на 12-й хромосоме. Этот ген кодирует альфа-1-субъединицу кальциевого канала L-типа.
- Синдром удлиненного интервала QT тип 9 (LQT9) обусловлен дефектом гена CAV3, локализованного на 3-й хромосоме. Продуктом его экспрессии является белок кавеолин 3, участвующий в формировании множества структур на поверхности кардиомиоцитов.
- Синдром удлиненного интервала QT тип 10 (LQT10) – причина этой разновидности заболевания кроется в мутации гена SCN4B, который располагается на 11-й хромосоме и отвечает за аминокислотную последовательность бета-субъединицы натриевых каналов.
- Синдром удлиненного интервала QT тип 11 (LQT11) вызывается дефектами в гене AKAP9, расположенном на 7-й хромосоме. Он кодирует специфический белок – А-киназу центросом и комплекса Гольджи. Функции этого протеина на сегодняшний день изучены недостаточно.
- Синдром удлиненного интервала QT тип 12 (LQT12) обусловлен мутацией гена SNTA1, локализованного на 20-й хромосоме. Он кодирует альфа-1-субъединицу белка синтрофина, участвующего в регуляции деятельности натриевых каналов кардиомиоцитов.
Несмотря на широкое генетическое разнообразие синдрома удлиненного интервала QT, общие звенья его патогенеза в целом одинаковы для каждой из форм. Данное заболевание относят к группе каналопатий из-за того, что его причиной выступают нарушения в строении тех или иных ионных каналов. В результате этого процессы реполяризации миокарда происходят неравномерно и не одновременно в различных частях желудочков, что становится причиной удлинения интервала QT. Кроме того, значительно возрастает чувствительность миокарда к влияниям симпатической нервной системы, что становится причиной частых тахиаритмий, способных приводить к жизнеугрожающим фибрилляциям желудочков. При этом у разных генетических типов синдрома удлиненного интервала QT отмечается различная чувствительность к тем или иным воздействиям. Например, LQT1 характеризуется синкопальными приступами и аритмией при физической нагрузке, при LQT2 аналогичные проявления наблюдаются при громких и резких звуках, для LQT3, напротив, более характерно развитие аритмий и фибрилляций в спокойном состоянии (например, во сне).
Симптомы удлиненного интервала QT
Проявления синдрома удлиненного интервала QT достаточно разнообразны. При более тяжелом клиническом типе Джервелла-Ланге-Нильсена у больных отмечается глухота, частые обмороки, головокружения, слабость. Кроме того, в ряде случаев при этом состоянии регистрируются эпилептоподобные судорожные припадки, что нередко приводит к неправильной диагностике и лечению. По данным некоторых врачей-генетиков, от 10 до 25% больных с синдромом удлиненного интервала QT получают неправильное лечение, и у них развивается внезапная сердечная или младенческая смерть. Возникновение тахиаритмий и синкопальных состояний зависит от внешних влияний – например, при LQT1 это может происходить на фоне физической нагрузки, при LQT2 потеря сознания и фибрилляция желудочков может возникать от резких и громких звуков.
Более легкая форма синдрома удлиненного интервала QT (тип Романо-Уорда) характеризуется преходящими синкопальными состояниями (обмороками) и редкими приступами тахиаритмии, однако нарушения слуха при этом отсутствуют. В ряде случаев подобная форма заболевания вообще ничем не проявляет себя, за исключением электрокардиографических данных, и является случайной находкой при медицинском обследовании. Тем не менее, даже при таком течении синдрома удлиненного интервала QT риск внезапной сердечной смерти из-за фибрилляции желудочков во много раз выше, нежели у здорового человека. Поэтому и эта разновидность патологии требует тщательного изучения и профилактического лечения.
Диагностика
Диагностика синдрома удлиненного интервала QT производится на основании изучения анамнеза больного, электрокардиологических и молекулярно-генетических исследований. При расспросе пациента часто обнаруживаются эпизоды обмороков, головокружений, ощущения сердцебиений, но при легких формах патологии их может и не быть. Иногда аналогичные проявления встречаются у кого-либо из родственников пациента, что указывает на семейный характер заболевания.
При любой форме синдрома удлиненного интервала QT будут выявляться изменения на ЭКГ – увеличение интервала QT до 0,6 секунд и более, возможно увеличение амплитуды зубца Т. Сочетание таких ЭКГ-признаков с врожденной глухотой говорит о наличии синдрома Джервелла-Ланге-Нильсена. Кроме того, часто необходимо холтеровское мониторирование работы сердца на протяжении суток для выявления возможных приступов тахиаритмий. Определение синдрома удлиненного интервала QT при помощи методов современной генетики на сегодняшний день возможно в отношении практических всех генетических типов этого заболевания.
Лечение синдрома удлиненного интервала QT
Терапия синдрома удлиненного интервала QT достаточно сложна, многие специалисты рекомендуют при этом заболевании одни схемы и отвергают другие, но какого-либо единого протокола лечения этой патологии не существует. Универсальными препаратами считаются бета-адреноблокаторы, которые уменьшают риск развития тахиаритмий и фибрилляций, а также снижают степень симпатических воздействий на миокард, но при LQT3 они малоэффективны. В случае синдрома удлиненного интервала QT типа 3 более разумно использовать антиаритмические препараты класса В1. Эти особенности лечения заболевания повышают потребность в молекулярно-генетической диагностике для определения типа патологии. В случае частых приступов тахиаритмий и высокого риска развития фибрилляции рекомендуется имплантация кардиостимулятора или дефибриллятора-кардиовертера.
Прогноз
Прогноз синдрома удлиненного интервала QT, по мнению большинства специалистов, неопределенный, так как это заболевание характеризуется широким спектром выраженности симптомов. Кроме того, отсутствие проявлений патологии, за исключением электрокардиографических данных, не гарантирует внезапного развития фатальной фибрилляции желудочков под воздействием внешних или внутренних факторов. При выявлении синдрома удлиненного интервала QT необходимо произвести тщательное кардиологическое обследование и генетическое определение типа заболевания. На основе полученных данных разрабатывается схема лечения, призванная снизить вероятность внезапной сердечной смерти, или принимается решение об имплантации кардиостимулятора.
Источник