Синдром дыхательного расстройства у детей
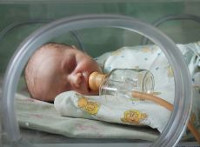
Синдром дыхательных расстройств — патологическое состояние новорожденных, возникающее в первые часы и сутки после рождения вследствие морфофункциональной незрелости легочной ткани и дефицита сурфактанта. Синдром дыхательных расстройств характеризуется дыхательной недостаточностью различной степени выраженности (тахипноэ, цианозом, втяжением уступчивых мест грудной клетки, участием вспомогательной мускулатуры в акте дыхания), признаками угнетения ЦНС и нарушения кровообращения. Синдром дыхательных расстройств диагностируется на основании клинических и рентгенологических данных, оценке показателей зрелости сурфактанта. Лечение синдрома дыхательных расстройств включает оксигенотерапию, инфузионную терапию, антибиотикотерапию, эндотрахеальную инстилляцию сурфактанта.
Общие сведения
Синдром дыхательных расстройств (СДР) – патология раннего неонатального периода, обусловленная структурно-функциональной незрелостью легких и связанным с ней нарушением образования сурфактанта. В зарубежной неонатологии и педиатрии термин «синдром дыхательных расстройств» тождественен понятиям «респираторный дистресс-синдром», «болезнь гиалиновых мембран», «пневмопатии». Синдром дыхательных расстройств развивается примерно у 20% недоношенных (у детей, рожденных ранее 27 недель гестации, – в 82-88% случаев) и 1-2% доношенных новорожденных. Среди причин перинатальной смертности на долю синдрома дыхательных расстройств приходится, по различным данным, от 35 до 75%, что указывает на актуальность и во многом еще нерешенность проблемы выхаживания детей с СДР.

Синдром дыхательных расстройств
Причины синдрома дыхательных расстройств
Как уже указывалось, патогенез синдрома дыхательных расстройств у новорожденных связан с незрелостью легочной ткани и обусловленной этим недостаточностью антиателектатического фактора — сурфактанта, его неполноценностью, ингибированием или повышенным разрушением.
Сурфактант представляет собой поверхностно-активный липопротеиновый слой, покрывающий альвеолярные клетки и уменьшающий поверхностное натяжение легких, т. е. предупреждающий спадение стенок альвеол. Сурфактант начинает синтезироваться альвеолоцитами с 25-26 недели внутриутробного развития плода, однако его наиболее активное образование происходит с 32-34 недели гестации. Под действием многих факторов, в числе которых гормональная регуляция глюкокортикоидами (кортизолом), катехоламинами (адреналином и норадреналином), эстрогенами, гормонами щитовидной железы, созревание системы сурфактанта завершается к 35-36-й неделе гестации.
Поэтому, чем ниже гестационный возраст новорожденного, тем меньше у него количество сурфактанта в легких. В свою очередь, это приводит к спадению стенок альвеол на выдохе, ателектазу, резкому снижению площади газообмена в легких, развитию гипоксемии, гиперкапнии и респираторного ацидоза. Нарушение альвеолокапиллярной проницаемости приводит к пропотеванию плазмы из капилляров и последующему выпадению гиалиноподобных веществ на поверхность бронхиол и альвеол, что еще в большей степени снижает синтез сурфактанта и способствует развитию ателектазов легких (болезнь гиалиновых мембран). Ацидоз и легочная гипертензия поддерживают сохранение фетальных коммуникаций (открытого овального окна и артериального протока) – это также усугубляет гипоксию, приводит к развитию ДВС-синдрома, отечно-геморрагического синдрома, дальнейшему нарушению образованию сурфактанта.
Риск развития синдрома дыхательных расстройств повышается при недоношенности, морфо-функциональной незрелости по отношению к гестационному возрасту, внутриутробных инфекциях, гипоксии плода и асфиксии новорожденного, ВПС, пороках развития легких, внутричерепных родовых травмах, многоплодии, аспирации мекония и околоплодных вод, врожденном гипотиреозе и др. Материнскими факторами риска развития синдрома дыхательных расстройств у новорожденного могут служить сахарный диабет, анемия, родовое кровотечение, родоразрешение с помощью кесарева сечения.
Классификация синдрома дыхательных расстройств
На основании этиологического принципа различают синдром дыхательных расстройств гипоксического, инфекционного, инфекционно-гипоксического, эндотоксического, генетического (при генетически обусловленной патологии сурфактанта) генеза.
На основании развивающихся патологических сдвигов выделяют 3 степени тяжести синдрома дыхательных расстройств.
I (легкая степень) – возникает у относительно зрелых детей, имеющих при рождении состояние средней тяжести. Симптоматика развивается только при функциональных нагрузках: кормлении, пеленании, проведении манипуляций. ЧД менее 72 в мин.; газовый состав крови не изменен. Состояние новорожденного нормализуется в течение 3-4 дней.
II (средне-тяжелая степень) – ребенок рождается в тяжелом состоянии, которое нередко требует проведения реанимационных мероприятий. Признаки синдрома дыхательных расстройств развиваются в течение 1-2 часов после рождения и сохраняются до 10 суток. Необходимость в дотации кислорода обычно отпадает на 7-8 сутки жизни. На фоне синдрома дыхательных расстройств у каждого второго ребенка возникает пневмония.
III (тяжелая степень) – обычно возникает у незрелых и глубоко недоношенных детей. Признаки синдрома дыхательных расстройств (гипоксия, апноэ, арефлексия, цианоз, резкое угнетение ЦНС, нарушение терморегуляции) возникают с момента рождения. Со стороны сердечно-сосудистой системы отмечается тахикардия или брадикардия, артериальная гипотония, признаки гипоксии миокарда на ЭКГ. Велика вероятность летального исхода.
Симптомы синдрома дыхательных расстройств
Клинические проявления синдрома дыхательных расстройств обычно развиваются на 1-2 сутки жизни новорожденного. Появляется и интенсивно нарастает одышка (ЧД до 60–80 в минуту) с участием в дыхательном акте вспомогательной мускулатуры, втяжением мечевидного отростка грудины и межреберий, раздуванием крыльев носа. Характерны экспираторные шумы («хрюкающий выдох»), обусловленные спазмом голосовой щели, приступы апноэ, синюшность кожных покровов (сначала периоральный и акроцианоз, затем – общий цианоз), пенистые выделения изо рта часто с примесью крови.
У новорожденных с синдромом дыхательных расстройств отмечаются признаки угнетения ЦНС, обусловленные гипоксией, нарастание отека мозга, склонность к внутрижелудочковым кровоизлияниям. ДВС-синдром может проявляться кровоточивостью из мест инъекций, легочным кровотечением и т. д. При тяжелой форме синдрома дыхательных расстройств стремительно развивается острая сердечная недостаточность с гепатомегалией, периферическими отеками.
Другими осложнениями синдрома дыхательных расстройств могут являться пневмонии, пневмоторакс, эмфизема легких, отек легких, ретинопатия недоношенных, некротический энтероколит, почечная недостаточность, сепсис и др. В исходе синдрома дыхательных расстройств у ребенка может отмечаться выздоровление, гиперреактивность бронхов, перинатальная энцефалопатия, нарушения иммунитета, ХНЗЛ (буллезная болезнь, пневмосклероз и др.).
Диагностика синдрома дыхательных расстройств
В клинической практике для оценки степени тяжести синдрома дыхательных расстройств используется шкала И. Сильвермана, где в баллах (от 0 до 2-х) оцениваются следующие критерии: экскурсия грудной клетки, втяжение межреберий на вдохе, западение грудины, раздувание ноздрей, опускание подбородка на вдохе, экспираторные шумы. Суммарная оценка ниже 5 баллов свидетельствует о легкой степени синдрома дыхательных расстройств; выше 5 – средней, 6—9 баллов — о тяжелой и от 10 баллов – о крайне тяжелой степени СДР.
В диагностике синдрома дыхательных расстройств решающее значение отводится рентгенографии легких. Рентгенологическая картина изменяется в различные патогенетические фазы. При рассеянных ателектазах выявляется мозаичная картина, обусловленная чередованием участков снижения пневматизации и вздутия легочной ткани. Для болезни гиалиновых мембран характерны «воздушная бронхограмма», ретикулярно-надозная сетка. В стадии отечно-геморрагического синдрома определяется нечеткость, размытость легочного рисунка, массивные ателектазы, определяющие картину «белого легкого».
Для оценки степени зрелости легочной ткани и системы сурфактанта при синдроме дыхательных расстройств применяется тест, определяющий отношение лецитина к сфингомиелину в околоплодных водах, трахеальном или желудочном аспирате; «пенный» тест с добавлением этанола в анализируемую биологическую жидкость и др. Возможно использование этих же тестов при проведении инвазивной пренатальной диагностики — амниоцентеза, осуществляемого после 32 недели гестации.
Состояние ребенка, обусловленное синдромом дыхательных расстройств, следует отличать от врожденной пневмонии, пороков дыхательной системы, атрезии хоан, ВПС, родовой травмы, врожденной диафрагмальной грыжи и др. В рамках дифференциальной диагностики выполняется нейросонография, рентгенография позвоночника, люмбальная пункция, ЭКГ, ЭхоКГ и пр.
Лечение синдрома дыхательных расстройств
Ведение ребенка с синдромом дыхательных расстройств осуществляется неонатологом, детским анестезиологом-реаниматологом с привлечением в случае необходимости детского невролога, детского пульмонолога, детского кардиолога и др.
Ребенок с синдромом дыхательных расстройств нуждается в непрерывном контроле ЧС, ЧД, газового состав крови, КОС; мониторинге показателей общего и биохимического анализа крови, коагулограммы, ЭКГ. Для поддержания оптимальной температуры тела ребенок помещается в кувез, где ему обеспечивается максимальный покой, ИВЛ или ингаляции увлажненного кислорода через носовой катетер, парентеральное питание. Ребенку периодически выполняется трахеальная аспирация, вибрационный и перкуторный массаж грудной клетки.
При синдроме дыхательных расстройств проводится инфузионная терапия раствором глюкозы, гидрокарбоната натрия; трансфузии альбумина и свежезамороженной плазмы; антибиотикотерапия, витаминотерапия, диуретическая терапия. Важным слагаемым профилактики и лечения синдрома дыхательных расстройств является эндотрахеальная инстилляция препаратов сурфактанта.
Прогноз и профилактика синдрома дыхательных расстройств
Последствия синдрома дыхательных расстройств определяются сроком родов, тяжестью дыхательной недостаточности, присоединившимися осложнениями, адекватностью проведения реанимационных и лечебных мероприятий.
В плане профилактики синдрома дыхательных расстройств наиболее важным представляется предупреждение преждевременных родов. В случае угрозы преждевременных родов необходимо проведение терапии, направленной на стимуляцию созревание легочной ткани у плода (дексаметазон, бетаметазон, тироксин, эуфиллин). Недоношенным детям необходимо проводить раннюю (в первые часы после рождения) заместительную терапию сурфактантом.
В дальнейшем дети, перенесшие синдром дыхательных расстройств, кроме участкового педиатра, должны наблюдаться детским неврологом, детским пульмонологом, детским офтальмологом.
Источник
Синдром дыхательных расстройств (СДР), по данным ВОЗ, занимает одно из ведущих мест в структуре перинатальной смертности. Летальность детей с СДР, по данным различных авторов, составляет от 35 до 75%. Чаще встречается у недоношенных детей, реже — у доношенных. К. А. Сотникова указывает, что термин “синдром дыхательных расстройств” является условным. По ее определению, “под синдромом дыхательных расстройств подразумевают особое клиническое состояние новорожденного, которое характеризуется ранним возникновением (в первые 2 сут жизни) и зачастую бурным нарастанием на фоне значительного угнетения жизненно важных функций организма симптомов дыхательной недостаточности”.Одной из основных причин СДР являются пневмопатии (гиалиновые мембраны, ателектазы, обширные кровоизлияния в легких, отечно-геморрагический синдром, врожденные пороки развития легких, спонтанный пневмоторакс) и внутриутробные пневмонии. В патогенезе, независимо от причины, вызвавшей СДР, основное значение имеют дефицит сурфактанта и обтурационный синдром, гипоксия, метаболический ацидоз, нарушениеобмена веществ, приводящие кизменению гомеостаза и нарушению функций центральной и вегетативной нервной системы, эндокринной и сердечно-сосудистой систем, нарушению соотношения между вентиляцией и кровотоком, угнетению иммунитета. Большое значение имеют нарушение соотношения между вентиляцией и кровотоком в легких, повышение проницаемости сосудов. Дефициту сурфактанта в настоящее время придают ведущее значение в патогенезе. Считают, что полностью система сурфактанта созревает к 35–36-й неделе внутриутробного развития. У ребенка, родившегося до этого срока, имеющиеся запасы сурфактанта обеспечивают начало дыхания, его недостаток приводит к спадению альвеол на выдохе, резкому возрастанию работы дыхательных мышц. Вследствие спадения альвеол непрерывного газообмена в легких не происходит, что приводит к развитию гипоксемии, гиперкапнии.
Диагностика
Диагноз СДР традиционно ставится на основании данных анамнеза, клинических и рентгенологических симптомов. Рентгенологически определяется характерная для СДР триада признаков, появляющаяся уже в первые часы заболевания:
- диффузное снижение прозрачности легочных полей
- ретикулогранулярная сетчатость
- наличие полосок просветления в области корня легкого (воздушная бронхограмма)
В тяжелых случаях возможно тотальное затемнение легочных полей, границы сердца могут не дифференцироваться.
В последнее время в арсенале медиков появились методы, определяющие степень зрелости как самой легочной ткани, так и системы сурфактанта. В качестве самого распространенного и информативного теста используется определение отношения лецитина к сфингомиелину в околоплодных водах, трахеальной жидкости или аспирате содержимого желудка при рождении. Если этот показатель больше 3, то легкие зрелые, а если менее 2, то риск развития СДР очень высок (50-75%).
Используется также «пенный» тест: при добавлении этанола в жидкость, содержащую сурфактант, и встряхивании образуется пена. Эти же методы могут использоваться и при пренатальной дианостике, но вопрос об амниоцентезе должен решаться индивидуально и при сроке беременности не менее 32 недель, так как в более ранние сроки гестации незрелость легких не вызывает сомнений, а ведение беременности предполагает минимум инвазивных исследований.
Лечение синдрома дыхательных расстройств
Этиологическим методом лечения является введение экзогенных сурфактантов. Применение их возможно как с профилактической, так и с терапевтической целью.
Препараты сурфактанта относятся к четырем категориям:
- естественные препараты, полученные из амниотической жидкости человека (при разрешении доношенной беременности путем кесарева сечения)
- естественные препараты, полученные из измельченных легких поросят и телят
- полусинтетические смеси измельченных легких теленка с дипальмитоилфосфатидилхолином (ДПФХ)
- полностью синтетические сурфактантные препараты.
При применении естественных сурфактантов быстрее наступает клинический эффект, но конечные результаты лечения не отличаются от таковых при назначении искусственных сурфактантов. Предполагается, что сурфактант, выделенный из легких телят и поросят, может вызвать иммунологическую реакцию на чужеродный белок, но убедительных данных получено не было. Наиболее естественный для ребенка сурфактант из амниотической жидкости не может широко использоваться, так как для лечения одного ребенка требуется использование амниотической жидкости от 10 операций кесарева сечения.
Источник
Год утверждения 2016
Профессиональные ассоциации:
- Российская ассоциация специалистов перинатальной медицины
- Российское общество неонатологов
Оглавление
1. Краткая информация
2. Диагностика
3. Лечение
4. Реабилитация
5. Профилактика
1. Краткая информация
1.1 Определение
Синдром дыхательных расстройств новорожденного или «респираторный дистресс-синдром» (РДС) — обусловленное первичным дефицитом сурфактанта и незрелостью лёгких расстройство дыхания у детей в первых дней жизни.
Частота РДС выше при меньшем гестационном возрасте и массе тела.
1.2 Этиология и патогенез
Основные причины РДС:
- нарушение синтеза и экскреции сурфактанта, обусловленное функциональной и структурной незрелостью лёгочной ткани;
- дефект структуры сурфактанта (крайне редко).
1.3 Эпидемиология
1.4 Код по МКБ — 10
Р22.0 — Синдром дыхательного расстройства у новорожденного.
1.5 Классификация
Нет.
1.6 Клиническая картина
- Одышка в первые минуты/часы жизни;
- Экспираторные шумы («стонущее дыхание»);
- Западение грудной клетки на вдохе с напряжением крыльев носа, раздуванием щек (дыхание «трубача»);
- Цианоз;
- Ослабление дыхания, крепитирующие хрипы.
- Нарастающая потребность в дополнительной оксигенации.
2. Диагностика
2.1 Жалобы и анамнез
Факторы риска
Предрасполагающие факторы:
- РДС у сибсов;
- Гестационный диабет и СД 1 типа матери;
- Гемолитическая болезнь плода;
- Преждевременная отслойка плаценты;
- Преждевременные роды;
- Мужской плод и преждевременные роды;
- Кесарево сечение до начала родовой деятельности;
- Асфиксия новорожденного.
2.2 Физикальное обследование
Оценка дыхательной недостаточности по шкале Сильверман (Silverman) для определения эффективности проводимой респираторной терапии или показания для ее начала.
2.3 Лабораторная диагностика
Всем новорожденным с дыхательными нарушениями в первые часы жизни:
- анализы крови на кислотно-основное состояние, газовый состав;
- уровень глюкозы;
- маркеры инфекционного процесса (прокальцитонин);
- клинический анализ крови с нейтрофильным индексом дважды с интервалом 48 часов;
- СРБ дважды с интервалом 48 часов;
- микробиологический посев крови.
При РДС отрицательные маркеры воспаления и микробиологическое исследование.
2.4 Инструментальная диагностика
Рентгенологическое исследование всем новорожденным с дыхательными нарушениями в первые сутки жизни.
Рентгенологическая картина при РДС от уменьшения пневматизации до «белых лёгких».
Характерные признаки РДС:
- диффузное снижение прозрачности лёгочных полей,
- ретикулогранулярный рисунок,
- полоски просветлений в корнях легкого (воздушная бронхограмма).
Изменения неспецифичны и возможны при раннем неонатальном сепсисе и врожденной пневмонии.
2.5 Иная диагностика
Дифференциальная диагностика
- Транзиторное тахипноэ;
- Ранний неонатальный сепсис, врожденная пневмония;
- Синдром мекониальной аспирации;
- Синдром утечки воздуха, пневмоторакс;
- Персистирующая легочная гипертензия;
- Аплазия/гипоплазия легких;
- Врождённая диафрагмальная грыжа.
3. Лечение
3.1 Консервативное лечение
3.1.1 Профилактика гипотермии в родильном зале у недоношенных новорожденных
Основные мероприятия по тепловой защите проводятся в первые 30 секунд жизни.
Объём мероприятий различается у недоношенных более 28 недель более 1000 г массы и у детей с массой тела менее 1000 г. до 28 недель.
3.1.2 Отсроченное пережатие и пересечение пуповины и сцеживание пуповины
У недоношенных новорожденных с ОНМТ и ЭНМТ пережатие и пересечение пуповины через 60 секунд после рождения значительно снижает частоту:
- некротического энтероколита;
- ВЖК;
- сепсиса;
- потребность в гемотрансфузиях.
Решение о пересечении принимается коллегиально акушерами-гинекологами и неонатологами.
Альтернатива при невозможности отсроченного пережатия и пересечения пуповины — сцеживание пуповины.
3.1.3 Неинвазивная респираторная терапия в родильном зале
Недоношенным до 32 недель со спонтанным дыханием предпочтительна стартовая СРАР терапия с давлением 6-8 см Н2О.
Недоношенным более 32 недель СРАР проводят при дыхательных нарушениях.
Продленный вдох:
- при отсутствии дыхания;
- дыхании типа «гаспинг»;
- нерегулярном дыхании.
Обязательное условие «продленного вдоха» лёгких — регистрация показателей ЧСС и пульсоксиметрия SрО2.
При отсутствии самостоятельного дыхания и/или при сохраняющейся брадикардии — начало ИВЛ маской с последующим:
- переходом на СРАР при восстановлении дыхания/ЧСС;
- интубацией при отсутствии дыхания и/или сохраняющейся брадикардии;
- другой алгоритм.
СРАР в родзале осуществляется:
- аппаратом ИВЛ с функцией СРАР;
- ручным аппаратом ИВЛ с Т-коннектором;
- различными системами СРАР.
СРАР проводиться при помощи:
- лицевой маски;
- назофарингеальной трубки;
- интубационной трубки;
- биназальных канюль.
Противопоказания к СРАР в родильном зале:
- атрезия хоан или другие пороки развития ЧЛО;
- пневмоторакс;
- врожденная диафрагмальная грыжа;
- несовместимые с жизнью врожденные пороки;
- кровотечение.
3.1.4 Инвазивная респираторная терапия в родильном зале
Интубация трахеи и ИВЛ при неэффективности СРАР и ИВЛ маской.
Для эффективной ИВЛ у глубоко недоношенных необходимы:
- контроль давления в дыхательных путях;
- поддержание Реер +5-6 см Н2О;
- возможность плавной регулировки концентрации кислорода от 21 до 100%;
- непрерывный мониторинг ЧСС и SрO2.
Стартовые параметры ИВЛ:
- Pip – 20-22 см Н2О,
- Рeep – 5 см Н2O,
- ЧД 40-60 в минуту.
Основной показатель эффективности ИВЛ — возрастание ЧСС>100 уд/мин.
Устройства для индикации СО2 в выдыхаемом воздухе быстро и надежно подтвердят корректное расположение интубационной трубки.
3.1.5 Оксигенотерапия и пульсоксиметрия
С первой минуты жизни мониторинг ЧСС и SрО2 пульсоксиметрия недоношенных в родильном зале.
Основные точки приложения пульсоксиметрии:
- с первых минут жизни непрерывный мониторинг ЧСС;
- предупреждение гипероксии SрО2 не более 95%;
- предупреждение гипоксии с SрО2 не менее 80% к 5 минуте жизни и не менее 85% к 10 минуте.
Стартовая респираторная терапия у детей до 28 недель гестации и менее с FiО2 = 0,3.
Респираторная терапия у детей большего гестационного возраста осуществляется воздухом.
С конца 1-й минуты жизни ориентироваться на показатели пульсоксиметра.
Концентрацию дополнительного О2 меняют ступенчато на 10-20% каждую последующую минуту до достижения целевых показателей.
Одновременно с началом непрямого массажа сердца концентрацию О2 увеличивают до 100%.
Далее при дополнительной оксигенации недоношенного SpO2 поддерживается на 90-94%.
3.1.6 Сурфактантная терапия
Ведение сурфактанта недоношенным с РДС независимо от массы тела.
Профилактически, в первые 20 минут жизни при сроке гестации 26 недель и менее, если мать не получила полный курс антенатальной профилактики стероидами.
Первые 20 минут жизни при гестационном возрасте >30 недель и потребности в интубации в родильном зале.
Первые 2 часа жизни недоношенного гестации >30 недель, потребности в интубации в родильном зале и зависимости от FiО2 >0,3-04.
Недоношенному на стартовой СРАР в родильном зале при потребности в FiО2 0,5 и более для достижения SpО2 = 85% к 10 минуте жизни и сохранении дыхательных нарушений, а также для улучшения оксигенации в последующие 10-15 минут.
К 20-25 минуте жизни необходимо принять решение о введении сурфактанта или транспортировке в ОРИТН на СРАР.
Метод введения сурфактанта на стартовой терапии СРАР в родильном зале:
- малоинвазивный при сроке гестации ≤ 28 недель;
- традиционный при гестации более 28 недель.
Метод введения сурфактанта малоинвазивный/ INSURE в отделении реанимации родившимся на сроке ≤ 35 недель, на СРАР/неинвазивной ИВЛ при >3 баллах по шкале Сильверман в первые сутки и/или потребности в FiО2 до 0,35 1000 г.
Повторное введение сурфактанта после рентгенографии ОРК при гестации ≤35 недель малоинвазивным /INSURE методом:
- на СРАР при переводе на ИВЛ из-за нарастания дыхательных нарушений (FiO2 до 0,3 у пациентов <1000г и до 0,4 у детей >1000г) в первые сутки жизни;
- на ИВЛ при ужесточении параметров вентиляции: МАР до 7 см Н2О и FiO2 до 0,3 у пациентов 1000г в первые сутки жизни.
Третье введение может быть показано детям на ИВЛ с тяжелым РДС.
Интервалы между введениями 6 часов или меньше при нарастании потребности в FiО2 до 0,4.
Разрешены к применению в РФ:
- Порактант альфа – наиболее эффективный
- Бовактант
- Берактант
- Сурфактант БЛ.
Сурфактант может использоваться при врожденной пневмонии у недоношенных.
3.1.7 Неинвазивная респираторная терапия в ОРИТН
Неинвазивная респираторная терапия в сочетании с сурфактантной по показаниям у недоношенных с дыхательными нарушениями.
Оптимальная стартовая неинвазивная респираторная поддержка — неинвазивная ИВЛ через назальные канюли или маску.
Показания:
- стартовая терапия после профилактического малоинвазивного введения сурфактанта без интубации;
- терапия недоношенных после экстубации;
- резистентные к СРАР и кофеину апноэ;
- у недоношенных на СРАР нарастание дыхательных нарушений до 3 баллов и более выше по шкале Сильвермана и/или увеличение потребности в FiО2 >0,4.
Противопоказания:
- шок;
- судороги;
- легочное кровотечение;
- синдром утечки воздуха,
Стартовые параметр для устройств с открытым контуром (вариабельный поток):
- Pip 8-10см Н2О;
- Peep 5-6 см Н2О;
- ЧД 20-30 в минуту;
- Время вдоха 0,7-1,0 секунда.
Стартовые параметры для устройств с полузакрытым контуром (постоянный поток):
- Pip 12-18 см Н2О;
- Peep 5 см Н2О;
- ЧД 40-60 в минуту;
- Время вдоха 0,3-0,5 секунды.
Снижение параметров при использовании неинвазивной ИВЛ:
- для терапии апноэ – снижение частоты искусственных вдохов;
- для коррекции дыхательных нарушений – снижение Pip.
Дальнейший перевод с неинвазивной ИВЛ на СРАР и на дыхание без респираторной поддержки.
Показания для перевода с неинвазивной ИВЛ на традиционную ИВЛ:
- PaCO2 > 60 мм рт.ст.
- FiО2 ≥ 0,4
- Оценка по шкале Сильверман 3 балла и выше.
- Апноэ, повторяющиеся более 4 раз в течение часа.
- Синдром утечки воздуха, судороги, шок, легочное кровотечение.
При отсутствии аппарата неинвазивной ИВЛ для стартовой неинвазивной респираторной поддержки применяется метод спонтанного дыхания через назальные канюли при постоянном положительном давлении в дыхательных путях.
У глубоко недоношенных новорожденных СРАР с вариабельным потоком имеет некоторое преимущество перед системами с постоянным потоком.
Канюли для СРАР должны быть максимально широкими и короткими.
Показания для поддержки спонтанного дыхания новорожденного с помощью назального CPAP:
- недоношенные с гестационным возрастом 32 недели и меньше профилактически в родзале;
- при гестационном возрасте более 32 недель с самостоятельным дыханием и более 3 баллов по шкале Сильверман.
Противопоказания:
- шок;
- судороги;
- легочное кровотечение;
- синдром утечки воздуха.
Стартовые параметры СРАР:
- 5-6 cm H2O,
- FiO2 0,21-0,3.
Повышение потребности в FiO2 более 0,3 у детей менее 1000г и более 0,35-0,4 у детей более 1000г в первые сутки жизни — показание для малоинвазивного/ INSURE введения сурфактанта.
Отмена СРАР — при снижении давления в дыхательных путях до 2 и менее смН2О и отсутствии потребности в дополнительной оксигенации.
Высокопоточные канюли 4-8 л/мин — альтернатива СРАР у некоторых детей при отлучении от респираторной терапии.
3.1.8 Искусственная вентиляция легких у недоношенных с РДС
Проведение ИВЛ через интубационную трубку при неэффективности респираторной поддержки.
Показания для перевода на ИВЛ:
- неэффективность неинвазивных методов респираторной поддержки;
- тяжелые сопутствующие состояния (шок, судорожный статус, легочное кровотечение).
Продолжительность ИВЛ должна быть минимальной.
ИВЛ проводится с контролем дыхательного объёма, что сокращает её длительность и минимизирует частоту БЛД и ВЖК.
Гипокарбия и тяжелая гиперкарбия способствуют повреждению мозга.
При отучении от респиратора допустима умеренная гиперкарбия при рН артериальной крови выше 7,22.
При отучении от ИВЛ используется кофеин.
Для снижения частоты БЛД кофеин следует назначать с рождения всем детям массой менее 1500г, нуждающимся в респираторной терапии.
Для более быстрого отучения от ИВЛ после 1-2 недель жизни возможен короткий курс малых доз дексаметазона.
Не рекомендуется рутинная седация и аналгезия всем детям на ИВЛ.
Показание для перевода на высокочастотную осцилляторную (ВЧО) ИВЛ:
- потребность в дополнительной оксигенации до 45-50%;
- давление к концу вдоха до 25 см Н2О и выше у недоношенных.
3.1.9 Антибактериальная терапия
Новорожденным при РДС не рекомендуется антибактериальная терапия.
В первые 48-72 часа жизни целесообразна антибактериальная терапия с последующей быстрой отменой при дифференциальной диагностики РДС с врожденной пневмонией или ранним неонатальным сепсисом.
Антибактериальная терапия при дифференциальной диагностике возможна:
- детям с массой менее 1500 г;
- детям на инвазивной ИВЛ;
- при сомнительных маркерах воспаления в первые часы жизни.
Препараты выбора:
- комбинация антибиотиков пенициллинового ряда и аминогликозидов;
- один антибиотик широкого спектра из группы защищенных пенициллинов.
Аамоксициллин+клавулоновая кислота противопоказана из-за неблагоприятного воздействия на кишечную стенку у недоношенных.
3.2 Хирургическое лечение
Хирургическое лечение не существует.
4. Реабилитация
Нет.
5. Профилактика и диспансерное наблюдение
При угрозе преждевременных родов транспортировка в акушерские стационары II – III уровня с отделением реанимации новорожденных.
При угрозе преждевременных родов на 32 неделе и ранее транспортировка в стационар III уровня (перинатальный центр).
При угрозе преждевременных родов на сроке 23-34 недели для профилактики РДС, ВЖК и НЭК показан курс кортикостероидов.
Схемы внутримышечной пренатальной профилактики РДС:
- Бетаметазон 12 мг 2 дозы через 24 часа;
- Дексаметазон 6 мг 4 дозы через 12 часов.
Максимальный эффект достигается через 24 часа и продолжается неделю.
Повторный курс при повторной угрозе преждевременных родов на сроке менее 33 недель проводится через 2-3 недели.
При плановом кесаревом сечении из-за отсутствия родовой деятельности при сроке 35-36 недель рекомендуется кортикостероидная терапия.
При угрозе преждевременных родов на ранних сроках короткий курс токолитиков:
- позволит транспортировку беременной в перинатальный центр,
- даст завершить курс антенатальной профилактики РДС кортикостероидами.
При преждевременном разрыве плодных оболочек показана антибактериальная терапия.
Источник
