Синдром ди джорджа с отсутствием тимуса

Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 29 ноября 2019;
проверки требует 1 правка.
Синдром Ди Георга (синдром Ди Джорджа, синдром Ди Джорджи, синдром дисэмбриогенеза 3-4 жаберной дуги, врождённая аплазия тимуса и паращитовидных желёз, синдром 22q11.2, CATCH 22 phenotype[2]) — разновидность идиопатического изолированного гипопаратиреоза; редкое врождённое заболевание. Генетической причиной синдрома Ди Георга является делеция центрального участка длинного плеча хромосомы 22 (22q11.2) размером 1.5-3 млн.п.н. Однако известны случаи, когда при тех же клинических проявлениях имеет место делеция других хромосом — 10р13, 17р13, 18q21 и других. В большинстве случаев делеция происходит во время мейоза при спермато- или овогенезе. Только в 5-10 % случаев дефектная хромосома наследуется по аутосомно-доминантному типу[3]. Характеризуется агенезией или дисгенезом паращитовидных (околощитовидных) желёз, аплазией тимуса (вилочковой железы), приводящей к резкому снижению популяции Т-лимфоцитов и иммунологической недостаточности, врождёнными аномалиями крупных сосудов (дефекты аорты, тетрада Фалло)[4].
Этиология и патогенез[править | править код]
Патология 22-й хромосомы (22q11.2) наследуется по аутосомно-доминантному типу.
Наиболее вероятная причина развития клинической симптоматики при данном синдроме — несбалансированная транслокация, делеция или микроделеция 22-й хромосомы (22q11.2). Большинство случаев спорадические, обусловлены делециями 22q11[5].
Заболевание развивается в результате повреждения закладки 3-4 жаберных карманов, в результате которого нарушается закладка паращитовидных желёз и тимуса. Тип наследования до конца не установлен — некоторые авторы предполагают аутосомно-доминантный тип с различной экспрессивностью[6].
Клиническая картина[править | править код]
Клинически наиболее постоянными проявлениями заболевания является гипопаратиреоз и кандидомикоз, отмечаются аномалии развития носа, рта, ушей[4].
Заболевание характеризуется аплазией тимуса и связано с нарушениями развития тимуса в эмбриональном периоде. Тимусный эпителий не может обеспечить нормальное развитие Т-клеток. В результате у пациентов с данной формой иммунодефицита страдает как клеточный, так и гуморальный иммунный ответ. Дети с подобным иммунодефицитным заболеванием проявляют повышенную чувствительность к вирусным, грибковым и некоторым бактериальным инфекциям.
Возможно течение синдрома в виде изолированной недостаточности паращитовидных желёз или врождённого отсутствия околощитовидных (паращитовидных) желез — гипокальциемические судороги, начиная с периода новорожденности (тетания) и вилочковой железы (различные инфекционные заболевания как следствие иммунологической недостаточности)[6].
Диагностика[править | править код]
Основывается на выявлении типичных для синдрома аномалий развития[6]:
- агенезия или дисгенез паращитовидных желёз;
- аплазия вилочковой железы;
- иммунологическая недостаточность;
- черепно-лицевые дисморфии (микрогнатия, гипертелоризм, антимонголоидный разрез глаз, расщелины губы и нёба, деформированные и/или низко расположенные ушные раковины).
Наиболее яркие проявления — гипопаратиреоз и кандидомикоз. Возможно сочетание с дефектами аорты и тетрадой Фалло. Иногда — катаракта и паховые грыжи. В крови определяется лимфоцитопения, гипокальциемия, гипогамма-глобулинемия[6].
Прогноз[править | править код]
Обычно больные умирают в раннем возрасте от инфекционных заболеваний и сердечной недостаточности[4].
См. также[править | править код]
- DGCR2 — ассоциированный ген
- Гипокальциемический криз
- Тетания
Примечания[править | править код]
- ↑ Disease Ontology release 2019-05-13 — 2019-05-13 — 2019.
- ↑ Burn J. Closing time for CATCH22 (англ.) // J. Med. Genet. (англ.)русск. : journal. — 1999. — October (vol. 36, no. 10). — P. 737—738. — doi:10.1136/jmg.36.10.737. — PMID 10528851.
- ↑ Синдром Ди Джорджи. Центр Молекулярной Генетики при Медико-генетическом научном центре. Дата обращения 18 марта 2016.
- ↑ 1 2 3 Малая энциклопедия врача-эндокринолога / Под ред. А. С. Ефимова. — 1-е изд. — К.: Медкнига, ДСГ Лтд, Киев, 2007. — С. 312. — 360 с. — («Библиотечка практикующего врача»). — 5000 экз. — ISBN 966-7013-23-5.
- ↑ Эндокринология / Под ред. Н. Лавина. — 2-е изд. Пер. с англ. — М.: Практика, 1999. — С. 485, 483, 441—442, 66, 64.. — 1128 с. — 10 000 экз. — ISBN 5-89816-018-3.
- ↑ 1 2 3 4 Симптомы и синдромы в эндокринологии / Под ред. Ю. И. Караченцева. — 1-е изд. — Х.: ООО «С.А.М.», Харьков, 2006. — С. 67-68. — 227 с. — (Справочное пособие). — 1000 экз. — ISBN 978-966-8591-14-3.
Ссылки[править | править код]
- Медиафайлы по теме Синдром Ди Георга в Викискладе
Источник
Общие сведения
Синдром Ди Джорджи еще в некоторых источниках указывают как синдром Ди Георга. Впервые патология была описана в 1965 году американским педиатром и эндокринологом — Анджело Мария Ди Джорджи (фото). По международной классификации десятого пересмотра (МКБ-10) данному иммунодефициту был присвоен код D82.1 и указан как синдром дивертикула глотки, вилочковой железы: алимфоплазия, аплазия либо гипоплазия с иммунной недостаточностью.

Angelo DiGeorge(15.04.1921-11.10.2009)
Синдром Ди Джорджа как первичный иммунодефицит является редким врожденным заболеванием (1 случай на 4-6 тыс. человек) и относится к идиопатическому изолированному гипопаратиреозу – состоянию, для которого характерно снижение выработки паратгормонов и гипокальциемия. Для синдрома свойственно множество фенотипов поражения, осложнений и присоединения сопутствующих нарушений.
Патогенез
Для синдрома Ди Георга характерна аплазия или гипоплазия вилочковой железы (тимуса), а также агенезия или дисгенезия паращитовидных желез в результате нарушений закладки и эмбриональной дифференцировки 3-4 жаберных (глоточных) карманов. Это вызывает резкое снижение популяции Т-лимфоцитов, нарушение их дифференцировки и как следствие — иммунологическую недостаточность. У детей могут развиваться различные врождённые аномалии крупных сосудов, например, дефекты аорты, межжелудочковой перегородки или синий порок сердца.
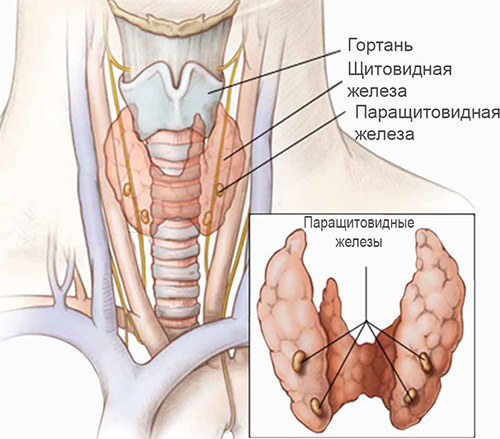
Расположение паращитовидных и щитовидных желез
Классификация
В зависимости от спектра клинических проявлений и врожденных аномалий синдром Ди Георга может быть полным и частичным, к примеру, протекать как изолированная недостаточность паращитовидных желёз либо врождённое отсутствие паращитовидных (околощитовидных) желез, которые приводят к гипокальциемическим судорогам, наблюдающимся у новорожденных в виде неонатальной тетании. Нарушения закладки тимуса приводят к развитию различных инфекционных заболеваний и обычно вызваны иммунологической недостаточностью.
Достаточно часто болезнь протекает в менее тяжелой форме и является наиболее распространенной причиной умственной отсталости с малым количеством других проявлений, поэтому может быть формально не диагностирована.
Причины
У синдрома Ди Джорджи или врождённой аплазии тимуса и паращитовидной железы генетическая причина развития. Патология развивается в результате делеции центрального участка более длинного плеча двадцать второй хромосомы, поэтому еще обозначается как синдром 22q 11.2. Однако, в некоторых случаях аналогичная клиническая картина наблюдалась и после других хромосомных перестроек – транслокаций и микроделеций, развивающихся в таких хромосомах как ТВХ1, 10р13, 17р13, 18q21 и пр. Эти мутации спорадические в 90% и обычно происходят на этапе мейоза спермато— или овогенеза.
Для данного синдрома дисэмбриогенеза 3-4 жаберной дуги — фенотипа CATCH 22 характерно наследование по аутосомно-доминантному типу, которое наблюдается лишь в 5-10% случаев, но при этом не исключается возможность аутосомно-рецессивного типа наследования с разной экспрессивностью.
Симптомы врождённой аплазии тимуса и паращитовидных желёз (Синдром Ди Джорджи)
Синдром Ди Джорджи – это первичный иммунодефицит, вызванный врожденным отсутствием или наличием аномалий развития тимуса и паращитовидных желез, который отличается триадой клинических симптомов, включающей:
- различные врожденные пороки сердца, дефекты крупных сосудов, носа, рта, ушей, что в результате дает специфические черты лица (как на фото): гипертелоризм (увеличенное расстояние между глазами), микрогнатия (недоразвитие нижней челюсти), низкое расположение ушных раковин;
- первичный иммунодефицит – нарушен как клеточный, так и гуморальный ответ иммунитета в результате аплазии вилочковой железы и невозможности обеспечения нормального развития Т-клеток;
- прогрессирующая гипокальциемия (пониженная концентрация кальция в кровотоке) – вызвана гипопаратиреозом, сопровождается судорожным синдромом и развитием скелетных аномалий.
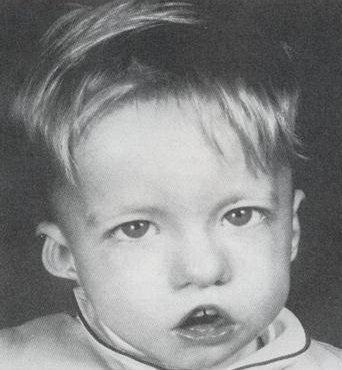
Ребенок со специфическими чертами, характерными для синдрома Ди Джорджи
Особенности синдрома могут широко варьироваться даже в пределах одной семьи и затрагивать различные системы органов. Сопутствующими проблемами становится:
- нарушение работы почек и их атрофия, развитие нефрокальциноза, гидронефроза и пр.;
- проблемы с пищеварением и перистальтикой ЖКТ;
- дефицит гормона роста;
- проблемы с речью;
- психические расстройства, в том числе шизофрения;
- потеря слуха (проводящая и нейросенсорная обычно вызвана черепно-лицевыми синдромами);
- нарушения координации, которые могут быть вызваны гипоплазией мозжечка;
- синюшность кожных покровов в результате плохого кровообращения;
- ревматоидный артрит;
- частые переломы костей;
- болезнь Грейвса;
- болезнь Паркинсона.
Анализы и диагностика
Для подтверждения диагноза синдром Ди Джорджа необходимо выявление агенезии или дисгенеза паращитовидных желёз, аплазии вилочковой железы, иммунологической недостаточности, черепно-лицевых дисморфий (микрогнатии, гипертелоризма, антимонголоидного разреза глаз, расщелины губы и нёба, деформированных и/или низко расположенных ушных раковин) и прочих типичных аномалий развития. При этом оказываются эффективными различные исследования, включая УЗИ, МРТ и пр., а также используются методы генетического тестирования, к примеру, FISH (метод флуоресцентной гибридизации in situ).
Наиболее яркими проявлениями является гипопаратериоз и молочница. Также при плановом обследовании выявляются дефекты аорты, тетрада Фалло, катаракта, паховая грыжа и тому подобное. При помощи серологических исследований можно выявить лимфоцитопению, гипокальциемию, гипоγ-глобулинемии. Благодаря иммунологическим методам удается обнаружить нарушения трансформации лимфоцитов и их функциональной активности, в 20% случаев наблюдается сниженное количество Т-клеток. После иммунологических исследований важно провести дифференциальный диагноз с прочими первичными иммунодефицитами, таким как: синдром Вискотта-Олдрича, Брутона.
Лечение
Так как недуг неизлечим больным обычно назначают симптоматическое и комплексное поддерживающее лечение. Основными приемами считается соблюдение диеты, стерильные условия, прием кальция, комплексов витамин, антибиотиков, противогрибковых, иммуномодулирующих, седативных препаратов и пр.
Доктора
Лекарства
В зависимости от особенностей течения и имеющихся проблем со здоровьем могут быть назначены:
- противовирусные, противогрибковые препараты, а также антибиотики широкого спектра действия для лечения инфекционных заболеваний;
- пожизненный прием витамина Д и кальция;
- заместительная терапия иммуноглобулином.
Процедуры и операции
Для наилучшего прогноза пациентов с синдромом Ди Георга необходимо раннее выявление всех аномалий развития и их устранение стандартными методами лечения:
- трансплантация эмбриональных тканей тимуса;
- кардиохирургия при врожденных пороках сердца.
Первичный иммунодефицит у детей
В результате клеточного иммунодефицита дети с синдромом Ди Джорджи очень подвержены действию инфекции вирусной, грибковой и некоторых разновидностей бактериальной природы. Чаще всего развивается затяжной и тяжелый ринит, пневмония, абсцесс, пиелонефрит, колит, сепсис и т.д. Если ребенку удается пережить пятилетний возраст, то может не обнаруживаться недостаточность Т-клеток, так как антиген-независимый этап созревания Т-клеток начинает происходить не в тимусе, а в многослойном плоском эпителии.
У новорожденных часто возникают судороги и проблемы с кормлением. Младенцы слабые, у них плохой аппетит. Нарушение перистальтики приводит к частым запором. В дальнейшем у деток наблюдается задержка роста и развития, возникают проблемы с обучением, а также когнитивные нарушения, например, приобретение аутистических черт поведения.
У детей с синдромом ДиДжорджа специфический профиль, выявляемый нейропсихологическими тестами. У них нормальный IQ и они способны проходить обучение в обычной школе, дома или заниматься в специальных классах, ведь очень часто у больных есть проблемы с речью (неразборчивость, ошибки артикуляции, сложности при приобретении словарного запаса).
Прогноз синдрома Ди Джорджи
К сожалению, не сегодняшний день, современная медицина оказывается бессильна перед данным генетическим заболеванием. Прогноз крайне неблагоприятный – дети умирают от различных инфекционных заболеваний или сердечной недостаточности, поэтому лучшим способом предупреждения развития врожденных патологий считается медико-генетическое консультирование и пренатальная диагностика наследственных болезней.
Список источников
- Стефани Д.В., Вельтищев Ю.Е. Иммунология и иммунопатология детского возраста.— М., 1996, -С. 27.
- Ивановская Т.Е., Цинзерлинг А.В. Патологическая анатоми.— М., 1976. -С. 136.
Источник
Синдром Ди Джорджи – врожденный дефект, который приводит к гипоплазии или отсутствию тимуса (вилочковой железы) в сочетании с пороками развития крупных сосудов, сердца, паращитовидных желез, костей лицевого черепа и верхних конечностей
СИМПТОМЫ
В связи с тем, что так называемый «полный» синдром Ди Джорджи с серьезными нарушениями иммунитета встречается крайне редко, пациенты с данной патологией обращаются в первую очередь к другим специалистам – кардиологам и хирургам. Характерными проявлениями синдрома Ди Джорджи являются:
Пороки сердца и крупных сосудов.
Гипоплазия (недоразвитие) тимуса ведет к повышенной чувствительности у этих детей к инфекционным заболеваниям (в первую очередь вирусной и грибковой природы).
Гипоплазия паращитовидных желез проявляется развитием судорог.
Синдром также может сопровождаться другими пороками развития:
Нарушения строения лицевого черепа (у детей описывают расщелины верхней губы и нёба, широкую переносицу, высокое нёбо, широкое расстояние между бровями, большой рот).
Нарушения строения глазного яблока.
Пороки развития желудочно-кишечного тракта.
Аномалии скелета (отсутствие ногтей, дополнительные пальчики на конечностях).
Пороки центральной нервной системы проявляются задержкой психомоторного развития.
Нарушение строения гортани, трахеи.
У пациентов с этим синдромом часто встречается патология аутоиммунного характера (аутоиммунный тиреоидит – поражение щитовидной железы, цитопении – снижение количества эритроцитов, нейтрофилов, тромбоцитов), а также повышен риск развития онкологических заболеваний.
ПРИЧИНЫ
Дефект возникает в результате микрополомок на 22 хромосоме приблизительно на 8 неделе беременности. В эти сроки при внутриутробном развитии человека формируются так называемые «глоточные» щели. В результате нарушения формирования 3 и 4-й глоточных щелей (карманов) нарушается и структура органов, происходящих из них – тимуса, дуги аорты, лицевой череп, паращитовидные железы.
В норме вилочковая железа является местом, где проходят созревание Т-клетки, при отсутствии тимуса соответственно страдает Т-клеточное звено иммунной системы. В результате недоразвития паращитовидных желез нарушается регуляция электролитного баланса: прежде всего развивается снижение уровня кальция в крови.
ДИАГНОСТИКА
Общий осмотр пациента : характерные пороки развития
Общий анализ крови: снижение уровня лимфоцитов
Исследование субпопуляций лифоцитов(иммунофенотипирование): снижение количества Т-лимфоцитов
Оценка функциональной активности Т-лимфоцитов: снижение пролиферативной активности Т-лимфоцитов (способности размножаться в ответ на стимуляцию специальным агентом)
Исследование гуморального звена иммунитета: уровень иммуноглобулинов А,М,G, Е — нормальный или понижен
Рентгенологическое исследование органов грудной клетки: отсутствие тени вилочковой железы
ЛЕЧЕНИЕ
Если синдром сопровождается выраженными иммунологическими нарушениями, то для жизни таких больных, как и пациентов с тяжелым комбинированным иммунодефицитом (ТКИН), необходимы стерильные условия, назначение профилактической антимикробной и противовирусной терапии. При снижении уровня гуморального звена иммунитета проводится заместительная терапия внутривенным иммуноглобулином.
При данном заболевании эффективна пересадка эпителиальной ткани тимуса, что ведет к восстановлению количества и функций Т-лимфоцитов. Для коррекции других пороков развития также требуется хирургическое вмешательство.
КОГДА ОБРАТИТЬСЯ К ВРАЧУ
При врожденных пороках развития сердца, лицевого скелета, ЖКТ
При судорогах
При тяжелом течении вирусных инфекций (генерализованная ЦМВ-инфекция, аденовирусная, ротавирусная инфекции)
При упорном грибковом поражении слизистых оболочек
При частых отитах, повторных пневмониях.
Другие статьи
Колонка эксперта — Беллы Брагвадзе. Удивительный мир иммунитета.
Белла Брагвадзе – наш постоянный эксперт, врач педиатр, аллерголог-иммунолог, ассистент кафедры иммунологии РНИМУ им. Н.И. Пирогова , педиатр в мобильной клинике @docplus.ru, врач-волонтер, автор проекта «Воображариум».
Белла ведет два блога в инстаграм:
https://www.instagram.com/bb_immunity/ и https://www.instagram.com/voobrajarium_postcard/ и будет рада новым подписчикам и вопросам.6 июня 2018
Чем настоящий иммунодефицит отличается от частой простуды
Почему дети должны болеть, о бессмысленности иммуномодуляторов и о том, чем настоящий иммунодефицит отличается от частой простуды, — иммунолог Анна Щербина
Иммунодефицит — это состояние, сопровождающееся значительными и долговременными изменениями в иммунной системе и серьезными симптомами. Есть иммунодефициты вторичные, а есть первичные (ПИД). Первичные обусловлены генетически. Как правило, симптомы возникают в раннем возрасте, однако иногда могут возникнуть и у взрослых. Но в любом случае проявления будут очень тяжелыми. С первичными иммунодефицитами встречаются крайне редко. Подтвердить многие такие заболевания можно, обнаружив дефект гена. Но пока, правда, найдены мутации не при всех ПИД, поиск продолжается.
Текст: Дарья Саркисян
Фотографии: Максим Шер
Журнал «Большой город»1 февраля 2018
ЧТО ТАКОЕ ПЕРВИЧНЫЙ ИММУНОДЕФИЦИТ
Что такое Первичный иммунодефицит, как передаётся, как часто встречается, какие есть формы?
1 февраля 2018
Как рассказать детям об иммунитете
Презентация для школьников о том, что такое иммунитет, какие нарушения встречаются, как живут дети с первичным иммунодефицитом и как им можно помочь.
24 ноября 2015
Первичный иммунодефицит. Х-сцепленный лимфопролиферативный синдром
Х-сцепленный лимфопролиферативный синдром – первичный иммунодефицит, при котором у пациентов мужского пола отмечается нарушение иммунного ответа на вирус Эпштейн-Барра.
6 июня 2014
Первичный иммунодефицит. Аутоиммунный лимфопролиферативный синдром
Аутоиммунный лимфопролиферативный синдром – первичный иммунодефицит, при котором отмечается хроническое незлокачественное увеличение лимфоузлов, печени и селезенки, аутоиммунная патология, повышение уровня иммуноглобулинов в крови.
6 июня 2014
Оптимизация диагностики и терапии наследственного ангионевротического отека у взрослых.
Особенности редкой формы первичного иммунодефицита, клинические проявления, иммунологические нарушения и принципы терапии наследственного ангионевротического отека. Индивидуальные планы самоконтроля для каждого пациента и оценкаа их эффективность.
Караулов А.В., Сидоренко И.В., Капустина А.С.
Первый Московский государственный медицинский университет им. И. М. Сеченова, Москва20 мая 2014
Наследственный ангионевротический отек
Наследственный ангионевротичекий отёк — редкое, жизнеугрожающее заболевание, которое относится к группе первичных иммунодефицитов. Причина — недостаточность общего уровня или снижение функциональной активности С1-ингибитора системы комплемента.
Жизнь таких больных становится кошмаром: они никогда не знают, где и когда начнется отек. Пациенты нередко испытывают страх очередного приступа, для них характерны чувство одиночества, ощущение безысходности и бесконечные проблемы на работе, в учебе и быту.20 мая 2014
Первичный иммунодефицит. Хроническая гранулематозная болезнь
Хроническая гранулематозная болезнь (ХГБ) – генетическое заболевание, связанное с дефектом фагоцитов, клеток иммунной системы, которые защищают организм путем поглощения (фагоцитоза) вредных чужеродных частиц, бактерий, а также мертвых или погибающих клеток, из-за которого снижается их антимикробная активность.
13 марта 2013
Иммунодефицитные состояния
Слово «иммунитет» давно вошло в обиход не только врачей, но и не связанных с медициной людей: нам часто приходится слышать его в различных рекламных роликах, передачах по охране окружающей среды и т.д. Действительно, динамические изменения показателей иммунной системы происходят в ответ на различные состояния организма: инфекции, травмы, опухоли. Является ли это патологией? В большинстве случаев – нет, это нормальная реакция живого организма. Ведь основная функция иммунной системы – это борьба со всем чужеродным, будь то бактерия или опухолевая клетка. Однако в некоторых случаях изменения иммунной системы носят долгосрочный, патологический характер, такие состояния называются иммунодефицитными (ИДС).
27 апреля 2012
Первичный иммунодефицит. ОВИН — общая вариабельная иммунная недостаточность
Общая вариабельная иммунная недостаточность — нарушение,
характеризующееся низкими уровнями иммуноглобулинов (антител) в сыворотке крови и повышенной чувствительностью к инфекциям.
Данная статья предназначена для пациентов и членов их семей и не должна заменять совета клинициста-иммунолога.27 июля 2011
Первичный иммунодефицит. Синдром Вискотта-Олдрича
Синдром Вискотта-Олдрича является первичным иммунодефицитным состоянием, поражающим как Т-
лимфоциты, так и В-лимфоциты. Также тяжело поражаются тромбоциты — клетки, помогающие останавливать кровотечение.
Информация в статье предназначена для пациентов и членов их семей и не должна заменять рекомендаций и назначений лечащего врача и клинициста-иммунолога.27 июля 2011
Первичный иммунодефицит. Х-сцепленная агаммаглобулинемия
У больных с Х-сцепленной агаммаглобулинемией основным дефектом является неспособность предшественников В-лимфоцитов созревать до состояния В-лимфоцитов, а затем плазматических клеток. Поскольку у этих больных нет клеток, вырабатывающих иммуноглобулины, наступает тяжелая недостаточность иммуноглобулинов.
Информация в статье предназначена для пациентов и членов их семей и не должна заменять рекомендаций и назначений лечащего врача и клинициста-иммунолога.18 июля 2011
Первичный иммунодефицит. ТКИН — тяжелая комбинированная иммунная недостаточность
Тяжелая комбинированная иммунная недостаточность (ТКИН) — самый тяжелый диагноз в списке первичных иммунодефицитов — является редким синдромом, обусловленным различными генетическими факторами, и сочетающим отсутствие функций Т- и В- лимфоцитов (а во многих случаях также отсутствие функции естественных киллеров или NK-лимфоцитов). Эти нарушения приводят к чрезвычайной чувствительности к тяжелым инфекциям.
Информация в статье предназначена для пациентов и членов их семей и не должна заменять рекомендаций и назначений лечащего врача и клинициста-иммунолога.18 июля 2011
12 настораживающих признаков первичного иммунодефицита
ПИД не СПИД.
Первичный иммунодефицит является врожденным нарушением в иммунной системе, имеющим генетическую природу.
Показанием для направления к иммунологу является сочетание рецидивирующих вирусных и бактериальных инфекций либо наличие тяжелых, затяжных бактериальных инфекций. Данные Всемирной организации здравоохранения свидетельствуют о том, что частота ОРВИ 8 раз в год является нормальным показателем для детей дошкольного и младшего школьного возраста, посещающих детские учреждения.29 июня 2011
Часто болеющие дети: чем они больны на самом деле?
Инфекции уха, горла, носа, а также бронхолёгочные инфекции составляют основной перечень заболеваний в детском возрасте.
Данные ВОЗ свидетельствуют о том, что частота ОРВИ 8 раз в год является нормальным показателем для детей дошкольного и младшего школьного возраста, посещающих детские учреждения.
Показанием для направления к иммунологу является сочетание рецидивирующих вирусных и бактериальных инфекций либо наличие тяжелых, затяжных бактериальных инфекций.29 июня 2011
Иммунодефициты у детей.
Диагноз «иммунодефицит» становится все более популярным у врачей разных специальностей. Создается впечатление, что зачастую врачи, вместо того, чтобы четко определить диагноз и проводить лечение заболевания в соответствии с утвержденными стандартами, назначают иммунотропные средства, не представляя эффект и последствия такой терапии.
29 июня 2011
Диагностика семей с иммунодефицитом
Первичные иммунодефициты, являются наследуемыми заболеваниями, при которых родители являются носителями больного гена и передают его детям. В результате чего у ребенка развивается заболевание. В настоящее время в связи с развитием генетики и иммунологии известны многие гены, мутация в которых приводит к развитию различных форм первичных иммунодефицитов.
9 ноября 2010
Новости фонда
Им нужна ваша помощь!
-

Бабанова Татьяна
6 лет,Республика Мордовия
-

Дамер Эмин
1 год 11 месяцев, Пензенская область
-

Задорова Наталья
4 года, Ярославская область
-

Каштанова Валерия
9 месяцев, Республика Бурятия
-

Кувина Алиса
2 года, Московская область
-

Теркунов Собир
8 лет, Московская область
-

Комарова Ульяна
2 года, респ. Хакасия
-

Пузанова Елизавета
2 года, Республика Бурятия.
-
Лаптев Даниил
7 лет, Нижний Новгород
-

Шеймаер Александр
13 лет, Воронежская область
-

Абдулхаева Амилия
6 месяцев, Москва
-

Ершов Кирилл
14 лет, Самарская область
-

Олейников Даниил
8 лет, Иркутская область
-
Карпухин Михаил
5 лет, Смоленская область
-

Мифтяхутдинов Гали
10 лет, Республика Татарстан
-

Ломаченко Антон
25 лет, Алтайский край
-

Турыхин Андрей
8 лет, Самарская область
-

Андрияшин Алексей
16 лет, Республика Крым
-

Велиева Илаха
6 лет, Оренбургская область
-

Тарасов Игнат
7 лет, Липецкая область
-
Королев Евгений
6 лет, Московская область
-

Жулин Ярослав
16 лет, Костромская область
-

Хабибов Хабиб
8 лет, Республика Дагестан
-

Бобков Григорий
7 месяцев, Ярославская область
-

Вагабов Амир
11 месяцев, Краснодарская область
-

Рузанов Виктор
1 год 4 месяца, Ростовская область
-

Матыцин Алексей
13 лет, Ленинградская область
-

Харламова Вероника
9 лет, Москва
-

Михеева София
3 года, г. Москва
-

Бжекшиева Аурика
17 лет, Кабардино-Балкарская Республика.
-

Репины Илья и Никита
17 лет и 12 лет, г. Ростов-на-Дону
-

Казорина Анастасия
10 лет, Краснодарский край, город Кропоткин
-

Гаджиева Сафият
4 года, Республика Дагестан
-

Плотникова Елена
37 лет, Челябинская область
-

Макаренко Арина
2 года, Чувашская Республика
-

Кузнецов Данил
3 года, Ростовская область
-

Смирнова София
2 года, Костромская область
-

Фазетдинова Даниил
5 года, Москва
-

Галимов Данил
13 лет, Челябинская область, г. Челябинск
-

Кирвович Георгий
9 лет, Волгоградская область
-
Сабурова Анастасия
12 лет, Удмуртская республика
-

Паршакова Арина
6 лет
Пермский край -

Иванов Алексей
7 лет, Республика Чувашия
-

Домошонкин Даниил
5 лет, Иркутская область
-

Хачатурян Милана
3 года, Ростовская область
-

Каюков Кирилл
3 года, Краснодарский край, г. Апшеронск
-

Абзалов Амирхан
7 лет, Республика Татарстан
-

Иванов Максим
16 лет, г. Калуга
-

Власова Мария
18 лет, г. Санкт-Петербург
-

Тыров Тимофей
06.10.2003 гр
Челябинская область -

Михеев Павел
11 лет
г. Владимир -

Юрченко Юлия
17 лет
Иркутская область -

Сухенко Кирилл
1 год
Ростов-на-Дону -

Попова Екатерина
6 месяцев , г. Санкт-Петербург
-

Авиабилеты и железнодорожные билеты
-

Генетические исследования
Лекарственное обеспечение детей с ПИД в отделении иммунологии в НМИЦ ДГОИ им. Дмитрия Рогачева
Фонд «ПОДСОЛНУХ» открывает новую программу по поддержке отделения иммунологии НМИЦ ДГОИ им. Дмитрия Рогачева
-

Чикунова Виктория
13 лет, поселок Знаменка (Тамбовская область)
- Все подопечные
Новости фонда
5 мая 2020
ОНЛАЙН-ПРИЁМ РУССКОГО КЛУБА В ЛЮКСЕМБУРГЕ — ПЕРЕДАЧА ЧЕКОВ БЛАГОТВОРИТЕЛЬНЫМ ФОНДАМ
29 апреля 2020
АНТИКРИЗИСНЫЙ ПРОЕКТ АДРЕСНОЙ ПОМОЩИ «СКАЗКА ПОМОГАЕТ» ПЕРЕЧИСЛИЛ ПЕРВОЕ ПОЖЕРТВОВАНИЕ ФОНДУ «ПОДСОЛНУХ»
27 апреля 2020
ЛЕКЦИЯ ПРОФЕССОРА АННЫ ЩЕРБИНЫ «ИММУНИТЕТ: ДРУГ ИЛИ ВРАГ? УРОКИ ИММУНОДЕФИЦИТОВ И COVID19»
22 апреля 2020
ОТКРЫТИЕ ВСЕМИРНОЙ НЕДЕЛИ ПЕРВИЧНЫХ ИММУНОДЕФИЦИТОВ
21 апреля 2020
#ПОДСОЛНУХПРОТИВКОРОНАВИРУСА
9 апреля 2020
СОВМЕСТНОЕ ЗАЯВЛЕНИЕ ОБ ЭПИДЕМИОЛОГИЧЕСКОЙ ОБСТАНОВКЕ НОВОГО КОРОНАВИРУСА SARS-CoV-2 — COVID-19
8 апреля 2020
НОВАЯ ПРОГРАММА ФОНДА SUNFLOWER TEEN CLUB
1 апреля 2020
COVID-19. НОВОСТИ ИЗ РЕГИОНОВ: КОММЕНТАРИИ ЧЛЕНОВ ПАЦИЕНТСКОГО КОМИТЕТА
31 марта 2020
ВАЖНАЯ ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТОВ С ПИД И ИХ РОДИТЕЛЕЙ
20 марта 2020
РЕЖИМ ПОВЫШЕННОЙ ГОТОВНОСТИ (COVID-19): КАК РЕАЛИЗОВАТЬ СВОИ ПРАВА
- Все новости
Источник


