Синдром дауна открытый артериальный проток
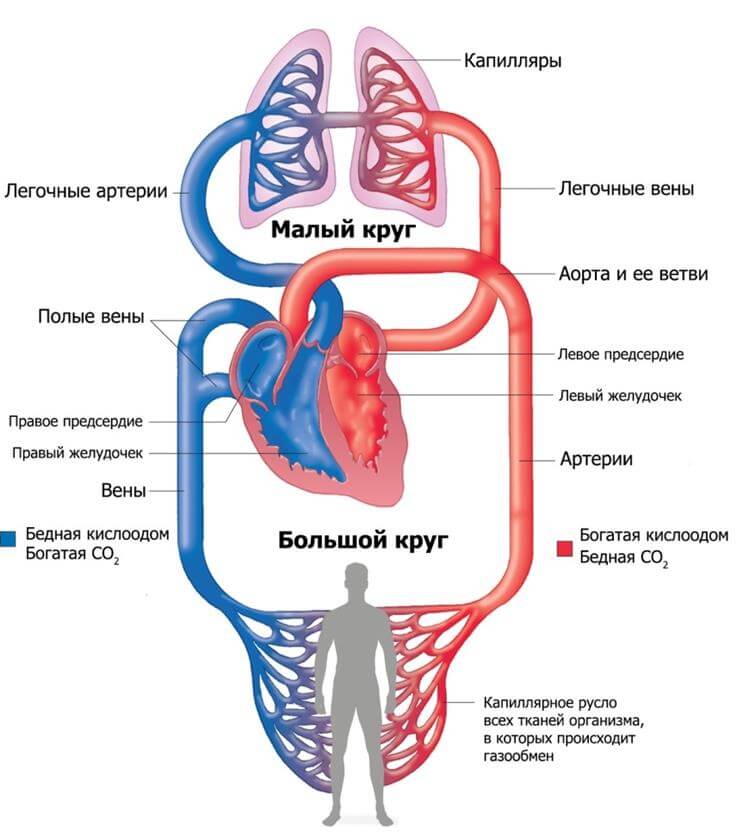
Хорошо известно, что врожденные аномалии сердца встречаются почти у половины детей с синдромом Дауна и оказывают большое влияние на младенческую выживаемость. С середины прошлого столетия проводилось множество исследований по выявлению частоты, специфичности и характера пороков сердца у этих детей. Так, в период 1970–1980-х гг. отмечалось повышение распространенности врожденных аномалий сердечнососудистой системы у пациентов с синдромом Дауна. Связано это было в основном с улучшением диагностики открытого артериального протока и дефекта межпредсердной перегородки (M. J. Khoury, J. D. Erickson, 1992). По данным зарубежных авторов, при синдроме Дауна наиболее часто встречаются дефект межжелудочковой перегородки, дефект межпредсердной перегородки, общий открытый атриовентрикулярный канал, тетрада Фалло и другие пороки, составляющие менее 1 %.
За годы научных наблюдений стало очевидным, что для выявления врожденного порока сердца у новорожденного с синдромом Дауна физическое обследование, включающее осмотр и аускультацию, является обязательным, но недостаточным. Так, McElhinney и др. установили, что информативность физического обследования для выявления сердечных аномалий у детей с синдромом Дауна не превышает 80 %. Оказалось, что 15 из 114 исследуемых детей при осмотре не имели признаков врожденных пороков сердца, но при ультразвуковом исследовании у них были диагностированы сердечные аномалии, а девяти из них в дальнейшем потребовалось оперативное лечение.
Материалы и методы
Нами проведено исследование частоты встречаемости и особенностей клинической картины врожденных пороков сердца и персистирующих фетальных коммуникаций у 522 детей с синдромом Дауна в возрасте от 0 до 8 лет, воспитывающихся в домашних условиях. Дети получали медико-психолого-педагогическую помощь в Центре ранней помощи Благотворительного фонда «Даунсайд Ап», где наблюдались с момента обращения (возраст при первом посещении варьировал от 0 до 7 лет) до 8 лет. При первичном обращении проводился сбор анамнеза, клиническое обследование, анализ медицинской документации. Все дети, даже в случае отсутствия клинически выраженных симптомов порока сердца, направлялись на электрокардиографическое и эхокардиографическое обследования и, при необходимости, на лечение в соответствующие профильные кардиологические стационары и диспансеры.
Результаты
У всех пациентов синдром Дауна был подтвержден хромосомным исследованием. Регулярная трисомия 21-й хромосомы была выявлена у 499 детей (499/522), что составило 90,4 %, транслокационная форма – у 24 (4,3 %), мозаицизм – у 28 (5,1 %), у одного ребенка трисомии 21-й и Х хромосом (кариотип 48,ХХХ,+21) – 0,2 %.
Получены результаты эхокардиографического исследования 428 детей (см. рис.). Врожденные пороки сердца диагностированы у 195 (195/428), что составило 45,6 %. В структуре этих аномалий у детей с синдромом Дауна чаще отмечался дефект межпредсердной перегородки (ДМПП), а именно в 30,2 % (59/195) случаев. Общий атриовентрикулярный канал (ОАВК) составил 24,1 % (47/195), дефект межжелудочковой перегородки (ДМЖП) – 23,1 % (45/195), сочетание дефектов межпредсердной и межжелудочковой перегородок (ДМПП+ДМЖП) – 10,8 %. Другие пороки, такие как тетрада Фалло, стеноз легочной артерии и др., в сумме составили 11,8 % (23/195). Персистенция гемодинамически значимого открытого артериального протока (ОАП), потребовавшего оперативного вмешательства, была выявлена в 2,8 % (12/428).
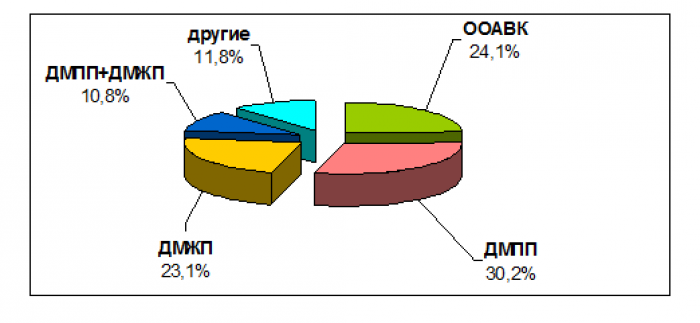 Структура сердечных аномалий у детей с синдромом Дауна
Структура сердечных аномалий у детей с синдромом Дауна
Почти все исследуемые нами дети родились доношенными. Срок родов составил 38,2 ± 1,3 недель. Однако при оценке антропометрических данных новорожденных с синдромом Дауна и врожденными пороками сердца оказалось, что их физическое развитие страдает еще внутриутробно. Задержка физического развития (ЗВУР) – масса тела при рождении ниже 10 перцентилей в соответствии со сроком гестации в сравнении с показателями физического развития Г. М. Дементьевой, Е. В. Короткой – отмечалась у 18,7% детей. У всех новорожденных с сердечными аномалиями наблюдалась асимметричная форма ЗВУР (Pounderal Index, PI>25). Вероятно, задержка физического развития формировалась под влиянием, в основном, не генетического фактора.
Известно, что у новорожденных с синдромом Дауна нередко отмечается морфофункциональная незрелость (по нашим данным, она встречается в 17,9 % случаев). У детей с морфофункциональной незрелостью часто недооцениваются размеры дефекта межпредсердной перегородки, который рассматривают как открытое овальное окно даже при гемодинамической его значимости, и артериального протока, в то время как имеет место недостаточность кровообращения. Застойная легочная гипертензия приводит к развитию пневмонии. Возникновение и затяжное течение пневмонии у детей с синдромом Дауна объясняется характерными для них иммунологическими нарушениями.
Хорошо известно, что манифестация сердечной недостаточности у детей раннего возраста, в отличие от детей старшего возраста, может протекать под маской других состояний. Помимо классических симптомов, таких как тахикардия (учащение сердцебиения), тахипноэ (увеличение частоты дыхания), цианоз кожи и слизистых, типичны вялое сосание, снижение темпов физического и психомоторного развития. В подобных случаях у педиатров возникают определенные затруднения в проведении дифференциальной диагностики при наличии у ребенка синдрома Дауна. У таких детей клинические симптомы недостаточности кровообращения могут расцениваться как проявления особенностей психомоторного развития, типичных для синдрома Дауна. Так, если возникают трудности вскармливания: ребенок вялый, неохотно берет грудь или соску, вяло сосет, не может высосать необходимый объем питания, вплоть до полного отказа от кормлений, такие проблемы часто объясняются мышечной гипотонией, общей вялостью, характерной для детей с синдромом Дауна, с последующим назначением общеукрепляющего массажа, что ухудшает состояние ребенка. В дальнейшем отмечается плохая прибавка в весе. Она направляет клиницистов на выявление патологии со стороны желудочно-кишечного тракта, гипогалактии у матери, исследования качества молока, его инфицированности. В борьбе с прогрессирующей гипотрофией младенца нередко переводят на искусственные смеси. Важно отметить, что гипотрофия может стать причиной отсрочки оперативного лечения порока сердца и/или неблагоприятно повлиять на его исход.
Таким образом, слабая нацеленность педиатров на выявление симптомов недостаточности кровообращения у ребенка с синдромом Дауна затрудняет ее своевременную диагностику, а следовательно, и адекватное лечение врожденного порока сердца.
Наглядным примером будет анализ истории болезни.
Андрей Б., от первой, физиологично протекавшей беременности. Роды в срок. Вес мальчика при рождении – 3000 г., рост – 51см, оценка по шкале АПГАР 88б. Состояние ребенка после рождения удовлетворительное. Отмечались признаки морфофункциональной незрелости, фенотипические признаки синдрома Дауна. С целью подтверждения хромосомной патологии была взята кровь для определения кариотипа. Выявлена регулярная трисомия 21-й хромосомы. С первых суток жизни отмечался систолический шум при аускультации грудной клетки. Для исключения аномалий развития сердца проведено ЭХОКГ и обнаружено открытое овальное окно размером 4 мм. Ребенок был выписан домой под наблюдение участкового педиатра и кардиолога по месту жительства. В дальнейшем мальчик стал вялым, неохотно брал грудь, отмечались частые срыгивания, редкий стул. За месяц ребенок прибавил в весе 210 г. При осмотре обращали на себя внимание признаки недостаточности кровообращения: одышка в покое, умеренная тахикардия. Мальчик был направлен в НЦССХ им. Бакулева, где диагностирован порок развития сердца – дефект межпредсердной перегородки размером 6 мм со значительным нарушением сердечной гемодинамики. Рентгенограмма грудной клетки показала расширение корней легких, КТИ = 57 %. По данным ЭКГ: отклонение электрической оси сердца вправо. В возрасте 4 месяцев проведено оперативное лечение дефекта межпредсердной перегородки.
Успехи в области кардиохирургии за последние десятилетия позволили повысить выживаемость младенцев с синдромом Дауна и патологией сердечнососудистой системы с 78 % в 1985 г до 90 % к 2004 г. (Claire Irving и др., 2008).
Hijii Т. и др. (1997) сообщили, что до 24-летнего возраста доживают 87,8 % пациентов с синдромом Дауна, перенесших оперативное лечение врожденного порока сердца.
При сравнении течения и исходов оперативного лечения полной формы атривентрикулярного канала у младенцев с синдромом Дауна и без синдрома, в работе, проведенной на базе НЦССХ им. Бакулева, Т. И. Задко отмечает, что у детей с синдромом Дауна быстрее развивается легочная гипертензия, важным механизмом в развитии которой, очевидно, является окислительный стресс. Генетически обусловленные особенности антиоксидантной системы, в том числе изначально низкий уровень глутатиона и более высокая антиоксидантная активность сыворотки у детей с синдромом Дауна (Н. П. Котлукова, О. И. Артеменко и др., 2008), свидетельствуют о более высоком окислительном стрессе при развитии легочной гипертензии при пороках сердца с легочной гиперволемией.
Из ранних осложнений хирургической коррекции атриовентрикулярного канала у детей с синдромом Дауна чаще встречаются инфекционно-септические осложнения, тогда как у детей без синдрома – острая сердечная недостаточность (Т. И. Задко, 2005). Это обстоятельство объясняется анатомическими особенностями порока и имеющимися иммунологическими нарушениями у младенцев с трисомией 21-й хромосомы.
Выводы
Полученные нами данные частоты сердечных аномалий не противоречат уже известным в литературе. Около половины детей с синдромом Дауна имеют патологию сердечнососудистой системы: 45,5 % – врожденные пороки сердца, 2,8 % – гемодинамически значимый открытый артериальный проток.
Анализ данных проведенных исследований, а также собственные полученные результаты делают очевидной необходимость раннего кардиологического обследования всех новорожденных с синдромом Дауна, включающего помимо осмотра и аускультации проведение эхокардиологического и электрокардиологического исследований. Внимательный подход и оценка клинических симптомов, а также знание генетически обусловленных особенностей детей с синдромом Дауна помогут своевременно диагностировать недостаточность кровообращения и начать адекватную терапию. Все дети с выявленными пороками сердца должны быть консультированы кардиохирургом для определения необходимости и сроков оперативного лечения.
Литература
- Задко Т. И. Синдром Дауна в сочетании с полной формой атриовентрикулярной коммуникации: актуальность, диагностика, сопутствующая патология, анатомия, особенности естественного течения, результаты хирургического лечения // Детские болезни сердца и сосудов. – 2005. – № 6. – С. 10–18.
- Роль окислительного стресса и антиоксидантной системы в патогенезе врожденных пороков сердца / Н. П. Котлукова, О. И. Артеменко, М. П. Давыдова, О. Н. Ильина, Л. А. Курбатова // Педиатрия. – 2009. – Т. 87, № 1. – С. 24–28.
- Cassidy S. B., Allanson J. E. Management of Genetic Syndromes. 2-nd ed. – P. 191–210. URL: https://www.wiley.com/en-us/Management+of+Genetic+Syndromes%2C+3rd+Edition-p-9780470191415
- Correlation between abnormal cardiac physical examination and echocardiographic findings in neonates with Down syndrome / D. B. McElhinney, M. Straka, E. Goldmuntz, E. H. Zackai // American Journal of Medical Genetics. – 2002. – Part A. – P. 238–241.
- Khory M. J., Erickson J. D. Improved ascertainment of cardiovascular malformation in infants with Down syndrome, Atlanta, 1968 through 1989 // Epidemiology. – 1992. – Vol. 136. – P. 1457–1464.
- Life expectancy and social adaptation in individuals with Down syndrome and without surgery for congenital heart disease / T. Hijii, J. Fukushige, H. Igarashi et al. // Clinical Pediatrics. – 1997. –Vol. 36. – P. 327–332.
- Twenty-year trends in prevalence and survival of Down syndrome / C. Irving, A. Basu, S. Richmond et al. // European Journal of Human Genetics. – 2008. – Vol. 16. – P. 1336–1340.
Источник
Откры́тый артериа́льный прото́к (ОАП) — врождённый порок сердца, при котором артериальный проток новорождённого (Боталлов проток) не зарастает после рождения. Относится к белым порокам. Ранние симптомы встречаются редко, но в первый год жизни могут наблюдать усиление работы дыхания и плохой набор веса. С возрастом ОАП может привести к остановке сердца, при отсутствии коррекционной терапии.
Этиология[править | править код]
Открытый артериальный проток может быть идиопатическим (то есть без установления причины) или вторичным по отношению к другим состояниям. К предрасполагающим факторам относят:
- Недоношенность
- Синдром врождённой краснухи
- Хромосомные заболевания, например синдром Дауна
Закрытие артериального протока в норме[править | править код]
У развивающегося плода артериальный проток соединяет лёгочную артерию и аорту, что позволяет снабжать наполненные жидкостью сжатые лёгкие плода оксигенированной кровью из правого желудочка и при этом не перегружать его. В период внутриутробного развития, этот шунт защищает правый желудочек от перегрузок путём сброса избыточной крови (которая не может пройти в легочные артерии из-за высокого сопротивления в сжатых лёгких) в аорту в обход малого круга кровообращения. Внутриутробное закрытие этого протока может привести к правожелудочковой недостаточности.
Когда новорождённый делает свой первый вдох, лёгкие расправляются и сопротивление сосудов лёгких уменьшается. После рождения лёгкие высвобождают брадикинин, который сокращает гладкие мышцы стенок артериального протока и уменьшает кровоток через него. Артериальный проток обычно сужается и полностью зарастает в течение 15-20 часов жизни, но не более 2-8 недель (в редких случаях до 15 недель при положительной динамике закрытия). Основной стимул закрытия протока — увеличение содержания кислорода в крови новорождённых. Выделение материнских циркулирующих простагландинов препятствует закрытию протока. В современной практике препараты, тормозящие образование простагландинов, используются как терапевтические средства для закрытия артериального протока у новорожденных при врожденном дефекте его закрытия. Рубец из фиброзных остатков артериального протока называют артериальной связкой, которая остаётся в нормальном сердце взрослого человека.
Клиническая картина[править | править код]
Общие симптомы:
- Тахикардия
- Дыхательные проблемы
- Одышка
- Длительный «машинный» шум, выслушиваемый во втором-третьем межреберье
- Увеличение размеров сердца
- Высокое пульсовое давление
- Замедленный рост и развитие[3]
Прогноз[править | править код]
Без лечения заболевание может прогрессировать из белого порока (со сбросом слева-направо) в синий порок (со сбросом справа-налево).
На ранних этапах развития недоношенного новорожденного функционирование ОАП может считаться нормой, необходимо оценить его гемодинамическую значимость[источник не указан 1820 дней].
Дополнительные изображения[править | править код]
Открытый артериальный проток
Примечания[править | править код]
Mosalli R, AlFaleh K, Paes B. Role of prophylactic surgical ligation of patent ductus arteriosus in extremely low birth weight infants: Systematic review and implications for clinical practice. Ann Pediatr Card 2009;2:120-6. Available from: https://www.annalspc.com/text.asp?2009/2/2/120/58313
Источник
Лечение открытого артериального протока зависит от возраста человека. Варианты могут включать в себя:
- Наблюдение. У недоношенных детей открытый артериальный проток часто закрывается сам по себе. Врач будет наблюдать за сердцем вашего ребенка, чтобы убедиться, что открытый артериальный проток закрывается должным образом. У доношенных младенцев, детей и взрослых, которые имеют артериальные протоки небольшого диаметра, которые не вызывают проблем со здоровьем, обычно бывает достаточно только наблюдения.
- Лекарственные препараты. У недоношенных детей нестероидные противовоспалительные препараты (НПВП), такие, как ибупрофен (Адвил, Мотрин, другие) или индометацин (Индоцин) – могут быть использованы, чтобы вызвать закрытие артериального протока. НПВС блокируют гормоноподобные химические вещества, которые препятствуют закрытию артериального протока. НПВС не эффективны для закрытия артериального протока у доношенных новорожденных, детей и взрослых.
- Операция на открытом сердце. Если лекарства не эффективны и состояние вашего ребенка тяжелое, если возникли осложнения, может быть рекомендована операция на открытом сердце. Хирург делает небольшой разрез между ребрами, чтобы достичь сердца и ушивает открытый артериальный проток или закрывает его с помощью специальной клипсы.
После операции ваш ребенок будет оставаться в больнице в течение нескольких дней. Обычно требуется несколько недель, чтобы полностью восстановиться после операции на открытом сердце. Операция на открытом сердце также может быть рекомендована взрослым, у которых открытый артериальный проток вызывает проблемы со здоровьем. Возможные риски включают появление осиплости голоса, кровотечения, инфекционных осложнений и паралич диафрагмы.
- Эндоваскулярное закрытие протока. Недоношенные дети слишком малы для этого вида лечения. Однако, если ваш ребенок не имеет проблем со здоровьем, связанных с открытым артериальным протоком, врач может рекомендовать подождать, пока ребенок не станет старше, чтобы сделать выполнить коррекцию порока с помощью эндоваскулярного вмешательства. Этот метод лечения может быть использован у доношенных младенцев, детей и взрослых.
Тонкая трубка (катетер) вводится в кровеносный сосуд в паховой области и проводится до сердца. Через катетер вводится специальное устройство (спираль или окклюдер), с помощью которого закрывают артериальный проток.
Если процедура проводится в амбулаторных условиях, ваш ребенок, вероятно, не будет оставаться в больнице на ночь. Осложнения включают кровотечение, инфекцию или смещение окклюдера или спирали.
Профилактический прием антибиотиков
В прошлом людям, которые имели в анамнезе открытый артериальный проток, советовали принимать антибиотики перед лечением у стоматолога и некоторыми хирургическими вмешательствами для предотвращения инфекции сердца (инфекционный эндокардит). Сегодня профилактическое применение антибиотиков больше не рекомендуется большинству людей с открытым артериальным протоком.
Вашему ребенку может потребоваться принимать антибиотики в течение первых шести месяцев после эндоваскулярного вмешательства или если проток остался открытым, несмотря на вмешательство. Поговорите со своим врачом о том, нужно ли вашему ребенку принимать антибиотики перед какими-либо процедурами.
Источник
Врожденные пороки сердца, согласно статистическим оценкам встречаются, примерно в 20% всех клинических ситуаций среди первичных патологий сердечнососудистой системы у детей.
Обычно выявляются они не сразу, если не считать критически опасных разновидностей нарушений. От момента рождения для выявления анатомического дефекта может пройти не один год, многие и вовсе обнаруживаются во взрослом возрасте.
Открытый артериальный проток у детей — это незаращение особого отверстия, влекущего сообщение двух крупных сосудов: легочной артерии и аорты.
Естественная структура может быть в диаметре от 2 до 20 мм, длинной от 4 до 15 мм. и присутствует у всех без исключения детей во внутриутробном периоде, потому как малый круг кровообращения не задействован.
Спустя несколько часов или суток с появления на свет, Боталлов проток у новорожденных (иное название отверстия между легочной артерией и аортой) закрывается самостоятельно.
Максимум до первого года жизни, затем вероятность спонтанного регресса отклонения минимальна.
Лечение нужно всегда. Известны случаи длительного малосимптоматичного течения патологического процесса. Примерно в 20% ситуаций анатомический дефект выявляется у лиц за 20 лет.
Механизм развития
Нормальная физиология внутриутробного (фетального) периода предполагает существование двух моментов: открытого Боталлова протока (собственно отверстия между аортой и легочной артерией) и овального окна.
Обе структуры призваны обеспечивать нормальное, эффективное кровообращение минуя малый (легочный) круг, который в это время не задействован, ведь ребенок получает кислород и питательные вещества через плаценту, от матери.
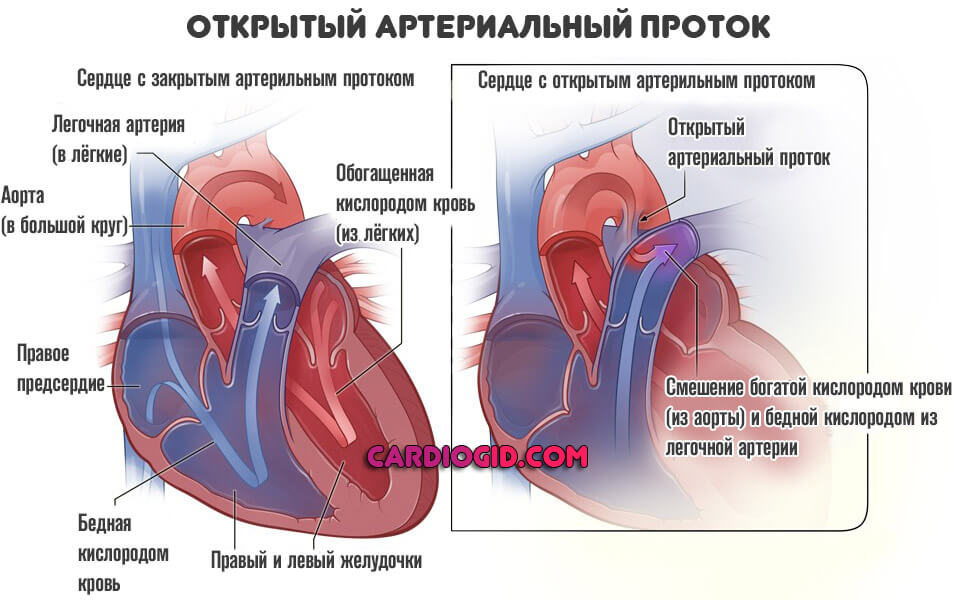
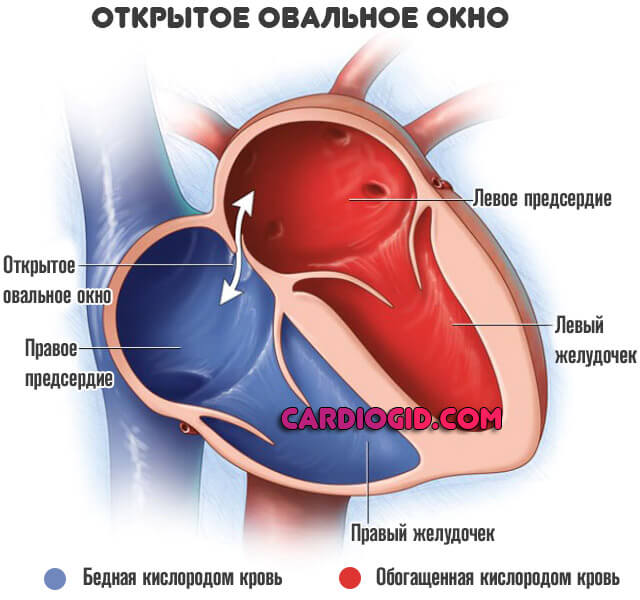
Оба анатомических явления считаются нормой. После рождения, в течение определенного времени отверстия, в том числе артериальный проток должны закрыться самостоятельно.
На процесс требуется от пары часов до года, затем вероятность самоустранения патологии несущественна.
Причины
В основе механизма лежат два фактора. Первый — спонтанные нарушения не связанные с генетическими заболеваниями. Становятся итогом влияния негативных моментов на мать во время гестации.
Другой — хромосомные отклонения, коих множество. От синдрома Дауна, Нунан до Тетрады Фалло.
Во второй ситуации открытым артериальным протоком дело не обходится. Наблюдаются генерализованные нарушения со стороны многих систем.
В то же время, в основе патологического процесса лежит нарушение синтеза и физических свойств соединительных тканей.
Классификация
Типизация проводится исходя из нескольких критериев. Основной — уровень давления в легочной артерии. Это функциональный показатель.
Выделяют 4 фазы заболевания:
- Легкую. Цифры не превышают 40% общих по организму (оценка проводится в ходе эхокардиографии, а средний уровень АД определяется с помощью тонометра).
- Умеренную. ОТ 45% и выше.
- Тяжелую. Более 75%.
- Терминальную. Давление в легочной артерии равно общему показателю в организме или выше него. Это критическое состояние. Трудно поддается лечению и заканчивается смертью в большинстве своем.
Стадиальность:
- 1 стадия. Продолжается до 5 лет. Отсчитывается с момента рождения. Сопровождается выраженной клиникой. Может закончиться гибелью, что и происходит, примерно, в четверти случаев, если не проводится качественное лечение.
- 2 стадия. Субкомпенсаторная. Явления исчезают, наступает период относительного благополучия. Длится он еще около 10-15 лет.
- 3 стадия. Примерно с 20 года жизни или чуть позднее возникает второй критический этап. Декомпенсация. Нарастают явление легочной гипертензии, роста давления в артериях малого круга.
Стенки сосудов утолщаются и теряют эластичность, просветы кровоснабжающих структур сужаются за счет рубцевания. Развиваются необратимые изменения. Они опасны для жизни и не поддаются полной коррекции.
Представленная стадиальность справедлива только для отсутствующего лечения. Если своевременно устранить анатомический дефект все встанет на свои места. Проблема в поздней диагностике.
В идеале проверять ребенка нужно сразу после рождения на предмет скрытых патологий сердечнососудистой системы.
Но виду отсутствия качественной программы раннего скрининга в России и странах бывшего Союза многие ситуации остаются незамеченными.
Особенности гемодинамики
Нормальный кровоток у человека протекает по двум кругам. Малый или легочный обеспечивает обогащение жидкой соединительной ткани кислородом, отведение окиси CO2 выдохом.
Большой отвечает за движение питательных веществ и O2 через аорту ко всем тканям тела без исключения. Процесс протекает постоянно, не останавливается ни на минуту.

У детей задействован только большой круг, потому как потребности обеспечивать кровь кислородом пока нет. Она и так идет обогащенной от матери.
На фоне открытого артериального протока наблюдается увеличение давления в легочной артерии, поскольку жидкая ткань попадает в нее.
Структуры малого круга не рассчитаны на существенное давление, потому быстро развивается другой порок — легочное сердце.
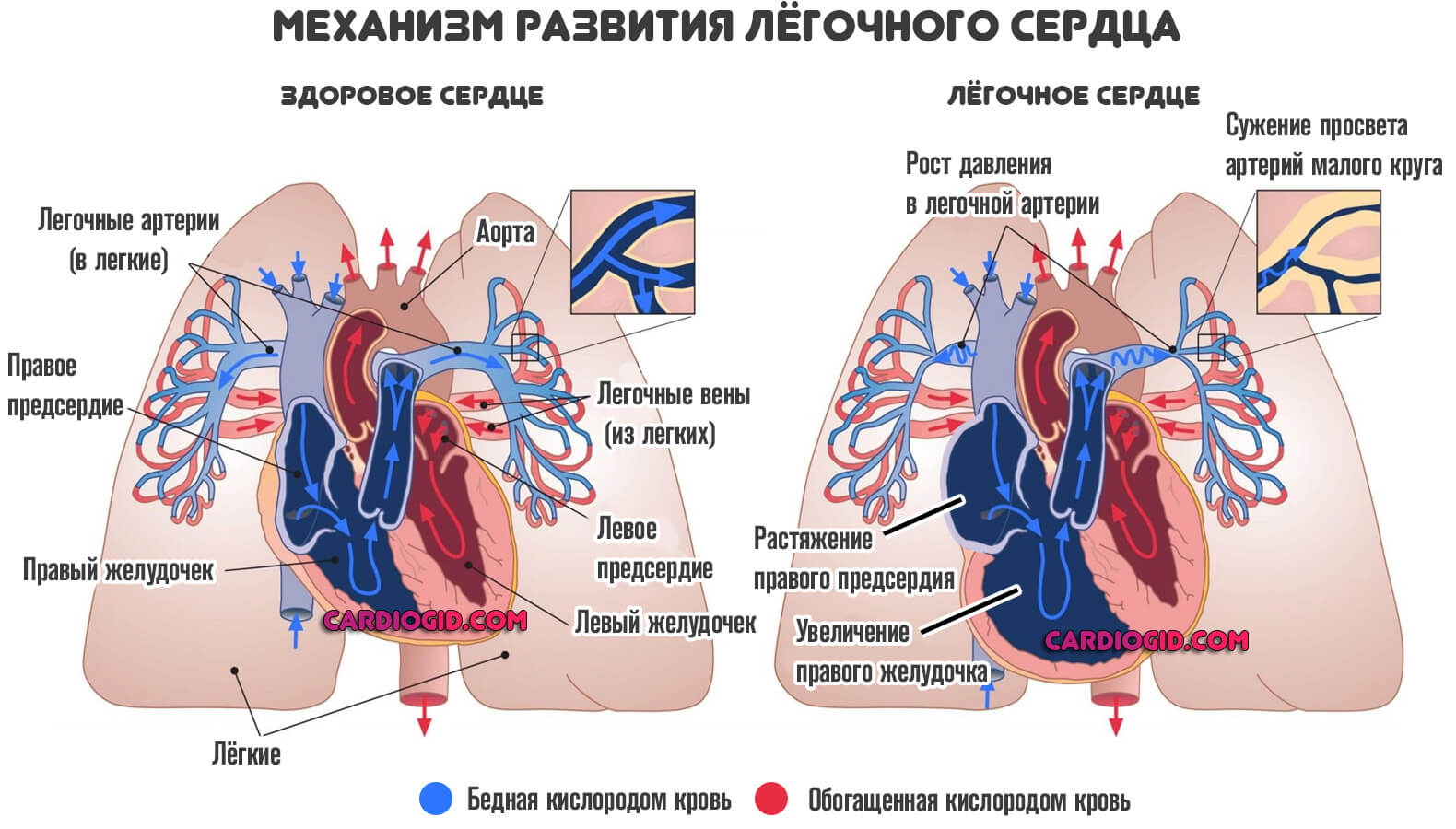
Без специфического лечения оно в течение нескольких лет приводит к смерти больного от кардиальной недостаточности и остановки работы органа как результата падения сократительной способности миокарда.
Чаще всего нарушение встречается у недоношенных детей, хотя прямая связь момента рождения и вероятности развития порока не установлена.
Симптомы
Проявления достаточно специфичны, если знать, что искать и в каком порядке. Анатомический дефект на ранних этапах не настолько агрессивен, чтобы в течение считанных месяцев закончиться смертью ребенка.
Потому прогрессирование постепенное, на протяжении длительного времени.
Начальные признаки таковы:
Одышка
Невозможность набрать воздуха. Объективно проявляется усталостью при кормлении. Младенцу необходимо перевести дух, чтобы продолжить.
Так может повторяться несколько раз в течение одного приема пищи. По мере взросления симптом никуда не уходит, приобретает те же черты.
Ребенок задыхается на фоне минимальной физической активности, а затем и вовсе в состоянии покоя.
Снижение толерантности к механическим нагрузкам
Сказывается на общем самочувствии ребенка. Он отказывается от игр, старается больше сидеть, лежать. В ранние дни признак проявляет себя длительным периодом сна, коротким бодрствованием.
И если в младенческие годы это можно связать с процессом формирования центральной нервной системы и быстрой физиологической утомляемостью, позднее вариантов не остается.
Бледность кожных покровов
ОАП сердца у новорожденных относится к так называемым белым порокам. Когда кожа становится мелового цвета или молочного оттенка. Связано это со спазмом периферических сосудов.
Сопровождается похолоданием конечностей. В противоположность им, синие пороки дают, преимущественно, цианоз носогубного треугольника и кожи.
Строгого разграничения нет. Оба симптома могут присутствовать одновременно.
Кашель
Постоянный, сначала непродуктивный, без выделения мокроты. Затем с отхождением небольшого количества слизистого вязкого экссудата.
По мере развития болезни возникает кровохаркание, выход жидкой соединительной ткани через дыхательные пути.
Это негативный признак, указывающий на выраженную клиническую картину, неблагоприятный прогноз и высокую вероятность смерти от сердечной недостаточности.
Гипергидроз
Повышенная потливость на фоне физической активности. В том числе кормления.
Частые инфекционно-воспалительные процессы
В легких и бронхах. Обусловлены застойными явлениями в малом круге. Представляют значительную опасность для детей, поскольку могут закончиться острой дыхательной недостаточностью и смертью от асфиксии.
Медленный набор веса
Степень отставания в физическом и даже ментальном развитии, зависит от тяжести патологического процесса.
Клиническая картина проявляет себя на 3-5 день с момента рождения.
Бывают исключения, когда порок никак не выделяется долгие годы, в таком случае возможно случайное обнаружение в ходе диагностики по поводу прочих патологий. Или же при обращении пациента к кардиологу по вопросу тревожных симптомов.
Каких именно:
- Боли в грудной клетке неясного происхождения. Обычно слабые, давящие или жгучие. Приступ продолжается от пары секунд до нескольких минут и заканчивается полной компенсацией состояния. Как будто ничего и не было.
- Аритмии. По типу синусовой тахикардии. Если порок декомпенсирован, то есть организм уже не в силах сглаживать нарушения им провоцируемые, возникает брадикардия как ответ на падение сократительной способности миокарда и ослабление трофики.
- Одышка. Выраженная, на фоне физической активности или в состоянии покоя. При перемене положения тела становится интенсивнее.
- Кашель, возможно с кровью. У пациентов старшей возрастной группы, 18+ требуется дифференциальная диагностика. Отграничить симптомы нужно от таковых при туберкулезе и раке легких, хотя у столь молодых людей подобные заболевания встречаются довольно редко.
- Периферические отеки. Сначала в процесс вовлекаются только ноги, затем руки и лицо. Это результат застойных явлений в организма. Последствие не самого порока, а хронической сердечной недостаточности. Она присутствует у большинства пациентов с длительным течением открытого артериального протока.
- Бледность кожных покровов. Может соседствовать с цианозом носогубного треугольника.
Хриплый голос, нарушение процессов говорения. Изменение тембра. - Головная боль. Цефалгия в затылке или теменной области. Также вертиго, нарушение ориентации в пространстве. Мир буквально идет кругом. Это не постоянные симптомы, они возникают спонтанно, на некоторое время. Затем отступают.
- Нарушения сознания. Обмороки. Все три проявления, указанные выше — результат ослабления трофики головного мозга. Неблагоприятный прогностический признак, если нет лечения. Вероятен инсульт и тяжелая инвалидность.
Внимание:
Типичная клиническая картина складывается из легочных и сердечных моментов, что говорит о нарушенной работе малого круга. Значит нужно смотреть именно в эту сторону.
Диагностика
Проводится под контролем кардиолога или профильного хирурга. При этом специально, целенаправленно ОАП сердца у детей ищут крайне редко. Только если проявления достаточно выражены для подозрений.
В остальных случаях анатомический дефект становится случайной находкой или продолжает существование неопределенно долгий срок, вплоть до взрослых лет.
Перечень диагностических мероприятий:
- Устный опрос пациента или же его родителей на предмет самочувствия или поведенческих моментов. Важно учитывать характер сна, переносимость физической нагрузки, питания. Объективизация признаков дает возможность выстроить четкую клиническую картину и выдвинуть гипотезы относительно диагноза.
- Сбор анамнеза. Играет меньшую роль, потому как порок всегда врожденный. Он не бывает приобретенным.
- Измерение артериального давления. На ранних цифры в норме. Частоты сердечных сокращений. Обнаруживается незначительная тахикардия. Количество ударов варьируется в пределах 100-120, редко чуть более.
- Эхокардиография. Основная методика исследования анатомического состояния кардиальных структур и окружающих тканей.
Позволяет быстро определиться с нарушением. Оценить уровень давления в легочной артерии и аорте.
Показывает интенсивность сердечного выброса, а значит, дает возможность определить сократительную способность миокарда.
- Электрокардиография. Назначается в рамках рутинной диагностики. Используется для обнаружения аритмических нарушений. Их характера и выраженности.
- Рентгенография грудной клетки. Назначается взрослым пациентам. С одной стороны позволяет исключить рак или туберкулез, с другой же — используется в для выявления типичных признаков открытого артериального протока. Так, примерно в 95% пациентов, диагностируется дилатация (расширение) предсердий.
- Измерение сатурации кислорода крови. Неинвазивная методика. Применяется на первичном приеме. В норме показатель составляет 97-98%. У больных уровни примерно на 2-7% ниже.
По необходимости назначается МРТ. Она позволяет уточнить локализацию и обширность процесса в статике. Но не дает информации о гемодинамических характеристиках, потому эталоном считаться не может. Требуется группа исследований.
Лечение
Терапия проводится кардиохирургическими методами по показаниям. В норме Боталлов проток закрывается в течение дня или максимум на первом году жизни. Потому врачи редко назначают операцию детям до 1 года.
Затем вероятность спонтанного разрешения практически равна нулю. Открытое сообщение легочной артерии и аорты — это большой риск для ребенка, потому медлить нельзя.
Основной способ лечения — эндоваскулярное закрытие ОАП. Через бедренную артерию вводится инструмент. Затем его транспортируют к сердцу под контролем камеры с осветительным прибором и механическим путем закрывают проток.
Если размер отверстия менее 3 мм в используют спираль, если более — специальный окклюдер.
Детям операция проводится под наркозом, пациентам от 12 лет и старше — под местной анестезией.
Вмешательство длится до получаса, имеет минимум осложнений и легко переносится, несмотря на значительную техническую трудность.
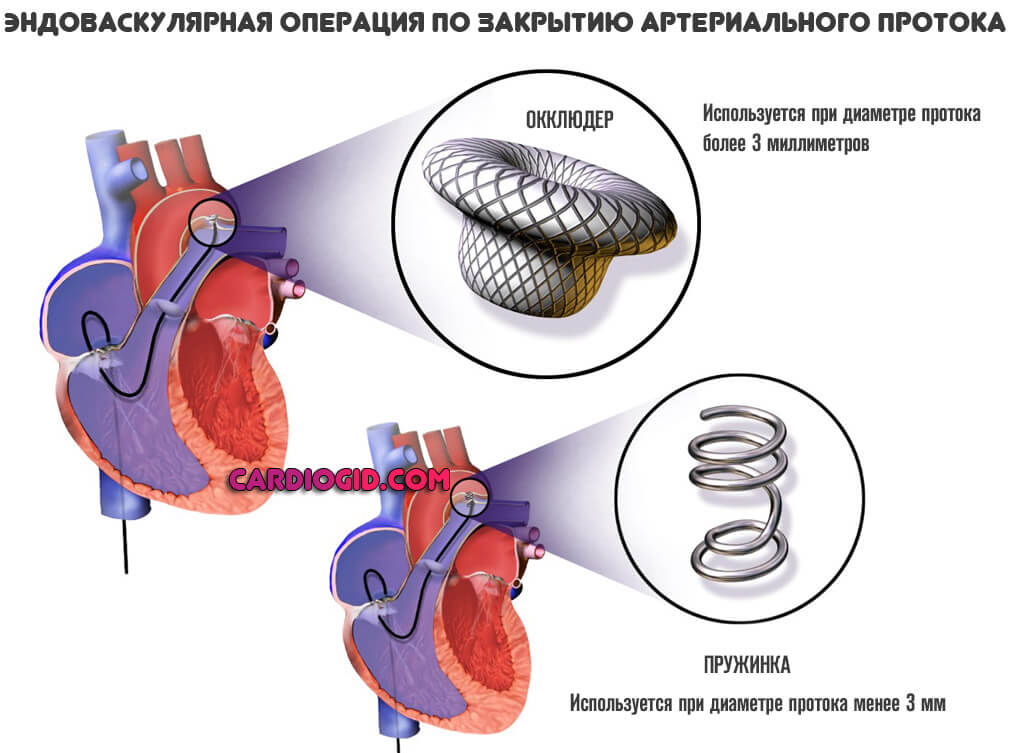
Медикаментозные методы не эффективны. Они практикуются только в первые 2 недели жизни пациента, и то действенность применения препаратов весьма сомнительна.
Открытая операция с рассечением грудной клетки не проводится. Это устаревшая методика. Но есть несколько исключений.
Например, комплексные пороки (множественные анатомические дефекты), безуспешность ранее проведенного малоинвазивного лечения или же недоношенность.
Диаметр бедренной артерии у детей, которые появились раньше срока, слишком мал для введения инструмента. Но здесь возможен вариант клипирования аретриального протока через миниторакотомию.
Реабилитационный период после операции длится около месяца. В это время запрещены интенсивные физические нагрузки, стрессы, для взрослых — курение, прием спиртного, также показан полный половой покой хотя бы на 2 недели. Отказ от посещения бани, сауны на протяжении 3-6 месяцев.
Каждые 14 дней рекомендуется навещать своего кардиолога для оценки течения послеоперационного периода. Затем же стоит скорректировать образ жизни в соответствии со сформировавшимися вторичными нарушениями работы сердечнососудистой системы. Если таковые есть.
Народные методы лечения неэффективны. Тратить на них время не стоит, также как и силы. Артериальный проток можно закрыть только механическим методом посредством малотравматичной операции.
Детям же травы и «бабушкины» рецепты и вовсе противопоказаны ввиду несформировавшейся иммунной системы и высоких рисков аллергической реакции.
Рекомендуется не медлить и обращаться к врачу для прохождения диагностики, верификации болезни и назначения планового лечения. Опасаться осложнений не стоит, вероятность негативного сценария минимальна.
Прогноз
При раннем начале лечения — благоприятный. Присоединение сердечной недостаточности, склерозирования сосудов малого круга увеличивает вероятность смерти в перспективе нескольких лет почти в 6 раз. Потому требуется раннее нача?
