Синдром бругада типы на экг

Синдром Бругада — наследственное заболевание[1], обусловленное мутацией гена SCN5A, расположенного в плече p 3-й хромосомы, кодирующего биосинтез белковых субъединиц натриевого канала кардиомиоцитов.
Впервые это понятие, позже ставшее эпонимом, предложили испано-бельгийские кардиологи — братья Педро и Хосеп Бругада[2].
Мутации генов[править | править код]
На сегодняшний день известны, по крайней мере, 5 генов, ответственных за развитие этого состояния. В зависимости от мутации гена выделяют следующие варианты:
Патогенез[править | править код]
Заболевание имеет аутосомно-доминантный тип наследования в 25 % семей. Клинические проявления синдрома Бругада развиваются обычно в молодом возрасте (до 35-40 лет), реже — наблюдаются даже в пожилом и старческом возрасте. При исследовании статистических данных, накопленных в странах Юго-Восточной Азии и Дальнего Востока, было отмечено, что в данном регионе значительно распространены случаи внезапной ночной смерти в молодом возрасте (в год от 4 до 10 случаев на 10 000 жителей, в том числе в Лаосе — 1 случай на 10 000 жителей; в Таиланде — 26-38 на 100 000).
[7]
Описаны также случаи приобретенного синдрома Бругада[2].
Синдром Бругада характеризуется наличием преходящей полной или неполной блокады правой ножки пучка Гиса, косонисходящим подъёмом сегмента S-T в правых грудных отведениях (V1-V3), рецидивирующей пароксизмальной полиморфной желудочковой тахикардией и высоким риском внезапной сердечной смерти.
Симптомокомплекс[править | править код]
Полная форма синдрома Бругада включает следующие клинико-электрокардиографические проявления:
- Типичная электрокардиографическая картина (косонисходящее повышение сегмента S-T над изолинией на 1 мм и больше в отведениях V1—V3, на некоторых ЭКГ напоминает морду бультерьера, поэтому данное изменение иногда называют «типом бультерьера»[2], спонтанное или индуцированное введением антиаритмических препаратов I класса (блокаторов натриевых каналов, например, аймалина (гилуритмала) в дозе 1 мг/кг или новокаинамида в дозе 10 мг/кг, флекаинида 2 мг/кг); полная или неполная блокада правой ножки пучка Гиса); возможно укорочение интервала Q-T и удлинение P-Q (P-R);
- Пароксизмы полиморфной желудочковой тахикардии, часто рецидивирующие;
- синкопальные (обморочные) состояния;
- высокий риск внезапной сердечной смерти вследствие полиморфной желудочковой тахикардии или фибрилляции желудочков.
Примечания[править | править код]
- ↑ Окороков А. Н., Диагностика болезней внутренних органов: Т. 10. Диагностика болезней сердца и сосудов.: — М.: Мед. лит., 2005. — 384 с.: ил. ISBN 5-89677-091-X; — ст. 239—241.
- ↑ 1 2 3 Л. А. Бокерия, О. Л. Бокерия, Л. Н. Киртбая. СИНДРОМ БРУГАДА: КЛЕТОЧНЫЕ МЕХАНИЗМЫ И ПОДХОДЫ К ЛЕЧЕНИЮ. Анналы аритмологии, № 3, 2010.
- ↑ 1 2 Antzelevitch C; Pollevick GD; Cordeiro JM; Casis, O.; Sanguinetti, M. C.; Aizawa, Y.; Guerchicoff, A.; Pfeiffer, R.; Oliva, A. Loss-of-Function Mutations in the Cardiac Calcium Channel Underlie a New Clinical Entity Characterized by ST-Segment Elevation, Short QT Intervals, and Sudden Cardiac Death (англ.) // Circulation (англ.)русск. : journal. — Lippincott Williams & Wilkins (англ.)русск., 2007. — Vol. 115, no. 4. — P. 442—229. — doi:10.1161/CIRCULATIONAHA.106.668392. — PMID 17224476.
- ↑ Delpon E; Cordeiro JM; Núñez L; Thomsen, P. E. B.; Guerchicoff, A.; Pollevick, G. D.; Wu, Y.; Kanters, J. K.; Larsen, C. T. Functional Effects of KCNE3 Mutation and its Role in the Development of Brugada Syndrome (англ.) // Circulation Arrhythmia and Electrophysiology : journal. — 2008. — Vol. 1, no. 3. — P. 209—218. — doi:10.1161/CIRCEP.107.748103. — PMID 19122847.
- ↑ Watanabe H; Koopmann TT; Le Scouarnec S; Yang, Tao; Ingram, Christiana R.; Schott, Jean-Jacques; Demolombe, Sophie; Probst, Vincent; Anselme, Frédéric. Sodium channel β1 subunit mutations associated with Brugada syndrome and cardiac conduction disease in humans (англ.) // Journal of Clinical Investigation (англ.)русск. : journal. — 2008. — June (vol. 118, no. 6). — P. 2260—2268. — doi:10.1172/JCI33891. — PMID 18464934.
- ↑ 1 2 Bezzina, Connie R; Barc, Julien; Mizusawa, Yuka; Remme, Carol Ann; Gourraud, Jean-Baptiste; Simonet, Floriane; Verkerk, Arie O; Schwartz, Peter J; Crotti, Lia; Dagradi, Federica; Guicheney, Pascale; Fressart, Véronique; Leenhardt, Antoine; Antzelevitch, Charles; Bartkowiak, Susan; Schulze-Bahr, Eric; Zumhagen, Sven; Behr, Elijah R; Bastiaenen, Rachel; Tfelt-Hansen, Jacob; Olesen, Morten Salling; Kääb, Stefan; Beckmann, Britt M; Weeke, Peter; Watanabe, Hiroshi; Endo, Naoto; Minamino, Tohru; Horie, Minoru; Ohno, Seiko; Hasegawa, Kanae; Makita, Naomasa; Nogami, Akihiko; Shimizu, Wataru; Aiba, Takeshi; Froguel, Philippe; Balkau, Beverley; Lantieri, Olivier; Torchio, Margherita; Wiese, Cornelia; Weber, David; Wolswinkel, Rianne; Coronel, Ruben; Boukens, Bas J; Bézieau, Stéphane; Charpentier, Eric; Chatel, Stéphanie; Despres, Aurore; Gros, Françoise; Kyndt, Florence; Lecointe, Simon; Lindenbaum, Pierre; Portero, Vincent; Violleau, Jade; Gessler, Manfred; Tan, Hanno L; Roden, Dan M; Christoffels, Vincent M; Marec, Hervé Le; Wilde, Arthur A; Probst, Vincent; Schott, Jean-Jacques; Dina, Christian; Redon, Richard. Common variants at SCN5A-SCN10A and HEY2 are associated with Brugada syndrome, a rare disease with high risk of sudden cardiac death (англ.) // Nature Genetics : journal. — 2013. — ISSN 1061-4036. — doi:10.1038/ng.2712.
- ↑ Л. М. Макаров. Синдром Бругада. журнал «Лечащий врач».
Источник
- 1 Синдром Бругада
- 1.1 Введение
- 1.1.1 Эпидемиология
- 1.1.2 Этиология
- 1.2 Классификация
- 1.3 Диагностика
- 1.4 Дифференциальная диагностика
Синдром Бругада
Введение
Синдром, характеризующийся ЭКГ признаками блокады правой ножки пучка Гиса с элевацией точки J и сегмента ST в правых прекордиальных отведениях и проявляющийся клинически рецидивирующими синкопальными состояниями, а также случаями внезапной сердечной смерти, которая наступает чаще у лиц мужского пола в возрасте 30–40 лет, описан P. Brugada и J. Brugada в 1992 г. Заболевание наследуется по аутосомно-доминантному типу, при этом характерна неполная пенетрантность генетических изменений.
Желудочковые тахикардии, (преимущественно полиморфная, крайне редко — мономорфная) характеризующиеся высоким риском трансформации в фибрилляцию желудочков, являются основным клиническим проявлением синдрома Бругада. Характерно их возникновение в покое, во время ночного сна (рис. 1), что делает более вероятным их выявление с помощью ХМ ЭКГ, а не при стандартной записи ЭКГ. Одним из клинических проявлений, сопровождающих эти аритмические события, могут быть эпизоды хриплого (агонального) дыхания во сне. Желудочковые тахикардии могут провоцироваться лихорадочными состояниями, а также рядом лекарственных препаратов (см. табл. 1). Симптомы заболевания проявляются обычно у взрослых, а средний возраст возникновения случаев внезапной сердечной смерти составляет 41±15 лет. Кроме того, при синдроме Бругада чаще чем в общей популяции регистрируют случаи суправентрикулярных тахиаритмий.
Рис. 1. Неустойчивый пароксизм (выделен рамкой) полиморфной желудочковой тахикардии (частота сердечных сокращений 160–180 уд./мин.). Холтеровская мониторная запись ЭКГ в 12 отведениях у больной синдромом Бругада. Время возникновения пароксизма — 23 часа. Стрелками в отведении V1 указана элевация точки J в сокращениях синусового ритма.
Эпидемиология
Распространённость заболевания в общей популяции в настоящее время неизвестна. Существенно чаще оно встречается в странах Юго-Восточной Азии (Азиатско-Тихоокеанский регион), где его распространённость достигает 0,5–1:1000. Синдром Бругада (Brugada Syndrome, BrS) выявляется у лиц, не имеющих признаков органического заболевания сердца, у мужчин встречается в 8–10 раз чаще, чем у женщин, что, предположительно, обусловлено большей силой кратковременного выходящего тока ионов калия Ito (одного из токов, участвующих в формировании синдрома) и действием более высоких концентраций тестостерона.
Этиология
Синдром Бругада вызывают генетические мутации, приводящие к уменьшению силы входящих натриевого (INa) и кальциевого (ICa,L) токов или увеличению силы выходящих калиевых токов (Ito,f, IKs, IK,ATP).
Классификация
В настоящее время известны 12 генетических вариантов синдрома, они представлены в табл. 1. Молекулярно-генетические методы позволяют обнаружить мутации приблизительно у 1/3 больных с явными клинико-инструментальными проявлениями синдрома Бругада, что указывает на генетическую гетерогенность заболевания и позволяет предполагать открытие большого числа новых, не известных в настоящее время мутаций, в будущем. Наиболее распространены мутации гена SCN5A, которые обнаруживают почти у 30% пациентов.
Таблица 1. Молекулярно-генетические типы синдрома Бругада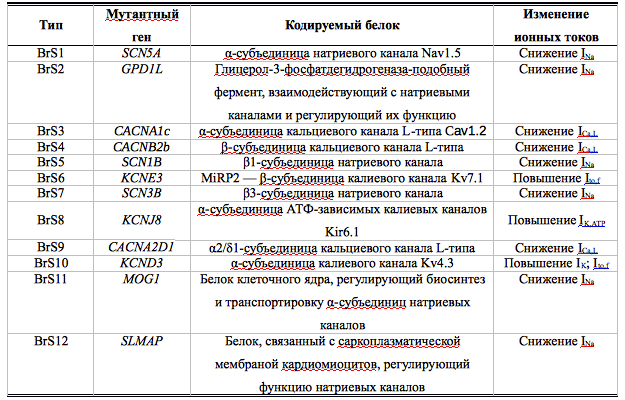
Диагностика
Основой диагностики синдрома Бругада является регистрация патогномоничных данному заболеванию изменений сегмента ST на ЭКГ при отсутствии структурного заболевания сердца и других состояний, при которых могут быть зарегистрированы подобные изменения ЭКГ (указаны далее). На основании характера изменений конечной части желудочкового комплекса выделяют три ЭКГ-типа феномена Бругада (табл. 2, рис 2).
Таблица 2. ЭКГ-типы феномена Бругада

Рис. 2. ЭКГ–типы Синдрома Бругада. Стрелками указана точка J. Элевация более 2 мм.
Регистрацию ЭКГ следует также проводить, располагая электроды правых прекордиальных отведений (V1–V2) выше стандартной позиции, вплоть до II межреберья. Выявление патогномоничных изменений ЭКГ в этих позициях имеет такую же диагностическую значимость, как и при стандартном расположении электродов. Изменения конечной части желудочкового комплекса, характерные для синдрома Бругада, могут иметь преходящий характер. Поэтому в тех случаях, когда имеющиеся записи ЭКГ не несут в себе признаков, в полной мере укладывающихся в диагностические критерии, но есть основание предполагать наличие синдрома Бругада, целесообразно проведение диагностических провокационных лекарственных проб с использованием блокаторов натриевых каналов, вводимых внутривенно, — аймалина (в дозе 1 мг/кг; в России не зарегистрирован) или прокаинамида (в дозе 10 мг/кг), позволяющих в части случаев «обнажить» признаки этого синдрома. Фармакологические провокационные пробы должны проводиться опытным медицинским персоналом при мониторировании ЭКГ больного и обязательной возможности организации реанимационных мероприятий в случае индукции опасных для жизни желудочковых аритмий под влиянием вводимых препаратов.
В соответствии с изменёнными диагностическими критериями, для постановки диагноза синдрома Бругада необходима регистрация на ЭКГ спонтанной или индуцированной лекарственными препаратами элевации сегмента ST по типу «свода» (тип 1) хотя бы в одном из правых прекордиальных отведений (V1–V2) при расположении электродов в типичном месте или установке их во II межреберье.
Методы молекулярно-генетической диагностики также имеют значение для диагностики заболевания, однако генетические мутации у больных синдромом Бругада удаётся обнаружить лишь приблизительно в 30% случаев, поэтому отрицательный результат генетического анализа не позволяет полностью исключить диагноз синдрома Бругада. В случае обнаружения у больного синдромом Бругада генетической мутации проведение скрининга, направленного на выявление этой мутации, рекомендовано всем близким родственникам, даже при отсутствии у них характерных этому заболеванию изменений ЭКГ. Проведение молекулярно-генетических исследований лицам, имеющим ЭКГ-изменения 2 и 3 типов, при отсутствии у них клинических проявлений синдрома Бругада и отягощённого по ВСС семейного анамнеза в настоящее время не рекомендовано.
Дифференциальная диагностика
Синдром Бругада следует дифференцировать от других возможных причин синкопальных состояний, учитывая относительно молодой возраст больных, прежде всего, от эпилепсии и вазо-вагальных обмороков, а также от других врождённых желудочковых нарушений ритма сердца.
Необходимо также отметить, что схожие с синдромом Бругада изменения ЭКГ могут быть выявлены при целом ряде патологических состояний. Причинами «бругадоподобных» изменений ЭКГ могут быть:
- атипичная блокада правой ножки пучка Гиса;
- гипертрофия левого желудочка;
- феномен ранней реполяризации желудочков;
- острый коронарный синдром;
- аневризма левого желудочка;
- стенокардия Принцметала;
- острый перикардит;
- гемоперикард;
- тромбоэмболия лёгочной артерии;
- расслаивающая аневризма аорты;
- электролитные нарушения (гиперкалиемия, гиперкальциемия);
- гипотермия/гипертермия;
- аритмогенная дисплазия-кардиомиопатия правого желудочка;
- механическая компрессия выносящего тракта правого желудочка (например, опухоль органов средостения);
- передозировка трициклических антидепрессантов;
- кокаиновая интоксикация;
- различные заболевания центральной и вегетативной нервной системы (субарахноидальное кровоизлияние; геморрагический инсульт; атаксия Фридриха);
- мышечная дистрофия Дюшена–Беккера.
Источник
ЭКГ при синдроме Бругада и его лечение
Синдром Бругада характеризуется наличием типичной ЭКГ-картины в виде косонисходящего подъема сегмента ST в отведениях V1, V2 и иногда V3 (как правило, вместе с неполной блокадой ПНПГ), отсутствием структурных изменений со стороны сердца и повышенным риском внезапной смерти от ФЖ или развитием синкопальных состояний вследствие полиморфной ЖТ. Распространенность составляет 1:5000.
Диагностика синдрома Бругада
Наиболее типичные изменения желудочкового комплекса обычно выявляются в отведениях V1 и V2 (I тип): желудочковый комплекс заканчивается положительным отклонением с амплитудой >2 мм (наподобие зубца J, наблюдаемого при гипотермии), за которым следует косонисходящий сегмент ST и отрицательный зубец Т. Интервал PR бывает удлинен. Пароксизмы ФП не являются редкостью. Часто выявляются поздние потенциалы.
У некоторых пациентов типичные ЭКГ-признаки бывают интермиттирующими. Временами подъем сегмента ST может принимать вогнутую или седловидную форму (II или III тип). Такого рода изменения сами по себе не являются достаточными диагностическими признаками синдрома Бругада. Кроме того, ЭКГ может становиться нормальной.
Диагностическое значение ЭКГ можно повысить, разместив грудные отведения на одно или два межреберья выше обычной позиции. Это следует иметь в виду при лечении пациентов, госпитализированных по поводу синкопального состояния неясного происхождения или реанимированных в связи с необъяснимой ФЖ.
С диагностической целью можно применить пробу с внутривенным введением аймалина (1 мг/кг за 5 мин) или, при его недоступности, флекаинида (2 мг/кг за 10 мин). При наличии на ЭКГ признаков, позволяющих предположить диагноз синдрома Бругада, введение данных препаратов приводит к появлению типичных ЭКГ-признаков синдрома Бругада I типа. Иногда ЭКГ-признаки появляются или усугубляются на фоне лихорадки.
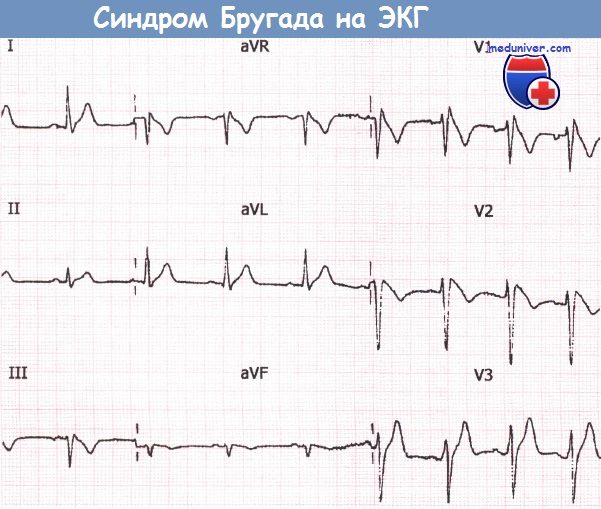
Рутинная ЭКГ с признаками синдрома Бругада, зарегистрированная у медицинского работника, который впоследствии внезапно скончался.
Причины синдрома Бругада
Причиной синдрома Бругада являются генетически обусловленные нарушения функции натриевых ионных каналов. Описано несколько генетических аномалий, связанных с этим синдромом. Не у всех пациентов в семейном анамнезе выявляются случаи внезапной сердечной смерти. Бывают случаи, обусловленные мутацией.
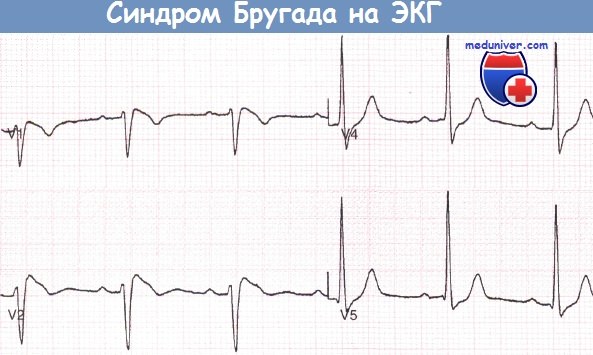
Запись грудных отведений ЭКГ пациента с синдромом Бругада, реанимированного после фибрилляции желудочков (ФЖ), развившейся во время управления автомобилем.
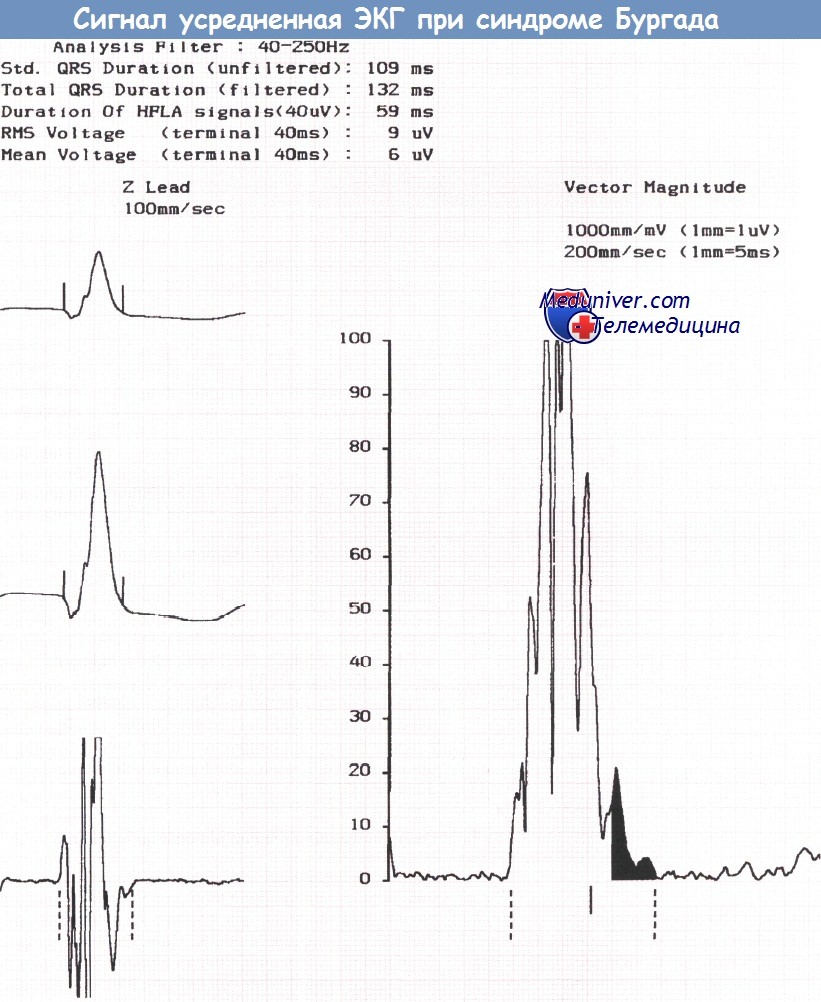
Сигнал-усредненная ЭКГ, зарегистрированная у того же пациента водителя автомобиля, что и на рисунке выше, демонстрирует наличие поздних потенциалов.
Фибрилляция желудочков при синдроме Бругада
Фибрилляция желудочков при синдроме Бругада чаще наблюдается в среднем возрасте. Она редко развивается в первые 2 десятилетия жизни. Как правило, аритмия возникает во сне или в покое. Хотя синдром Бругада обусловлен аутосомно-доминантным геном, нарушения ритма намного чаще наблюдаются у мужчин.
Ни один из известных антиаритмических препаратов не продемонстрировал способность эффективно предотвращать ФЖ, однако существуют данные об эффективности хинидина при «аритмическом шторме». Единственным методом лечения является имплантация автоматического дефибриллятора. Такое устройство должно быть имплантировано всем пациентам, перенесшим синко-пальное состояние или реанимацию в связи с ФЖ.
Факторы риска при синдроме Бругада
Надежных критериев выявления пациентов с высоким риском, к сожалению, не существует. Исследования в этой области весьма ограничены в связи с относительно малым количеством больных и коротким периодом наблюдения, а также из-за больших различий в частоте зарегистрированных случаев внезапной смерти.
В некоторых работах сообщается о довольно высокой частоте фибрилляции желудочков (ФЖ) у ранее бессимптомных пациентов (8% за 3 года), в то время как другие авторы приводят данные о более низком риске (2% за 5 лет или 0,5% за 30 мес).
Есть мнение о целесообразности стимуляции желудочков при синдроме Бругада I типа. В соответствии с этой позицией имплантация дефибриллятора должна быть рекомендована пациентам, у которых в ходе такого исследования развивается ФЖ, однако в последующих исследованиях это положение не нашло подтверждения.
В качестве возможных факторов риска разными исследователями рассматривались поздние потенциалы желудочков и увеличение продолжительности комплекса QRS, а также нарастание степени выраженности подъема сегмента ST во время теста с физической нагрузкой. Удивительно, но наличие случаев внезапной сердечной смерти в семейном анамнезе, по-видимому, также нельзя считать фактором риска.
Общее мнение заключается в том, что риск меньше у пациентов, у которых отсутствуют спонтанные ЭКГ-признаки синдрома Бругада 1 типа.
Лечение синдрома Бругада
Рутинная имплантация дефибрилляторов бессимптомным пациентам не оправданна в связи с низким риском внезапной смерти, а также хорошо известной и довольно высокой частотой осложнений, связанных с использованием этих устройств, в том числе и при длительном наблюдении за больными. Недавно было предложено назначать в таких случаях хинидин.
Пациентам с синдромом Бругада рекомендуется воздерживаться от приема антиаритмических препаратов I класса (таких как флекаинид) и как можно быстрее начинать лечение любого заболевания, сопровождающегося лихорадкой.
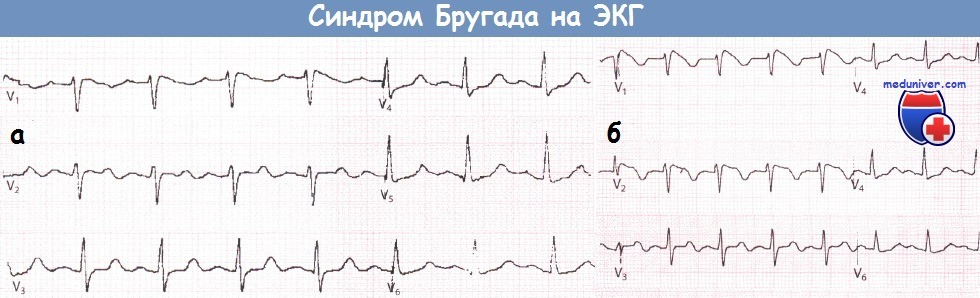
ЭКГ, записанная в грудных отведениях у пациента с подозрением на синдром Бругада (а).
После введения аймалина регистрируется ЭКГ, типичная для синдрома Бругада I типа (б).
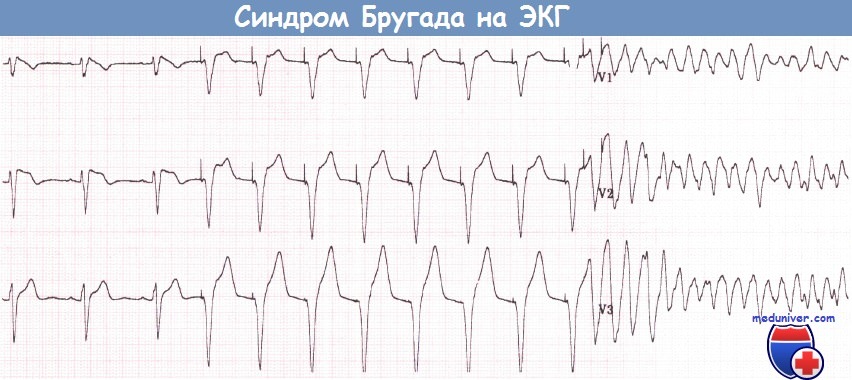
Бессимптомный пациент с синдромом Бругада (отведения V1-V3), у которого во время исследования со стимуляцией желудочков развилась ФЖ.
После 8-го навязанного комплекса при частоте стимуляции 120 имп./мин парой преждевременных стимулов инициирована ФЖ.
(Больному был установлен имплантируемый кардиовертер-дефибриллятор (ИКД) и в последующем отмечалось несколько адекватных нанесений электрических разрядов.)
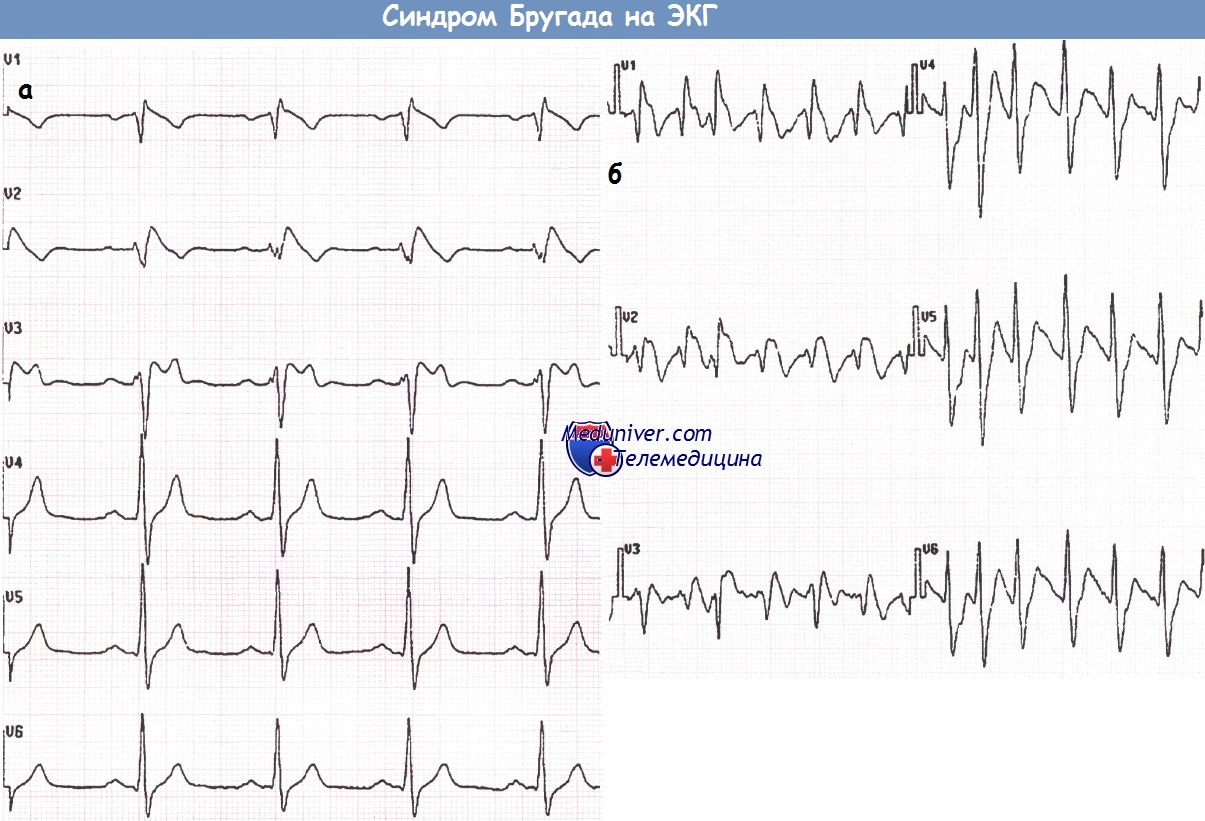
Пациент с синдромом Бругада (а), у которого развилась фибрилляция предсердий (ФП) (б)
Учебное видео ЭКГ при синдроме Бругада
При проблемах с просмотром скачайте видео со страницы Здесь
— Также рекомендуем «ЭКГ при синдроме ранней реполяризации желудочков»
Оглавление темы «Нарушения ритма сердца»:
- ЭКГ при фасцикулярной тахикардии
- ЭКГ при неустойчивой желудочковой тахикардии
- ЭКГ при ускоренном идиовентрикулярном ритме
- ЭКГ при полиморфной желудочковой тахикардии
- ЭКГ при тахикардии типа пируэт и ее лечение
- ЭКГ при врожденном удлинении интервала QT
- Лечение врожденного удлинения интервала QT на ЭКГ
- ЭКГ при фибрилляции желудочков
- ЭКГ при синдроме Бругада и его лечение
- ЭКГ при синдроме ранней реполяризации желудочков
Источник
