Синдром бронхиальной обструкции симптомы у детей
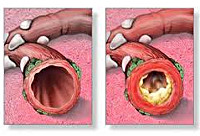

Обструктивный бронхит у детей — воспалительное поражение бронхиального дерева, протекающее с явлением обструкции, т. е. нарушением проходимости бронхов. Течение обструктивного бронхита у детей сопровождается малопродуктивным кашлем, шумным свистящим дыханием с форсированным выдохом, тахипноэ, дистанционными хрипами. При диагностике обструктивного бронхита у детей учитываются данные аускультации, рентгенографии грудной клетки, спирометрии, бронхоскопии, исследования крови (общего анализа, газов крови). Лечение обструктивного бронхита у детей проводится с помощью ингаляционных бронхолитиков, небулайзерной терапии, муколитиков, массажа, дыхательной гимнастики.
Общие сведения
Бронхиты у детей являются самими распространенными заболеваниями респираторного тракта. У детей раннего возраста воспаление бронхов нередко протекает с бронхообструктивным синдромом, обусловленным отеком слизистой, повышенной бронхиальной секрецией и бронхоспазмом. В первые три года жизни обструктивный бронхит переносят около 20% детей; у половины из них в дальнейшем эпизоды бронхообструкции повторяются, как минимум 2-3 раза.
Дети, неоднократно болеющие острыми и обструктивными бронхитами, составляют группу риска по развитию хронической бронхолегочной патологии (хронического бронхита, облитерирующего бронхиолита, бронхиальной астмы, бронхоэктатической болезни, эмфиземы легких). В связи с этим вопросы трактовки этиологии и патогенеза, клинического течения, дифференциальной диагностики и современного терапевтического лечения являются приоритетными для педиатрии и детской пульмонологии.

Обструктивный бронхит у детей
Причины
В этиологии обструктивного бронхита у детей первостепенную роль играют респираторно-синцитиальный вирус, вирус парагриппа 3 типа, энтеровирусы, вирусы гриппа, адено- и риновирусы. Подтверждением ведущего значения вирусных возбудителей служит тот факт, что в большинстве наблюдений манифестации обструктивного бронхита у ребенка предшествует ОРВИ.
При повторных эпизодах обструктивного бронхита у детей в смыве с бронхов часто выявляется ДНК персистирующих инфекций — хламидий, микоплазм, герпесвирусов, цитомегаловируса. Часто бронхит с обструктивным синдромом у детей провоцируется плесневым грибком, который интенсивно размножается на стенах помещений с повышенной влажностью. Оценить этиологическое значение бактериальной флоры довольно затруднительно, поскольку многие ее представители выступают условно-патогенными компонентами нормальной микрофлоры дыхательных путей.
Немаловажную роль в развитии обструктивного бронхита у детей играет аллергический фактор – повышенная индивидуальная чувствительность к пищевым продуктам, лекарственным препаратам, домашней пыли, шерсти животных, пыльце растений. Именно поэтому обструктивному бронхиту у детей часто сопутствуют аллергический конъюнктивит, аллергический ринит, атопический дерматит.
Рецидивам эпизодов обструктивного бронхита у детей способствует глистная инвазия, наличие очагов хронической инфекции (синуситов, тонзиллита, кариеса и др.), активное или пассивное курение, вдыхание дыма, проживание в экологически неблагоприятных регионах и т. д.
Патогенез
Патогенез обструктивного бронхита у детей сложен. Вторжение вирусного агента сопровождается воспалительной инфильтрацией слизистой бронхов плазматическими клетками, моноцитами, нейтрофилами и макрофагами, эозинофилами. Выделение медиаторов воспаления (гистамина, простагландинов и др.) и цитокинов приводит к отеку бронхиальной стенки, сокращению гладкой мускулатуры бронхов и развитию бронхоспазма.
Вследствие отека и воспаления увеличивается количество бокаловидных клеток, активно вырабатывающих бронхиальный секрет (гиперкриния). Гиперпродукция и повышенная вязкость слизи (дискриния) вызывают нарушение функции реснитчатого эпителия и возникновение мукоцилиарной недостаточности (мукостаза). Вследствие нарушения откашливания, развивается обтурация дыхательных путей бронхиальным секретом. На этом фоне создаются условия для дальнейшего размножения возбудителей, поддерживающих патогенетические механизмы обструктивного бронхита у детей.
Некоторые исследователи в бронхообструкции видят не только нарушение процесса внешнего дыхания, но и своего рода приспособительные реакции, которые в условиях поражения реснитчатого эпителия защищают легочную паренхиму от проникновения в нее патогенов из верхних дыхательных путей. Действительно, в отличие от простого бронхита, воспаление с обструктивным компонентом значительно реже осложняется пневмонией у детей.
Для обозначения обструктивного бронхита у детей иногда используются термины «астматический бронхит» и «спастический бронхит», однако они являются более узкими и не отражают всей полноты патогенетических механизмов заболевания.
По течению обструктивный бронхит у детей может быть острым, рецидивирующим и хроническим или непрерывно-рецидивирующим (при бронхолегочной дисплазии, облетирующем бронхиолите и др.). По степени выраженности бронхиальной обструкции выделяют: легкую (I), среднетяжелую (II), тяжелую (III) степень обструктивного бронхита у детей.
Симптомы обструктивного бронхита у детей
Чаще всего первый эпизод обструктивного бронхита развивается у ребенка на 2-3-м году жизни. В начальном периоде клиническая картина определяется симптомами ОРВИ – повышенной температурой тела, першением в горле, насморком, общим недомоганием. У детей раннего возраста нередко развиваются диспептические симптомы.
Бронхиальная обструкция может присоединяться уже в первые сутки заболевания или через 2-3 дня. При этом отмечается увеличение частоты дыхания (до 50-60 в мин.) и продолжительности выдоха, который становится шумным, свистящим, слышимым на расстоянии. Кроме тахипноэ, экспираторной или смешанной одышки у детей с обструктивным бронхитом отмечается задействованность в акте дыхания вспомогательной мускулатуры, увеличение переднезаднего размера грудной клетки, втяжение ее уступчивые мест при дыхании, раздувание крыльев носа. Кашель у детей с обструктивным бронхитом малопродуктивный, со скудной мокротой, иногда мучительный, приступообразный, не приносящий облегчения. Даже при влажном кашле мокрота отходит с трудом. Отмечается бледность кожных покровов или периоральный цианоз. Проявления обструктивного бронхита у детей могут сопровождаться шейным лимфаденитом. Бронхообструкция держится 3-7 дней, исчезает постепенно по мере стихания воспалительных изменений в бронхах.
У детей первого полугодия, особенно соматически ослабленных и недоношенных, может развиваться наиболее тяжелая форма обструктивного синдрома — острый бронхиолит, в клинике которого преобладают признаки тяжелой дыхательной недостаточности. Острый обструктивный бронхит и бронхиолит нередко требуют госпитализации детей, поскольку данные заболевания приблизительно в 1% случаев заканчиваются летальным исходом. Затяжное течение обструктивного бронхита наблюдается у детей с отягощенным преморбидным фоном: рахитом, хронической ЛОР-патологией, астенизацией, анемией.
Диагностика
Клинико-лабораторное и инструментальное обследование детей с обструктивным бронхитом проводится педиатром и детским пульмонологом; по показаниям ребенку назначаются консультации детского аллерголога-иммунолога, детского отоларинголога и других специалистов. При аускультации выслушивается удлиненный выдох, разнокалиберные влажные и рассеянные сухие хрипы с двух сторон; при перкуссии над легкими определяется коробочный оттенок.
На рентгенограммах органов грудной клетки выражены признаки гипервентиляции: повышение прозрачности легочной ткани, горизонтальное расположение ребер, низкое стояние купола диафрагмы. В общем анализе крови может выявляться лейкопения, лимфоцитоз, небольшое увеличение СОЭ, эозинофилия. При исследовании газового состава крови обнаруживается умеренная гипоксемия. В случае необходимости дополнительно проводится иммунологическое, серологическое, биохимическое исследование крови; определение ДНК основных респираторных патогенов в крови методом ПЦР, постановка аллергологических проб. Выявлению возбудителей могут способствовать микроскопическое исследование мокроты, бакпосев мокроты на микрофлору, исследование смывов из носоглотки.
При обструктивном бронхите у детей необходимо исследование дыхательных объемов (ФВД), в том числе с лекарственными пробами. С целью визуальной оценки состояния слизистой оболочки бронхов, проведения бронхоальвеолярного лаважа, цитологического и бактериологического исследования промывных вод детям с обструктвиным бронхитом выполняется бронхоскопия.
Повторные эпизоды обструктивного бронхита требуют дифференциальной диагностики с бронхиальной астмой у детей.
Лечение обструктивного бронхита у детей
Терапия обструктивного бронхита у детей раннего возраста проводится в стационаре; более старшие дети подлежат госпитализации при тяжелом течении заболевания. Общие рекомендации включают соблюдение полупостельного режима и гипоаллергенной (преимущественно молочно-растительной) диеты, обильное питье (чаи, отвары, морсы, щелочные минеральные воды). Важными режимными моментами служат увлажнение воздуха, регулярная влажная уборка и проветривание палаты, где лечатся дети с обструктивным бронхитом.
При выраженной бронхообструкции активно применяется кислородотерапия, горячие ножные ванны, баночный массаж, удаление слизи из верхних дыхательных путей электроотсосом. Для снятия обструкции целесообразно использовать ингаляции адреномиметиков (сальбутамола, тербуталина, фенотерола) через небулайзер или спейсер. При неэффективности бронхолитиков лечение обструктивного бронхита у детей дополняется кортикостероидами.
Для разжижения мокроты показано применение препаратов с муколитическим и отхаркивающим эффектами, лекарственных и щелочных ингаляций. При обструктивном бронхите детям назначаются спазмолитические и противоаллергические средства. Антибактериальная терапия проводится только в случае присоединения вторичной инфекции.
С целью обеспечения адекватного дренажа бронхиального дерева детям с обструктивным бронхитом показана дыхательная гимнастика, вибрационный массаж, постуральный дренаж.
Прогноз и профилактика
Около 30-50% детей склонны к повторению обструктивного бронхита в течение одного года. Факторами риска рецидива бронхообструкции служат частые ОРВИ, наличие аллергии и очагов хронической инфекции. У большинства детей эпизоды обструкции прекращаются в дошкольном возрасте. Бронхиальная астма развивается у четверти детей, перенесших рецидивирующий обструктивный бронхит.
К мерам профилактики обструктивного бронхита у детей относится предупреждение вирусных инфекций, в том числе при помощи вакцинации; обеспечение гипоаллергенной среды, закаливание, оздоровление на климатических курортах. После перенесенного обструктивного бронхита дети находятся на диспансерном наблюдении у педиатра, возможно — детского пульмонолога и аллерголога.
Источник
Бронхообструктивный синдром (БОС) в раннем детском возрасте часто связан с атопией и бронхиальной астмой (БА). В то же время причиной бронхообструкции могут быть инфекции дыхательных путей; некоторые наследственные и врожденные заболевания; патология периода новорожденности.
У новорожденных бронхообструктивный синдром может проявляться при синдроме дыхательных расстройств (СДР); аспирационном синдроме (околоплодные воды, грыжа пищевода, трахеоэзофагальная фистула и др.); перинатальной энцефалопатии.
Бронхообструктивный синдром и сопутствующие заболевания
Бронхообструктивный синдром сопровождается рядом наследственных и врожденных заболеваний:
- муковисцидоз;
- альфа-1-антитрипсина;
- врожденный стридор;
- гастроэзофагальный рефлюкс;
- врожденные пороки развития сердца и сосудов;
- бронхоэктазы;
- бронхолёгочная дисплазия и др.
Среди инфекционных респираторных заболеваний наиболее часто БОС развивается при остром обструктивном бронхите; остром бронхиолите; рецидивирующем бронхите; хроническом бронхите; ларинготрахеите; после перенесенного коклюша; реже – при пневмонии.
Преимущественно аллергическая природа БОС наблюдается при поллинозе; аллергической реакции на медикаменты; синдроме Лёффлера; бронхиальной астме (БА).
Бронхиальная астма
БА относится к наиболее распространенным заболеваниям, которыми страдают около 15% детского и 7% взрослого населения. Хотя этот показатель и невысок, тем не менее, течение БОС и особенно БА в раннем детстве нередко тяжелое, с частыми обострениями, формирование резистентных форм к лечению, приводящее к инвалидности и даже к летальному исходу.
Гиперреактивность бронхов наблюдается у большинства больных БА в раннем детском возрасте. Она формируется чаще, чем у старших детей и взрослых из-за особенностей нейрорегуляторных механизмов у них. У детей первого года жизни преобладает функция парасимпатического отдела. Активность симпатического отдела существенно снижается в вечернее, ночное и утреннее время. Поэтому усиление парасимпатического влияния в эти часы способствует возникновению ночных приступов бронхообструкции.
Стимуляция парасимпатических нервных окончаний, афферентные рецепторы которых расположены на бронхиальном эпителии и в стенках альвеол, вызывает сужение и отек слизистой бронхов; расширение сосудов; гиперсекрецию слизи. Вследствие этого в периоде раннего детства даже у здоровых детей наблюдается дисфункция вегетативной регуляции. Она легко усугубляется при различных повреждениях плода и новорожденного.
В условиях участившегося в последние годы оперативного родоразрешения в роддомах и связанного с ним синдрома медикаментозной депрессии новорожденного, а также использования принудительной искусственной вентиляции легких (ИВЛ) более часто формируются патологические изменения в респираторном тракте – бронхолёгочные дисплазии, интерстициальная эмфизема и др. Это в свою очередь создает благоприятный фон для раннего развития аллергической патологии. В частности, приводит к тому, чтобы начал формироваться бронхообструктивный синдром.
Генетические аспекты заболевания
Известно, что основную роль в развитие БА играет атопия, предрасположенность к развитию IgE–опосредованных реакций, которая встречается у 30-40% населения развитых стран с тенденцией к росту. В то же время немалую роль играют генетические аспекты БА.
Благодаря современным молекулярно-генетическим исследованиям уже идентифицированы потенциальные гены-кандидаты наследственной предрасположенности к БА и атопии. Наиболее важным является селекция генов, продукты которых известны как медиаторы имунновоспалительных процессов и повреждения тканей дыхательных путей при БА. Среди них выделены гены, кодирующие цитокины Т-хелперов (ТН 1, ТН 2), ?2 – адренорецепторов, регуляторы уровня иммуноглобулинов, гиперреактивовность бронхов и др.
Не менее важным компонентом в развитии БА являются факторы внешней среды, которые могут дать толчок в реализации генетической предпосылки, наследственной предрасположенности. Сюда относят внешние факторы среды – аллергены различного происхождения (растительного, животного, вирусного, бактериального, в том числе и химические вещества с повышенной концентрацией аллергенов искусственного происхождения) и внутренние факторы (хронические заболевания ЖКТ, гельминтозы, несбалансированная диета и др.).
Указанные факторы, по мнению многих авторов, приводят к снижению природной антигенной нагрузки в раннем детском возрасте и способствуют формированию извращенного иммунного ответа с преобладанием Т2 – хелперов. При этом увеличивается риск появления патологической аллергической реакции и атопии на воздействие обычных факторов среды.
 Бронхообструктивный синдром и бронхиальная астма
Бронхообструктивный синдром и бронхиальная астма
Диагностические критерии бронхиальной астмы у детей
Диагностические критерии БА у детей раннего возраста затруднительны, так как ведущие симптомы (экспираторная отдышка, шумное свистящее дыхание с удлиненным выдохом, повышенная воздушность легких) мало специфичны и могут встречаться при распространенных в детском возрасте респираторных заболеваниях.
Первый эпизод обструкции у ребенка с атопией часто провоцируется вирусной инфекцией и протекает на фоне повышения температуры тела, в виде отдышки смешанного характера, шумного свистящего дыхания, спазматического кашля. Как правило, это позволяет предположить у такого ребенка диагноз острого обструктивного бронхита или бронхиолита. Но у большинства детей с атопией после первого эпизода бронхиальной обструкции далее повторно наблюдается приступы экспираторной отдышки чаще на фоне нормальной температуры. Такие рецидивирующие приступы бронхиальной обструкции есть проявление формирующейся БА. В то время как большинство практических врачей не решаются выставить такой диагноз. Они предпочитают формулировку «рецидивирующий обструктивный бронхит», «ОРВИ с астматическим синдромом» и др.
Лечение бронхиальной астмы
Учитывая особенность течения БОС у детей раннего возраста и формирования БА у них, традиционное лечение указанного синдрома включает применение холинолитических препаратов в виде индивидуальных дозированных аэрозолей через спейсер или маску (с помощью бебихалера).
Несмотря на достигнутые успехи лечения БОС, во всем мире сохраняется тенденция к «омоложению» и росту заболеваемости. Поэтому в мировом медицинском сообществе ведутся постоянные поиски оптимизации лечения синдрома бронхиальной обструкции и БА у детей. Наряду с традиционным лечением, включающим холинолитики и ?2-агонисты в аэрозоле, в/в инъекции эуфилина, глюкокортикостероиды, кислородотерапию (в случае тяжелого или среднетяжелого течения), в последние годы стало возможным использование новых способов доставки лекарств через небулайзер – специальное устройство для образования мелкодисперсных аэрозолей лекарств под воздействием сжатого воздуха, нагнетаемого компрессором (струйный небулайзер).
Небулайзерная терапия
Небулайзерная терапия (НТ) имеет ряд преимуществ перед другими способами доставки лекарственных препаратов. Во-первых, небулайзер является единственным средством доставки лекарственного препарата в альвеолы и позволяет создать высокую концентрацию мельчайших частиц (от 5 мкм до 0,8 мкм) распыляемого вещества а также доставить его за короткий промежуток времени к месту патологического процесса.
Во-вторых, ингалируемое вещество практически не всасывается в кровь и не оказывает побочных действий на другие органы и системы, как это бывает при приеме таблеток или инъекциях. Особенно важным является то, что при использовании НТ нет необходимости координировать вдох и ингаляции; а также простота и легкость выполнения, высокая эффективность и возможность применения с первых месяцев жизни делает это метод незаменимым и единственно возможным у детей до пяти лет, а также у пожилых пациентов. В НТ не используется фрион, есть возможность комбинирования лекарственных препаратов, одновременно ингалировать кислород и возможно подключение в контур ИВЛ.
Статистика лечения
Под наблюдением в пульмонологическом отделении ГБ № 3 г. Донецка находилось 64 ребенка в возрасте от 6 месяцев до 14 лет с синдромом бронхиальной обструкции, в том числе 35 детей с обструктивным бронхитом, 19 детей с бронхиальной астмой и 10 пациентов с острым стенозирующим ларинготрахеобронхитом. С целью оптимизации лечения использовалось НТ компрессорным небулайзером OMRON СХ3 (сертифицированным в соответствии с Европейским стандартом для небулайзеров prEN13544-1) со специальным растворами в том числе ?2-агонисты, холинолитики, комбинированные препарат – 0,25% раствор беродуала 250 мкг/1мл, муколитики, кортикостероиды (суспензия пульмикорта – 0,25 и 0,5 мг в 1 мл) в возрастной дозировке.
У 52 детей (81,3%) наблюдалось улучшение состояния и регресс обструкции уже в первые или во вторые сутки после ингаляции бронхоспазмолитика. Недостаточный эффект был у 12 (18,7%) детей. Из них 6 пациентов в терапию включены глюкокортикостероиды (преднизалон) в дозе 1,5-2мг/кг парентерально, эуфилин 2,4% раствор внутривенно -5-10 мг/кг/сутки. Остальные 6 детей получили пульмикорт через небулайзер в дозе 0,5-1 мг два раза в день в течение 3-5 дней. После НТ состояние детей стабилизировалось на вторые – третьи сутки. В то же время при включении в терапию системных стероидов улучшение было более медленным (на 4-5 сутки), чем при назначении пульмикорта.
Таким образом, использование ингаляционного стероида через небулайзер у детей раннего возраста было более эффективным, чем применение системных стероидов и может быть предпочтительнее в комплексной терапии тяжелого течения БОС и БА.
Литература
С.И. Овчаренко, О.А. Передельская. Небулайзерная терапия тяжелой бронхиальной астмы. Российский мед.журнал-2002, № 1, с. 24-28.
Н.Г. Горовенко. Генетические аспекты развития аллергических заболеваний. ж. «Доктор», 2003г. № 6, с. 29-30.
Н.А. Геппе, Н.А. Селиверстова, А.Б. Малахов, М.Н. Лисицин, М.Н. Снегоцкая, В.С. Малышев. Ингаляционные кортикостероиды (пульмикорд) для небулайзерной терапии у детей.
О.И. Ласица, Е.Н. Охотникова. Применение холинолитиков при бронхообструктивном синдроме детей.
Источник
