Синдром альпорта у детей клинические рекомендации

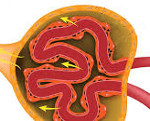
Синдром Альпорта – наследственное заболевание почек, вызванное изменением синтеза коллагена типа IV, образующего базальные мембраны почечных клубочков, структуры внутреннего уха, хрусталика глаза. Мужчины страдают развернутой формой болезни с тяжелой симптоматикой. Женщины часто являются носителями гена, оставаясь здоровыми, или проявления болезни у них выражены слабо. Основные симптомы – микрогематурия, протеинурия, почечная недостаточность, сенсорная тугоухость, деформация и вывих хрусталика, катаракта. Диагноз устанавливается согласно клинико-анамнестическим данным, результатам общего анализа мочи, исследования биоптата почки, аудиометрии и офтальмологического осмотра. Лечение симптоматическое, включает терапию иАПФ и БРА.
Общие сведения
Семейные случаи гематурической нефропатии впервые привлекли внимание исследователей в 1902 году. Спустя почти 30 лет, в 1927 году американский врач А. Альпорт обнаружил частую сочетаемость гематурии с тугоухостью и уремией у мужчин, в то время как у женщин симптомы отсутствовали или были слабовыраженными. Он предположил наследственный характер болезни, которая впоследствии была названа синдромом Альпорта. Синонимы – наследственный нефрит 1 типа, гематурический нефрит, семейный гломерулонефрит. Распространенность невысока – 1 случай на 5 тысяч человек. На долю патологии приходится 1% больных с почечной недостаточностью, 2,3% пациентов, перенесших трансплантацию почек. Заболевание диагностируется у людей всех рас, но соотношение различных форм неодинаково.
Синдром Альпорта
Причины
По своей природе синдром является гетерогенным наследственным заболеванием – его развитие провоцируется дефектом генов, которые кодируют структуру различных цепей IV типа коллагена. Генетические изменения представлены делециями, сплайсинг, миссенс и нонсенс-мутациями. Их локализация определяет тип наследования болезни:
- X-сцепленный доминантный. Связан с мутацией в локусе COL4A5, который находится на половой хромосоме X. Ген кодирует а5-цепь коллагена 4 типа. Данный генетический дефект обуславливает 80-85% случаев наследственного нефрита. В полной мере заболевание проявляется у мальчиков и мужчин, у представительниц женского пола оставшийся нормальный ген в X-хромосоме компенсирует производство функционального коллагена.
- Аутосомно-рецессивный. Развивается на основе мутаций в генах C0L4A3 и COL4A4. Они локализованы на второй хромосоме, отвечают за структуру а3- и а4-цепи коллагена. Пациенты с этим вариантом синдрома составляют около 15% больных. Выраженность симптомов не зависит от пола.
- Аутосомно-доминантный. Нефрит возникает в результате мутаций генов COL4A3-COLA4, находящихся на 2 хромосоме. Как и в случае аутосомно-рецессивной формой болезни, нарушается синтез а4- и а3-цепей коллагена четвертого типа. Распространенность – 1% всех случаев генетического нефрита.
Патогенез
Гломерулярная базальная мембрана имеет сложное строение, ее образует строгая геометрическая последовательность молекул коллагена 4-го типа и полисахаридные компоненты. При синдроме Альпорта имеются мутации, которые задают дефектное строение спиралевидных коллагеновых молекул. На первых этапах болезни базальная мембрана истончается, начинает расщепляться и расслаиваться. Одновременно возникают утолщенные участки с неравномерными просветлениями. Внутри скапливается тонкогранулярное вещество. Прогрессирование болезни сопровождается полным разрушением базальной гломерулярной мембраны клубочковых капилляров, канальцев почек, структур внутреннего уха и глаз. Таким образом, патогенетически синдром Альпорта представлен четырьмя звеньями: мутацией гена, дефектом строения коллагена, деструкцией базальных мембран, патологией почек (иногда – нарушением слуха и зрения).
Симптомы
Самым распространенным проявлением синдрома Альпорта является гематурия. Микроскопически этот симптом определяется у 95% женщин и у 100% мужчин. При рутинном обследовании мальчиков гематурия обнаруживается уже в первые годы жизни. Другой распространенный признак заболевания – протеинурия. Выведение белка с мочой у пациентов мужского пола с X-сцепленным синдромом начинается в раннем детском возрасте, у остальных – позже. У девочек и женщин уровень экскреции белка повышается незначительно, случаи выраженной протеинурии крайне редки. У всех больных отмечается неуклонное прогрессирование симптома.
Артериальная гипертензия характерна для мужчин с классическим типом синдрома и для пациентов обоих полов с аутосомно-рецессивным вариантом наследования. Тяжесть гипертонии увеличивается вместе с нарастанием ХПН. У юношей, мужчин снижение функции почек достигает терминальной стадии к 16-35 годам, при медленном течении болезни – к 45-65 годам. Иногда выявляются диффузные гладкомышечные опухоли пищевода и бронхов, проявляющиеся в позднем детстве дисфагией, рвотой, болями в эпигастрии и за грудиной, одышкой, частыми бронхитами.
Часто у больных формируется нейросенсорная тугоухость. Нарушения слуха дебютируют в детстве, но становятся заметными в подростничестве или молодости. У детей тугоухость распространяется только на звуки высокой частоты, обнаруживается в специально созданных условиях – при аудиометрии. По мере взросления и прогрессирования синдрома нарушается слуховое восприятие средних и низких частот, в том числе человеческой речи. При X-связанном синдроме расстройство слуха к 25 годам имеется у 50% больных мужчин, к 40 годам – у 90%. Тяжесть тугоухости вариабельна, от изменений только в результатах аудиограммы до полной глухоты. Патологии вестибулярного аппарата отсутствуют.
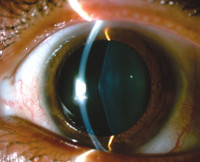
Расстройства зрения включают передний лентиконус – выпячивание центра хрусталика глаза вперед и ретинопатию. Обе патологии проявляются прогрессирующим ухудшением зрительной функции, покраснением, болью в глазах. У некоторых больных имеются стигмы дизэмбриогенеза – анатомические аномалии мочевыделительной системы, глаз, ушных раковин, конечностей. Может наблюдаться высокое расположение неба, укорочение и искривление мизинцев, сращивание пальцев ног, широко расставленные глаза.
Осложнения
Отсутствие лечения больных синдромом Альпорта приводит к быстрому прогрессированию глухоты и слепоты, формированию катаракт. У части пациентов развивается полиневропатия – поражение нервов, сопровождающееся мышечной слабостью, болями, судорогами, тремором, парестезиями, снижением чувствительности. Другим осложнением является тромбоцитопения с высоким риском кровотечений. Наиболее опасным состоянием при наследственном нефрите считается терминальная стадия почечной недостаточности. Больше всего ей подвержены мужчины с типом наследования, сцепленным с половой X-хромосомой. К 60 годам 100% больных этой группы нуждаются в процедурах гемодиализа, перитонеального диализа, трансплантации донорской почки.
Диагностика
В диагностическом процессе принимают участие врачи-нефрологи, урологи, терапевты и генетики. При опросе выясняется возраст дебюта симптомов, наличие у родственников первой линии гематурии, протеинурии или смертельных исходов вследствие ХПН. Для синдрома Альпорта характерно раннее начало и отягощенный семейный анамнез. Дифференциальная диагностика направлена на исключение гематурической формы гломерулонефритов, вторичных нефропатий. Для подтверждения диагноза проводятся следующие процедуры:
- Физикальное обследование. Определяется бледность кожных покров и слизистых оболочек, сниженный мышечный тонус, внешние и соматические признаки дизэмбриогенеза – высокое небо, аномалии строения конечностей, увеличенное расстояние между глазами, сосками. На ранних стадиях болезни диагностируется артериальная гипотония, на поздних – артериальная гипертония.
- Общий анализ мочи. Обнаруживаются эритроциты и повышенное содержание белка – признаки гематурии и протеинурии. Показатель белка мочи напрямую коррелирует с тяжестью синдрома, по его изменению оценивается прогрессирование патологии, вероятность нефротического синдрома, ХПН. Возможно наличие признаков лейкоцитурии абактериального характера.
- Исследование биоптата почек. При микроскопии визуализируется истонченная базальная мембрана, расщепление и разделение ее слоев. На поздней стадии отмечаются утолщенные дистрофичные участки с «сотами» просветления, зоны полной деструкции слоя.
- Молекулярно-генетическое исследование. Генетическая диагностика не является обязательной, но позволяет составить более точный прогноз, подобрать оптимальную схему лечения. Изучается строение генов, мутации в которых обуславливают развитие синдрома. У большей части больных выявляются мутации гена COL4A5.
- Аудиометрия, офтальмологическое исследование. Дополнительно пациентам могут быть назначены диагностические консультации сурдолога и офтальмолога. При аудиометрии обнаруживается снижение слуха: в детском и подростковом возрасте – билатеральная высокочастотная тугоухость, во взрослом возрасте – низкочастотная и среднечастотная тугоухость. Офтальмолог определяет искажение формы хрусталика, поражение сетчатки, наличие катаракты, снижение зрения.
Лечение синдрома Альпорта
Специфическая терапия отсутствует. С раннего возраста проводится активное симптоматическое лечение, снижающее протеинурию. Оно позволяет предотвратить поражение и атрофию почечных канальцев, развитие интерстициального фиброза. С помощью ингибиторов ангиотензинпревращающего фермента и блокаторов рецепторов к ангиотензину II удается приостановить прогрессирование заболевания, добиться регрессии гломерулосклероза, тубулоинтерстициальных и сосудистых изменений в почках. Пациентам с терминальной стадией ХПН назначается гемодиализ, перитонеальный диализ, решается вопрос о целесообразности трансплантации почек.
Прогноз и профилактика
Синдром прогностически благоприятен в случаях, когда гематурия протекает без протеинурии, нет расстройств зрения и тугоухости. Кроме этого, прогноз хороший у большинства женщин – даже при наличии гематурии болезнь прогрессирует медленно, не ухудшает общего состояния. Ввиду наследственного характера патологии предупредить ее развитие невозможно. В семьях, где установлено наличие X-сцепленной формы синдрома, возможно проведение пренатальной диагностики. Генетический скрининг особенно рекомендован женщинам, вынашивающим мальчиков.
Источник
Синдром Альпорта у детей (иначе – заболевание тонких мембран) – редкая наследственная патология почек, характеризующаяся изменением выработки коллагеновых волокон IV типа, при этом меняется мембранная структура почечных клубочков с одновременным изменением структуры отделов внутреннего уха и глаз. По статистике, встречается 1 случай на 5000 человек. Примечательно, что синдром диагностируют у 1% больных с различными нефроурологическими патологиями и у 3% пациентов, ранее перенесших трансплантацию почки.
Синдром Альпорта у детей относится к наследственным заболеваниям
Причины и пути наследования
Механизм развития заболевания обусловлен дефектностью генетической единицы, отвечающей за структуру цепей коллагена IV типа. По типу наследования синдром классифицируют:
- на доминантный, или X-сцепленный. Заболевание обусловлено мутацией гена в женской половой хромосоме X. Такой путь наследования встречается в 85% всех клинических случаев;
- аутосомно-рецессивный. Обусловлен мутациями в генах второй порядковой хромосомной единицы, встречается в 10% всех случаев синдрома Альпорта;
- аутосомно-доминантный. Наследственный нефрит вызван мутацией генов во второй порядковой хромосоме, встречается в 1–2% случаев и напоминает течение аутосомно-рецессивного типа.
По мере прогрессирования болезни полностью разрушаются оболочки гломерул, почечных канальцев, внутренних глазных и ушных структур. Механизм развития патологического изменения почечных структур можно объяснить несколькими ключевыми факторами: генной мутацией, нарушением выработки и строения коллагена, разрушением канальцевых и гломерулярных почечных единиц, патологией почек.
Типичные признаки
Болезнь тонких базальных мембран редко диагностируется сразу после рождения или внутриутробно. Специфические симптомы наблюдаются спустя 3–4 года после рождения и выражаются в следующих состояниях:
- гематурический синдром. Одно из ранних проявлений болезни. Обычно выявляется лабораторно. У мальчиков микрогематурия отмечается еще до 1 года, но планово такой анализ на фоне общего здоровья не проводится. Ученые считают, что если до 10 лет ребенка гематурия не выявлялась ни разу, то синдром Альпорта можно исключать на 98%;
- белок в моче. Состояние протеинурии чаще отмечается у мальчиков с доминантным путем наследования мутации. Обычно белок в моче не выявляется или его появление носит эпизодический характер;
- артериальная гипертензия. Стойкое повышение артериального давления характеризуется прогрессированием почечной недостаточности. Чем ниже клиренс креатинина, тем интенсивнее развитие гипертензии;
- тугоухость. Нарушение слуха на фоне нефротического синдрома возникает не всегда. Известны случаи семейного синдрома Альпорта, когда у всех больных нет слуховых изменений. Ранняя стадия тугоухости определяется только при аудиометрии;
- лентиконус передний. Состояние характеризуется выпячиванием глазного хрусталика кнаружи, встречается у 20–25% больных с наследственным нефритом. Офтальмологическое заболевание постоянно прогрессирует, поэтому больные вынуждены часто менять очки;
- роговичная дистрофия. Истончение сетчатки глаза встречается редко. Почти 90% больных с дистрофией роговицы имеют X-сцепленный путь геномной мутации;
- лейомиоматоз бронхов и пищевода. У детей возникает ранняя дисфагия – нарушение глотания. Появляются и иные симптомы: загрудинные и эпигастральные боли, рвота, одышка, сухой кашель. Подтвердить лейомиоматоз можно с помощью МРТ или компьютерной томографии.
По мере взросления ребенка нарастают симптомы почечной недостаточности: недомогание, интоксикация, артериальная гипертензия, резкое увеличение креатинина и мочевины в составе крови, ацидоз.
Диагностика
Наследственный нефрит редко диагностируется после рождения, обычно первые признаки проявляются только к 3–5 годам
Комплексное обследование детей с синдромом Альпорта включает сбор анамнеза жизни, наследственного и клинического анамнеза, изучение жалоб. Учитывая наследственную природу заболевания, значение имеют случаи почечной недостаточности у близких родственников. Для уточнения диагноза проводят ряд исследований:
- общеклинические лабораторные исследования;
- УЗИ почек и почечных структур, органов мочеполовой системы;
- рентгенконтрастные методы исследования (экскреторная урография);
- ДНК-тест;
- биопсия почек.
Диагностика требует дополнительной консультации нефролога, уролога, генетика, офтальмолога, кардиолога, отоларинголога. Заболевание дифференцируют от других геномных мутаций, в частности, от синдрома «кошачьего крика» — нарушения строения 5 хромосомы, когда типичные признаки выражаются в нарушении слуха и зрения еще в раннем возрасте.
Лечение
Заболевание неизлечимо, на причины генетических мутаций невозможно повлиять медикаментозно или хирургически. Терапия направлена на облегчение симптомов болезни. Обычно схема лечения включает следующие группы препаратов:
- мочегонные (петлевые, тиазидные, растительного происхождения);
- внутривенное введение физраствора для предупреждения обезвоживания;
- средства на основе глюконата кальция и глюкозы для восстановления минерального и электролитного баланса;
- антигипертензивная терапия при вторичной артериальной гипертензии (ингибиторы АПФ, блокаторы медленных кальциевых каналов);
- гормоны;
- железосодержащие препараты при выраженном гематурическом синдроме.
При развитии тяжелой почечной недостаточности встает вопрос о заместительной терапии. Лучшим способом заместительной терапии у детей является трансплантация почки. Пересадка органа позволяет вернуть прежний образ жизни, улучшить состояние больного.
Общие клинические рекомендации для больных наследственной нефропатией заключаются в соблюдении охранительного режима и диеты, регулярных прогулках на свежем воздухе, приеме витаминных комплексов. Все лечебные меры должны отвечать возрастным интересам ребенка.
Осложнения
Основными осложнениями при синдроме Альпорта у детей являются глухота, нарушение зрения и недостаточность функции почек. Последнее состояние провоцирует развитие вторичных осложнений, угрожает жизни пациентов.
Прогноз при синдроме Альпорта у детей преимущественно благоприятный, если прогрессия крайне медленная, а симптомы заболевания не выражены. Если гематурия не сопровождается протеинурией, состояние пациента не осложнено, то важно соблюдать предупредительные лечебные меры. Учитывая генетическую природу заболевания, предупредить развитие патологии у детей невозможно.
Также интересно почитать: причины микроцефалии у детей
Источник

Синдром Альпорта — генетически детерминированное воспалительное заболевание почек, сопровождающееся поражением слухового и зрительного анализаторов. Это достаточно редкая наследственная патология, встречающаяся у 1 из 10 тысяч новорожденных детей. По данным ВОЗ лица с синдромом Альпорта составляют 1% от всех больных с дисфункцией почек. По МКБ-10 заболевание имеет код Q87.8.
При синдроме Альпорта поражается ген, кодирующий строение белка коллагена, расположенного в базальной мембране почечных канальцев, внутреннего уха и органа зрения. Основная функция базальной мембраны – поддержание и отделение тканей друг от друга. Наследственная неиммунная гломерулопатия проявляется гематурией, нейросенсорной тугоухостью, расстройством зрения. По мере прогрессирования синдрома у больных развивается почечная недостаточность, к которой присоединяются заболевания глаз и ушей. Болезнь носит прогрессирующий характер и не поддается лечению.

Наследственный нефрит или семейный гломерулонефрит — наименования одной и той же патологии. Впервые ее описал в 1927 году ученый из Великобритании Артур Альпорт. Он наблюдал за членами одной семьи, которые страдали тугоухостью и имели эритроциты в анализах мочи. Спустя несколько лет были выявлены поражения глаз у лиц с данным заболеванием. И только в 1985 году ученые установили причину таких аномалий. Ею стала мутация гена, отвечающего за синтез и строение коллагена IV типа.
Чаще всего именно этот недуг становится причиной тяжелой почечной дисфункции у лиц мужского пола. Женщины могут передать мутантный ген своим детям, не имея клинических проявлений. Синдром манифестирует с первых лет жизни. Но чаще всего обнаруживается у малышей в возрасте 3-8 лет. У больных детей сначала появляются признаки поражения почек. Проблемы со слухом и зрением развиваются несколько позже. В позднем детском и юношеском возрасте формируется тяжелая патология почек, потеря зрения и слуха.
По способу наследования аномалии выделяют 3 формы патологии: Х-сцепленная доминантная, аутосомно-рецессивная, аутосомно-доминантная. Каждой форме соответствуют те или иные морфологические и функциональные изменения внутренних органов. В первом случае развивается классическая форма, при которой воспаление почечной ткани проявляется кровью в моче и сопровождается снижение слуха и зрения. При этом болезнь имеет прогрессивное течение, быстро развивается недостаточность почек. Гистологической особенностью подобных процессов является истончение базальной мембраны. Во втором случае врожденный недуг протекает намного легче и отличается изолированным воспалением почек с гематурией. Аутосомно-доминантная форма также считается доброкачественной, отличается благоприятным прогнозом и проявляется только гематурией или же протекает бессимптомно.

Обнаруживают наследственное воспаление почек случайно, во время профосмотра или диагностического обследования других заболеваний.
Этиология
Истинные этиопатогенетические факторы патологии до сих пор полностью не изучены. Предполагают, что синдром Альпорта — наследственное заболевание, обусловленное мутацией гена, расположенного в длинном плече Х хромосомы и кодирующего белок коллаген IV типа. Основная функция коллагена – обеспечение прочности и эластичности соединительнотканных волокон. При данном синдроме отмечается поражение сосудистой стенки почек, кортиева органа, капсулы хрусталика.
Мутантный ген чаще всего передается от родителей детям. Существует основные формы наследования патологии:
- Доминантный Х-сцепленный тип наследования характеризуется передачей пораженного гена от матери сыну или дочери, а от отца – только дочери. Синдром более тяжело протекает у мальчиков. У больных отцов рождаются здоровые сыновья и больные дочери.
- Аутосомно-рецессивный тип характеризуется получением одного гена от отца, а второго — от матери. Больные дети рождаются в 25% случаев, причем одинаково часто как среди девочек, так и среди мальчиков.
В семье с наследственными заболеваниями мочевыделительной системы вероятность рождения больных детей увеличивается в разы. Если больной ребенок рождается в семье, где все члены имеют идеально здоровые почки, причиной синдрома является спонтанная генетическая мутация.
Факторы, способствующие развитию болезни:
- родственники с почечными патологиями;
- родственные браки;
- сдвиги со стороны иммунной системы;
- снижение слуха в молодом возрасте;
- острые инфекции бактериального или вирусного происхождения;
- вакцинация;
- физическое перенапряжение.
Экспрессия мутантного гена у разных индивидуумов варьируется от слабой до значительной выраженности клинических проявлений наследственного нефрита. Процесс разрушения базальной мембраны находится в непосредственной зависимости от тяжести патологического процесса.
Патогенез
Патогенетические звенья синдрома:
- нарушение биосинтеза коллагена или его дефицит,
- деструкция базальной мембраны почек, внутреннего уха и глазного аппарата,
- прорастание коллагеновых волокон V и VI типов,
- поражение почечных клубочков,
- иммунонегативный гломерулит,
- гиалиноз клубочков, атрофия канальцев и фиброз стромы почек,
- гломерулосклероз,
- скопление в почечной ткани липидов и липофагов,
- снижение в крови уровня Ig A, повышение IgM и G,
- снижение активности Т- и В-лимфоцитов,
- нарушение фильтрационной функции почек,
- дисфункция органа зрения и слуха,
- накопление в крови токсинов и продуктов обмена,
- протеинурия,
- гематурия,
- развитие острой почечной недостаточности,
- смерть.

Заболевание развивается постепенно с ренальных симптомов. На ранних стадиях патологии почки работают полноценно, в моче имеются следы белка, лейкоцитов и крови. Поллакиурия и никтурия сопровождаются гипертензией и другими признаками мочевого синдрома. У больных расширяются чашечки и лоханки почек, возникает аминоацидурия. Спустя некоторое время присоединяется тугоухость неврогенного происхождения.
Мужчины в наибольшей степени подвержены развитию почечной дисфункции. При отсутствии лечения смерть наступает в возрасте 15-30 лет. Женщины обычно страдают скрытой формой патологии с признаками гематурического синдрома и незначительным снижением слуха.
Симптоматика
Наследственный нефрит у детей может протекать по гломерулонефротическому или пиелонефротическому типу. Клинические признаки синдрома Альпорта условно делятся две большие группы – ренальные и экстраренальные.

Основными проявлениями почечной симптоматики являются: гематурия – кровь в моче и протеинурия – белок в моче. Эритроциты в моче у больных детей появляются сразу после рождения. Сначала это бессимптомная микрогематурия. Ближе к 5-7 годам кровь в моче становится отчетливо видна. Это патогномоничный признак синдрома Альпорта. Интенсивность гематурии возрастает после острых инфекционных заболеваний — ОРВИ, ветряной оспы, кори. Активные физические нагрузки и профилактические прививки также могут спровоцировать значительное повышение эритроцитов в крови. Несколько реже у мальчиков развивается протеинурия. У девочек этот симптом обычно отсутствует. Потеря белка с мочой сопровождается отеками, повышением артериального давления, общей интоксикацией организма. Возможна лейкоцитурия без бактериурии, анемия.
Развиваясь, болезнь Альпорта осложняется развитием почечной недостаточности. Ее классические признаки — сухая, желтоватая кожа, снижение тургора, сухость во рту, олигурия, тремор кистей, ломота в мышцах и суставах. При отсутствии правильного лечения возникает терминальная стадия патологии. В таких случаях поможет поддержать жизненные силы организма только гемодиализ. Своевременная заместительная терапия или пересадка больной почки позволяют продлить жизнь больным.
К внепочечным симптомам относятся:
- тугоухость, обусловленная невритом слухового нерва;
- ухудшение зрения, связанное с катарактой, изменением формы хрусталика, появлением белых или желтых вкраплений на сетчатке в районе макулы, миопией, кератоконусом;
- задержка в психофизическом развитии;
- врожденные дефекты – высокое небо, синдактилия, эпикант, деформация ушей, патологии прикуса;
- лейомиоматоз пищевода, трахеи, бронхов.
К неспецифическим общеинтоксикационным признакам патологии относятся:
- головная боль,
- миалгия,
- головокружение,
- резкие колебания артериального давления,
- одышка,
- частое, поверхностное дыхание,
- шум в ушах,
- бледность кожи,
- частые позывы к мочеиспусканию,
- диспепсия,
- ухудшение аппетита,
- нарушение режима сна и бодрствования,
- зуд кожи,
- судороги,
- боль в груди,
- спутанность сознания.
У больных развивается компенсированная клубочковая и канальцевая недостаточность, нарушается транспорт аминокислот и электролитов, концентрационная способность почек, ацидогенез, поражается система канальцев нефрона. По мере прогрессирования патологии признаки мочевого синдрома дополняются выраженной интоксикацией, астенизацией и анемизацией организма. Подобные процессы развиваются у мальчиков, имеющих пораженный ген. У девочек заболевание протекает намного легче, стойкая дисфункция почек у них не развивается. Только во время беременности девушки страдают от симптомов недуга.
Осложнения синдрома Альпорта развиваются при отсутствии адекватной терапии. У больных нарастают признаки недостаточности почек: появляются отеки на лице и конечностях, гипотермия, охриплость, олигурия или анурия. Часто присоединяется вторичная бактериальная инфекция – развивается пиелонефрит или гнойный отит. В таком случае прогноз неблагоприятный.
Диагностика

Диагностикой и лечением синдрома Альпорта занимаются педиатры, нефрологи, генетики, ЛОР-врачи, офтальмологи.
Диагностические мероприятия начинаются со сбора анамнеза и выслушивания жалоб больного. Особое значение имеет семейный анамнез. Специалисты выясняют, имелись ли случаи гематурии или протеинурии у родственников, а также случаи смерти от почечной дисфункции. Для постановки диагноза важны данные генеалогического анализа и акушерского анамнеза.
- Специфическое поражение базальной мембраны у больных обнаруживают по результатам биопсии.
- В общем анализе мочи — эритроциты, белок, лейкоциты.
- Генетическое исследование – выявление мутации генов.
- Аудиометрия обнаруживает нарушения слуха.
- Обследование у офтальмолога позволяет выявить врожденную патологию зрения.
- Ультразвуковое исследование почек и мочеточников, магнитно-резонансная томография, рентген и сцинтиграфия — дополнительные диагностические методики.
Лечение
Синдром Альпорта — неизлечимое заболевание. Замедлить развитие почечной недостаточности помогут следующие рекомендации специалистов:
- Рациональное и витаминизированное питание,
- Оптимальные физические нагрузи,
- Частые и длительные прогулки на свежем воздухе,
- Санация очагов хронической инфекции,
- Профилактика инфекционных заболеваний,
- Запрет на стандартные прививки больным детям,
- Фитосбор из крапивы, тысячелистника и черноплодной рябины показан больным детям с гематурией,
- Витаминотерапия и биостимуляторы для улучшения обмена веществ.
Правильное питание заключается в употреблении легкоусвояемых продуктов с достаточным содержанием основных нутриентов. Из рациона больных следует исключить солености и копчености, пряные и острые блюда, алкоголь, продукты с искусственными красителями, стабилизаторами, ароматизаторами. В случае нарушения функций почек необходимо ограничить потребление фосфора и кальция. Подобные рекомендации следует соблюдать больным в течение всей жизни.

Медикаментозная симптоматическая терапия:
- Для устранения гипертензии назначают ингибиторы АПФ – «Каптоприл», «Лизиноприл» и блокаторы рецепторов ангиотензина – «Лориста», «Вазотенз».
- Пиелонефрит развивается в результате присоединения инфекции. В таком случае применяют антибактериальные и противовоспалительные медикаменты.
- Для коррекции нарушений водно-электролитного обмена назначают «Фуросемид», «Верошпирон», внутривенно физраствор, глюкозу, кальция глюконат.
- Анаболические гормоны и железосодержащие препараты показаны для ускоренного образования эритроцитов.
- Иммуномодулирующая терапия – «Левамизол».
- Антигистаминные препараты – «Зиртек», «Цетрин», «Супрастин».
- Комплекс витаминов и лекарств, улучшающих обмен веществ.
Гипербарическая оксигенация оказывает положительный эффект на выраженность гематурии и функционирование почек. При переходе почечной недостаточности в терминальную стадию требуется гемодиализ и пересадка почки. Оперативное вмешательство проводится после достижения больными пятнадцатилетнего возраста. Рецидив заболевания в трансплантате не отмечается. В отдельных случаях возможно развитие нефрита.
Генотерапия синдрома в настоящее время активно разрабатывается. Ее основная цель – предупреждение и замедление ухудшения функционирования почек. Этот перспективный вариант лечения сегодня внедряется в лечебную практику западными медицинскими лабораториями.
Прогноз и профилактика
Синдром Альпорта — наследственное заболевание, предупредить появление которого просто невозможно. Соблюдение всех предписаний врача и ведение здорового образа жизни помогут улучшить общее состояние больных.
Прогноз синдрома считается благоприятным, если у больных обнаруживается гематурия без протеинурии и тугоухости. Почечная недостаточность не развивается также у женщин без поражения слухового анализатора. Даже при наличии стойкой микрогематурии заболевание у них практически не прогрессирует и не ухудшает общего состояния больных.
Наследственный нефрит в сочетании с быстрым развитием почечной недостаточности имеет неблагоприятный прогноз у мальчиков. У них рано развиваются дисфункции почек, глаз и ушей. При отсутствии своевременного и грамотного лечения больные погибают в возрасте 20-30 лет.
Синдром Альпорта – опасное заболевание, которое без оказания квалифицированной медицинской помощи ухудшает качество жизни пациентов и заканчивается их смертью. Чтобы облегчить течение наследственного нефрита, необходимо неукоснительно соблюдать все врачебные рекомендации.
Видео: лекция по синдрому Альпорта
Источник
