Шерешевского тернера синдром частота встречаемости

Синдром Шерешевского–Тернера обусловлен полной или частичной X-моносомией, представленной во всех или в части клеток организма.
Частота встречаемости синдрома Шерешевского–Тернера 1:2000 – 1:2500 новорожденных девочек. Она отражает незначительную часть X-хромосомных аномалий, имеющихся у плода; по данным литературы, только около 1% эмбрионов с кариотипом 45,X достигают стадии зрелого плода, около 10% случаев невынашиваемости связаны с 45,X-моносомией (J. G. Hall et al., 1990 и A. Robinson, 1990).
Цитогенетические нарушения при синдроме Шерешевского–Тернера связаны в большинстве случаев с моносомией 45X. Отмечаются и мозаичные варианты хромосомных аномалий (45XO/46XX, 45XO/46XY), структурные аномалии X-хромосомы: изохромосома Х (Хi), кольцевая Х-хромосома (rX), делеция короткого плеча Х-хромосомы (Хр-), делеция длинного плеча Х-хромосомы (Хq-).
Основные клинические проявления заболевания – низкорослость (рост, как правило, не достигает 150 см) и гипергонадотропный гипогонадизм. Отмечаются склонность к сердечно-сосудистым нарушениям (в частности, коарктация аорты), различные заболевания почек, гастроинтестинальная патология. Примерно у 30% больных при рождении имеется лимфатический отек верхних и нижних конечностей. У пациентов с синдромом Шерешевского–Тернера вторичное оволосение развивается спонтанно под влиянием надпочечниковых андрогенов к 12–13 годам. Наружные половые органы инфантильные (иногда с гипертрофией клитора), внутренние половые органы сформированы обычно правильно, но при дефиците половых стероидов, отсутствии гормональной стимуляции они остаются инфантильными. Молочные железы развиты слабо.
По данным литературы, у 5–7% девочек-подростков с синдромом Шерешевского–Тернера (преимущественно с мозаичным вариантом) отмечается спонтанный пубертат. Спонтанные беременности развиваются менее чем у 5% пациенток и сопряжены с высоким риском потери плода.
Данные различных исследований показывают, что больные с синдромом Шерешевского–Тернера имеют высокий риск развития аутоиммунных заболеваний щитовидной железы, повышающийся при наличии изо-Х-хромосомы.
Нарушения толерантности к глюкозе, гиперинсулинемия, ожирение, дислипидемия, гипертензия, по данным авторов, отмечаются с высокой частотой у подростков.
В настоящее время большое внимание уделяется изучению остеопенического синдрома у больных с синдромом Шерешевского–Тернера. Согласно гистологическим данным, дефицит костной массы при синдроме Шерешевского–Тернера связан с ускоренным костным обменом, что подтверждается с помощью маркеров костного метаболизма. Сочетание синдрома Шерешевского–Тернера с целиакией, по данным литературы, встречается у новорожденных девочек с частотой 1:250 – 1:500.
Настоящее клиническое наблюдение отражает особенности течения данного заболевания, несвоевременность постановки правильного диагноза, что может помочь практикующим врачам эндокринологического, нефрологического, гастроэнтерологического и ортопедического профилей, встречающихся с данной патологией; выявить заболевание в раннем детском возрасте и провести своевременную адекватную терапию. Приводим наше наблюдение.
Пациентка Н. 05.04.1997 г. р. (13 лет), проживающая на момент осмотра в г. Минске, обратилась за консультацией в городской детский эндокринологический центр с жалобами на низкий рост, избыточную массу тела, постоянные тупые боли в области мезогастрия, усиливающиеся при физической нагрузке, подъеме тяжестей, стрессовых ситуациях, повышенную утомляемость, слабость. Больная направлена межрайонным детским гастроэнтерологическим кабинетом с диагнозом: низкорослость, хронический гастрит, хронический дуоденит с эрозиями луковицы 12-перстной кишки, период ремиссии.
Анамнез жизни. Девочка от первой беременности (39–40 нед.), первых срочных родов в головном предлежании, осложненных разрывом шейки матки I ст. Послеродовый период: без особенностей. Неоднократное антенатальное ультразвуковое исследование (УЗИ) отклонений со стороны плода не отмечает. Вес ребенка при рождении 2770 г, рост 47,0 см. Оценка по шкале Апгар 7/8 баллов; кефалогематома правой теменной области, гипербилирубинемия. Пуповинный остаток отпал на 5-е сут. Период ранней адаптации – удовлетворительный. Раннее нервно-психическое развитие – без особенностей. Грудное вскармливание – до 4 месяцев. Перенесенные заболевания: гипохромная анемия средней степени тяжести, инфекция мочевыводящих путей, рецидивирующий ларинготрахеит, хронический тонзиллит, хронический гастродуоденит с эрозиями луковицы двенадцатиперстной кишки.
Наследственность: бабушка (по материнской линии) – артериальная гипертензия, сахарный диабет 2-го типа.
Социальный анамнез. Семья неполная: мать, 36 лет, образование – среднее специальное.
При сборе анамнеза заболевания мама ребенка указала на то, что считает ее больной с 6 месяцев, когда после перенесенной острой респираторной инфекции появились беспричинная рвота, стойкие изменения лабораторных показателей со стороны крови и мочи в виде анемии средней степени тяжести, лейкоцитурии, умеренной протеинурии.
Впервые на осмотр к эндокринологу с жалобой на низкий рост обратились в 8 лет.
Находилась на стационарном лечении и обследовании в отделении гастроэнтерологии 3-й городской детской клинической больницы с 17.03.2010 по 01.04.2010 г. с жалобами на постоянную тупую боль в животе, не связанную с приемом пищи, периодически возникающую боль во время акта дефекации.
Данные лабораторно-инструментального обследования. Общий анализ крови от 17.03.2010: эритроциты – 4,99, Нb – 137, Нt – 43,6, тромбоциты – 314, лейкоциты – 8,5, палочкоядерные – 3, сегментоядерные – 61, эозинофилы – 1, лимфоциты – 33, моноциты – 2, СОЭ – 15 мм/ч.
Общий анализ мочи от 18.03.2010: цвет – с/ж, прозрачный, удельный вес 1014, рH – кислая, б. – отр., сах. – отр., э – 2–3, л. – 1–2, бакт. – +.
Биохимический анализ крови от 18.03.2010: общ. белок – 69,4; билирубин общ. – 13,6; прямой – 4,4; непрямой – 9,2; глюкоза – 5,0; щелочная фосфатаза – 115; АСТ – 24; АЛТ – 33; γ-глутаминтранспептидаза – 14, α-амилаза – 157; холестерин общий – 5,2; триглицериды – 1,67.
Кровь на маркеры гепатита от 23.03.2010 – отриц.
Копрограмма от 19.03.2010: мышечные волокна+, непереваримая клетчатка+.
Кал на я/г от 19.03.2010 – отр.
Энтеробиоз от 18.03.2010 – отр.
УЗИ органов брюшной полости от 18.03.2010. Печень: размеры – увеличены, контуры – ровные, четкие. Эхогенность снижена диффузно равномерно. Структура однородная. Желчный пузырь: изогнут, расположение типичное, по задней стенке сладж, дающий мощную акустическую тень, стенки плотные. Общий желчный проток не расширен. Портальная вена 8 мм. Поджелудочная железа: расположена типично, форма подковообразная, контуры четкие, ровные. Лоцируется: головка 18 мм, тело 10 мм, хвост 20 мм. Структура однородная, эхогенность повышена (+). Вирсунгов проток – норма. Селезенка: размеры: 107 × 59 мм, форма серповидная, контуры четкие, ровные, структура однородная. Почки: правая – 93 × 35 × 12 мм, левая – 100 × 46 × 17 мм. Размеры – норма. Положение типичное, контуры четкие, ровные. Надпочечники: не визуализируются. Мочевой пузырь: не заполнен. Особенности: желудок и 12-перстная кишка с гиперсекрецией натощак.
Фиброгастродуоденоскопия от 17.03.2010 г.: эритематозная гастропатия легкой степени. Дуоденопатия умеренной степени с эрозиями. Биопсия: хр. атрофический дуоденит с межэпителиальными лимфоцитами. Морфологическая картина соответствует целиакии, стадия Marsh 3c (№ 235/34 от 31.03.2010 г.).
УЗИ органов малого таза при трансабдоминальном исследовании. Матка: лоцируется в виде тяжа размером 30 × 14 × 5 мм, по эхогенности сопоставимого с мышечной тканью, отсутствует дифференцировка на тело и шейку, с отсутствием угла между ними. Эндометрий не лоцируется. УЗИ-признаки рудиментарной матки. Яичники. Визуализировать яичники не удалось в связи с гиперпневматизацией кишечника. Мочевой пузырь заполнен. Взят кариотип по месту жительства (45 Х0, № 1289 от 05.03.2010 г.)
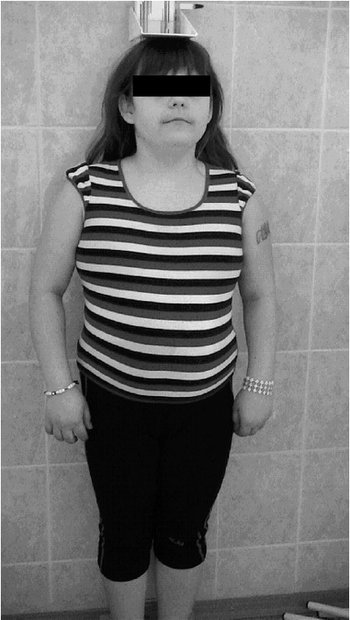
Рис. 1. Телосложение гиперстеническое, широкая грудная клетка.
Пациентка для дообследования направлена во 2-ю детскую клиническую больницу. При осмотре состояние удовлетворительное. Телосложение гиперстеническое, широкая грудная клетка (рис. 1), короткая шея, низкий рост волос на шее с линией роста, направленной вверх, низко расположенные ушные раковины (рис. 2), эпикантус, микрогнатия, «готическое» нёбо.

Рис. 2. Короткая шея, низкий рост волос на шее с линией роста, направленной вверх, низко расположенные ушные раковины.
Антропометрические данные: рост – 134,0 см, вес – 47,0 кг, индекс массы тела – 26,1 кг/м2 (рис. 3). Рост матери – 156,0 см, рост отца – 175,0 см. Генетический рост – 159,25 см. Коэффициент стандартного отклонения (SDS) роста: –3,0. Скорость роста – 4 см/год. SDS скорости роста: –3,26. Костный возраст – 11,8 лет (R-грамма № 1245 от 04.04.2010 г.) Хронологический возраст – 12,99 лет.

Рис. 3. Рост 134 см.
На рис. 4 представлены перцентильные кривые роста и веса девочки.
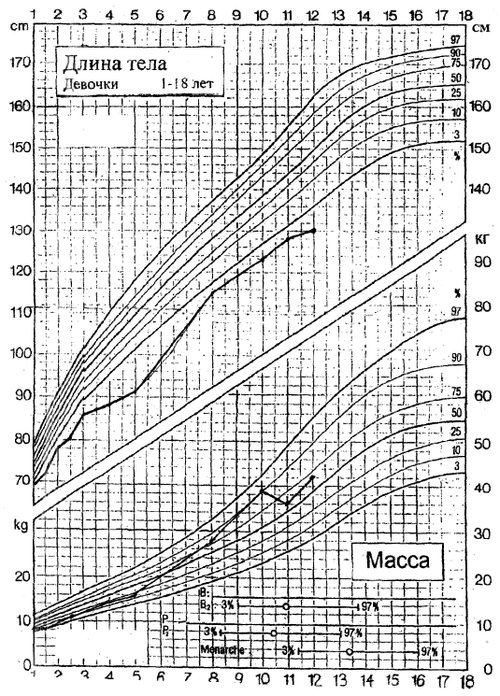
Рис. 4. Перцентильные кривые веса и роста девочки.
Фенотип женский. Кожа смуглая, множественные пигментные невусы, видимые слизистые оболочки розовые, язык обложен белым налетом у основания. Подкожная жировая клетчатка развита чрезмерно, распределена равномерно. Отеков нет, умеренная пастозность в области лица и голеней.
Щитовидная железа не увеличена, однородная, эластичная, перешеек подвижный, безболезненный.
Электрокардиограмма: ЧСС – 77 уд./мин, ритм синусовый, вертикальное положение электрической оси сердца.
Аускультативно со стороны сердца: тоны ритмичные, громкие; систолический шум в области верхушки сердца.
УЗИ сердца: ПМК I степени, R0-1. Дополнительная хорда левого желудочка.
Костно-мышечная система без видимых деформаций; укорочение 4-го и 5-го пальцев кистей рук и гипоплазия ногтей (рис. 5).

Рис. 5. Укорочение 4-го и 5-го пальцев кистей рук и гипоплазия ногтей.
Органы дыхания: перкуторно звук ясный, дыхание везикулярное, хрипов нет.
Половое развитие по Таннеру: Ах1Р1Ма1Меabs.
Результаты гормонального анализа крови от 07.06.2010 г.: фолликулостимулирующий гормон – 93,9 мМЕ/мл (норма 1,8–10,5 (фолликулиновая фаза), лютеинизирующий гормон –
32,9 мМЕ/мл (1,0–10,0), дегидроэпиандростерон – 170,0 мкг/дл (20–263), кортизол – 606,5 нмоль/л (55–690), иммунореактивный инсулин – 12,4 мкЕД/л (8,2–24,8), тиреотропный гормон 2,52 (0,3–5,0), свободный тироксин – 15,9 пмоль/л (11,0–23,0).
Данные биохимического анализа крови: гиперхолестеринемия – 6,3 ммоль/л.
Результаты орального глюкозотолерантного теста через 60 и 120 мин. после нагрузки 75 г сухой глюкозы, предварительно разведенной в 250 мл воды: глюкоза натощак и через 60 и 120 мин. после нагрузки – 4,7; 9,4; 6,6 ммоль/л соответственно.
Стимуляционные пробы на соматотропный гормон с инсулином от 14.06.2010 г.: 0 мин. – 0,1; 15 мин. – 0,1; 30 мин. – 0,3; 45 мин. – 6,2; 60 мин. – 8,2; 90 мин. – 2,0; 120 мин. – 1,4 (< 10); с клофелином от 15.06.2010: 0 мин. – 0,3; 30 мин. – 1,4; 60 мин. – 5,1; 90 мин. – 2,3; 120 мин. – 2,0; 150 мин. – 0,5 (< 10).
На основании анамнеза, клинической картины, данных лабораторных и инструментальных методов исследования установлен диагноз «синдром Шерешевского–Тернера (45 Х0). Гипергонадотропный гипогонадизм. Генитальный инфантилизм. Дефицит гормона роста относительный. Целиакия, атипичная форма, активная стадия. Хронический поверхностный гастрит, вне обострения. Гиперхолестеринемия».
В данной статье представлен случай поздней диагностики синдрома Шерешевского–Тернера, при котором имеется одновременно сопутствующая соматическая патология, требующая коррекции. Ранняя диагностика нарушений, своевременное и полноценное обследование и наблюдение могут обеспечить девушкам с синдромом Шерешевского–Тернера полноценную жизнь.
(Григоренко Ю. А., Солнцева А. В., Сукало А. В. Белорусский государственный медицинский университет; Городской детский эндокринологический центр, г. Минск.
Опубликовано: «Медицинская панорама» № 8, ноябрь 2010).
Источник
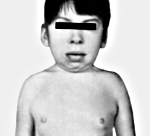
Синдром Шерешевского-Тёрнера — хромосомная патология, обусловленная частичной или полной Х-моносомией. Клиническими признаками синдрома Шерешевского-Тёрнера служат низкорослость, гипогонадизм, пороки развития (ВПС, подковообразая почка, косоглазие и др.), лимфостаз, деформация суставов, крыловидные складки кожи на шее и др. Решающими аргументами в постановке диагноза синдрома Шерешевского-Тёрнера служат характерные клинические особенности, данные исследования полового хроматина и кариотипа; возможна дородовая диагностика патологии у плода. Больные с синдромом Шерешевского-Тёрнера нуждаются в гормональной терапии (гормоном роста, половыми гормонами), коррекции врожденных пороков развития и эстетических недостатков.
Общие сведения
Синдром Шерешевского-Тёрнера — генетически детерминированная первичная дисгенезия гонад, развивающаяся вследствие нарушения половой Х-хромосомы. С синдромом Шерешевского-Тёрнера рождается 1 из 3000 новорожденных, однако истинная популяционная частота заболевания неизвестна, поскольку нередко происходит самопроизвольное прерывание беременности на ранних сроках. В литературе данное заболевание встречается под различными названиями — синдром Шерешевского-Тёрнера, синдром Шерешевского, синдром Тёрнера, синдром Ульриха-Тёрнера – по имени авторов, внесших свой вклад в изучение патологии. Синдром Тёрнера в подавляющем большинстве случаев встречается у девочек, крайне редко наблюдается у мальчиков.
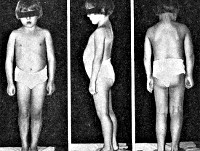
Синдром Шерешевского-Тёрнера
Причины синдрома Шерешевского-Тёрнера
В основе развития синдрома Шерешевского-Тёрнера лежит структурная или количественная аномалия Х-хромосомы. Более чем в 60% случаев наблюдается полная моносомия по Х-хромосоме (кариотип 45,Х0), т. е. отсутствие второй половой хромосомы. Около 20% случаев синдрома Шерешевского-Тёрнера обусловлены структурными перестройками Х-хромосомы: делецией короткого или длинного плеча, изохромососмой Х по длинному или короткому плечу, транслокацией Х/Х, кольцевой Х-хромосомой и пр. В оставшихся 20% цитогенетических вариантах имеет место мозаицизм (45,Х0/46,ХХ; 45,X0/46,XY и др.). Механизм возникновения синдрома Шерешевского-Тёрнера у мужчин объясняется транслокацией или хромосомным мозаицизмом.
Риск развития у плода синдрома Шерешевского-Тёрнера никак не связан с возрастом матери. Истинными причинами количественных, качественных или структурных аномалий Х-хромосомы является нарушение мейотического расхождения хромосом, приводящее к анеуплоидии (при Х-моносомии), либо нарушение дробления зиготы (при хромосомном мозаицизме). Практически во всех случаях при кариотипе 45,Х0 имеет место утрата отцовской Х-хромосомы.
Отсутствие или структурные дефекты половой X-хромосомы вызывают нарушение формирования половых желез и многочисленные пороки внутриутробного развития. Беременность плодом, имеющим синдром Шерешевского-Тёрнера, обычно сопровождается токсикозом, угрозой выкидыша и преждевременных родов.
Симптомы синдрома Шерешевского-Тёрнера
Дети с синдромом Шерешевского-Тёрнера могут рождаться недоношенными, однако даже в случае доношенной беременности росто-весовые показатели ребенка нередко снижены (масса тела 2500—2800 г, длина 42-48 см). Уже при рождении у ребенка могут быть обнаружены типичные признаки синдрома Шерешевского-Тёрнера: короткая шея со складками кожи по бокам (птеригиум-синдром), врожденные пороки сердца, лимфостаз, отечность стоп и кистей и др. В период новорожденности таким детям свойственно нарушение сосания, моторное беспокойство, частые срыгивания фонтаном. В раннем возрасте дети с синдромом Шерешевского-Тёрнера отличаются отставанием в физическом развитии, задержкой речевого развития, частыми повторными средними отитами, приводящими к кондуктивной тугоухости.
К моменту пубертатного периода рост больных составляет 130-145 см. Кроме низкорослости, типичный внешний вид характеризуется короткой шеей с крыловидными складками, «лицом сфинкса», низкой границей роста волос, микрогнатией, деформацией ушных раковин, широкой грудной клеткой. Изменения костно-суставной системы у больных с синдромом Шерешевского-Тёрнера могут быть представлены врожденной дисплазией тазобедренных суставов, девиацией локтевых суставов, сколиозом. Ранее развитие остеопророза вследствие дефицита эстрогенов обусловливает высокую частоту переломов костей запястий, позвоночника, шейки бедра. Нарушения черепно-лицевого скелета включают микрогнатию, высокое готическое нёбо, аномалии прикуса.
Наиболее частыми сердечно-сосудистыми пороками, сопровождающими синдром Шерешевского-Тёрнера, служат ДМЖП, открытый артериальный проток, коарктация аорты, аневризма аорты. Со стороны мочевыделительной системы у больных может отмечаться наличие подковообразной почки, удвоение лоханок, стеноз почечных артерий, приводящий к артериальной гипертензии. Нарушения развития зрительной системы при синдроме Шерешевского-Тёрнера в большинстве случаев представлены птозом, косоглазием, близорукостью, дальтонизмом.
Интеллект, как правило, сохранен; в редких случаях отмечается олигофрения. Среди сопутствующих заболеваний у лиц с синдромом Шерешевского-Тёрнера обычно выявляются гипотиреоз, тиреоидит Хашимото, витилиго, множественные пигментные невусы, алопеция, гипертрихоз, сахарный диабет 1-го и 2-го типа, целиакия, ожирение, ИБС. У больных с синдромом Шерешевского-Тёрнера значительно повышен риск развития рака толстой кишки.
Ведущим признаком синдрома Шерешевского-Тёрнера является первичный гипогонадизм (половой инфантилизм), который выявляется почти у 100% пациенток. Яичники представлены двухсторонними фиброзными тяжами, не содержащими фолликулов; отмечается гипоплазия матки. Иногда встречаются рудиментарные яичники с овариальной стромой и отдельными примордиальными фолликулами. Большие половые губы имеют мошонкообразный вид; малые половые губы, клитор и девственная плева недоразвиты. При синдроме Шерешевского-Тёрнера отмечается первичная аменорея, недоразвитие молочных желез, непигментированные втянутые соски, скудное подмышечное и лобковое оволосение. В подавляющем большинстве случаев женщины с синдромом Шерешевского-Тернера страдают бесплодием, однако при мозаичных вариантах возможно зачатие и вынашивание плода.
У мужчин с синдромом Шерешевского-Тёрнера, кроме характерных внешних признаков и соматических пороков, отмечается гипоплазия яичек, двусторонний крипторхизм, иногда – анорхия, низкий уровень тестостерона.
Диагностика синдрома Шерешевского-Тёрнера
У новорожденных синдром Шерешевского-Тёрнера может быть заподозрен неонатологом или педиатром по наличию крыловидной складки шеи и лимфедемы. При отсутствии явных внешних признаков диагноз нередко устанавливается только в пубертатном периоде на основании низкого роста, отсутствия менархе, невыраженности вторичных половых признаков.
При исследовании уровня гормонов определяется повышение гонадотропинов и снижение эстрогенов в крови. Решающее значение в диагностике синдрома Шерешевского-Тёрнера принадлежит определению полового хроматина и исследованию кариотипа. При обнаружении характерных признаков синдрома Шерешевского-Тёрнера у плода по данным акушерского УЗИ, решается вопрос о проведении инвазивной пренатальной диагностики.
Больные с синдромом Шерешевского-Тёрнера нуждаются в консультации генетика, эндокринолога, кардиолога, кардиохирурга, нефролога, офтальмолога, отоларинголога, лимфолога, гинеколога-эндокринолога (женщины), андролога (мужчины). Для обнаружения врожденных пороков и сопутствующих заболеваний показано выполнение ЭхоКГ, МРТ сердца, ЭКГ, УЗИ почек, рентгенографии позвоночника, денситометрии, рентгенографии костей стоп и кистей и др. В рамках диагностического обследования женщинам проводится гинекологическое исследование, УЗИ органов малого таза; мужчинам – УЗИ мошонки, исследование андрогенного профиля. В случае аномалиях зубных рядов детям необходима консультация ортодонта.
С целью дифференциальной диагностики синдрома Шерешевского-Тёрнера и гипофизарного нанизма необходимо проведение исследования уровня гормонов гипофиза в крови, рентгенографии турецкого седла, электроэнцефалографии.
Лечение синдрома Шерешевского-Тёрнера
Основными задачами лечения пациенток с синдромом Шерешевского-Тёрнера служат стимуляция роста, индукция формирования вторичных половых признаков и регулярного менструального цикла. В раннем детстве лечение неспецифично — массаж, ЛФК, витамины, полноценное питание, охранительный режим.
С целью увеличения конечного роста назначается рекомбинантный гормон роста (соматотропин) в виде ежедневных подкожных инъекций до достижения пациенткой костного возраста 15 лет и уменьшения скорости роста до 2 см в год. В большинстве случаев ростостимулирующая терапия помогает больным вырасти до 150–155 см. Лечение гормоном роста рекомендуется сочетать терапией анаболическими стероидами.
Для имитации нормального полового созревания с 13-14 лет назначается заместительная терапия эстрогенами, а через 12–18 месяцев циклическая терапия эстроген-прогестагеновыми оральными контрацептивами. Заместительная гормонотерапия проводится до возраста естественной менопаузы у здоровых женщин (примерно до 50 лет). Мужчинам с синдромом Шерешевского-Тернера назначается ЗГТ мужскими половыми гормонами.
При гемодинамически значимых ВПС осуществляется их хирургическая коррекция. Устранение крыловидных складок шеи проводится методами пластической хирургии.
При достижении адекватного уровня полового развития женщины с синдромом Шерешевского-Тернера могут иметь детей с помощью ЭКО, используя донорскую яйцеклетку. При наличии кратковременной овариальной активности возможно использование для оплодотворения собственных ооцитов. Проблема избыточного роста волос решается с помощью эпиляции.
Прогноз и профилактика синдроме Шерешевского-Тёрнера
В целом синдром Шерешевского-Тёрнера не оказывает значимого влияния на продолжительность жизни. Исключение составляют случаи тяжелых ВПС, раннего развития и декомпенсации сопутствующих заболеваний. При адекватной терапии больные с синдромом Шерешевского-Тёрнера способны создавать семьи, вести нормальную сексуальную жизнь, однако большая часть из них остается бесплодными.
Учитывая полиморфизм проявлений синдрома Шерешевского-Тёрнера, ведение и наблюдение таких больных осуществляется специалистами в области генетики, педиатрии, эндокринологии, гинекологии, андрологии, урологии, кардиологии, офтальмологии и др.
Единственно возможными методами профилактики рождения ребенка с синдромом Шерешевского-Тёрнера могут служить медико-генетическое консультирование и пренатальная диагностика.
Источник
