Сепсис и синдром системной воспалительной реакции

Синдром системного воспалительного ответа[1] (англ. «systemic inflammatory response syndrome» (SIRS)) — медицинский термин, введённый в 1992 году на конференции Американской коллегии торакальных хирургов (англ. American College of Chest Physicians) и Общества специалистов интенсивной терапии (англ. Society of Critical Care Medicine) в Чикаго[2] для обозначения общей воспалительной реакции организма в ответ на тяжелое поражение, вне зависимости от локализации очага. Процесс идет при участии медиаторов воспаления с вовлечением практически всех систем организма.
Воспалительная реакция организма в ответ на внедрение в организм инфекции, обширные травмы, развития некроза тканей, тяжелые ожоги развивается по одним и тем же общим закономерностям. Эта реакция является приспособительной функцией организма и направлена на уничтожение агента, вызвавшего процесс, и восстановление поврежденной ткани. При легких поражениях воспалительный процесс ограничивается локальными воспалительными изменениями и умеренной, малозаметной общей реакцией органов и систем.
Диагностика[править | править код]
Диагноз синдрома системной воспалительной реакции организма правомочен в случае наличия как минимум двух следующих критериев:
- Температура тела ≥ 38 °C (фебрильная температура) или ≤ 36 °C (гипотермия)
- Частота сердечных сокращений ≥ 90/мин (тахикардия)
- Тахипноэ: частота дыхания ≥ 20/мин или гипервентиляция с содержанием диоксида углерода в крови ≤ 32 mmHg
- Лейкоцитоз (≥ 12000/μl) или лейкопения (≤ 4000/μl) или смещение лейкоцитарной формулы влево.
Комбинация «фебрильная температура+лейкоцитоз» является самой частой для синдрома системной реакции организма на воспаление и соответствует нормальной реакции иммунной системы. В случае «гипотермия+лейкоцитоз», который встречается гораздо реже, говорят о «холодном» синдроме системной реакции организма на воспаление —— подобная реакция организма встречается при иммунодефиците.
Причины[править | править код]
Причинами синдрома системного воспалительного ответа могут быть: сепсис, гипоксия, шок, ожоги, острый панкреатит, обширные хирургические операции, тяжелые травмы и другие тяжелые заболевания. Чаще всего факторы повреждения классифицируют исходя из механизма патологического воздействия:[1]
- Механическое повреждение тканей (примеры: ожоги, синдром длительного сдавления).
- Глобальный недостаток перфузии тканей (примеры: шок, остановка кровообращения).
- Регионарный недостаток перфузии тканей (примеры: тромбоэмболия, травма крупных сосудов).
- Некроз тканей вследствие ишемии (примеры: инфаркт миокарда, острый панкреатит).
- Инфекционный процесс (примеры: иммунодефицит, хирургическая инфекция, инфицированная травма, внутрибольничная инфекция).
- Выброс эндотоксинов (пример: сепсис, вызванный грам-негативными бактериями).
- Невскрытые абсцессы (например, интраабдоминальные).
Примечания[править | править код]
Литература[править | править код]
- М. И. Кузин, О. С. Шкроб, Н. М. Кузин. Синдром системного ответа на воспаление // Хирургические болезни. — 3 издание. — М.: Медицина, 2002. — С. 13-22. — 784 с. — ISBN 5-225-00920-4.
- Определение SIRS (нем.) (недоступная ссылка). Дата обращения 11 февраля 2014. Архивировано 26 июня 2013 года.
- S-2 Рекомендации по профилактике, диагностике, лечению и реабилитации SIRS (нем.) (недоступная ссылка). Deutsche Sepsis Gesellschaft. Дата обращения 11 февраля 2014. Архивировано 1 октября 2010 года.
- R. C. Bone; R. A. Balk; F. B. Cerra; R. P. Dellinger; A. M. Fein; W. A. Knaus; R. M. Schein; W. J. Sibbald. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. The ACCP/SCCM Consensus Conference Committee. American College of Chest Physicians/Society of Critical Care Medicine (англ.) // Chest. — 1992. — Vol. 101, no. 6. — doi:10.1378/chest.101.6.1644.
Источник

СЕПСИС Синдром системной воспалительной реакции. (ССВР)

Встречаемость и экономическая составляющая. • Частота больных с тяжелым сепсисом колеблется от 2 до 18%. • Сепсис является наиболее частой причиной смерти в ОРИТ • В США в 2003 году зарегистрировано 751000 случаев тяжелого • • • сепсиса. Смертность составила 28. 6%. У детей сепсис составляет около 10% У больных старше 85 лет -38, 4%. Количество новых случаев заболевания растет примерно на 1. 5 % в год. (Angus D. C. et al 2001). Септический шок- самая частая причина смерти больных в отделениях реанимации. Только в США в 1993 году отмечено 100000 случаев гибели больных от этого заболевания. Ежегодные затраты на лечение септических больных в США составляют 17 миллиардов и эта сумма продолжает расти. (Quartin A. A. et al 1997).

История вопроса • С древних времен, в античной медицине и в последующие периоды развития медицинской науки, все видные ученые-медики, отмечали ряд заболеваний, протекающих с особой тяжестью и заканчивающихся, как правило смертью. Лечение подобных пациентов всегда считалось делом сложным и неблагодарным, так, как шансы на выздоровления были крайне малы. • Гиппократ описывал подобные состояния так: при начале нагноения страдания и лихорадка происходят больше, чем когда оно уже совершилось. Поты опасны. Проявляющиеся в продолжение критических дней, сильные и быстрые, выходящие на лбу, как капли и ручьи воды, весьма холодные и обильные, ибо по необходимости такой пот происходит с насилием, с чрезмерным страданием и продолжительным изнурением… В лихорадках не перемежающихся, если губа, или нос, или глаз. Или бровь будут искривляться, если больной не будет ни видеть, ни слышать, будучи при этом слабым. То все, что ни было из этих признаков показывает наступлении смерти…( В. И. Руднев перевод с греческого. 1994. )

Этиология наиболее частых причин сепсиса • Escherichia coli (наиболее частый • • • возбудитель), Klebsiella, Enterobacter, Proteus, Pseudomonas, Staphylococcus aureus, Streptococcus pneumoniae.

Определения: • Транзиторная бактериемия – кратковременная бактериемия при проведении инвазивных процедур; • Периодическая бактериемия – повторная инвазия, связанная с попаданием бактерий из области ограниченного гнойного очага; • Постоянная бактериемия – постоянная инвазия микроорганизмов, попадающих в кровоток из неограниченных очагов инфекции (эндокардит, инфицированная аневризма);

Определения 1: • Сепсис – генерализованное воспаление в ответ • • на периодическую или постоянную бактериемию. Одонтогенный сепсис – генерализованное воспаление , при котором входными воротами для возбудителя инфекции служит дефект твердых тканей зуба или зубодесневого прикрепления. Тяжелый сепсис – сепсис с развитием органной дисфункции или недостаточности. Септический (инфекционно-токсический) шок – тяжелый сепсис с развитием стойкой артериальной гипотензии. Полиорганная недостаточность.

• Прорыв в понимании механизмов патогенеза сепсиса произошел в 1991 году, когда в США, в Чикаго на согласительной конференции врачейинтенсивистов и пульмонологов были выработаны критерии получившие названия системной воспалительной реакции (SIRS-systemic inflammatory response syndrome).

• Воспаление — это сформировавшаяся в процессе эволюции защитноприспособительная реакция организма, направленная на локализацию, уничтожение и/или удаление из организма патогенного агента и характеризующаяся явлениями альтерации, экссудации и пролиферации. Патогенетические признаки воспаления • • • Rubor Tumor Calor Dolar Functio laesa.

Патогенное воздействие на организм медиаторов воспаления и провоспалительных цитокинов • Гистамин. Угнетение деятельности синусного узла сердца, • • возможные провокации фибрилляции желудочков. Кинины. Резкое падение артериального давления, коллапс. ФHO альфа. Активизация общего коагуляционного потенциала крови, усиление продукции эндотелиоцитами прокоагулянтных факторов. Интерлейкин 1. Повышение прокоагулянтной активности эндотелия сосудов. Интерлейкин 2. Уменьшение системного сосудистого сопротивления, снижение артериального давления, провокация проявлений сердечной недостаточности. Интерлейкин 12. Стимуляция агрегации тромбоцитов, повышение тромбообразования. Тромбоксан А 2. Ускорение агрегации тромбоцитов, усиление тромбообразования, бронхоспазм и спазм сосудов мозга. Простагландин I 2. Снижение артериального давления за счет мощной вазодилатации.

Патогенное воздействие на организм медиаторов воспаления и провоспалительных цитокинов 1 Если суммировать приведенные данные, то можно сказать, что системное действие основных медиаторов и цитокинов заключается в следующем: • повышение тромбообразования, развитие ДВСсиндрома ; • отрицательные инотропные влияния на сердце, провокации аритмий, вплоть до фибрилляции желудочков; • снижение сосудистого сопротивления, падение артериального давления; • нарушения мозгового кровообращения.

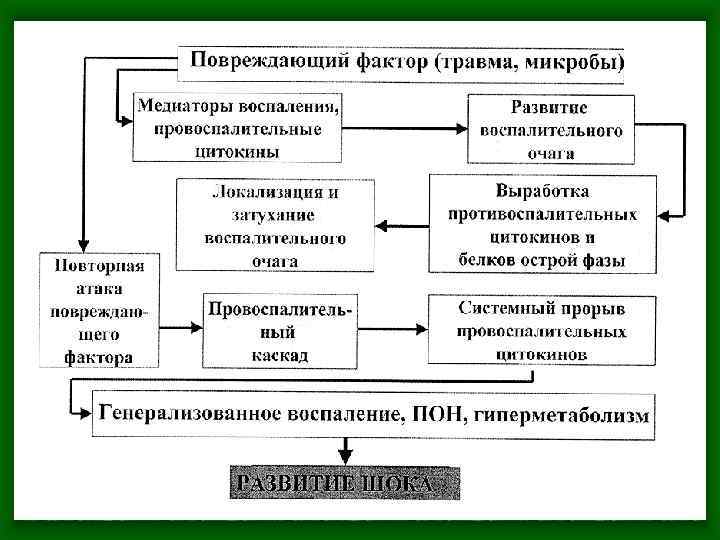
Патогенез сепсиса. • Синонимом сепсиса, в современном представлении является выражение- «медиаторная» буря, или «медиаторный взрыв» . Это говорит о том, что в основе всех патологических реакций лежит неконтролируемый, массивный выброс медиаторов воспаления в системный кроваток. С последующим развитием нарушения перфузии органов и тканей, запуском апоптоза, метаболическим нарушениям на уровне клетки. Развитием ДВС- синдрома. , и. т. д. • Основным индуктором системной воспалительной реакции считается эндотоксин (он же липид «А» ), экзотоксин для грамм+ бактерий и фрагменты клеточной стенки, в частности липополисахарид.

Патогенез сепсиса 1. • Образование этих индукторов происходит в следствии гибели микробной клетки при взаимодействии с клетками иммунной системы ( нормальные киллеры) и/или применении антибиотиков. • Контактируя с лимфоцитами и нейтрофилами (макрофаги, моноциты и базофилы) в системный кроваток осуществляется массивная секреция провоспалительных цитокинов и лейкотриенов. • Последние в свою очередь вызывают воспалительную реакцию в масштабе всего организма, что и приводит к последовательному развитию сепсиса и септического шока.
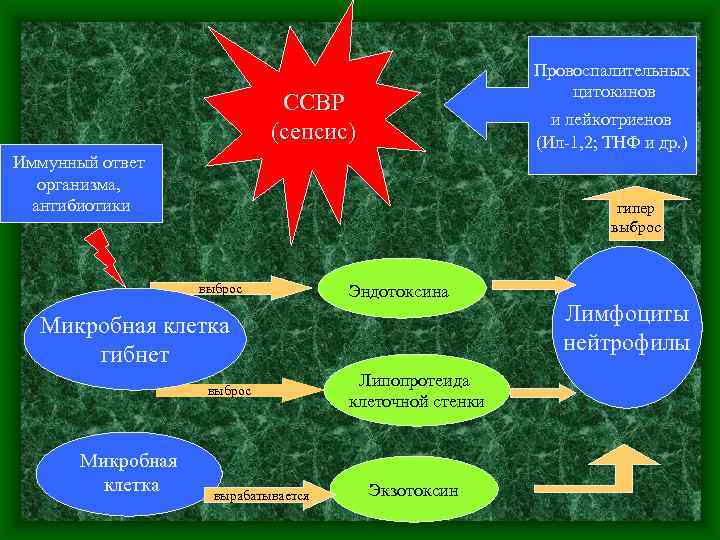
Провоспалительных цитокинов ССВР (сепсис) и лейкотриенов (Ил-1, 2; ТНФ и др. ) Иммунный ответ организма, антибиотики гипер выброс Эндотоксина Микробная клетка гибнет выброс Микробная клетка вырабатывается Липопротеида клеточной стенки Экзотоксин Лимфоциты нейтрофилы

Критерии диагностики синдрома системной воспалительной реакции. № Критерии септического синдрома . Клинические признаки инфекции Температура тела выше 38 о С или ниже 36 о С 1 Частота дыхания > 20 в минуту или РСо 2 ниже 2 35 Число сердечных сокращений > 90 в минуту 3 Количество лейкоцитов больше 12, 0 х109/л или 9 4 меньше 4, 0 х10 /л или при 10% незрелых форм • Сепсис был квалифицирован, как синдром системной воспалительной реакции и подтвержденного инфекционного очага. Наличия инфекционного заболевания или наличие бактериемии. Причем последние не обязательно. • Сам сепсис был представлен несколькими патологическими состояниями следующими друг за другом:

Стадии шока: • А- компенсированный (гипердинамическая фаза, артериальное давление стабильное, имеется умеренная тахикардия. Повышен сердечный выброс. Кожа теплая. Одышки нет. Метаболический алкалоз. • Б– субкомпенсированный- гемодинамика стабильная. Отмечается выраженная тахикардия, появляется одышка смешанного типа. Конечности холодные (нарушение периферического кровообращения), дыхательный алкалоз и метаболический ацидоз, больной возбужден. Олигоурия( диурез менее 30 мл/час).

Стадии шока 1: • В-декомпенсированный – гиподинамическая фаза. Гипотензия ( А/Д ниже 80/60), тахикардия с переходом в брадикардию. Патологические виды дыхания (Чейн. Стокса, Биота. ) Грубый метаболический кетоацидоз. Энцефалопатия (неадекватное отношение к своему состоянию, психомоторное возбуждение, или заторможенность). Холодный липкий пот, спавшиеся вены на конечностях, нитевидный пульс или его отсутствие на периферии. Анурия. • Г- рефрактерный – отсутствие реакции на вазопрессоры, прогрессирующая гипотензия, аритмии, клиническая смерть. • По течению шок может проявляться в виде молниеносного, острого и подострого. Вариант течения связан с реактивностью иммунной системы.

Факторы риска развития сепсиса. • 1 — Возраст (менее года, недоношенность, старше 80 лет) • 2 — Ожоги, травмы. • 3 — Длительное использование инвазивных методик • • диагностики и лечения. 4 — применение химио и иммуносупрессивных препаратов. 5 — Недостаточное питание. 6 — СПИД. 7 — Генетическая предрасположенность.

Диагностика • • Диагностика сепсиса базируется на основании тех же принципов и подходов, что и любое другое заболевание, т. е. на: • анамнезе • клинико-лабораторных данных • дополнительных методах обследования • а так же зачастую на интуитивных ощущениях врача, которые в условиях неясности диагноза, недостаточности клинических данных и множества различных сопутствующих заболеваний, порою позволяют заподозрить септическое состояние.

Диагностика 1 • Диагностика инфекционного очага. — этот момент в диагностики сепсиса является чуть ли не основным для большинства практикующих врачей. В этой связи в первую очередь важен анамнез, при его сборе выясняется не только возможные инфекционные заболевания, но и хронические очаги инфекции. Транслокация из которых возможна при воздействии какого либо стресса, возможно не инфекционного характера. В это же время выясняется наличие каких либо перенесенных операций, длительного лечения с применением гормональных или иммуносупрессивных препаратов. • При отсутствии явного бактериального очага рекомендуется скрининговое обследование всех органов и систем, с прицельным посевом крови, мочи и других возможных источников инфекции, посевы со слизистых. Все посевы делаются через 24 часа подряд, желательно на пике лихорадки. Дополнительные методы обследования ( УЗИ, рентген, гастро и колоноскопия, другие методы исследования).

Диагностика 2 • В настоящее время явным фаворитом в ранней диагностики сепсиса является исследование уровня и нарастание титра прокальцитонина. Этот маркер относится к стресс-белку, концентрация которого в сыворотке крови прямо коррелирует с прогрессированием ССВР. Причем в проведенных исследованиях доказано, что чувствительность этого метода составляет 96% а специфичность 92 % В настоящий момент более чувствительных методов нет.

Терапия. • Основными направлениями интенсивной терапии больных с • • • сепсисом являются: — ранняя диагностика и санация инфекционного очага. -адекватный выбор антибактериальных средств. — торможение гиперергической реакции организма на инфекцию -гемодинамическая поддержка с учетом стадий шока. — адекватная респираторная поддержка. А также диагностика и коррекция респираторного дистресс-синдрома. -кишечная деконтаминация. Коррекция эндотоксикоза и профилактика полиорганной недостаточности. — коррекция ДВС- синдрома. — подавление активности медиаторов септического шока. Лечение сепсиса, на каждом этапе его течения складывается прежде всего из основных патогенетических моментов.

Терапия 1 • Санация первичного очага воспаления должна быть произведена как • • • можно раньше и радикальнее. При выборе антибактериальных средств необходимо пользоваться следующими правилами: если терапия эмпирическая, то антибиотик должен быть максимально широкого спектра, хорошо проникать в органы и ткани предполагаемого инфекционного очага, быть минимально токсичным, быстро выводится, сочетаться с другими лечебными средствами. Доза препарата должна быть максимальной. Длительность применения не менее 7 дней. Торможение гиперергической воспалительной реакции: Применение кортикостероидов и иммуноглобулинов. Различные виды афереза, использование ионообменных смол. Инфузионная терапия выполняет две принципиальные задачи: 1 — восполнение ОЦК. Обеспечение ударного объема и поддержание микроциркуляции. 2 — Повышение метаболической активности клетки. Механическое разведение концентрации токсинов. Увеличение диуреза.

Спасибо за внимание!
Источник
Понятие «синдром системной воспалительной реакции» лишь немногим более 10 лет используется в медицинской науке и практике для обозначения общих изменений в организме, возникающих под влиянием различных повреждающих факторов.
Системная воспалительная реакция — патогенетическая и клинико-физиологическая основа различных патологических процессов и заболеваний хирургического, инфекционного, онкологического, гематологического и другого характера.
Термин «сепсис» в значении, близком к современному, использовался ещё в VIII—VII веках до н.э. в «Илиаде» Гомера.
Великий врач древности Гиппократ словом «сепсис» описывал процесс распада тканей, сопровождающихся гниением, болезнью и смертью.
Многовековое учение о сепсисе завершилось в последние десятилетия пониманием, что в основе этого патологического процесса лежит универсальный ответ организма на повреждение — системная воспалительная реакция.
Достижения фундаментальных наук и практической медицины позволили прийти к заключению, что в основе реакции макроорганизма на любые повреждающие факторы механической, химической и биологической природы лежат активация и выброс различных клеточных, внеклеточных и органных медиаторов. Эта реакция в зависимости от интенсивности повреждающего действия может носить генерализованный, системный характер.
Пусковую роль при этом играют гуморальные факторы и медиаторы, определяющие развитие воспалительной реакции.
Такой генерализованный ответ макроорганизма на повреждение получил название системной воспалительной реакции.
Концепция системной воспалительной реакции прочно вошла в клиническую медицину для описания патофизиологических сдвигов в ответ на повреждающее действие нижеследующих факторов:
- инфекция (бактериальная, вирусная, грибковая, паразитарная);
- травма, в том числе хирургическая;
- неадекватная анестезия;
- ожоги;
- ишемия;
- панкреатит;
- лекарственная реакция;
- аутоиммунные процессы;
- гипоксия.
Гуморальные факторы системной воспалительной реакции включают практически все известные эндогенные биологически активные субстанции — цитокины, ферменты, гормоны, продукты и регуляторы метаболизма (всего более 200 биологически активных веществ).
Основные эндогенные медиаторы системной воспалительной реакции:
— Про- и противовоспалительные цитокины
- фактор некроза опухоли (TNFa);
- интерлейкины (ИЛ) 1, 2, 4, 6, 8, 10
— Фактор активации тромбоцитов (PAF)
— Эйксаноиды:
- лейкотриены;
- тромбоксан;
- простагландины
— Интерферон-у
— Колониестимулирующий фактор гранулоцитов-макрофагов
— Оксид азота
— Эндотелии
— Фрагменты комплемента СЗа, С5а
— Продукты полиморфноядерных клеток:
- токсические радикалы кислорода
- протеолитические ферменты
— Молекулы адгезии
— Фактор проницаемости сосудов
— Кинины
— Факторы коагуляции
— Эндорфины
— Тканевые гормоны
— Основные регуляторные гормоны
Гиперпродукция этих веществ, дисбаланс их активности на регионарных и системных уровнях быстро приводят к повреждению эндотелия и органной дисфункции, проявляющейся синдромом полиорганной недостаточности.
Как известно, воспаление — комплексная сосудисто-тканевая защитно-приспособительная реакция организма на действие патогенного раздражителя (повреждающего фактора). В зависимости от интенсивности действия повреждающего фактора и состояния макроорганизма эта реакция может носить как локальный, так и генерализованный характер.
Проявлениями местной воспалительной реакции являются 5 основных признаков, описанных ещё классиками древней медицины А. Цельсом и К. Галеном, — краснота (rubor), припухлость (tumor), боль (dolor), повышение температуры (calor) и нарушение функций (function laesa).
Древние говорили о воспалении как о местной лихорадке, однако отмеченная ими характеристика этого процесса распространяется и на системное, генерализованное воспаление.
Действительно, классические симптомы воспаления типичны и для системной реакции.
Краснота — распространённая гиперемия, связанная с вазодилатацией, снижением сосудистого сопротивления и повышением СВ, что характерно для септического шока — воспалительной реакции под действием инфекта.
Припухлость — отёк тканей вследствие повышенной сосудистой проницаемости, приводящей к синдрому «капиллярной утечки», в том числе отёку лёгочного интерстиция и острому повреждению лёгких.
Повышение температуры — гипертермия, один из симптомов системной воспалительной реакции, в основе которой лежит нарушение гуморальной регуляции температуры тела, в частности под влиянием простагландинов.
Боль вполне соотносится с болевыми ощущениями и изменениями ЦНС, характерными для системной воспалительной реакции инфекционного генеза, т.е. для сепсиса.
Нарушение функций, впервые описанное Галеном, соответствует полиорганной дисфункции, столь типичной для системной воспалительной реакции любой этиологии.
Системная воспалительная реакция полиэтиологична и может возникать при введении высокотоксичных химиотерапевтических средств и даже антибиотиков, отравлениях, панкреатической гиперферментемии (стерильный панкреонекроз), применении искусственного кровообращения и экстракорпоральных методов детоксикации.
Во многих случаях эта реакция носит компенсаторный, защитный характер, играя ведущую роль в саногенезе. Однако в патологических ситуациях происходит дисрегуляция этой реакции, образно говоря, «злокачественное системное воспаление», которое ведёт к полиорганной дисфункции с необратимыми фатальными нарушениями.
Начальной фазой системного воспаления является активация цитокинов и ферментов иммунокомпетентных клеток. Практически одновременно активируются эндотелиальные клетки, полиморфноядерные лейкоциты, моноциты и макрофаги.
Особую роль в системной воспалительной реакции играет повреждение эндотелия.
Эндотелий (площадь его составляет около 700 м2, а масса — 1,5 кг) — не просто выстилка сосудов, это крайне важная система, ключевые функции которой включают регуляцию сосудистого тонуса, гемостаза, проницаемости сосудов, адгезии и подвижности форменных элементов, в частности лейкоцитов.
В клетках эндотелия постоянно синтезируется в небольшом количестве оксид азота (NO), который играет вазодилатирующую роль и поддерживает сосуды в открытом состоянии. Активация эндотелиальных клеток при системном воспалении ведёт, прежде всего, к гиперпродукции оксида азота, что сопровождается чрезмерной вазодилатацией, повреждением стенки капилляров и повышением их проницаемости («капиллярной утечке»).
Каскадные реакции, присущие системному воспалению, перечислены ниже.
Нарушения, характерные для системной воспалительной реакции (реакция повреждения)
- Активация комплемента
- Активация и повреждение эндотелия
- «Капиллярная утечка», формирование отёка тканей
- Активация и выброс адгезивных молекул, цитокинов
- Экстравазация полиморфноядерных клеток и моноцитов
- Активация фагоцитоза
- Активация коагуляции
- Подавление фибринолиза с последующим его усилением
- Лихорадка
- Гиперпродукция белков острой фазы
- Гиперпролиферация лейкоцитов
- Активация и пролиферация В- и Т-лимфоцитов
- Активация глюкокортикоидной функции надпочечников
- Активация симпатической нервной системы
- Угнетенияе функций щитовидной железы
- Гиперкатаболизм
Естественно, что возникновение воспалительной реакции немедленно включает противовоспалительные механизмы, способствующие подавлению этой реакции.
Эти противовоспалительные механизмы включают активацию и выброс цитокинов ИЛ-4, ИЛ-10, ИЛ-13, рецепторов-антагонистов цитокина ИЛ-1, растворимых рецепторов TNFa. Прямым противовоспалительным эффектом обладают глюкокортикоиды и катехоламины, которые подавляют продукцию TNFa и ИЛ-1 и усиливают действие ключевого антивоспалительного цитокина ИЛ-10.
Однако этих и других пока малоизученных механизмов ограничения системной воспалительной реакции при чрезмерном действии повреждающих факторов недостаточно для её устранения.
Образно говоря, медиаторный взрыв сжигает организм больного.
Дисрегуляция про- и противовоспалительных процессов ведёт к дальнейшей деструкции эндотелиальных и других клеток, что является патофизиологической основой полиорганных функциональных и морфологических нарушении.
Клинико-лабораторные признаки системной воспалительной реакции включают достаточно простые диагностические параметры: гипер- или гипотермию тела, тахипноэ или гипокапнию, тахикардию, лейкоцитоз или лейкопению. Однако причиной возникновения этих симптомов являются глубокие «закулисные» процессы — выброс цитокинов, оксида азота, катехоламинов и других гуморальных медиаторов, синтез простагландинов, повреждение эндотелия, нарушение проницаемости капиллярных мембран и функций лёгких.
Эти клинические признаки неспецифичны, но несмотря на это, их выявление и сохранение у хирургического больного в течение достаточно продолжительного времени имеет большое прогностическое значение, особенно в послеоперационном периоде. Они могут быть предикторами (предсказателями) исхода лечения.
Это положение подтверждается весьма демонстративными клиническими исследованиями.
Так, при анализе результатов хирургического лечения более 3000 больных установлено, что в группе больных, не имеющих на 2-й день после операции ни одного из четырёх симптомов (гипертермия, тахипноэ, тахикардия, лейкоцитоз) синдрома системной воспалительной реакции, госпитальная летальность составила около 4%, при наличии одного симптома — более 8%, двух — 18,5%, трёх симптомов — 24%, а четырёх признаков системной воспалительной реакции — 40%. Эти данные демонстрируют клиническую значимость синдрома системной воспалительной реакции и подчёркивают необходимость выяснения причины её развития в каждом случае.
По своей сути признаки системного воспаления — реакция тревоги и для больного, и для клинициста, требующая должного диагностического поиска, лежащего в основе своевременного и адекватного лечения.
Дифференцировать характер и специфику системного воспаления можно лишь на основании анализа клинической ситуации и оценки вероятных этиологических факторов.
В частности, септический характер синдрома системной воспалительной реакции устанавливают с помощью выявления очага инфекции, экспресс-микробиологического обследования и определения дифференциально-диагностических маркёров инфекционного процесса.
Особое дифференциальное значение имеет определение концентрации в плазме прокальцитонина или Ореактивного белка, существенное повышение которых свидетельствует об инфекционной бактериальной этиологии воспалительной реакции.
Савельев В.С.
Хирургические болезни
Опубликовал Константин Моканов
Источник
