Псевдоэксфолиативный синдром мкб код
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Дополнительные факты
- Причины
- Патогенез
- Классификация
- Симптомы
- Возможные осложнения
- Диагностика
- Лечение
- Прогноз
- Профилактика
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: Псевдоэксфолиативный синдром.

Псевдоэксфолиативный синдром
Описание
Псевдоэксфолиативный синдром. Это увеопатия, характеризующаяся отложением амилоидоподобного вещества на структурах переднего сегмента глазного яблока. Клиническая картина представлена зрительной дисфункцией, появлением «помутнений» и «радужных кругов» перед глазами, затуманиванием зрения. Диагностика базируется на проведении ультразвуковой биомикроскопии, классической биомикроскопии с использованием щелевой лампы, скополаминовой пробы, УЗИ, визометрии, тонометрии, периметрии, гониоскопии. Консервативная терапия основывается на применении антиоксидантов, антигипоксантов, гипотензивных средств, витаминов группы В, А, Е.
Дополнительные факты
Псевдоэксфолиативный синдром впервые был описан финским ученым Дж. Линдбергом в 1917 году. Наблюдается взаимосвязь между развитием болезни и возрастом пациента. В 50-59 лет вероятность возникновения патологии составляет 1-2,5%, в 60-69 лет – 30%, после 70 лет – 42%. Согласно статистическим данным, заболевание диагностируется у 30% россиян старше 50 лет. Риск развития глаукомы у пациентов с псевдоэксфолиативным синдромом равен 64,6%. Патология чаще встречается среди представителей женского пола, однако тяжелее протекает у мужчин. Распространенность наиболее высока в серверных регионах.
Псевдоэксфолиативный синдром
Причины
Этиология заболевания до конца не изучена. Продолжительное время ученые связывали развитие патологии с изменениями строения эпителия хрусталика, однако диагностика псевдоэксфолиативного синдрома после интракапсулярной экстракции катаракты позволила опровергнуть эту теорию. На сегодняшний день ведущая роль в развитии болезни отводится действию следующих факторов:
• Ультрафиолетовое излучение. Воздействие ультрафиолета индуцирует свободно-радикальное окисление и деструкцию клеточной мембраны. Это влечет за собой атрофию с типичными признаками эксфолиации.
• Травматическое повреждение. Травмы глазного яблока приводят к локальным изменениям, которые у генетически скомпрометированных лиц являются пусковым фактором пигментной дисперсии.
• Внутриорбитальные инфекции. Многие авторы полагают, что поражение глаз обусловлено повышенной проницаемостью гематоофтальмического барьера (ГОБ). Способностью проникать через ГОБ наделена токсоплазма, вирус опоясывающего герпеса и краснухи.
• Нарушения иммунного статуса. В пользу этой этиологической теории псевдоэксфолиативного синдрома свидетельствует обнаружение в слезной жидкости повышенной концентрации интерлейкинов 6, 10, иммуноглобулина класса А и лактоферрина.
• Генетическая предрасположенность. У некоторых пациентов можно установить нарушение экспрессии генов в ядре и митохондриях. Встречаемость ПЭС среди родственников гораздо выше, чем в популяции. Прослеживается аутосомно-доминантный тип наследования.
Ученые полагают, что развитию болезни способствует курение и аутоиммунные патологии. Удается проследить взаимосвязь между возникновением ПЭС и артериальной гипертензией, атеросклерозом, аневризмой аорты в анамнезе. Некоторые исследователи полагают, что данные изменения – это следствие системной васкулопатии, поэтому пациенты с ПЭС часто страдают кардиоваскулярными заболеваниями.
Патогенез
Ключевая роль в механизме развития заболевания отводится образованию и депонированию аномального экстрацеллюлярного микрофибриллярного белка на поверхности передней капсулы хрусталика и радужки, цилиарном теле, цинновых связках, по краю зрачкового отверстия. Реже визуализируются патологические отложения в области передней камеры. Установлено, что белок относится к амилоидоподобной субстанции, за его синтез отвечает пигментный эпителий и меланоциты радужки. Согласно современным представлениям, патогенез ПЭС связан с нарушением эпителио-мезенхимальных взаимоотношений в структурах глазного яблока. Проникновение белковых структур в толщу его оболочек ведет к их дистрофическому перерождению.
Псевдоэксфолиативный синдром принято рассматривать как системное нарушение метаболизма соединительной ткани. Подтверждением этой теории является обнаружение специфических отложений в паренхиматозных органах (печень, почки, сердце, головной мозг) и кожных покровах. Учеными было обнаружено 14 антигенов главного комплекса гистосовместимости (HLA) при наследуемой форме патологии. Прогрессирование заболевания ведет к атрофии пигментной каймы, что проявляется выраженной дисперсией пигмента. Пигментоциты удается обнаружить в УПК и на радужной оболочке. Из-за поражения дренажной сети нарушается отток водянистой влаги с последующим повышением внутриглазного давления.
Классификация
В офтальмологии различают генетически детерминированный и иммуноопосредованный вариант развития. Вне зависимости от патогенеза болезнь всегда возникает в преклонном возрасте. По выраженности дистрофических изменений выделяют следующие степени псевдоэксфолиативного синдрома:
• I. Проявляется легкой атрофией радужки. Патологический процесс не распространяется за пределы корня оболочки. Кайма зрачка имеет неравномерную структуру. В области хрусталика определяется маловыраженное наслоение амилоида.
• II. Атрофия стромы радужной оболочки умеренная. На поверхности радужки и в зоне УПК выявляются выраженные псевдоэксфолиативные и пигментные отложения.
• III. Атрофические изменения резко выражены. Пигментная кайма имеет вид «целлофановой пленки», что обусловлено дисперсией пигмента. Поражение связочного аппарата вызывает подвывих, реже – вывих хрусталика.
Клиническая классификация базируется на результатах ультразвуковой биомикроскопии. Различают следующие стадии патологического процесса:
• I. Признаки поражения соответствуют псевдоэксфолиативному синдрому. Удается визуализировать точечные включения в передних отделах глаз.
• II. К вышеописанным изменениям присоединяются начальные признаки повреждения цинновой связки в виде чередования зон истончения с утолщением. Длина волокон разная.
• III. Аномальные включения становятся более плотными, провоцируют разрушение связочного аппарата.
• IV. Включения объединяются в большие конгломераты, которые приводят к увеличению продольной оси глазного яблока за счет удлинения переднего сегмента.
Симптомы
Для заболевания характерно длительное бессимптомное течение. Вначале поражается один глаз (зачастую левый). Вовлечение второго глазного яблока, как правило, наблюдается спустя 5-10 лет после развития первых симптомов. Жалобы обычно возникают уже после массивного отложения амилоида. Пациенты отмечают появление «помутнений» перед глазами. При взгляде на источник света появляются специфические «радужные круги». Снижение остроты зрения обусловлено поражением хрусталика, повышением ВГД и атрофией сфинктера радужки. Нарушается аккомодационная способность, в дальнейшем расстройства аккомодации сопровождаются затуманиванием зрения, нарушением рефракции. Болевой синдром появляется только при повреждении связочного аппарата.
Возможные осложнения
Отложение белка в толще хрусталиковых масс провоцирует развитие вторичной катаракты ядерного типа, которая зачастую сопровождается слабостью связочного аппарата. Это приводит к тому, что более чем у половины больных катарактой возникает сублюксация, реже – люксация хрусталика. В большинстве случаев патология осложняется офтальмогипертензией. Поражение трабекулярной сети ведет к возникновению псевдоэксфолиативной открытоугольной глаукомы, а с прогрессированием заболевания – к глаукомной оптической нейропатии или слепоте. Поражение мейбомиевых желез становится причиной ксерофтальмии.
Диагностика
Постановка диагноза на доклинической стадии затруднена. Выявить первые признаки можно только при помощи ультразвуковой биомикроскопии. Специфические методы диагностики включают:
• Биомикроскопию глаза. Позволяет визуализировать скопления белого или сероватого оттенка, напоминающи е хлопья на поверхности оболочек переднего отдела органа зрения. Хаотичные скопления пигмента могут формировать веретено Крукенберга. Псевдоэксфолиации по структуре похожи на воспалительные преципитаты.
• Гониоскопию. В передней камере определяются множественные включения, которые на поздних стадиях формируют крупные конгломераты. При нарушении проницаемости гематоофтальмического барьера в водянистой влаге обнаруживается взвесь крови. Объем камеры не изменен.
• Бесконтактную тонометрию. Характерно повышение внутриглазного давления, которое при вторичной глаукоме тяжело поддается снижению медикаментозным путем. При поражении дренажной системы дополнительно проводится электронная тонография.
• УЗИ глаза. При использовании ультразвуковой диагностики можно обнаружить разрыв цинновой связки с возникновением сферофакии. Из-за массивных отложений белка нарушается соотношение размеров переднего и заднего сегментов. Методика также применяется с целью обследования заднего сегмента глаз при снижении прозрачности оптических сред.
• Ультразвуковую биомикроскопию. Дает возможность выявить мелкоточечные включения слабой акустической плотности на оболочках глаза, разницу длины и лизис отдельных волокон цинновой связки.
• Скопаламиновую пробу. При 1 степени при проведении пробы зрачковое отверстие расширяется до 5 мм, при 2 – до 3,5-4 При 3 степени патологии реакция зрачка отсутствует.
• Визометрию. Зрительная дисфункция наблюдается при помутнении оптических сред или вторичной глаукоме. При тяжелом течении острота зрения снижается вплоть до светоощущения.
• Периметрию. Определяется концентрическое сужение поля зрения. В ряде случаев удается диагностировать выпадение отдельных участков из зрительных полей, скотомы.
Пациентам с данной патологией в анамнезе показана консультация невропатолога, ревматолога, кардиолога, гастроэнтеролога, отоларинголога. Необходимость проведения комплексного обследования вызвана системным поражением фиброзной ткани. Часто выявление первых симптомов поражения глаза позволяет диагностировать отложения амилоида в других паренхиматозных органах.
Лечение
Этиотропная терапия псевдоэксфолиативного синдрома не разработана. Цель консервативного лечения – предупредить развитие тяжелых осложнений. На ранних стадиях показано применение:
• Антиоксидантов. Используются лекарственные средства, в состав которых входит супероксиддисмутаза. СОД относится к классу металлопротеидов. Антиоксиданты вызывают разрушение активных форм кислорода, которые оказывают повреждающее влияние на ткани глаза.
• Антигипоксантов. С целью улучшения метаболизма и стимуляции процесса тканевого дыхания применяется цитохром С. Инстилляции препарата способствуют ускорению эпителизации и репарации повреждений структур передних сегментов глаз.
• Гипотензивных средств. Показаны при повышении внутриглазного давления, признаках офтальмогипертензии и начальных стадиях развития псевдоэксфолиативной глаукомы.
• Витаминотерапии. Доказана эффективность применения метилэтилпиридинола (структурный аналог витамина В6), который обладает фибринолитическим и антиоксидантным действием. В окислительно-восстановительных процессах также участвует витамин А (ретинола ацетат) и Е (токоферола ацетат).
При длительном течении патологии целью лечения является устранение или снижение выраженности вторичных осложнений. Медикаментозная терапия псевдоэксфолиативной глаукомы зачастую не оказывает должного эффекта. Возникает необходимость в лазерном или хирургическом вмешательстве. Наиболее целесообразно проведение ранней лазерной трабекулопластики, однако спустя 3-4 года возникают рецидивы повышения ВГД. При выборе метода удаления сублюксированного хрусталика следует отдавать предпочтение факоэмульсификации. Методикой резерва остается экстракапсулярная экстракция.
Прогноз
Исход заболевания зависит от степени тяжести, характера поражения структур переднего отдела глаз и типа осложнений. При своевременной диагностике и лечении осложнений прогноз в отношении зрительных функций благоприятный. Возникновение вторичной глаукомы ассоциировано с резистентностью к консервативной терапии и риском необратимой потери зрения.
Профилактика
Специфическая профилактика не разработана. Даже при ранних симптомах псевдоэксфолиативного синдрома необходима постановка на диспансерный учет у офтальмолога из-за высокой вероятности развития глаукомы. Показан регулярный контроль внутриглазного давления. Больные должны проходить комплексное офтальмологическое обследование не реже, чем два раза в год.
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
ПЭГ – разновидность глаукомы, развивающаяся на фоне псевдоэксфолиативного синдрома. Псевдоэксфолиативный синдром (ПЭС) определяется как распространенная патология экстрацеллюлярного матрикса, сопровождающаяся избыточной продукцией и накоплением патологического внеклеточного материала в различных интра- и экстраокулярных тканях.
Код по МКБ-10: H40.1 Capsular glaucoma with pseudoexfoliation of lens (в русской версии – «глаукома кaпсулярнaя с ложным отслоением хрустaликa»).
Эпидемиология
Установлено, что ПЭС встречается у 60-70 млн. человек в мире, около 25% из них имеют офтальмогипертензию, примерно в трети случаев (5-6 млн.) развивается глаукома (что почти в 10 раз чаще, чем в общей популяции). Частота ПЭГ заметно варьирует в различных регионах. Значительная распространенность глаукомы на фоне псевдоэксфолиативных отложений характерна для европейских стран (особенно у жителей Скандинавии), составляя в некоторых регионах до 50-60% случаев открытоугольной глаукомы. В Австралии доля ПЭГ не превышает 5,3%, в США – 12% (с преобладанием среди белого населения), на африканском континенте – около четверти случаев глауком. В азиатских странах этот показатель не столь велик: в Японии – 16%, Гонконге – менее 1%. Причины неоднородности распространения ПЭГ на планете дискутабельны. Возможно, это определяется влиянием средовых и наследственных факторов (генетическая специфичность ПЭГ подтверждена многочисленными исследованиями последних лет). Широко распространено заболевание на территории России. В частности в Центральном и Центрально-Черноземном регионах доля ПЭГ составила 64,6%, а в отдельных областях превысила 70%.
Особенности клинической картины
Заболевание протекает с типичными изменениями поля зрения и диска зрительного нерва, характерными для открытоугольной глаукомы. Однако клиническая картина ПЭГ имеет ряд специфических признаков, отличающих её от ПОУГ. Заболевание редко возникает у пациентов моложе 50 лет, средний возраст пациентов с ПЭГ выше, чем у лиц с ПОУГ. С возрастом частота ПЭГ увеличивается. Заболевание в сравнении с другими формами глаукомы протекает с более быстрой и тяжелой деградацией зрительных функций. На этапе выявления заболевания степень нарушения зрительных функций, в первую очередь поля зрения, выражена при ПЭГ сильнее. В подавляющем большинстве случаев ПЭГ относится к глаукоме высокого давления.
В сравнении с ПОУГ ПЭГ характеризуется:
• более высокими цифрами среднего уровня ВГД;
• более выраженными суточными колебаниями офтальмотонуса;
• более высокими значениями максимального ВГД в течение суток.
Возможно, именно эти особенности объясняют значительную частоту слепоты от ПЭГ, почти в 2 раза превышающую аналогичный показатель у лиц, страдающих ПОУГ. В конечном итоге, клинические характеристики глаукомы в сочетании с ПЭС обуславливают худший прогноз заболевания.
Имеет место ассиметричный характер глаукомы (в европейских странах соотношение клинически одностороннего и двустороннего процесса составляет 3:1).
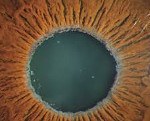
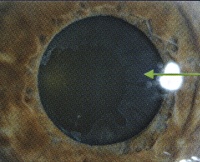
Специфические клинические проявления ПЭГ определяются характером псевдоэксфолиативного процесса. Биомикроскопия позволяет выявить наличие абсолютных и косвенных признаков псевдоэксфолиативного синдрома. К первым относят обнаружение псевдоэксфолиативного материала по зрачковому краю радужки и на передней капсуле хрусталика (рис. 1 и 2), ко вторым – дисперсия пигмента на структурах передней камеры после инстилляции расширяющих зрачок средств, затрудненный мидриаз и др.
Классическая картина отложений на передней капсуле характеризуется наличием трех зон: центрального диска, периферической зоны и разделяющей их промежуточной зоны без псевдоэксфолиативных отложений (формирующейся в результате слущивания прекапсулярной пленки за счет трения радужки при сокращении сфинктера зрачка). Наличие центрального диска не является обязательным признаком, в то время как периферические отложения присутствуют у всех пациентов. Указанная клиническая картина ПЭС представляет собой достаточно позднюю стадию процесса. Согласно современным представлениям развитие клинической картины ПЭС проходит следующие стадии: преклиническую (не выявляемую доступными методами исследования), стадию «подозрения на ПЭС» (характеризующуюся формированием гомогенного прекапсулярного слоя на передней поверхности хрусталика), стадию «мини-ПЭС» (с развитием фокальных дефектов прекапсулярного слоя) и «классический» ПЭС. Только мидриаз позволяет выявить 2- и 3-ю стадии процесса, что подчеркивает важность диагностики синдрома с обязательным соблюдением данного условия. Исследование после расширения зрачка позволяет обнаружить ПЭС дополнительно у 10-12% пациентов.
ПЭС считается фактором риска развития и прогрессирования катаракты (преимущественно ядерной) (рис. 3). Нередко ПЭГ сопровождается факодонезом и сублюксацией хрусталика вследствие поражения связочного аппарата (рис. 4). Отложения ПЭМ на цилиарных отростках и цинновой связке могут определяться уже на ранних стадиях заболевания. Это сопровождается нарастающей слабостью связочного аппарата на фоне деформации и разрывов зонулярных связок.
Патология радужки характеризуется отложением псевдоэксфолиативного материала по зрачковому краю, ригидностью зрачка. Имеет место деструкция пигментного листка и выщелачивание пигмента в области зрачкового пояса, которые наилучшим образом визуализируются в виде красного просвечивания в отраженном свете (феномен «трансиллюминации») (рис. 5). Характерны дистрофические изменения переднего отрезка глаза с «распылением» пигмента по поверхности радужки (преимущественно в зрачковом поясе). В отличие от синдрома пигментной дисперсии зерна пигмента равномерно распределяются по передней поверхности радужной оболочки и не определяются в криптах.
Нередко псевдоэксфолиации обнаруживаются на эндотелии роговицы. Их необходимо дифференцировать с роговичными преципитатами воспалительной природы. Иногда обнаруживается диффузное отложение зерен пигмента на задней поверхности роговицы, преимущественно в нижней половине. Установлено снижение плотности и количества эндотелиальных клеток и одновременное увеличение центральной толщины роговицы (впрочем, в ряде исследований указывается на уменьшение ЦТР при ПЭГ в сравнении с ПОУГ).
При гониоскопии преобладает открытый угол, нередко (до 30% случаев) – узкий. Описан феномен «ложнооткрытого угла», когда закрытие УПК может быть не замечено за счет его интенсивной экзогенной пигментации и множественных псевдоэксфолиативных отложений. ПЭГ сочетается с экзогенной гиперпигментацией. Пигмент локализуется преимущественно в нижней половине УПК. Одним из признаков синдрома считается отложение пигмента кпереди от переднего пограничного кольца Швальбе в виде волнистой линии (так называемая линия Sampaolesi) (рис. 6).
В большом количестве публикаций отмечается, что ПЭГ в сравнении с ПОУГ хуже поддается медикаментозной терапии. Монотерапия часто оказывается несостоятельной и требует дополнительных гипотензивных препаратов. Переход к лазерному или хирургическому лечению у таких пациентов происходит чаще, чем при ПОУГ.
ПЭС и закрытоугольная глаукома
Долгое время возникновение закрытоугольной глаукомы у пациентов с ПЭС считалось крайне редким. Однако работы последних десятилетий, в том числе с использованием морфологических исследований, выявили иную закономерность (показано, что более четверти случаев ЗУГ сопровождалось наличием ПЭС).
Развитие ЗУГ при ПЭС обусловлено преимущественно возникновением зрачкового блока. Последний является следствием следующих факторов или их комбинации:
• нестабильности связочного аппарата хрусталика, его сублюксации кпереди;
• ригидной радужки и снижения мидриатической способности зрачка;
• возникновения задних синехий.
Литература
1. Брежнев А.Ю., Иванов В.П., Баранов В.И. и др. Роль генов антиоксидантной защиты в развитии псевдоэксфолиативной глаукомы // Национальный журнал глаукома. – 2015. – Т. 14, № 2. – С. 38-44.
2. Брежнев А.Ю., Курышева Н.И., Трубилин В.Н., Баранов В.И. Проблемы ранней клинической диагностики псевдоэксфолиативного синдрома // Офтальмология. – 2012. – № 1. – С. 49-52.
3. Кроль Д.С. Псевдоэксфолиативный синдром и эксфолиативная глаукома: Автореф. дис. … д-ра мед. наук. – Саратов, 1970.
4. Курышева Н.И., Брежнев А.Ю., Капкова С.Г. Распространенность псевдоэксфолиативной глаукомы в Центральном и Центрально-Черноземном регионах России // Глаукома. – 2008. – № 3. – С. 11-15.
5. Щуко А.Г., Юрьева Т.Н., Чекмарева Л.Т. Глаукома и патология радужки. – М.: Боргес, 2009. – 166 с.
6. Hollo G., Konstas A. Exfoliation syndrome and exfoliative glaucoma. – EGS, 2009. – 161 p.
7. Konstas A.G., HolloG., Akopov E.L. et al. Factors associated with long-term progression or stability in exfoliation glaucoma // Arch. Ophthalmol. – 2004. – Vol. 122, № 1. – P. 29-33.
8. Konstas A., Tsironi S., Ritch R. Current concepts in the pathogenesis and management of exfoliation syndrome and exfoliative glaucoma //Comp. Ophthalmol. Update. – 2006. – Vol. 7, № 3. – P. 131-141.
9. Konstas A.G., Jay J.L., Marshall G.E. et al. Prevalence, diagnostic features, and the response to trabeculectomy in exfoliative glaucoma // Ophthalmology. – 1993. – Vol. 100, № 5. – P. 619-627.
10. Konstas A.G., Tsatsos I., Kardasopoulos A. et al. Preoperative features of patients with exfoliation glaucoma and primary open-angle glaucoma // Acta Ophthalmol. Scand. – 1998. – Vol. 76, № 2. – P. 208-212.
11. Martinez A., Sanchez M. Ocular haemodynamics in pseudoexfoliative and primary open-angle glaucoma // Eye. – 2008. – Vol. 22, № 4. – P. 515-520.
12. Ritch R., Schlotzer-Schrehardt U. Exfoliation syndrome // Surv. Ophthalmol. – 2001. – Vol. 45, № 4. – P. 265-315.
13. Ritch R., Schlotzer-Schrehardt U., Konstas A. Why is glaucoma associated with exfoliation syndrome? // Prog. Ret. Eye Res. – 2003. – Vol. 22, № 3. – P. 253-275.
14. Thorleifsson G., Magnusson K.P., Sulem P. et al. Common sequence variants in LOXL1 gene confer suspectibility to exfoliation glaucoma // Science. – 2007. – Vol. 317, № 5843. – P. 1397-1400.
15. Schlotzer-Schrehardt U. Molecular pathology of pseudoexfoliation syndrome/ glaucoma – new insights from LOXL1 gene associations // Exp. Eye Res. – 2009. – Vol. 88, № 4. – P. 776-785.
Источник
