Причины гиперхолестеринемии при нефротическом синдроме
Этим термином обозначается симптомокомплекс, характеризующийся массивной протеинурией(более 3 г белка/сутки), гипо- и диспротеинемией, гиперлипидемией, гиперхолестеринемией, распространенными отеками и водянкой серозных полостей.
По этиологииразличают первичный и вторичный нефротический синдром. Причиной развития первичного нефротического синдромаявляются первично возникающие заболевания почек, такие, как гломерулопатия с минимальными изменениями в виде слияния малых ножек подоцитов (липоидный нефроз), мембранозный гломерулонефрит, фокально-сегментарный гломерулосклероз, мембранозно-пролиферативный гломерулонефрит.
Вторичный нефротический синдромвозникает при многих заболеваниях, в основном системного характера, при которых почки поражаются вторично. К числу таких заболеваний относятся сахарный диабет (диабетическая нефропатия), амилоидоз, злокачественные опухоли, коллагенозы (системная красная волчанка, склеродермия, ревматизм, узелковый периартериит), хронические инфекционные процессы в организме, паразитарные заболевания
(токсоплазмоз, шистоматоз и др.), аллергические заболевания (сывороточная болезнь и др.). Кроме этого вторичный нефротический синдром возникает при интоксикациях (золото, ртуть, висмут, пенициламин, нестероидные противовоспалительные средства, яды насекомых и змей), нефропатии беременных, тромбозе почечных сосудов и др.
Этиология нефротического синдрома в значительной степени зависит от возраста. Наиболее частой причиной развития этого синдрома у детей является нефропатия с минимальными изменениями; у взрослых среди причин развития нефротического синдрома на первом месте стоит мембранозный гломерулонефрит; у людей старше 60 лет, наряду с мембранозным гломерулонефритом, развитие нефротического синдрома во многих случаях связано с диабетической нефропатией и другими системными заболеваниями, вторично нарушающими функцию почек.
Патогенез.Во всех случаях нефротического синдрома имеет место повышенная проницаемость базальной мембраны капилляров клубочков для белка. Протеинурияможет иметь как селективный, так и неселективный характер. При нефротическом синдроме с минимальными изменениями повышение клубочковой проницаемости связано с уменьшением постоянного электрического заряда стенки капиллярных петель, что обусловлено исчезновением из нее сиалопротеида, в норме тонким слоем покрывающего эндотелий и отростки подоцитов, лежащих на базальной мембране. При мембранозном гломерулонефрите главную роль играет потеря функции барьера, зависящего от размера пор в базальной мембране, которые в норме ограничивают прохождение плазменных белков с молекулярной массой более 150 кД.
Повышение проницаемости фильтрующих мембран клубочков связывают с повреждающим действием откладывающихся на них иммунных комплексов, а также лизосомальных ферментов и активных форм кислорода, выделяемых нейтрофилами и моноцитами. Кроме того, в плазме крови больных с нефротическим синдромом обнаружен фактор, предположительно образуемый лимфоцитами, который повышает проницаемость клубочкового барьера. При любом механизме повреждения происходит повышенное поступление белков плазмы крови, преимущественно альбуминов, в клубочковый фильтрат, и развивается резко выраженная протеинурия (более 3 г белка/сутки, в отдельных случаях — до 50 г белка/сутки). Следствием этого является гипопротеинемия(менее 60 г белка/л),
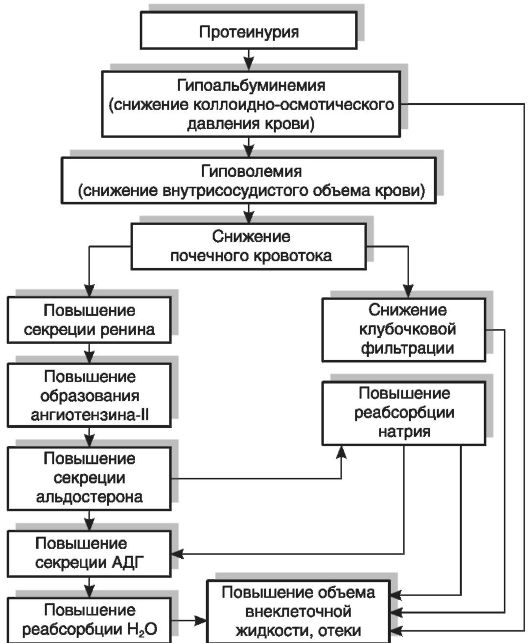
главным образом за счет снижения содержания альбуминов. Вызываемое гипопротеинемией падение коллоидно-осмотического давления сопровождается усиленным выходом жидкости из сосудов в межклеточное пространство и серозные полости тела и развитием гиповолемии, что, в свою очередь, вызывает повышение активности РААС и усиление продукции альдостерона; последний снижает экскрецию натрия с мочой и увеличивает его концентрацию в крови. При проведении ряда клинических и экспериментальных исследований было установлено, что, кроме описанного механизма, развитию гипернатриемии при нефротическом синдроме способствует снижение реакции почек на действие предсердного натрийдиуретического пептида, стимулирующего выведение натрия с мочой. Установлено, что пониженная реакция нефротической почки на предсердный натрийуретический пептид обусловлена пострецепторным дефектом в механизме действия этого фактора на уровне канальцевого эпителия. Возникающее при этом повышение осмотического давления стимулирует секрецию АДГ, который усиливает задержку в организме воды, что ведет к развитию отеков (рис. 19-2).
Стимуляция секреции АДГ под действием гипернатриемии сопровождается увеличением объема плазмы крови, но происходит ее разжижение, гипопротеинемия и гипоонкия возрастают. Вследствие этого избыточная вода не задерживается в кровеносном русле, а перемещается в ткани, что способствует дальнейшему нарастанию отеков, т.е. возникает «порочный круг».
Развитию гипопротеинемии при нефротическом синдроме, кроме протеинурии, способствуют повышенный выход белка в ткани в составе транссудата и потеря его через отечную слизистую кишечника. Гипопротеинемия сочетается с диспротеинемией,так как наряду с альбуминами нередко снижается содержание в крови γ-глобулинов, которые также могут поступать в мочу. Вместе с тем развивается гиперлипидемияза счет повышения содержания липопротеинов низкой и очень низкой плотности (ЛПОНП) при нормальном или пониженном уровне липопротеинов высокой плотности. В плазме крови повышается содержание холестерина и триацилглицеролов. За развитие гиперлипидемии ответственны два механизма: повышение продукции липопротеинов в печени и нарушение катаболизма хиломикронов и ЛПОНП. Предполагается, что пониженный катаболизм липопротеинов может быть обусловлен потерей с мочой некоторых субстанций (например, ли-
 Рис. 19-2.Механизм развития отеков при нефротическом синдроме. АДГ — антидиуретический гормон
Рис. 19-2.Механизм развития отеков при нефротическом синдроме. АДГ — антидиуретический гормон
попротеиновой липазы). Однако ни один из компонентов, выделенных из мочи этих больных, полностью не устраняет нарушения обмена липопротеинов. Гиперхолестеринемия и гиперлипидемия повышают риск развития у таких пациентов сердечно-сосудистых нарушений.
При нефротическом синдроме многие транспортные белки, связывающие эндогенные и экзогенные субстанции, теряются с мочой. В связи с этим в плазме крови у больных с нефротическим синдромом понижен уровень ряда микроэлементов (Fe, Cu
и Zn), метаболитов витамина D, тареоидньгх и стероидных гормонов. Многие лекарства в плазме крови связаны с альбуминами, поэтому при гипоальбуминемии повышается количество свободно циркулирующих форм, что может повысить их токсичность.
Развитие обширных отеков(вплоть до отека легких и мозга) и накопление транссудата в серозных полостях могут сопровождаться тяжелыми нарушениями функции жизненно важных органов и стать причиной летального исхода. Наряду с этим при нефротическом синдроме возникает ряд осложнений, являющихся факторами риска для таких больных.
Главную опасность при нефротическом синдроме составляют тромбоэмболические осложнения.У больных мембранозным гломерулонефритом часто возникает тромбоз почечной вены (у 20-30% взрослых пациентов); нередко происходит тромбоз глубоких вен голени. Другим опасным осложнением является эмболия легочной артерии. Артериальные тромбозы менее часты, но они могут привести к нарушению коронарного кровообращения, что повышает риск развития инфаркта миокарда. Главными факторами, ответственными за состояние гиперкоагуляции при нефротическом синдроме, являются повышение содержания прокоагулянтов — фибриногена и плазменных факторов V и VIII, снижение содержания антикоагулянта антитромбина III, ослабление активности фибринолитической системы вследствие снижения содержания плазминогена и повышение активности а2-антиплазмина; кроме того, происходит увеличение количества тромбоцитов и повышается их способность к адгезии и агрегации, что способствует нарушению микроциркуляции в различных органах и тканях.
Другую опасность для больных с нефротическим синдромом представляют инфекционные осложнения. Ранее дети с этим синдромом умирали от бактериальной инфекции, в частности от пневмококкового перитонита. Повышенная чувствительность к бактериальной инфекции обусловлена снижением уровня иммуноглобулинов А и G вследствие потери их с мочой.
Нередко происходит развитие гипокалыщемии,что обусловлено потерей с мочой связанного с белком кальция и метаболитов витамина D и снижением продукции этого витамина в проксимальных канальцах нефронов. Следствием гипокальциемии является развитие гиперпаратиреоза и остеопороза.Из других осложнений следует указать на возможность развития острой почечной недостаточности в связи с резко выраженной гиповолемией.
Ренальные показатели при нефротическом синдроме в значительной степени зависят от заболевания, на фоне которого он развился. В наиболее чистом виде они выражены при нефропатии с минимальными изменениями. При этом состоянии развивается олигурия,относительная плотность мочи повышена (1030-1050); кроме массивной протеинурии, регистрируется липидурия;в осадке мочи обнаруживаются гиалиновые, восковидные и эпителиальные цилиндры с жировыми включениями. При других вариантах нефротического синдрома в осадке мочи могут присутствовать эритроциты и лейкоциты. Массивная протеинурия повреждает эпителий канальцев, и это может сопровождаться развитием глюкозурии, гипераминоацидурии, фосфатурии, почечного канальцевого ацидоза; возникает состояние, подобное синдрому де Тони- Дебре-Фанкони.
Считается, что прогноз нефротического синдрома благоприятен при нефропатии с минимальными изменениями (при условии своевременно начатого лечения). При нефротическом синдроме другой этиологии исход зависит от вида заболевания, возникших осложнений, возраста пациента, своевременности и правильности лечения.
Источник
Ярким признаком HC является гиперлипидемия. Для нефротической гиперлипидемии характерно в первую очередь увеличение общего и эстерифицированного холестерина (липопротеиды низкой плотности, апоВ). При выраженном HC повышается и уровень триглицеридов (липопротеиды очень низкой плотности). Содержание липопротеидов высокой плотности (ЛВП) чаще нормально или снижено.
Концентрация неэстерифицированных жирных кислот обычно не изменена. Однако в целом их метаболизм, по всей видимости, нарушен, так как в результате гипоальбуминемии значительная часть жирных кислот транспортируется несвязанными, что в свою очередь отражается на обмене липопротеинов.
Тяжесть нефротической гиперлипидемии нередко определяется нозологической формой ГН (например, менее выражена при НС, обусловленном люпус-нефритом), течением HC (особенно высока при персистирующем течении), приемом глюкокортикостероидов.
Механизм развития нефротической гиперлипидемии полностью не выяснен. Наиболее распространенной в настоящее время является теория о ведущей роли гипоальбуминемии, стимулирующей при HC увеличение синтеза как белка, так и липопротеинов. В дальнейшем белок теряется с мочой, а гиперлипопротеинемия сохраняется. Эта теория подтверждается обнаруживаемой многими авторами связью выраженности нефротической гиперлипидемии с гипоальбуминемией. В реализации этого механизма имеет значение изменение двух факторов на пути синтеза в печени холестерина — увеличения активности ГМГ-КоА-редуктазы и снижения катаболизма мевалоната.
Наряду с мнением о гиперпродукции липопротеинов существует теория, отводящая основную роль нарушению их катаболизма, что связывают в первую очередь со снижением активности липопротеин-липазы вследствие потери с мочой ее активаторов. Это подтверждается снижением содержания липидов в крови, сопровождающим уменьшение протеинурии при неизменном уровне альбумина крови у больных с НС, леченных иАПФ.
Клиническое значение нефротической гиперлипидемии определяется ее атерогенным эффектом и вкладом в прогрессирование повреждения почек. Возможность ускоренного развития атеросклероза на фоне нефротической гиперлипидемии до настоящего времени подвергается сомнению ввиду отсутствия убедительных проспективных исследований. Вместе с тем существуют клинические подтверждения атеросклеротического повреждения аорты даже у 5-месячных детей. Представляют интерес результаты J.D. Ordonez и соавт., сопоставивших частоту тяжелых проявлений ишемической болезни сердца в группе из 142 больных с HG, каждый из которых имел пару среди 142 лиц контрольной группы. Авторами установлено, что при HC частота инфарктов миокарда (11 случаев) и смертей от осложнений ишемической болезни сердца (7 случаев) была значительно выше, чем в контрольной группе (соответственно 4 и 3 случая).
Морфологические маркеры липидогенных воздействий на почки представлены крупными внутриклеточными липидными включениями в ряде случаев с формированием пенистых клеток. По данным Н.И. Неверова, помимо гиперлипидемии, появление гломерулярных липидогенных маркеров определяется морфологической картиной нефропатии. Так, они почти всегда обнаруживаются в случаях нефротической гиперлипидемии, обусловленной так называемыми невоспалительными нефропатиями (минимальные изменения клубочков, мембранозная нефропатия, ФСГС). Внутриклеточное и внеклеточное накопление липидов в структурах клубочка стимулирует пролиферативные и склеротические процессы. Вероятность такого механизма подтверждена корреляциями между выраженностью липидогенных морфологических изменений и интенсивностью склеротических (избыточное накопление коллагена IV типа, появление коллагенов I и III типов) и пресклеротических (утолщение ГБМ, накопление мезангиального матрикса) процессов в клубочке.
Характерным признаком HC является нарушение метаболизма витамина D и связанного с ним фосфорно-кальциевого обмена. Эти нарушения выражаются в гипокальциемии (главным образом за счет белковосвязанного кальция, но также и его ионизированной фракции), гипокальциурии с клиническими признаками тетании (чаще у детей), остеопороза и остеомаляции. В основе этих нарушений лежит дефицит одного или нескольких метаболитов витамина D. Один из метаболитов (25-гидроксивитамин D) циркулирует в крови вместе с а-глобулином, витамин-D-связывающим белком и при нарушенной проницаемости ГБМ выходит в клубочковый фильтрат. Дигидроксилированные метаболиты [в основном 1,25а(ОH)2D3] образуются в проксимальных канальцах, и при массивной протеинурии, ведущей к поражению канальцев, их синтез снижается. Дефицит метаболитов витамина D ведет к развитию резистентности скелета к кальциймобилизующему действию паратгормона и нарушению всасывания кальция в кишечнике и тем самым к снижению ионизированного кальция. Большое значение имеет снижение связанного с белком кальция, обусловленное гипоальбуминемией. Снижение содержания ионизированного кальция стимулирует активность паращитовидных желез с развитием вторичного гиперпаратиреоза.
У части больных с HC выявляется диабетоподобный ответ на нагрузку глюкозой, а также повышение экскреции инсулина, а в крови — количества гормона роста. Эти расстройства чаще наблюдались у больных мембранозной нефропатией и фокально-гломерулярным склерозом. Нередко обнаруживается гипогликемия натощак одновременно с базальной гиперинсулинемией; гликемические кривые у этих больных уплощенные, резко замедленные.
В наших наблюдениях уровень иммунореактивного инсулина (ИРИ) был максимально высоким (24,0 мкед U/мл) в сыворотке крови больных с нефротическим синдромом по сравнению с показателем ИРИ у доноров (17,0 мкед U/мл), у больных с изолированным мочевым синдромом (19,0 мкед U/мл) и у больных с ХПН (22,0). Это позволило предположить, что при НС, характеризующемся усиленным липолизом, гиперлипидемией и катаболизмом, имеет место реактивный усиленный синтез инсулина как важнейшего гормона антилиполиза, липогенеза и анаболизма — своего рода адаптивная реакция поджелудочной железы. Тот факт, что базальная гиперинсулинемия при HC была достоверно выше (30) у больных с благоприятным прогнозом по сравнению с больными, имевшими плохой прогноз (21,0 мкед U/мл), позволяет рассматривать ее как компенсаторный позитивный признак.
При HC изменяются состав и количественное соотношение основных микроэлементов как в плазме крови, так и в клеточных элементах. В частности, могут выявляться резко выраженная гипоцинкемия, пониженное содержание железа и кобальта, на фоне чего развиваются анемия, тяжелые дистрофические изменения кожи и ее дериватов, отставание в росте детей с длительно существующим НС.
У больных с массивной протеинурией иногда могут быть различные расстройства функции проксимальных канальцев — аминоацидурия, глюкозурия, фосфатурия, почечный канальцевый ацидоз; в редких случаях эти расстройства сочетаются, давая клиническую картину синдрома Фанкони.
Источник
Патогенез гиперлипемии, гиперхолестеринемии, гиперлипопротеидемии, изменений фракционного состава липопротеидов сыворотки крови и липолитической активности остается неясным. Данные литературы по этому вопросу противоречивы. На наличие определенной связи между нарушениями белкового и липидного обменов при болезнях почек указывают ряд зарубежных и отечественных авторов. Зависимость между гиперхолестеринемией и низким содержанием белка в крови больных с нефротическим синдромом Epstein (1917), Baxter et. al. (1957). H. А. Ратнер и др. (1963), А. Я. Ярошевский (1971), Markiewick (1966) связывали гиперхолестеринемию и гиперлипидемию при хроническом нефрите с нефротическим синдромом со снижением содержания белка сыворотки крови. Markiewick (1966) у больных хроническим нефритом с нефротическим синдромом установил, что увеличение уровня β-липопротеидов крови коррелирует с нарастанием гипопротеинемии и гипоальбуминемии.
При изучении связи между показателями липидного обмена и содержанием белка сыворотки крови у больных с различными вариантами хронического диффузного гломерулонефрита установлены высокие коэффициенты корреляции между уровнем холестерина, β-липопротеидов сыворотки крови, увеличением фракций β-липопротеидов и уменьшением α-липопротеидов, с одной стороны, и нарастающей гипопротеинемией — с другой (А. А. Стороженко, 1974). Это подтверждает положение о том, что ряд изменений в липидном обмене при хроническом нефрите можно объяснить имеющей место при этом гипопротеинемией. Но гипопротеинемия не является единственным фактором, ответственным за развитие изменений в липидном обмене при нефропатиях.
Нуждается в уточнении и предположение о том, что гиперхолестеринемия у больных с нефропатиями является компенсаторной реакцией в ответ на развивающуюся гипопротеинемию. По-видимому, правильнее говорить о компенсаторной гипер-пре-β- и β-липопротеидемии. Гиперхолестеринемия же является следствием нарушения обмена липопротеидов. Для подтверждения этого предположения мы проверили коррелятивную связь между некоторыми показателями липидного обмена при различных формах хронического нефрита. Оказалось, что имеется достоверная корреляция между содержанием холестерина и количеством β-липопротеидов сыворотки крови; содержанием холестерина и изменением фракций пре-β-, β-липопротеидов и α-липопротеидов на липидограммах сыворотки крови. Таким образом, предположение о том, что гиперхолестеринемия может быть следствием превращения α-липопротеидов в пре-β- и β-липопротеиды с освобождением при этом холестерина, подтверждается высоким коэффициентом корреляции.
Однако зависимость между гиперлипемией и гипопротеинемией признается не всеми авторами. Squire (1955), а также Heyman и др. (1956) полагали, что в патогенезе гиперлипемии главная роль принадлежит недостаточному использованию и расщеплению липидов. Некоторые авторы связывали повышение содержания холестерина при нефропатиях с нарушением функции печени (Н. Д. Стражеско, 1932). Но Б. И. Шулутко (1972), изучая биоптаты печени больных с заболеваниями почек, показал, что изменения в печени при этом весьма незначительны и свидетельствуют о функциональной полноценности гепатоцита. Высокая функциональная активность печени сохраняется даже у больных с выраженными явлениями почечной недостаточности.
Некоторые исследователи связывают увеличение β-липопротеидов при хроническом нефрите с нефротическим синдромом с повышением концентрации холестерина сыворотки крови (М. П. Матвеев и др., 1969), однако данные Д. Б. Цыкина (1972) не подтверждают данного предположения. Об отсутствии соответствия содержания β-липопротеидов с концентрацией холестерина в сыворотке крови говорят и результаты исследований Mitchell и др. (1966).
В литературе обсуждается вопрос о нарушении специальной функции почек при нефротическом синдроме, обеспечивающей расщепление липидов ферментами почечной ткани. Frey (1951) писал, что почки являются органом, участвующим в липидном обмене, а гиперхолестеринемия развивается вследствие поражения канальцев так же, как повышение остаточного азота является результатом поражения клубочков.
В патогенезе гиперлипемии определенную роль может играть недостаточная активность фактора просветления (липопротеидная липаза). Однако данные об активности липопротеидной липазы при заболеваниях почек малочисленны и противоречивы. Известно, что субстратом липопротеидной липазы являются два класса липопротеидов: хиломикроны и β-липопротеиды низкой плотности (Graham, 1951).
Nikkila (1953), Franken (1955), Fischer (1959) указывали на изменение электрофоретической подвижности белков плазмы крови после реакции просветления, что позволило высказать предположение о возможности трансформации β-липопротеидов в α-липопротеиды.
Korn (1959) считает, что липопротеидная липаза участвует в метаболизме липидов на клеточном уровне и транспорте липидов из крови в межклеточную жидкость и клетки. В настоящее время известно, что липопротеидная липаза является единственным ферментом, катализирующим расщепление, а в некоторых тканях, возможно, и синтез липопротеидов (Ф. Л. Лейтес, 1965).
Определенную роль в механизме нарушения липидного обмена при нефропатиях играет и гепарин. Гепарин при внутривенном введении активирует липопротеидную липазу, вызывает снижение количества липопротеидов низкой плотности и просветление сыворотки крови; он снижает содержание высокоплотных липопротеидов, концентрацию нейтральных жиров и уровень холестерина. Высокий уровень гепарина при нефротическом синдроме можно в известной мере рассматривать как компенсаторный в ответ на гиперлипидемию. Braunsteiner обратил внимание на то, что повышение уровня липидов при нефрозе сопровождается увеличением содержания базофилов в крови, базофилию он рассматривает как компенсаторный процесс, связанный с повышенной потребностью в гепарине для активаций липопротеидной липазы.
Таким образом, при нефропатиях изменяются и показатели липолитической активности (липопротеидная липаза И гепарин), но до сих пор остается неясной их роль в интимных процессах нарушения липидного обмена у почечных больных.
Для многих почечных заболеваний характерно не только нарушение липидного обмена, но и возникновение липидурии, механизмы развития которой остаются во многом неясными. Липиды могут проникать в мочу при распаде почечного эпителия, в результате хилурии и перехода лимфы в мочевые пути (Н. Я. Червяковский, 1940). Chaptal и др. (1955) считают, что липиды полностью реабсорбируются в канальцах, вызывают их ожирение и попадают в мочу только с отторгнутым эпителием. Установлен параллелизм между протеинурией и липидурией, а поскольку липопротеиды в своей основе содержат протеин, то высказано предположение об одинаковом характере патогенеза протеинурии и липидурии при заболеваниях почек (Bing, Stamp, 1935).
В настоящее время существуют различные представления о происхождении протеинурии, при этом придают значение увеличению проницаемости клубочков, уменьшению реабсорбции белка в канальцах, изменению свойств белка с более легкой его фильтрацией, секреции белка эпителием канальцев, примеси белка к моче из лимфы (Lowgren, 1955).
По мнению большинства авторов (Е. М. Тареев, 1958; М. С. Вовси, 1960; erg, 1955; Reubi, 1955, и др.), решающее значение в генезе протеинурии принадлежит повышению проницаемости клубочкового фильтра, главным образом мембраны клубочков, для плазменных белков и липопротеидов. Существенная роль в механизме выделения белка с мочой отводится канальцевому фактору, в частности, нарушению процесса реабсорбции в проксимальных отделах канальцев (В. В. Серов, 1968; Freeman и др., 1957). Не исключается и возможность появления белка в моче вследствие секреции его патологически измененным канальцевым эпителием.
Остается не совсем ясной причина развития липопротеидурии при некоторых формах нефропатии: хроническом нефрите с нефротическим синдромом, амилоидозе почек, терминальной стадии хронического нефрита. По-видимому, это определяется особенностью поражения клубочковой мембраны при этих нефропатиях, при котором мембрана начинает пропускать и крупномолекулярные липопротеидные комплексы. Поэтому определение липопротеидов в моче может рассматриваться одним из показателей степени поражения клубочковой мембраны.
Источник
