Полигландулярный аутоиммунный синдром 1 типа
Аутоимму́нный полиэндокри́нный синдро́м (аутоиммунный полигландулярный синдром, синдром полигландулярной недостаточности) — аутоиммунное заболевание, объединяющее поражение нескольких эндокринных органов.
Аутоиммунный полиэндокринный синдром типа 1[править | править код]
Синдро́м MEDAC (аутоиммунный полиэндокринный синдром тип 1, синдром полигландулярной недостаточности типа 1, синдром кандидоза-эндокринопатии, акроним MEDAC: Multiple Endocrine Deficiency, Autoimmune, Candidiasis) — характеризуется монилиазом слизистых оболочек и кожи, сахарный диабет (редко), гипопаратиреозом и недостаточностью надпочечников. В 2/3 случаев синдром выявляется в неполной форме, включающей два из трёх основных компонентов[2].
Аутоиммунный полиэндокринный синдром типа 2[править | править код]
Синдро́м Шми́дта (аутоиммунный полигландулярный синдром типа 2, синдром полигландулярной недостаточности типа 2, тиреоадренокортикальная недостаточность, англ. Schmidt’s syndrome) — включает недостаточность надпочечников, лимфоцитарный тиреоидит, гипопаратиреоз и недостаточность половых желез в любом сочетании этих симптомов друг с другом; также возможен сахарный диабет 1-го типа[3][4]. Синдром назван в честь Schmidt A.[5], впервые описавшего данный симптомокомплекс в 1926 году. Является наиболее распространённым типом синдрома полигландулярной недостаточности[6]. Чаще болеют женщины (75% всех случаев)[6].
Аутоиммунный полиэндокринный синдром типа 3[править | править код]
Наиболее распространённая клиническая форма аутоиммунного полигландулярного синдрома и представляет собой сочетание патологии островкового аппарата поджелудочной железы (сахарный диабет 1-го типа) и щитовидной железы (аутоиммунный тиреоидит, диффузный токсический зоб). Синдром генетически детерминирован. В основе патогенеза — извращённая реакция клеточного и гуморального звеньев иммунной системы, обусловленная дефектом Т-супрессорных лимфоцитов[7].
См. также[править | править код]
- Зоб Хашимото
- Сахарный диабет 1-го типа
Примечания[править | править код]
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ Симптомы и синдромы в эндокринологии / Под ред. Ю. И. Караченцева. — 1-е изд. — Х.: ООО «С.А.М.», Харьков, 2006. — С. 27—28. — 227 с. — (Справочное пособие). — 1000 экз. — ISBN 978-966-8591-14-3.
- ↑ Симптомы и синдромы в эндокринологии / Под ред. Ю. И. Караченцева. — 1-е изд. — Х.: ООО «С.А.М.», Харьков, 2006. — С. 180—181. — 227 с. — (Справочное пособие). — 1000 экз. — ISBN 978-966-8591-14-3.
- ↑ Betterle C., Zanchetta R. Update on autoimmune polyendocrine syndromes (APS) // Acta Biomed. — 2003. — Апрель (т. 74, № 1). — С. 9—33. — PMID 12817789.
- ↑ Heuss D., Engelhardt A., Göbel H., Neundörfer B. Myopathological findings in interstitial myositis in type II polyendocrine autoimmune syndrome (Schmidt’s syndrome) (англ.) // Neurol. Res. : journal. — 1995. — June (vol. 17, no. 3). — P. 233—237. — PMID 7643982.
- ↑ 1 2 Greenspan, Francis S.; Gardner, David C. Basic clinical endocrinology. — New York: McGraw-Hill Education, 2004. — С. 103. — ISBN 0-07-140297-7.
- ↑ Симптомы и синдромы в эндокринологии / Под ред. Ю. И. Караченцева. — 1-е изд. — Х.: ООО «С.А.М.», Харьков, 2006. — С. 26—28. — 227 с. — (Справочное пособие). — 1000 экз. — ISBN 978-966-8591-14-3.
Ссылки[править | править код]
Источник

Аутоиммунный полигландулярный синдром – эндокринопатия аутоиммунного генеза, протекающая с одновременным первичным множественным поражением желез внутренней секреции и других органов. При аутоиммунном полигландулярном синдроме 1 типа отмечается надпочечниковая недостаточность, кандидоз кожи и слизистых, гипопаратиреоз; аутоиммунный полигландулярный синдром 2 типа протекает с развитием надпочечниковой недостаточности, гипер- или гипотиреоза, инсулинозависимого сахарного диабета, первичного гипогонадизма, миастении, стеатореи и др. нарушений. Диагностика включает определение комплекса лабораторных показателей (биохимического анализа, гормонов крови и мочи), УЗИ и КТ надпочечников, УЗИ щитовидной железы. Лечение аутоиммунного полигландулярного синдрома требует назначения заместительной терапии гормонами (кортикостероидами и минералокортикоидами, L-тироксином).
Общие сведения
Аутоиммунный полигландулярный синдром (АПГС) – иммуноэндокринное нарушение, характеризующееся первичной функциональной недостаточностью нескольких желез внутренней секреции, а также неэндокринными органоспецифическими заболеваниями. В эндокринологии различают аутоиммунный полигландулярный синдром 1 и 2 типов (АПГС-1, 2), которые имеют свои генетические, иммунологические и клинические особенности.
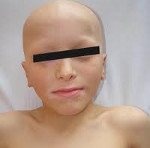
Аутоиммунный полигландулярный синдром 1 типа обычно манифестирует в детском возрасте (10-12 лет) и иногда обозначается в литературе термином «ювенильная семейная полиэндокринопатия». В целом распространенность АПГС-1 невелика, однако заболевание несколько чаще встречается в мужской популяции, преимущественно у жителей Финляндии, Сардинии, Ирана, что объясняется длительной генетической обособленностью этих народов. Аутоиммунный полигландулярный синдром 1 типа включает триаду признаков: надпочечниковую недостаточность, гипопаратироз и кандидамикоз.
Наиболее частым вариантом множественной эндокринопатии аутоиммунной природы является аутоиммунный полигландулярный синдром 2 типа, который развивается у взрослых (старше 20-30 лет); среди заболевших преобладают женщины. Компонентами АПГС-2 являются надпочечниковая недостаточность, сахарный диабет 1-го типа, аутоиммунное поражение щитовидной железы по типу первичного гипотиреоза или тиреотоксикоза. Кроме эндокринных нарушений, аутоиммунному полигландулярному синдрому 1 и 2 типов сопутствуют другие органоспецифические проявления.
Аутоиммунный полигландулярный синдром
Причины аутоиммунного полигландулярного синдрома
Оба типа аутоиммунного полигландулярного синдрома являются генетически детерминированными, на что указывает семейно-наследственный характер заболевания. При этом АПГС-1 поражаются братья и сестры одного поколения; аутоиммунным полигландулярным синдромом 2 типа – представители одной семьи на протяжении нескольких поколений.
Аутоиммунный полигландулярный синдром 1 типа – единственное известное аутоиммунное заболевание, имеющее моногенную природу. К развитию АПГС-1 приводит мутация гена аутоиммунного регулятора (AIRE), расположенного на длинном плече 21 хромосомы (21q22.3). Аутоиммунный полигландулярный синдром-1 наследуется по аутосомно-рецессивному типу и не связан с гаплотипами HLA.
Аутоиммунный полигландулярный синдром 2 типа ассоциирован с HLA-гаплотипом (антигенами DR3, DR4, DR5, В8, Dw3). Вероятно, что механизм развития АПГС-2 связан с аномальной экспрессией антигенов HLA-системы на клеточных мембранах желез внутренней секреции, которая запускается под воздействием каких-либо внешних факторов.
Симптомы аутоиммунного полигландулярного синдрома 1 типа
Аутоиммунный полигландулярный синдром 1 типа обычно впервые заявляет о себе в первые 10 лет жизни развитием гранулематозного кандидоза (кандидамикоза кожи и слизистых) и гипопаратиреоза. В дальнейшем (часто спустя десятилетия) присоединяется хроническая надпочечниковая недостаточность (аддисонова болезнь). Клиническими критериями установления диагноза синдрома служит сочетание двух из трех упомянутых эндокринных нарушений.
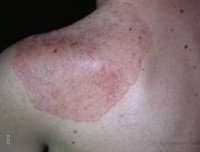
Кандидоз при АПГС-1 носит генерализованный характер и поражает слизистые оболочки полости рта, гениталий, дыхательных путей и желудочно-кишечного тракта, а также кожу, ногтевые валики, ногти. Гипопаратиреоз проявляется судорогами мышц конечностей, парестезией кожи, ларингоспазмом, судорожными припадками, напоминающими эпилепсию. Надпочечниковая недостаточность при аутоиммунном полигландулярном синдроме нарастает скрыто и может впервые проявится аддисоническим кризом на фоне стрессового состояния.
Классическая триада при аутоиммунном полигландулярном синдроме часто сочетается с первичным гипогонадизмом (45%), алопецией (30%), синдромом мальабсорбции (23%), пернициозной анемией (14%), хроническим аутоиммунным гепатитом (12%), аутоиммунным тиреоидитом (10%), инсулинозависимым сахарным диабетом (4%), витилиго (4%). Реже встречается дистрофия ногтевых пластин, гипоплазия зубной эмали, гломерулонефрит, бронхиальная астма, катаракта.
На фоне аутоиммунного полигландулярного синдрома 1 типа у женщин отмечается гипоплазия яичников (аутоиммунный оофорит), сопровождающийся первичной или вторичной аменореей. Мужской гипогонадизм проявляется снижением либидо, импотенцией, бесплодием.
Симптомы аутоиммунного полигландулярного синдрома 2 типа
Манифестация аутоиммунного полигландулярного синдрома 2 типа приходится на зрелый возраст (около 30 лет). Первым проявлением эндокринопатии обычно служит хроническая надпочечниковая недостаточность. Другие аутоиммунные компоненты (сахарный диабет 1-го типа, аутоиммунный тиреоидит), как правило, присоединяются через 7-10 и более лет.
У пациентов с аутоиммунным полигландулярным синдромом 2 типа часто развивается первичный гипогонадизм, миастения, витилиго, дерматит, алопеция, аутоиммунный гастрит, целиакия, стеаторея, полисерозиты (плеврит, перикардит, асцит), тимома. При аутоиммунном полигландулярном синдроме могут наблюдаться атрофия зрительных нервов, опухоли гипофиза, аутоиммунная тромбоцитопеническая пурпура и т. д.
Наиболее часто в клинической практике встречается вариант аутоиммунного полигландулярного синдрома 2-го типа, сочетающий первичную хроническую надпочечниковую недостаточность с аутоиммунным поражением щитовидной железы: аутоиммунным тиреоидитом, реже — диффузным токсическим зобом (синдром Шмидта). Множественные эндокринопатии взаимно отягощают друг друга и утяжеляют течение заболевания.
Диагностика аутоиммунного полигландулярного синдрома
Критериями для постановки клинического диагноза служат подтвержденные лабораторным и инструментальным путем изолированные компоненты аутоиммунного полигландулярного синдрома (кожно-слизистый кандидоз, гипопаратиреоз и ХНН при АПГС-1; ХНН, аутоиммунный тиреоидит и сахарный диабет при АПГС-2). При АПГС 1 типа наиболее показательно проведение молекулярно-генетического анализа, позволяющего выявить характерную генную мутацию.
Лабораторное обследование при аутоиммунном полигландулярном синдроме включает определение биохимических показателей крови (уровня общего и ионизированного кальция, фосфора, калия, натрия, билирубина, трансаминаз, щелочной фосфатазы, общего белка, мочевины, креатинина, глюкозы), КОС крови и др. Важные диагностические сведения дают результаты исследований гормонов: ТТГ, свободного тироксина, паратгормона, АКТГ, инсулина, С-пептида, кортизола, ренина, альдостерона, соматомедина С, АТ-ТПО, АТ к бета-клеткам поджелудочной железы и GAD, тестостерона, ЛГ, ФСГ и др.
Инструментальные исследования включают УЗИ брюшной полости, щитовидной железы, органов малого таза (у женщин) и мошонки у мужчин, ЭхоКГ, КТ надпочечников. При наличии показаний проводятся консультации узких специалистов – диабетолога, гастроэнтеролога, гепатолога, дерматолога, миколога, невролога, гематолога, офтальмолога, гинеколога-эндокринолога, андролога, ревматолога.
Лечение аутоиммунного полигландулярного синдрома
Терапия аутоиммунного полигландулярного синдрома представляет сложную задачу и складывается из лечения его отдельных компонентов. Основу патогенетической терапии составляет постоянная заместительная гормонотерапия при функциональной недостаточной пораженных эндокринных желез. При надпочечниковой недостаточности назначаются глюкокортикоиды (гидрокортизон, дексаметазон, преднизолон, триамцинолон), минералокортикоиды (ДОКСА, триметилацетат дезоксикортикостерона и др.), при гипотиреозе — L-тироксин.
При кандидамикозе, сопровождающем аутоиммунный полигландулярный синдром 1 типа, используются противогрибковые препараты. При сахарном диабете на фоне аутоиммунного полигландулярного синдрома 2 типа может потребоваться иммуносупрессивная терапия циклоспорином. Пациентам рекомендуется употребление повышенного количества аскорбиновой кислоты и соли. Запрещается прием алкоголя, некоторых лекарственных препаратов.
Прогноз аутоиммунного полигландулярного синдрома
Раннее выявление аутоиммунного полигландулярного синдрома и проведение адекватной заместительной терапии позволяют контролировать течение заболевания. Однако трудоспособность, как правило, снижается – пациентам присваивается II-III группа инвалидности.
Пациенты с аутоиммунным полигландулярным синдромом подлежат диспансерному наблюдению эндокринолога и других специалистов. При стрессовых состояниях, интеркуррентных инфекциях, физическом или умственном перенапряжении больным необходимо увеличение дозы гормонов. Необходимо немедленное обращение к врачу при любом ухудшении самочувствия. Летальный исход при аутоиммунном полигландулярном синдроме может наступать от ларингоспазма, висцерального кандидамикоза, острой надпочечниковой недостаточности.
Источник
ПОЛИЭНДОКРИНОПАТИИ
АУТОИММУННЫЕ ПОЛИГЛАНДУЛЯРНЫЕ СИНДРОМЫ – сочетания аутоиммунных поражений сразу нескольких эндокринных желез формируют два клинических синдрома – АПС I, АПС II
Аутоиммунные полигландулярные синдромы (АПС) — это первичное аутоиммунное поражение двух и более периферических эндокринных желез, приводящее к их недостаточности, часто сочетающееся с различными органоспецифическими неэндокринными заболеваниями аутоиммунного генеза
АПС I – моногенное аутосомно-рецессивное заболевание вследствие мутации гена AIRE, кодирующего белок «аутоиммунный регулятор»
· характерна классическая триада: слизисто-кожный кандидоз, гипопаратиреоз, первичная хроническая надпочечниковая недостаточность (болезнь Аддисона). Для диагноза необходимы только два из этих признаков, а у сибсов – достаточно одного.
Патогенез
В основе патогенеза лежит аутоиммунная деструкция эндокринных желез. При АПС-l с высокой частотой определяются антитела к ферментам надпочечникового стероидогенеза P450scc (20,22-десмолаза), Р450с17 (17α-гидроксилаза) и Р450с21 (21α-гидроксилаза), антитела против панкреатических β-клеток (к глутаматациддекарбоксилазе и L-аминоациддекарбоксилазе) и других пораженных тканей.
Клинические проявления
· 1 признак АПС 1го типа – хронический кандидоз кожи и слизистых (чаще всего до 2х лет) — поражение слизистых оболочек полости рта, гениталий, а также кожи, ногтевых валиков, ногтей
· 2 признак – развитие гипопаратиреоза (чаще до 7-9 лет)
· 3 признак – первичная надпочечниковая недостаточность (чаще до 12 лет)
Если у пациента есть родственник 1 порядка с установленным диагнозом АПС 1 типа или характерными его симптомами, достаточно 1 из 3х перечисленных признаков.
Доп. Признаки:
· Алопеция (40%)
· Мальабсорбция (30%)
· У 10-20 % женщин с АПС-l встречается первичный гипогонадизм, развивающийся в результате аутоиммунной деструкции яичников (аутоиммунный оофорит); клинически он проявляется первичной или вторичной аменореей.
· АИТ (30%)
· В12-дефицитная анемия (30%)
· СД1 (20%)
· Первичный гипогонадизм (70%)
· Аутоиммунный гепатит (20%)
· Витилиго, седые волосы (25%)
· Кератоконъюктивит, сухой кератит (10%)
· Дисплазия зубной эмали (30%)
· Гипоплазия ногтей (20%)
· Гипоспления (10%)
Новые симптомы заболевания могут присоединяться в течение жизни.
АПС II – многофакторное заболевание с наследственной предрасположенностью. Существует ассоциация между АПС 2 типа и экспрессией некоторых генов главного комплекса гистосовместимости HLA.
АПС-2 обозначаются различные варианты сочетаний аутоиммунной патологии надпочечников (болезнь Аддисона), щитовидной железы (аутоиммунный тиреоидит (АИТ) или болезнь Грейвса) и сахарного диабета 1 типа (СД-1). Наиболее типичными и частыми вариантами АПС-2 являются синдром Шмидта (сочетание первичного гипокортицизма и гипотиреоза в исходе АИТ) и синдром Карпентера (сочетание СД-1 и АИТ).
АПС-2 примерно в 8 раз чаще встречается у женщин, манифестирует в среднем в возрасте между 20 и 50 годами. АПС II наиболее частый синдром полигландулярной недостаточности.
Основные клинические критерии:
· Первичная ХНН
· Хронический АИТ
· СД 1
+/- гипогонадизм, миастения, целиакия, пернициозная анемия, алопеция, серозит, витилиго…
-Целиакия обычно поддается лечению безглютеновой диетой.
-В отсутствии лечения может иметь место гипоCa-мия (не вследствие гипопаратиреоза), остеопения, а иногда и лимфома ЖКТ.
Диагностика:
1. Анамнез:
a. Близкородственные связи
b. Случаи заболеваний эндокринной системы
c. Ранняя инвалидизация и смерть
2. Обследование физикальное
a. Гипогонадизм: измерение роста, массы, оценка полового развития отражает тяжесть течение АПС
b. Кандидоз и алопеция: состояние ногтей, волос, слизистых оболочек
c. Надпочечниковая недостаточность, гипотиреоз: гиперпигментация, витилиго/сухость кожных покровов
d. Гипопаратиреоз: +с-мы Хвостека и Труссо (гипоCa-мия)
3. Лаборатория
a. Гипопаратиреоз: ионизированный кальций, кальций общий, фосфор и ПТГ
b. НН: калий, натрий, кортизол и АКТГ, АРП. Сандартный тест – синактен-депо (пролонгированная форма синтетического аналога АКТГ). Самым ранним симптомом может стать гипогликемия, снижение потребности в инсулине у СД1.
c. Гипотиреоз: повышение ТТГ. Низкий сТ4
d. Половые железы: ЛГ, ФСГ (резко повышены при первичном гипогонадизме), тестостерона и эстрадиола
e. Недостаточность гормона роста: задержка роста > СТГ-стимулированные тесты (исключение СТГ-недостаточности)
f. СД: глюкоза плазмы, HbA1c, ПГТТ
g. Функция печени: гамма-ГТ, АЛТ, АСТ, ЩФ протеинограмма
h. В-12 деф.анемия
i. Гипокальциемия при АПС II мб вследствие целиакии (реже – из-за гипопаратиреоза)
j. Аутоиммунная природа заболевания: АТ к органам-мишеням – к микросомальной тиропероксидазе, к рТТГ в ЩЖ; к GAD, ICA, IAA клеток ПЖ.
4. Молекулярно-генетическая диагностика: определение мутаций гена AIRE. Рекомендовано всем пациентам с хроническим кандидозом кожи и слизистых оболочек, гипопаратиреозом и НН неустановленной этиологии.
5. Инструментальные исследования:
a. УЗИ органов брюшной полости (признаки гепатита и цирроза печени) и ЩЖ
b. ЭГДС (гастрит, эзофагит, грибковые поражения слиз.оболочки верхних отделов ЖКТ)
c. МРТ и КТ головного мозга (признаки гипопитуитаризма, кальцинатов – синдром Фара)
d. Рентген кистей (оценка костного возраста у детей с задержкой роста)
6. Лечение
a. Симптоматическое
b. Одновременное выявление НН + гипотиреоза = в первую очередь ЗГТ глюко- и минералокортикоидами. Однако ЗГТ левотироксином может усугубить явления некомпенсированной НН и привести к развитию адреналового криза. При назначении заместительной терапии глюкокортикоидами следует иметь в виду, что передозировка может способствовать декомпенсации гипопаратиреоза и спровоцировать гипокальциемию.
c. Гипопаратиреоз: витD + кальций.
d. ГКС угнетают абсорбцию кальция в кишечнике > если у пациента НН + гипопаратирез, уровень кальция в крови мб повышен
e. Кандидоз кожи: флуконазол. Нежелательно применять кетоконазол, т.к. он угнетает синтез стероидных гормонов в надпочечниках (общий ингибитор ферментов цитохрома Р450) и половых желез, может спровоцировать адреналовый криз
7. Для пациентов: осведомить о риске рождения больного ребенка, необходимости обследования родственников первого порядка.
Источник
