Патология глаз при псевдоэксфолиативном синдроме тахчиди
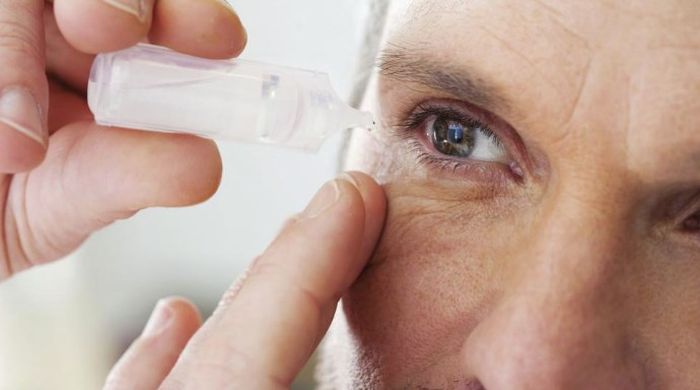
Псевдоэксфолиативный синдром – это увеопатия, характеризующаяся отложением амилоидоподобного вещества на структурах переднего сегмента глазного яблока. Клиническая картина представлена зрительной дисфункцией, появлением «помутнений» и «радужных кругов» перед глазами, затуманиванием зрения. Диагностика базируется на проведении ультразвуковой биомикроскопии, классической биомикроскопии с использованием щелевой лампы, скополаминовой пробы, УЗИ, визометрии, тонометрии, периметрии, гониоскопии. Консервативная терапия основывается на применении антиоксидантов, антигипоксантов, гипотензивных средств, витаминов группы В, А, Е.
Общие сведения
Псевдоэксфолиативный синдром впервые был описан финским ученым Дж. Линдбергом в 1917 году. Наблюдается взаимосвязь между развитием болезни и возрастом пациента. В 50-59 лет вероятность возникновения патологии составляет 1-2,5%, в 60-69 лет – 30%, после 70 лет – 42%. Согласно статистическим данным, заболевание диагностируется у 30% россиян старше 50 лет. Риск развития глаукомы у пациентов с псевдоэксфолиативным синдромом равен 64,6%. Патология чаще встречается среди представителей женского пола, однако тяжелее протекает у мужчин. Распространенность наиболее высока в серверных регионах.
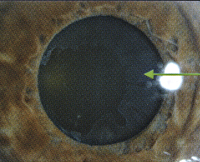
Псевдоэксфолиативный синдром
Причины псевдоэксфолиативного синдрома
Этиология заболевания до конца не изучена. Продолжительное время ученые связывали развитие патологии с изменениями строения эпителия хрусталика, однако диагностика псевдоэксфолиативного синдрома после интракапсулярной экстракции катаракты позволила опровергнуть эту теорию. На сегодняшний день ведущая роль в развитии болезни отводится действию следующих факторов:
- Ультрафиолетовое излучение. Воздействие ультрафиолета индуцирует свободно-радикальное окисление и деструкцию клеточной мембраны. Это влечет за собой атрофию с типичными признаками эксфолиации.
- Травматическое повреждение. Травмы глазного яблока приводят к локальным изменениям, которые у генетически скомпрометированных лиц являются пусковым фактором пигментной дисперсии.
- Внутриорбитальные инфекции. Многие авторы полагают, что поражение глаз обусловлено повышенной проницаемостью гематоофтальмического барьера (ГОБ). Способностью проникать через ГОБ наделена токсоплазма, вирус опоясывающего герпеса и краснухи.
- Нарушения иммунного статуса. В пользу этой этиологической теории псевдоэксфолиативного синдрома свидетельствует обнаружение в слезной жидкости повышенной концентрации интерлейкинов 6, 10, иммуноглобулина класса А и лактоферрина.
- Генетическая предрасположенность. У некоторых пациентов можно установить нарушение экспрессии генов в ядре и митохондриях. Встречаемость ПЭС среди родственников гораздо выше, чем в популяции. Прослеживается аутосомно-доминантный тип наследования.
Ученые полагают, что развитию болезни способствует курение и аутоиммунные патологии. Удается проследить взаимосвязь между возникновением ПЭС и артериальной гипертензией, атеросклерозом, аневризмой аорты в анамнезе. Некоторые исследователи полагают, что данные изменения – это следствие системной васкулопатии, поэтому пациенты с ПЭС часто страдают кардиоваскулярными заболеваниями.
Патогенез
Ключевая роль в механизме развития заболевания отводится образованию и депонированию аномального экстрацеллюлярного микрофибриллярного белка на поверхности передней капсулы хрусталика и радужки, цилиарном теле, цинновых связках, по краю зрачкового отверстия. Реже визуализируются патологические отложения в области передней камеры. Установлено, что белок относится к амилоидоподобной субстанции, за его синтез отвечает пигментный эпителий и меланоциты радужки. Согласно современным представлениям, патогенез ПЭС связан с нарушением эпителио-мезенхимальных взаимоотношений в структурах глазного яблока. Проникновение белковых структур в толщу его оболочек ведет к их дистрофическому перерождению.
Псевдоэксфолиативный синдром принято рассматривать как системное нарушение метаболизма соединительной ткани. Подтверждением этой теории является обнаружение специфических отложений в паренхиматозных органах (печень, почки, сердце, головной мозг) и кожных покровах. Учеными было обнаружено 14 антигенов главного комплекса гистосовместимости (HLA) при наследуемой форме патологии. Прогрессирование заболевания ведет к атрофии пигментной каймы, что проявляется выраженной дисперсией пигмента. Пигментоциты удается обнаружить в УПК и на радужной оболочке. Из-за поражения дренажной сети нарушается отток водянистой влаги с последующим повышением внутриглазного давления.
Классификация
В офтальмологии различают генетически детерминированный и иммуноопосредованный вариант развития. Вне зависимости от патогенеза болезнь всегда возникает в преклонном возрасте. По выраженности дистрофических изменений выделяют следующие степени псевдоэксфолиативного синдрома:
- I – проявляется легкой атрофией радужки. Патологический процесс не распространяется за пределы корня оболочки. Кайма зрачка имеет неравномерную структуру. В области хрусталика определяется маловыраженное наслоение амилоида.
- II – атрофия стромы радужной оболочки умеренная. На поверхности радужки и в зоне УПК выявляются выраженные псевдоэксфолиативные и пигментные отложения.
- III – атрофические изменения резко выражены. Пигментная кайма имеет вид «целлофановой пленки», что обусловлено дисперсией пигмента. Поражение связочного аппарата вызывает подвывих, реже – вывих хрусталика.
Клиническая классификация базируется на результатах ультразвуковой биомикроскопии. Различают следующие стадии патологического процесса:
- I – признаки поражения соответствуют псевдоэксфолиативному синдрому. Удается визуализировать точечные включения в передних отделах глаз.
- II – к вышеописанным изменениям присоединяются начальные признаки повреждения цинновой связки в виде чередования зон истончения с утолщением. Длина волокон разная.
- III – аномальные включения становятся более плотными, провоцируют разрушение связочного аппарата.
- IV – включения объединяются в большие конгломераты, которые приводят к увеличению продольной оси глазного яблока за счет удлинения переднего сегмента.
Симптомы псевдоэксфолиативного синдрома
Для заболевания характерно длительное бессимптомное течение. Вначале поражается один глаз (зачастую левый). Вовлечение второго глазного яблока, как правило, наблюдается спустя 5-10 лет после развития первых симптомов. Жалобы обычно возникают уже после массивного отложения амилоида. Пациенты отмечают появление «помутнений» перед глазами. При взгляде на источник света появляются специфические «радужные круги». Снижение остроты зрения обусловлено поражением хрусталика, повышением ВГД и атрофией сфинктера радужки. Нарушается аккомодационная способность, в дальнейшем расстройства аккомодации сопровождаются затуманиванием зрения, нарушением рефракции. Болевой синдром появляется только при повреждении связочного аппарата.
Заболевание очень медленно прогрессирует. Пациенты часто игнорируют клинические проявления. Помимо жалоб со стороны глаз при отложении белка во внутренних органах возникают симптомы их поражения. При депонировании амилоида в печени отмечается чувство тяжести в правом подреберье, реже – желтушность кожных покровов. Боль в пояснице по типу почечной колики, нарушения мочеиспускания являются типичными признаками скопления белковых масс в паренхиме почек. При распространении патологического процесса в толщу миокарда наблюдается ощущение сдавливания за грудиной, покалывание в области сердца. Доказано, что ПЭС широко распространена среди больных сенильной деменцией, когнитивными расстройствами, хронической ишемией головного мозга, болезнью Альцгеймера.
Осложнения
Отложение белка в толще хрусталиковых масс провоцирует развитие вторичной катаракты ядерного типа, которая зачастую сопровождается слабостью связочного аппарата. Это приводит к тому, что более чем у половины больных катарактой возникает сублюксация, реже – люксация хрусталика. В большинстве случаев патология осложняется офтальмогипертензией. Поражение трабекулярной сети ведет к возникновению псевдоэксфолиативной открытоугольной глаукомы, а с прогрессированием заболевания – к глаукомной оптической нейропатии или слепоте. Поражение мейбомиевых желез становится причиной ксерофтальмии.
Диагностика
Постановка диагноза на доклинической стадии затруднена. Выявить первые признаки можно только при помощи ультразвуковой биомикроскопии. Специфические методы диагностики включают:
- Биомикроскопию глаза. Позволяет визуализировать скопления белого или сероватого оттенка, напоминающи е хлопья на поверхности оболочек переднего отдела органа зрения. Хаотичные скопления пигмента могут формировать веретено Крукенберга. Псевдоэксфолиации по структуре похожи на воспалительные преципитаты.
- Гониоскопию. В передней камере определяются множественные включения, которые на поздних стадиях формируют крупные конгломераты. При нарушении проницаемости гематоофтальмического барьера в водянистой влаге обнаруживается взвесь крови. Объем камеры не изменен.
- Бесконтактную тонометрию. Характерно повышение внутриглазного давления, которое при вторичной глаукоме тяжело поддается снижению медикаментозным путем. При поражении дренажной системы дополнительно проводится электронная тонография.
- УЗИ глаза. При использовании ультразвуковой диагностики можно обнаружить разрыв цинновой связки с возникновением сферофакии. Из-за массивных отложений белка нарушается соотношение размеров переднего и заднего сегментов. Методика также применяется с целью обследования заднего сегмента глаз при снижении прозрачности оптических сред.
- Ультразвуковую биомикроскопию. Дает возможность выявить мелкоточечные включения слабой акустической плотности на оболочках глаза, разницу длины и лизис отдельных волокон цинновой связки.
- Скопаламиновую пробу. При 1 степени при проведении пробы зрачковое отверстие расширяется до 5 мм, при 2 – до 3,5-4 мм. При 3 степени патологии реакция зрачка отсутствует.
- Визометрию. Зрительная дисфункция наблюдается при помутнении оптических сред или вторичной глаукоме. При тяжелом течении острота зрения снижается вплоть до светоощущения.
- Периметрию. Определяется концентрическое сужение поля зрения. В ряде случаев удается диагностировать выпадение отдельных участков из зрительных полей, скотомы.
Пациентам с данной патологией в анамнезе показана консультация невропатолога, ревматолога, кардиолога, гастроэнтеролога, отоларинголога. Необходимость проведения комплексного обследования вызвана системным поражением фиброзной ткани. Часто выявление первых симптомов поражения глаза позволяет диагностировать отложения амилоида в других паренхиматозных органах.
Лечение псевдоэксфолиативного синдрома
Этиотропная терапия псевдоэксфолиативного синдрома не разработана. Цель консервативного лечения – предупредить развитие тяжелых осложнений. На ранних стадиях показано применение:
- Антиоксидантов. Используются лекарственные средства, в состав которых входит супероксиддисмутаза. СОД относится к классу металлопротеидов. Антиоксиданты вызывают разрушение активных форм кислорода, которые оказывают повреждающее влияние на ткани глаза.
- Антигипоксантов. С целью улучшения метаболизма и стимуляции процесса тканевого дыхания применяется цитохром С. Инстилляции препарата способствуют ускорению эпителизации и репарации повреждений структур передних сегментов глаз.
- Гипотензивных средств. Показаны при повышении внутриглазного давления, признаках офтальмогипертензии и начальных стадиях развития псевдоэксфолиативной глаукомы.
- Витаминотерапии. Доказана эффективность применения метилэтилпиридинола (структурный аналог витамина В6), который обладает фибринолитическим и антиоксидантным действием. В окислительно-восстановительных процессах также участвует витамин А (ретинола ацетат) и Е (токоферола ацетат).
При длительном течении патологии целью лечения является устранение или снижение выраженности вторичных осложнений. Медикаментозная терапия псевдоэксфолиативной глаукомы зачастую не оказывает должного эффекта. Возникает необходимость в лазерном или хирургическом вмешательстве. Наиболее целесообразно проведение ранней лазерной трабекулопластики, однако спустя 3-4 года возникают рецидивы повышения ВГД. При выборе метода удаления сублюксированного хрусталика следует отдавать предпочтение факоэмульсификации. Методикой резерва остается экстракапсулярная экстракция.
Прогноз и профилактика
Исход заболевания зависит от степени тяжести, характера поражения структур переднего отдела глаз и типа осложнений. При своевременной диагностике и лечении осложнений прогноз в отношении зрительных функций благоприятный. Возникновение вторичной глаукомы ассоциировано с резистентностью к консервативной терапии и риском необратимой потери зрения. Специфическая профилактика не разработана. Даже при ранних симптомах псевдоэксфолиативного синдрома необходима постановка на диспансерный учет у офтальмолога из-за высокой вероятности развития глаукомы. Показан регулярный контроль внутриглазного давления. Больные должны проходить комплексное офтальмологическое обследование не реже, чем два раза в год.
Источник
Под псевдоэкфолиативным синдромом понимается увеопатия, при которой возникают отложения на передних частях глазного яблока амилоидоподобного вещества. При заболевании возникают нарушения зрения, характерно помутнение и появление кругов.
С целью постановки диагноза применяется классическая и ультразвуковая биомикроскопия, УЗИ, визометрия, скополаминовая проба, периметрия, тонометрия, гониоскопия. Лечение предполагает использование антиоксидантов, витаминных средств, антигипоксантов, а также медикаментов для снижения давления.
Поделиться
Твитнуть
Поделиться
Класснуть
Отправить
Вотсапнуть
Общие сведения
В первый раз данное заболевание было описано в 1917 году учёным Дж. Линдбергом. Существует связь между его появлением и возрастом больного. У лиц до 60 лет вероятность появления болезни составляет 1-2,5%, в 60-69 лет – около 30%, а после 70 лет – 42%.

По статистике псевдоэксфолиативный синдром диагностируется примерно у трети россиян старше 50 лет. У пациентов, страдающих болезнью, риск появления глаукомы составляет 64,6%.
СПРАВКА. Болезнь чаще встречается у женщин, но у мужчин проходит тяжелее. Распространённость выше в северных краях.
Причины
На данный момент происхождение данного заболевания не было изучено в полной мере. Длительное время специалисты связывали его появление с изменениями строения хрусталика, но эта теория была опровергнута. Считается, что к развитию заболевания обычно приводят такие факторы:
- Ультрафиолетовое излучение. Оно способствует окислению свободных радикалов, ввиду чего разрушается клеточная мембрана. Это в свою очередь провоцирует атрофию с характерными для эксфолиации симптомами.
- Травмы глазного яблока. Травмирование провоцирует местные изменения, провоцирующие генетически скомпрометированных лиц пусковой фактор пигментной дисперсии.
- Внутриорбитальные инфекции. Существует мнение, что поражение органов зрения связано с высокой проницаемостью гематоофтальмологического барьера. Проникать сквозь него может токсоплазма, а также такие вирусы, как опоясывающий герпес и краснуха.
- Нарушения иммунитета. Эту теорию подтверждает выявление в слёзной жидкости существенного содержания лактоферина, иммуноглобулина класса А и интерлейкинов 6, 10.
- Наследственная предрасположенность. У ряда пациентов выявляются нарушения экспрессии генов в митохондриях и ядре. Заболевание чаще встречается среди родственников, нежели в популяции. Отмечается аутосомно-доминантный тип.
Факторы риска
По мнению специалистов, к факторам риска относится курение, а также аутоиммунные заболевания. Также отмечается связь между псевдоэкфолиативным синдромом и наличием в анамнезе атеросклероза, аневризмы аорты, артериальной гипертензии.
Некоторые учёные считают причиной таких изменений системную васкулопатию, ввиду чего пациенты, имеющие псевдоэксфолиативный синдром, нередко имеют кардиоваскулярные заболевания.
Патогенез
Основой псевдоэксфолиативных отложений является внеклеточный амилоидоподобный матричный материал, из которого образуются серо-белые гранулы либо фибриллы. Наиболее часто он находится на передней капсуле хрусталика, в радужке, конъюнктиве, в цилиарном теле, зонулярной области либо в передних частях стекловидного тела.

ВНИМАНИЕ! Псевдоэксфолиативный синдром может развиться при эксфолиативной фибропатии, которая проявляется на коже либо внутренних органах. Данный процесс является системным и говорит о дезорганизации.
Классификация
Различают иммунноопосредованный и генетически детерминированный варианты развития синдрома. Независимо от патогенеза псевдоэкфолиатический синдром появляется в пожилом возрасте. В соответствии с тем, насколько выражены дистрофические изменения, выделяются такие степени болезни:
- Первая степень. Возникает легкаяатрофия радужки. Патологические процессы не выходят за границы корня оболочки. Отмечается неравномерная структура каймы зрачка. В зоне хрусталика заметно небольшое наслоение амилоида.
- Вторая степень. Проявляется умеренная атрофия стромы радужки. В области УПК видны существенные пигментные и псевдоэкфолиативные отложения.
- Третья степень. Атрофия выражена резко. Пигментная кайма смотрится как целлофановая плёнка, что связано с дисперсией пигмента. По причине поражения связочного аппарата появляется подвывих или (реже) вывих пигмента.
Основой клинической классификации являются результаты ультразвуковой биомикроскопии. Выделяются такие стадии развития патологии:
- Первая стадия. Симптомы соответствуют псевдоэксфолиативному синдрому. Возможна визуализация точечных включений в передних частях органов зрения.
- Вторая стадия. Указанные вые изменения дополняются начальными симптомами поражения цинновой связки. Последнее проявляется как чередование зон уплощения и истончения. Волокна могут иметь различную длину.
- Третья стадия. Включения уплощаются и приводят к разрушению связочных структур.
- Четвёртая стадия. Включения соединяются между собой. Крупные образования удлиняют передний сегмент, а ввиду этого увеличивается продольная ось яблока глаза.
Симптомы
В течение длительного периода болезнь может никак себя не проявлять. Сначала страдает только один орган зрения (обычно левый). Второй вовлекается в процесс через несколько лет после проявления первичных признаков. Обычно пациент жалуется на симптомы уже тогда, когда возникают серьёзные осложнения амилоида.
Возникают помутнения перед глазами. Когда человек смотрит на источник света, перед глазами возникают цветные круги. Зрение становится менее острым ввиду того, что поражается хрусталик, повышается внутриглазное давление и происходит атрофия сфинктера радужной оболочки.
Происходит нарушение аккомодационной способности. Далее нарушается аккомодация, зрение затуманивается, ухудшается рефракция.

Боль возникает исключительно в том случае, если поражается связочный аппарат.
Болезнь прогрессирует крайне медленно. Нередко пациентами игнорируются симптомы. Кроме жалоб непосредственно на органы зрения возможны расстройства иных органов и систем. Так, может проявиться тяжесть в правом подреберье, иногда возникает желтушность кожи.
При скоплении белковых масс в паренхиме почек появляется боль в пояснице, похожая на почечную колику, нарушается мочеиспускание. Когда деструктивные изменения затрагивают толщу миокарда, человек чувствует давление в грудине и покалывание в сердечной зоне.
Было доказано, что псевдоэксфолиативный синдром широко распространён среди тех, кто страдает когнитивными расстройствами, сенильной деменцией, болезнью Альцгеймера и ишемией головного мозга.
Осложнения
При отложении белка в толще масс хрусталика возникает вторичная катаракта ядерного типа. Она нередко дополняется ослаблением связочного аппарата. Ввиду этого больше половины больных катарактой сталкиваются с сублюксацией, реже – с люксацией хрусталика.
Чаще всего болезнь сопровождается офтальмогипернензией. Также может возникнуть псевдоэкфолиативная открытоугольная глаукома. По мере развития заболевания возможны такие осложнения, как глаукомная оптическая нейропатия либо слепота. При повреждении мейбомиевых желёз развивается ксерофтальмия.
Диагностика
На доклинической стадии поставить диагноз довольно сложно. Определить первые симптомы возможно лишь при применении ультразвуковой биомикроскопии. Специфические способы диагностировать болезнь следующие:
- Биомикроксопия глаза. Даёт возможность визуализировать похожиена хлопья светлые скопления на поверхности оболочек переднего отдела глаза.
- Гониоскопия. Определяет множественные включения в передней камере. В дальнейшем они могут формировать большие конгломераты. В случаенарушения проницаемости гематоофтальмологического барьера в водянистой влаге можно заметить взвесь крови. При этом объём камеры не меняется.
- Бесконтактная тонометрия. При заболевании повышается внутриглазное давление. При возникновении вторичной глаукомы снизить ВГД посредством медикаментов тяжело. В случае поражения дренажной системы показано также проведение электронной томографии.
- УЗИ глаза. При применении диагностики посредством ультразвука возможно выявить разрыв цинновой связки с появлением сферофакии. По причине серьёзных отложений белка происходит нарушение соотношения габаритов заднего и переднего сегментов. Также этот способ используется для осмотра заднего сегмента органов зрения в случае прозрачности оптической среды.
- Ультразвуковая биомикроскопия. Позволяет определить мелкие включения слабой акустической плотности на глазных оболочках. Также выявляет разницу в длине и лизис отдельных волокон цинновой связки.
- Скопаламиновая проба. При первой степени отверстие зрачка расширяется до 5 мм, при второй – до 3,5-4 мм. Если речь идет о третей степени заболевания, реакции со стороны зрачка не будет.
- Визометрия. Дисфункция зрения будет заметна при вторичной глаукоме либо помутнении оптических сред. При серьёзном течении возможно существенное снижение остроты зрения до светоощущения.
- Периметрия. Выявляет концентрическое сужение поля зрения. Иногда получается определить выпадение конкретных участков из зрительных полей либо скотомы.
При наличии данного заболевания в анамнезе также нужно получить консультацию других врачей. Нужно обследовать сердце, опорно-двигательный аппарат, пищеварительную систему, ЛОР-органы. Комплексное обследование требуется по причине системного поражения фиброзной ткани. Нередко первые признаки поражения дают возможность провести диагностику отложений амилоида в иных паренхиматозных структурах.
Лечение
На данный момент специалисты не разработали этиотропного лечения болезни. Консервативные меры лечения направлены на предупреждение опасных осложнений. В начале развития могут быть показаны такие препараты:
- Антиоксиданты. Обычно показаны медикаменты, включающие в себя супероксиддисмутазу. Последняя относится к металлопротеидам. Антиоксиданты способствуют разрушению кислорода в активных формах, что предупреждает негативное влияние на ткани органов зрения.
- Антигипоксанты. Для улучшения обмена веществ и стимуляции дыхания тканей используется цитохром С. Это средство помогает ускоритьэпителизацию и восстановление поражённых структур передних частей глаз.
- Гипотензивные препараты. Назначаются при высоком внутриглазном давлении, симптомах офтальмогипертензиии, а также на начальных этапах развития псевдоэксфолиативной глаукомы.
- Витамины. Нужное действие даёт мелилэтилпиридинол. По структуре это аналогВ6, имеющий антиоксидантное и фибринолитическое свойство. Также в процессах окисления и восстановления принимают участие витамины А и Е.
Если заболевание протекает долго, терапия направлена на борьбу со вторичными осложнениями либо на то, чтобы сделать их менее выраженными.
Нередко медикаментозное лечение заболевания является неэффективным. В таком случае может быть показано хирургическое или лазерное вмешательство. Наилучшим вариантом считается ранняя лазерная трабекулопластика, но через 3-4 года появляются рецидивы повышения внутриглазного давления.
ВНИМАНИЕ! Лучшим методом удаления сублюксированного хрусталика считается факоэмульсификация. Резервная методика — это экстракапсулярная экстракция.
Прогноз
Мнение эксперта
Слонимский Михаил Германович
Офтальмолог высшей квалификационной категории. Имеет огромный опыт диагностики и лечения заболеваний глаз взрослых и детей. Более 20 лет опыта работы.
В данном случае прогноз зависит от уровня тяжести протекания болезни, особенностями повреждения структур и имеющимися осложнениями. Если диагностика будет сделана своевременно, а лечение будет правильным, прогноз благоприятный. В случае появления вторичной глаукомы возможна резистентность к консервативному лечению и риски необратимой утраты зрительной функции.
Профилактика
Как таковой специфической профилактики псевдоэкфолиативного синдрома не существует. Даже при проявлении ранних признаков заболевания нужно стать на учёт у офтальмолога. Это связано с повышенным риском глаукомы. Также важно постоянно контролировать внутриглазное давление. Пациентам рекомендовано прибегать к комплексному обследованию органов зрения не менее, чем раз в полгода.
Заключение
Псевдоэксфолиативный синдром – ещё не до конца изученное заболевание. Поскольку специфическая профилактика болезни отсутствует, очень важно при проявлении первых признаков болезни пройти обследование и своевременно принять меры.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Источник
