Патогенез синдрома обструктивного апноэ сна

Этиология
Во сне закономерно снижается общий мышечный тонус, в частности расслабляются подвижные структуры на уровне глотки. Если имеются предрасполагающие факторы, приводящие к сужению глотки, то может возникнуть храп, обусловленный биением мягкого неба о стенки дыхательных путей. Дальнейшее сужение просвета дыхательных путей может приводить к полному их спадению и развитию эпизода обструктивного апноэ.
Величина просвета верхних дыхательных путей на уровне глотки зависит от исходного внутреннего диаметра, степени снижения давления в просвете во время вдоха и тонуса глоточных мышц во время сна. На рис.1 представлены причины развития патологического сужения и спадения дыхательных путей во время сна.

Рис.1. Причины и механизм обструкции дыхательных путей во сне.
Наиболее частой причиной сужения просвета дыхательных путей на уровне глотки у взрослых является ожирение (рис.2). У пациентов с индексом массы тела (ИМТ), превышающим 29 кг/м2 (ожирение 1 степени и выше), вероятность наличия СОАС в 8-12 раз выше, чем у пациентов без ожирения. У пациентов с ожирением 3 степени (ИМТ>40) тяжелая форма СОАС отмечается более чем в 60% случаев.




А Б
Рис.2.Сагиттальный и поперечный срез головы в норме (А) и у пациента с ожирением и тяжелой формой СОАС (Б). Отложения жира отображаются белым цветом. Магнитно-резонансная томография.
На рис 2Б на сагиттальном срезе отмечается значительное сужение просвета глотки на уровне мягкого неба, корня языка и надгортанника; на поперечном срезе видны значительные отложения висцерального жира рядом с латеральными стенками глотки.
При осмотре у пациентов с ожирением отмечается существенное сужение просвета глотки как за счет отложения жира в самих ее структурах (мягкое небо, небный язычок, боковые дужки), так и сдавления глотки висцеральным жиром преимущественно в области латеральных стенок (рис.3).


А Б
Рис.3. Просвет глотки при визуальном осмотре в норме (А) и при ожирении (Б) (собственные данные).
Увеличение небных миндалин также может приводить к значительному сужению просвета дыхательных путей на уровне глотки и их спадению во время сна (рис.4).



Рис. 4. Гипертрофия небных миндалин 3-й степени (собственные данные).
Основными причинами формирования СОАС у детей являются адено-тонзиллярная гипертрофия, деформации лицевого скелета и ожирение. Важную роль играет аллергический ринит, который рассматривается как самостоятельный фактор риска СОАС у детей. При данном заболевании часто отмечаются хроническая носовая обструкция и аденоиды аллергического или воспалительного генеза. Это обуславливает постоянное дыхание через рот. Впоследствии развивается вторичная гипертрофия небных миндалин. Длительно сохраняющееся ротовое дыхание приводит к формированию у ребенка вытянутого по вертикали лица, маленькой и смещенной назад нижней челюсти (микро- и ретрогнатия), «скученности» зубов, увеличенного с горбинкой носа. Данный характерный вид получил название «птичьего» лица (рис.5).



Рис.5. Пациентка К., 11 лет. Тяжелая форма СОАС (ИАГ 60 в час) (собственные данные).
У пациентки имеется носовая обструкция, обусловленная аденоидами, гипертрофия небных миндалин 3-й степени, «птичье» лицо: выраженная ретро- и микрогнатия, «скученность» зубов, нос с горбинкой.
Если ребенка с хронической носовой обструкцией активно не лечить с самого начала болезни, то сформированные к 10-12 годам дефекты развития лицевого скелета сами по себе будут являться факторами риска развития храпа и СОАС. И даже удаление аденоидов и увеличенных небных миндалин в этом возрасте не всегда даст четкий положительный эффект. У этих пациентов к 25-30 годам могут развиваться умеренные и тяжелые формы СОАС даже без существенного набора массы тела (рис.6).





Рис.6.Пациент С., 34 года. Тяжелая форма СОАС (ИАГ-54 в час), ИМТ -28 (собственные данные).
Пациент с характерным «птичьим» лицом. В анамнезе с детства практически не леченная хроническая носовая обструкция на фоне аллергического ринита, аденоидов и хронического тонзиллита. Аденэктомия не производилась. Тонзиллэктомия в возрасте 18 лет в армии. В 30 лет безуспешное оперативное лечение храпа методом лазерной увулопалатопластики (удаленный небный язычок, рубцовые изменения небных дужек).
Предрасположенность к развитию СОАС у пациентов с гипотиреозом обусловлена набором массы тела, глобальным снижением мышечного тонуса и отеком висцеральных тканей при снижении функции щитовидной железы. При акромегалии у взрослых отмечается непропорциональный рост отдельных органов и, в частности, языка. Это, в свою очередь, обуславливает сужение просвета глотки на уровне корня языка и увеличивает риск развития СОАС .
Нервно-мышечные дистрофические процессы (старение, нейромышечные заболевания, боковой амиотрофический склероз) обуславливают нарушение работы мышц, в частности, отвечающих за поддержание просвета дыхательных путей в открытом состоянии во сне. Это увеличивает риск спадения стенок глотки и развития СОАС.
Алкоголь обладает миорелаксирующим действием и тормозит активность головного мозга, что способствует возникновению храпа и СОАС. Курение также оказывает разноплановое отрицательное воздействие на верхние дыхательные пути, что провоцирует нарушения дыхания во сне.
Следует учитывать, что у одного пациента может сочетаться 2-3-4 различных этиологических фактора СОАС. Это важно учитывать с точки зрения выбора комплексной тактики лечения пациента.
ПАТОГЕНЕЗ
Реализация механизма обструкции дыхательных путей во сне на уровне глотки происходит следующим образом. Человек засыпает. Происходит постепенное расслабление мышц мягкого неба и стенок глотки. Данные структуры начинают вибрировать при прохождении струи воздуха и создавать звуковой феномен храпа. Дальнейшее углубление сна и снижение мышечного тонуса приводит в определенный момент к полному спадению глотки и развитию острого эпизода удушья.
Зона, в которой наступает нарушение проходимости верхних дыхательных путей во время сна, может находиться на уровне мягкого неба, корня языка или надгортанника, то есть в нижней части носоглотки и ротоглотке (рис.1).

Рис.1. Локализация обструкции верхних дыхательных путей во время сна.
При этом дыхательные усилия сохраняются и даже усиливаются в ответ на развивающуюся гипоксемию. Острый недостаток кислорода в артериальной крови приводит к стрессовой реакции, сопровождающейся активацией симпатоадреналовой системы и подъемом АД. В конце концов, негативная информация от различных органов и систем вызывает частичное пробуждение мозга (микроактивацию). Мозг, в свою очередь, восстанавливает контроль над глоточной мускулатурой и быстро открывает дыхательные пути. Человек громко всхрапывает, делает несколько глубоких вдохов. В организме восстанавливается нормальное содержание кислорода, мозг успокаивается и засыпает вновь…цикл повторяется. За ночь может отмечаться до 400-500 остановок дыхания длительностью до минуты и более. В нашей практике максимальная остановка дыхания у пациента составила 3 минуты 10 секунд. При этом сатурация упала ниже 50% и оставалась в этом диапазоне около полутора минут. Интересно отметить, что, по мнению реаниматологов, снижение сатурации ниже 50% в течение 2 минут приводит к смерти коры мозга.
Частые эпизоды удушья и выраженной гипоксемии обуславливают развитие сердечно-сосудистых, метаболических, эндокринных, неврологических и психических нарушений.
Источник
Синдром
обструктивного апноэ сна (СОАГС) – заболевание, которое характеризуется
периодически наступающей остановкой дыхания во сне длительностью более 10
секунд в сочетании с храпом, частыми пробуждениями и выраженной дневной
сонливостью.
- Наши специалисты
Диагностику и лечение нарушений сна проводит Светлана Вострухова, кардиолог-сомнолог, кандидат медицинских наук. Доктор Вострухова — специалист по лечению синдрома апноэ сна, храпа, соннозависимой дыхательной недостаточности, синдрома ожирения-гиповентиляции, бессонницы. Лечение осуществляется в тесном взаимодействии с кардиологами, пульмонологами, эндокринологами, оториноларингологами, неврологами, психотерапевтами, реабилитологами и семейным врачом пациента.
- Механизм СОАС
При СОАС происходит периодическое спадение верхних
дыхательных путей. При этом движения грудной клетки – попытки вдоха – сохраняются.
Дыхание останавливается, уровень кислорода в крови начинает снижаться. Недостаток
кислорода стимулирует дыхательный центр, диафрагма начинает сокращаться чаще и
сильнее, но ее усилий не хватает для того, чтобы преодолеть спадение верхних дыхательных
путей, протянув воздух через «пробку» из мягких тканей. Таким образом, пациенту
нужно сделать еще более сильный вдох, подключив грудные мышцы. Но когда человек
спит, его скелетная мускулатура расслаблена. И для того, чтобы сделать сильный
резкий вдох, необходимо микропробуждение, которое длится 3-4 секунды. Сознание
за это время, как правило, включиться не успевает. До того, как снова
погрузиться в сон, человек успевает сделать несколько глубоких вдохов, уровень
кислорода в крови повышается. Но как только пациент засыпает, у него снова
возникает остановка дыхания, и снова возникает микропробуждение. Таких
микропробуждений у больного с синдромом апноэ сна может быть до сотни за час, и
глубоких фаз сна пациент либо вообще не достигает, либо они продолжаются очень
короткое время. Неудивительно, что пациенты с апноэ просыпаются утром с тяжелой
головой, невыспавшиеся, часто с высоким артериальным давлением, а днем страдают
от сонливости, с которой не могут справиться и засыпают на рабочем месте или,
что много хуже, за рулем.
- Неосложнённый храп
Человек может умеренно храпеть в положении на спине на
протяжении нескольких лет, при этом остановок дыхания во сне нет. Достаточно повернуться
на бок и дальше спокойно спать без храпа. Однако опасен не звуковой феномен
храпа, а то, что за храпом может скрываться. Неосложнённый храп довольно часто
встречается у молодых пациентов и у людей с искривленной носовой перегородкой. Важно
помнить, что неосложнённый храп рано или поздно станет осложненным, то есть
храп является предвестником синдрома апноэ во сне.
- Статистика
Синдром апноэ/гипопноэ сна – довольно распространённое
явление. Каждый третий мужчина старше 60 лет имеет СОАГС. Среди пациентов,
страдающих гипертонической болезнью, не меньше трети больных имеют синдром
апноэ сна. Среди пациентов, чья гипертония плохо поддаётся лечению (особенно ночная
гипертензия), доля апноиков достигает 80%. Более 90% людей с ожирением и индексом
массы тела больше 40 имеют синдром обструктивного апноэ сна средней или тяжёлой
степени.
- Избыточная масса тела
и СОАГС
СОАГС подвержены пациенты с избыточным весом. Объем жировой
клетчатки у таких людей увеличен не только в области живота и бедер, но и в области
лица и шеи, а также в мягком небе, глотке, корне языка. Язык становится больше, мягкое нёбо провисает
ниже, глотка сужается. Когда человек засыпает, мышцы расслабляются. Язык несколько
заваливается в сторону глотки, мягкое нёбо опускается ещё ниже, и происходит
характерное смыкание мягких тканей. На начальных стадиях болезни такое смыкание,
как правило, происходит только в положении лёжа на спине, особенно если немного
запрокинута голова.
В дальнейшем по мере нарастания жировой массы, отёка мягких
тканей ротоглотки, которые каждую ночь бьются и трутся друг о друга, храп
присоединяется и в положении на боку. Если к тому же человек курит, это ещё
больше ухудшает состояние слизистой и ситуацию в целом. СОАС подвержены пациенты
с массивной шеей. Когда объём шеи больше 43 см, это уже повод задуматься.
Нарушения дыхания развиваются у пациента с ожирением и за
счет висцерального («нутряного») жира. Чтобы сделать глубокий вдох, диафрагме
нужно опуститься, но в положении лежа опускаться ей некуда, живот подпирает ее.
Нередко приходится наблюдать, как у больного с выраженным ожирением исходно
нормальное насыщение крови кислородом в положении лежа значительно снижается.
То есть, пока человек стоит или сидит, насыщение крови кислородом (сатурация) близко
к 100%, стоит ему лечь, особенно с низким изголовьем – и мы видим снижение
сатурации на 6-10%, а иногда и более. Как только такой пациент засыпает, на
фоновый дефицит кислорода накладываются провалы сатурации, связанные с
остановками дыхания. Такое состояние называется хронической соннозависимой
гипоксемией.
У мужчин СОАС встречается чаще чем у женщин из-за того, что
у них больше висцерального жира — жира, который скапливается не в
подкожных слоях организма, а вокруг жизненно важных органов брюшной полости. Однако
если женщина набирает вес по андроидному типу – массивное туловище и тонкие
ноги — то риски апноэ у нее эквивалентны риску у мужчины.
- Патология ЛОР-органов
и СОАГС
Синдром апноэ сна встречается и у худых людей. Такие
пациенты чаще становятся клиентами ЛОР-врачей, чем сомнологов. У них, помимо
храпа, часто бывает затруднено носовое дыхание. Кроме того, к апноэ
предрасполагают особенности строения лицевого скелета: при маленькой нижней челюсти,
при изменённой конфигурации верхней челюсти, при «волчьей пасти». Также
способствует появлению апноэ наличие гипертрофии глоточных или нёбных миндалин.
В этом случае тонзиллэктомия или аденотомия могут не только избавить пациента
от очага хронической инфекции, но и решить проблему храпа.
- Если у человека в
наличии два или более из перечисленных ниже симптомов, то это повод заподозрить
апноэ и провести скрининговое обследование
Храп, остановки дыхания во сне (со слов пациента или
родственников), избыточная масса тела, повышенное артериальное давление по
утрам, дневная сонливость, учащенное ночное мочеиспускание, головные боли по
утрам, неосвежающий ночной сон, пересыхание рта и заложенность носа по ночам, ночная
изжога, маленькая нижняя челюсть, или иные особенности строения лицевого
скелета
- Снижение критики к
своему состоянию
Человек, страдающий синдромом обструктивного апноэ сна,
встаёт с тяжёлой головой, постоянно не высыпается. Он засыпает на совещаниях,
засыпает за рулём, тем самым создавая опасную ситуацию на дороге. При этом
пациенты с СОАС сами редко высказывают жалобы. Вследствие того, что треть суток
они находятся в довольно глубокой гипоксии, у них снижается критика к своему
состоянию. Когда врач спрашивает пациента с тяжелым сонным апноэ, беспокоит ли
того дневная сонливость, тот отвечает: «нет», но при этом клюёт носом и почти
засыпает. Поскольку в описанное состояние пациент входит постепенно, в течение
длительного времени, то у него нет никаких маркеров – боли, временной утраты
функции, которые могли бы резко и однозначно заставить пациента озаботиться
своей проблемой. Поэтому нередко пациентов приводят супруги или другие члены
семьи, обеспокоенные, что близкий человек по ночам плохо дышит.
Снижение когнитивных функций при тяжёлых формах СОАГС
затрагивает все сферы жизни, в том числе, хоть и несколько медленнее, профессиональные
навыки. Постепенно больному СОАГС становится всё тяжелей справляться с работой,
его работоспособность снижается. Возникают трудности с концентрацией внимания, ухудшается
память, падает инициативность. Конечно, здесь многое зависит от исходных
характеристик личности. Если человек до СОАГС был активен, его когнитивные
функции будут угасать медленнее, чем у того, кто был более пассивен. Если
вспомнить Илью Ильича, главного героя романа И. Гончарова «Обломов», то он ещё
до развития у него синдрома апноэ сна деятельным человеком не был. Автор романа
гениально описал клинику синдрома апноэ сна у своего героя. Чем дальше, тем более у Обломова
прогрессировала дневная сонливость. Собственно, именно во время послеобеденного
сна его и настиг инсульт. С ним случилось три удара во сне, и последний был
фатальным. Апноэ наложилось на природные особенности его личности и привело к
смерти в возрасте сорока с небольшим лет.
- Главная угроза –
инфаркт и инсульт
Инфаркты и инсульты во время сна – это главная угроза СОАГС.
В практике, увы, встречаются пациенты моложе 40 лет, перенесшие инсульт по
причине апноэ и ставшие инвалидами, а также летальные случаи. Более 80% ночных
инфарктов и инсультов случаются у больных СОАГС, своевременно не обратившихся к
сомнологу и не восстановивших своё дыхание во время сна.
Механизм развития сосудистой катастрофы в этом случае таков:
если дыхание остановится ненадолго, на 10-15 секунд, то давление будет
снижаться – 1 фаза гипоксии. Но если остановка дыхания длится достаточно долго –
30-80 секунд – тогда по мере нарастания гипоксии происходит компенсаторное
повышение артериального давления – 2 фаза гипоксии. Резкий подъём давления во
время сна вызывает перегрузку сосудистого русла, и, соответственно, инфаркты и
инсульты.
Апноэ приводит к нарушению функции сердечного автоматизма, также
связанному с гипоксией. Наиболее часто развиваются ночные брадиаритмии,
мерцание предсердий, преходящие блокады проводящих путей сердца.
- Жалобы пациентов с
СОАГС
СОАГС коварен в первую очередь тем, что это «немое»
заболевание, не вызывающее у пациента явного дискомфорта, а те симптомы,
которые все же беспокоят пациента, он сам объясняет другими причинами. Как
правило, на храп жалуется партнёр пациента по спальне, но не сам больной. Ночные
пробуждения с чувством нехватки воздуха, паническим ужасом, кошмарными
сновидениями больной нередко расценивает как психическое или неврологическое
заболевание и идет на прием к соответствующему специалисту. Учащенное ночной
мочеиспускание заставляет пациента предположить неполадки с мочевым пузырем или
предстательной железой, и он обращается к урологам. Хотя, по сути, в случае с
СОАС позыв к мочеиспусканию – это способ разбудить мозг. В условиях хронической
гипоксии вырабатывается повышенное количество натрийуретического пептида,
который заставляет человека просыпаться. Диагностический критерий таков: если
человек встаёт 3-6 раз за ночь и каждый раз выделяет полный объём мочи, то вероятнее
всего, мы имеем дело с апноэ сна. Если мочи выделяется мало – то это, скорее,
аденома простаты или иные урологические проблемы.
Изжога ночью или утром при пробуждении – симптом, который
ведет пациента к гастроэнтерологу. На самом деле, многократные попытки вдоха
через препятствие сопровождаются усиленными сокращениями диафрагмы и вызывают
заброс кислоты из желудка в пищевод, особенно если пациент накануне плотно
поужинал перед сном. В таких случаях изжога
при пробуждении практически обеспечена.
Часто пациенты с синдромом апноэ сна жалуются на тяжесть в
голове по утрам – именно на тяжесть, как с похмелья, а не на интенсивную
головную боль. В момент пробуждения у человека
с СОАГС нередко наблюдается высокое давление, которое снижается самостоятельно
в течение получаса, без приема лекарств. Также пациенты жалуются на дневную
сонливость и снижение работоспособности. Со всеми этими жалобами пациенты
обращаются, как правило, к терапевту, неврологу, кардиологу, в то время как
нормализация дыхания во время сна решает целый комплекс проблем, экономит
время, деньги, а главное, возвращает здоровье.
- Диагностика СОАС
Ночная мониторная
пульсоксиметрия – скрининговое исследование, которое любой специалист –
терапевт, хирург, невролог, уролог — должен провести пациенту с подозрением на
СОАГС. Исследование можно провести на дому: прибор выдаётся пациенту на ночь, пациент
надевает его самостоятельно и ложится спать в привычных условиях. Прибор
представляет собой браслет с регистрирующим устройством, который надевается на запястье,
и пульсоксиметрический датчик, который надевается на палец. В течение ночи
датчик регистрирует пульс и насыщение крови кислородом. Сомнолог анализирует
полученные данные. Характерными изменениями, которые позволяют заподозрить
апноэ сна у пациента, являются «провалы» насыщения крови кислородом. К примеру,
базовое насыщение крови кислородом у человека составляет 95%, что соответствует
норме. Если врач видит периодические снижения сатурации более, чем на 5%,
вероятнее всего они связаны с нарушениями дыхания во время сна. Если таких
эпизодов выявляется более 30 за час, то у человека достоверно тяжелые нарушения
дыхания во время сна и высокие риски сердечно-сосудистых катастроф.
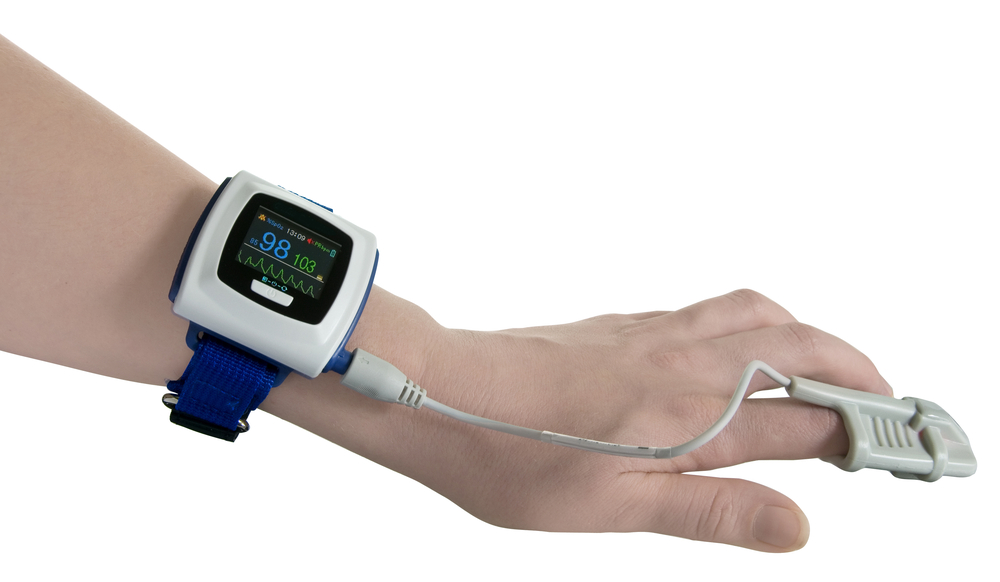
Пульсоксиметр
Полисомнография –
наиболее информативный метод диагностики, позволяющий выявлять не только СОАС,
но и другие болезни сна и неврологические синдромы. Это исследование проводится
в условиях стационара. Во время ночного сна пациенту одновременно выполняются
электроэнцефалография и электромиография, датчики регистрируют положение тела,
дыхательные усилия, движения глаз, скорость воздушного потока при вдохе и
выдохе. Несмотря на обилие датчиков, это относительно комфортное исследование:
во время сна датчики не давят, не издают звуков. Аппаратура не ограничивает
движений, не мешает пойти ночью в уборную.
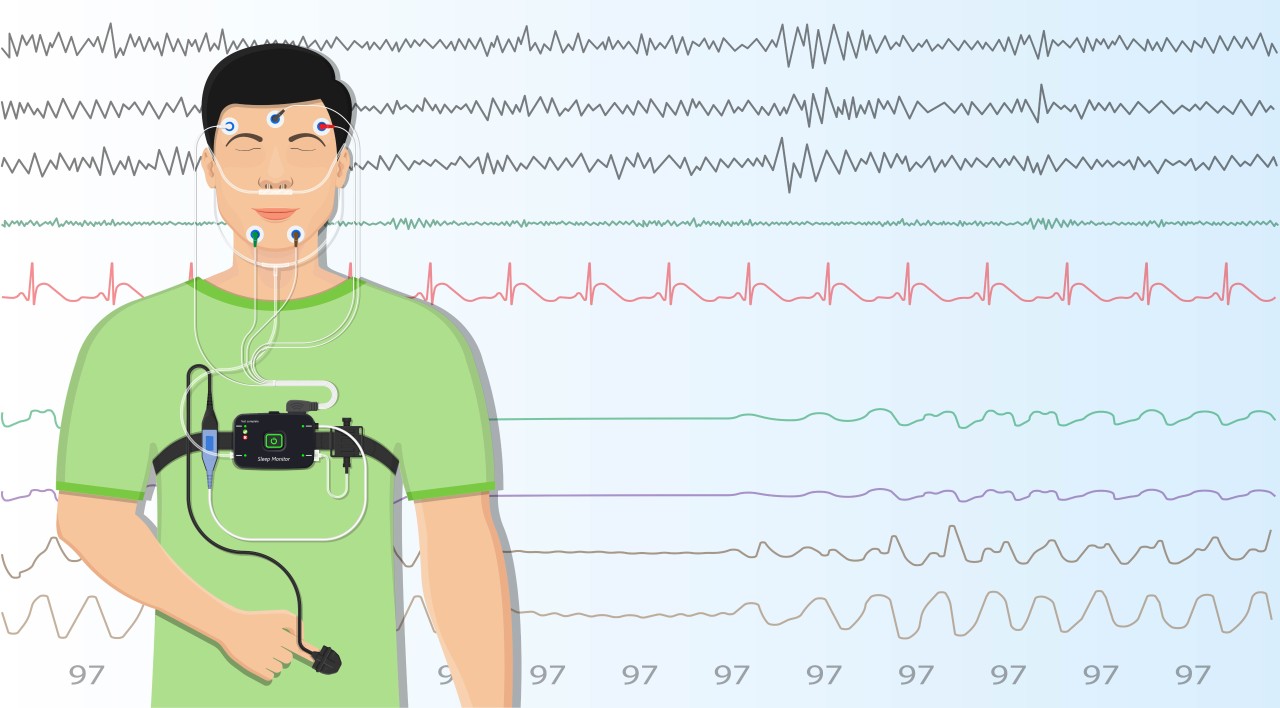
Полисомнография
- СИПАП – дыхательный
протез
На данный момент существует три методики лечения СОАС, доказавшие
свою эффективность. Первая – СИПАП-терапия (от
англ. Constant Positive
Airway Pressure, CPAP). Пациент спит со специальным аппаратом, нагнетающим
воздух в дыхательные пути. Задача – расправить их и не дать тканям спасться. По
сути СИПАП – это дыхательный протез. Современные аппараты достаточно комфортны
и не мешают пациенту спать. Как правило, на адаптацию к СИПАП-терапии нужно 2-3
ночи. Методика наиболее эффективна у пациентов с тяжелыми формами апноэ сна. Когда
пациент с тяжёлым апноэ наконец-то начинает нормально дышать во время сна, он
чувствует, как приятно наутро встать со свежей головой, ни разу не встать ночью
в туалет, не страдать днем от непреодолимой сонливости. Утром у него нормальное
давление и не отёчное лицо. При таком ходе событий пациенту уже не приходится
объяснять, что аппаратом пользоваться нужно, организм сам подскажет решение.

Аппарат СИПАП
Чаще всего спадение мягких тканей происходит на уровне корня
языка, задней стенки глотки и мягкого нёба, реже – на уровне носоглотки или
даже над голосовыми связками. Аппарат автоСИПАП всегда поддерживает положительное
давление воздуха в верхних дыхательных путях, т.е. не даёт тканям спасться. Прибор
нагнетает воздух под более высоким давлением на вдохе и немного сбрасывает
давление на выдохе, что обеспечивает пациенту комфорт во время выдоха.
Для пациентов с морбидным ожирением (хроническое
заболевание, при котором индекс массы тела превышает 40), с обструктивной
болезнью лёгких есть аппараты автоБИПАП (BPAP), которые дают двухуровневую
поддержку: давление вдоха, давление выдоха, а также подъем давления в конце
выдоха для того, чтобы предотвратить обструкцию мелких бронхов. Кроме того, у
некоторых аппаратов автоБИПАП есть функция автоматической вентиляции лёгких: если
у пациента останавливается дыхание несмотря на респираторную поддержку, аппарат
может некоторое время «дышать» за пациента. Для оценки эффективности
СИПАП-терапии проводится контрольная мониторная пульсоксиметрия на фоне
использования СИПАП-аппарата. Некоторые аппараты имеют возможность
подсоединения пульсоксиметрического датчика, либо пульсоксиметрия проводится
параллельно, как правило, на 2-3 ночь пробной СИПАП-терапии. Первая ночь –
адаптационная, поскольку не все пациенты при использовании аппарата сразу
чувствуют себя комфортно. Как правило, ко второй-третьей ночи терапии пациент
уже адаптируется к наличию маски и работе аппарата, и результаты
пульсоксиметрии к этому времени уже получаются достоверные.
- ЛОР-хирургия
При наличии четких показаний проводятся соответствующие
хирургические вмешательства. Это может быть полипэктомия, аденотомия, пластика
мягкого нёба. Если искривление носовой перегородки привело к нарушению носового
дыхания и к храпу – выполняется пластика носовой перегородки. Иногда резекция
нёбного язычка даёт положительный эффект. Следует помнить, что у людей, страдающих ожирением,
этот метод эффективен не более, чем в 30% случаев.
- Внутриротовые
приспособления
Для лечения могут применяться внутриротовые аппликаторы, специальные
капы. Капы удерживают нижнюю челюсть и не дают ей западать назад. Методика
подходит пациентам с нормальной массой тела, маленькой нижней челюстью, при
наличии собственных передних зубов. На импланты капы надевать нельзя, иначе
могут развиться парадонтоз и расшатывание.
Все остальные методы – такие, как фармакологические
средства, сон на боку, а не на спине, наклейки на нос, раскрывающие ноздри –
вполне подходят для лёгких степеней СОАС и для неосложнённого храпа. Но при наличии
тяжелых форм СОАС эти методы малоэффективны.
Источник
