Острый коронарный синдром инфаркт миокарда

Острый коронарный синдром, инфаркт миокарда
(с позиций реаниматолога)
Профессор, академик РАЕН и МАНЭБ Назаров И.П.
Часть 1. Патофизиология, диагностика ОКС
Часть 2. Лечение ОИМ
Часть 3. Агрессивная тактика лечения
Часть 4. Метаболическая терапия ОИМ
Часть 1. Патофизиология, диагностика ОКС
Коронарная болезнь сердца (КБС) протекает с периодами стабильного течения и обострений. Период обострения КБС обозначается как острый коронарный синдром (ОКС). Термин ОКС объединяет инфаркт миокарда (ИМ), включая ИМ без зубца Q, мелкоочаговый, микроинфаркт, и нестабильную стенокардию (НС).
НС и ИМ являются разными клиническими проявлениями единого патофизиологического процесса, а именно тромбоза различной выраженности над надрывом атеросклеротической бляшки или эрозией эндотелия коронарной артерии, и последующих дистальных тромбоэмболий.
ОКС по клиническим и ЭКГ-признакам может быть отнесен к одной из двух форм:
1. ОКС с подъемами сегмента ST
2. ОКС без подъемов сегмента ST
ОКСсподъемамисегментаST – острый процесс ишемии миокарда с болевым синдромом и стойкими подъемами ST или «новой» блокады левой ножки пучка Гиса. СтойкиеподъемыSTотражаютналичиеостройполнойокклюзиикоронарнойартерии. Цельюлеченияявляется быстрое и стойкое восстановление просвета сосуда (тромболитические препараты или ЧТКА и стентирование).
ОКС без подъемов ST – ишемия миокарда достаточной интенсивности и продолжительности, чтобы вызвать некроз миокарда. На начальных ЭКГ нет подъема ST, но, в конце концов, может диагностироваться ИМ без Q. В лечении таких больных тромболитики не эффективны и не используются. Отличается от НС наличием повышения уровней маркеров некроза миокарда.
Нестабильная стенокардия – острый процесс ишемии миокарда, тяжесть и продолжительность которого недостаточны для развития ИМ. Обычно на ЭКГ нет подъемов ST, отсутствует выброс в кровоток биомаркеров некроза миокарда в количествах, достаточных для диагноза ИМ.

Острый инфаркт миокарда
В последние десятилетия ИБС, в частности ОИМ, является основной причиной смертности населения в экономически развитых странах. По данным ВОЗ, ИБС уносит почти 25% жизней из числа всех погибших. В США ежегодно заболевает и внезапно умирает от ОИМ 514 тыс. человек. Все чаще от ОИМ погибают люди молодого возраста (35-44 года). В Москве, среди мужчин в возрасте 50-59 лет показатель смертности от ОИМ и острой коронарной недостаточности (ОКН) составляет 450-600 на 100 тыс. населения.
Общая смертность при ОИМ в первый месяц составляет около 50% и половина этих смертей приходится на первые два часа. По данным Фремингемского исследования, среди лиц с первым сердечным приступом летальный исход наступил у 34%, причем большинство из них умерли в течение первого часа, часто до госпитализации.
До создания блоков интенсивного наблюдения (60-десятые годы) внутрибольничная смертность доходила до 25-30%. Создание палат интенсивного наблюдения позволило снизить смертность сразу на 30% (частота фатального исхода снизилась до 18%). Внедрение в практику тромболитической терапии в 80-е годы позволило снизить летальность от ОИМ ещё на 25%. Смертность в первый месяц несколько снизилась и составляет 13-27%, а в стационарах ведущих клиник мира госпитальная летальность уменьшилась до 5-7%.
Кардиогенный шок остается основной причиной внутрибольничной смертности, который влияет и на отдаленную выживаемость. Потеря более 40% функционирующей массы ЛЖ является основой развития кардиогенного шока. Тромбомболитическая терапия (ТЛТ), чрезкожная транскоронарная ангиоплатика (ЧТКА) и операция аортокоронарного шунтирования (АКШ) позволили снизить летальность при ОИМ. Усовершенствование методов защиты миокарда и вспомогательного кровообращения помогли разработать современную тактику лечения ИМ, осложненного кардиогенным шоком.
Уменьшение зоны ИМ, особенно за счет защиты здорового миокарда в приграничных областях, при таких состояниях, как гипотензия и аритмии, позволяет улучшить результаты не только самого лечения, но также даёт возможность остановить прогрессирование сердечной недостаточности.
Лечение стенокардии
До недавнего времени одной из основных причин смертности от ОИМ были нарушения ритма, в частности первичная фибриляция желудочков. В последние годы в связи с созданием специализированных бригад скорой помощи и ПИТ, широким внедрением кардиомониторинга и дефибрилляторов, частота фибриляции желудочков, как причины смерти, значительно уменьшилась. В связи с этим на первое место вышли острая и хроническая сердечная недостаточность, кардиогенный шок.
Время ишемии у людей определить трудно, вследствие наличия коллатерального кровотока, который в основном и определяет обширность зоны некроза. Однако при аритмиях, гипотонии и при увеличении конечного диастолического давления в ЛЖ, коллатеральный кровоток ухудшается, что может привести к дополнительному некрозу миокардиальной ткани, находящейся в регионе окклюзированной коронарной артерии.
Время реперфузии в первые 6 часов ведет к уменьшению зоны ишемии и в целом улучшает выживаемость (DeWood et al.). Однако агрессивная тактика ведения больных, ИМ у которых развился более чем 6 часов назад, способна приостановить увеличение зоны ишемии после выполнения реперфузии.
Консервативная тактика с применением нитроглицерина и внутриаортальной контрапульсации эффективна у пациентов за счет улучшения кровотока по коронарным артериям и уменьшения работы ЛЖ. В связи с этим, следует учитывать влияние консервативной терапии на формирование окончательной зоны ИМ.
Факторы, влияющие на эволюцию и тяжесть ОИМ:
Анатомия
- Место окклюзии
- Опасные зоны ишемии
- Коллатеральный кровоток
Физиология
- Аритмии
- Давление коронарной перфузии
- Потребление миокардом кислорода
- Реперфузионное повреждение
- Станнированный миокард
Терапевтическая тактика
- Консервативное ведение
- Реваскуляризация
- Тромболитическая терапия
- ЧТКА
- Операция на коронарных артериях
Контролируемая реперфузия
- Кардиоплегический раствор Buckberg и его методика
- Механическая поддержка гемодинамики.
Однако при реперфузии может усиливаться повреждение миокарда, что происходит за счет свободных кислородных радикалов, которые разрушают эндотелиальные клетки и способствуют развитию интерстициального отека. Проводя методы реперфузии, следует учитывать, что восстановление коронарного кровотока при ОИМ закономерно сопровождается нарушениями сердечного ритма («реперфузионный синдром»).
Профилактическое применение антиаритмических препаратов позволяет снизить частоту реперфузионных аритмий в 3,5 раза и предотвратить развитие фатальных аритмий (фибрилляции желудочков). Однако многие антиритмики способны существенно увеличивать процент внезапных асистолий (смотри ниже).
Кардиогенный шок
Клинически проявляется снижением АДс ниже 80 мм.рт.ст., периферической вазоконстрикцией, похолоданием нижних конечностей, изменением сознания, уменьшением выделения мочи (меньше 20 мл/час). Гемодинамическиекритериишока: СИ меньше 1.8 л/мин/м2, УИ меньше 20 мл/м2, ДЗЛА более 18 мм.рт.ст., тахикардия и ОПСС выше 2400 дин/см. Такие пациенты относятся к 4 типу по классификации Killip, наиболее часто исползуемой для определения тяжести и прогноза ИМ.
Классификация Киллипа:
- Класс 1 – без признаков недостаточности кровообращения; смертность 2-6%.
- Класс П – признаки недостаточности кровообращения выражены умеренно (выслушивается ритм галопа, в нижних отделах легких – влажные хрипы); смертность 10-20%.
- Класс Ш – острая левожелудочковая недостаточность (отек легких); смертность 30-40%.
- Класс 1У – кардиогенный шок; смертность более 50%
Ключ к успешной терапии пациентов в шоковом состоянии заключается в рано начатой терапии и выполнении реваскуляризации. Использование метода механической поддержки сердечной деятельности может играть свою роль в лечении и улучшать результат лечения, а также предохранять от развития необратимой полиорганной недостаточности, что может иметь место у больных, долгое время находящихся в состоянии кардиогенного шока.
Пусковым механизмом в генезе кардиогенного шока является ослабление сократительной способности пораженного миокарда и уменьшение УО и МОС. Организм компенсирует эти изменения и поддерживает кровообращение жизненно важных органов за счет тахикардии и спазма периферических сосудов. При первичной недостаточности подобной компенсаторной реакции наблюдается умеренное снижение АД, которое хорошо поддается лечению прессорными аминами.
Умеренное снижение АД может быть обусловлено и рефлекторными нарушениями в результате болевого синдрома. Эффективное устранение боли способствует спонтанному устранению гемодинамических расстройств.
При нарастающей слабости миокарда ПСС значительно усиливается и становится генерализованным. Вазоконстрикции способствует и повышенная активность САС, увеличение концентрации КХ в крови больных ИМ. Выраженные гемодинамические нарушения в подобных случаях обусловлены недостаточностью сократительной способности миокарда, чем объясняется частая неэффективность лечения прессорными аминами.
Как и при шоковых состояниях другой этиологии, в развитии кардиогенного шока большое значение имеют нарушения в системе микроциркуляции. ОПСС при кардиогенном шоке, как правило, повышено. Однако не всегда развитие кардиогенного шока проходит через фазу вазоконстрикции, а изменения в различных сосудистых областях могут быть разнонаправленными.
Изменения общего периферического сопротивления при КШ носят фазовый характер. На ранних этапах ОПС кратковременно снижается, сменяясь в последующем отчетливым повышением. Вероятно, при КШ в фазовости нарушения общего ПСС имеет значение изменение ЦНС и вегетативной нервной системы, уровень гормонов и БАВ. Установлено наличие корреляционной зависимости между тяжестью КШ и степенью повышения ОПСС. Наблюдается резкое его повышение в случаях тяжелого течения шока.
Повышается проницаемость сосудистой стенки, усиливается пропотевание безбелковой части крови из кровеносного русла, возникает гиповолемия. Нарушается перфузия тканей, развивается гипоксия, ацидоз, ишемическая аноксия тканей. Резко возрастает емкость сосудистого русла, кровоток замедляется, происходит стаз крови, её депонирование, изменения реологических свойств крови, повышается вязкость крови, нарастает агрегация форменных элементов, изменяется активность свертывающей и фибринолитической систем крови, повышается концентрация фибриногена, образуются микротромбы.
Кровоток на периферии практически прекращается, происходит сброс крови, минуя капиллярную систему, через артерио-венозные шунты. Развивается тканевая гипоксия с появлением очагов некроза в различных органах. Наступает момент необратимых морфологических изменений в жизненно важных органах. Уменьшается приток венозной крови к сердцу, происходит дальнейшее падение ЦВД, АД, МОС, уменьшается коронарный кровоток, ещё больше ухудшается функциональное состояние сердечной мышцы – возникает порочный замкнутый круг.
Шок может влиять на увеличение зоны ишемии. Трёхсосудистая патология коронарного русла является частой находкой у пациентов с кардиогенным шоком, а увеличение зоны ишемии – очень важный признак, подтверждающий развитие кардиогенного шока. Ограничение зоны ишемии является основным ключом в консервативной и «агрессивной» терапии пациентов с КШ и ИМ.
Недостаточность коронарного кровотока может приводить к появлению одного из трёх типов повреждения миокарда:
- инфаркту,
- гибернации,
- станнированию.
Инфаркт – это состояние необратимой клеточной смерти вследствие длительной ишемии.
Гибернированныймиокард–это обратимое состояние миокардиальной ткани, вторично проявляется угнетением контрактильной функции миокарда вследствие тяжелой ишемии и способен к восстановлению сразу после реваскуляризации.
Станнирование – это полностью обратимый процесс, при условии, что клетки остаются жизнеспособными. Однако дисфункция миокарда, биохимические нарушения и ультраструктурные повреждения продолжают существовать даже после восстановления кровотока.
Станнированный миокард имеет место в участках миокарда, прилежащих к зоне некротической ткани, после длительной окклюзии коронарных артерий и может быть связан с ишемией, спазмом артерий при выполнении кардиоплегии в момент подключения аппарата ИК. Клинически эти участки отечны, местами с кровоизлияниями. В них имеются тригерные зоны, приводящие к развитию аритмий, экстенсии станнированного желудочка и гипотонии с частым развитием инфарктов в данной области.
Механизмы развития контрактильной дисфункции при феномене станнирования миокарда (Bolli):
- Образованиесвободных кислородных радикалов (первично основной механизм появления феномена станирования).
- Несоответствие возбуждение/сокращение, вследствие дисфункции саркоплазматического ретикулума.
- Перегрузка Са.
- Нарушение продукции энергии митохондриями.
- Нарушение потребления энергии миофибриллами.
- Дисфункция симпатической нервной системы.
- Повреждение внеклеточного матрикса.
- Снижение чувствительности миофиламентов к Са.
Существует несколько подходов к лечению этой критической группы пациентов:
- Уменьшение продукции свободных кислородных радикалов должно уменьшить отек и гибель клеток в зоне станнированного миокарда.
- За счет уменьшения интенсивности процессов воспаления у поврежденных эндотелиальных клеток можно замедлить процессы тромбообразования и тем самым усилить восстановительные функции желудочка.
- Когда желудочковая экстрасистолия и ЖТ рецидивирует, несмотря на введение лидокаина, можно использовать электроимпульсную терапию (ЭИТ) или прокаинамид внутривенно болюсно в дозе 1-2 мг/кг с интервалом 5 минут до общей дозы не более 1000 мг, с последующей инфузией 20-80 мкг/кг/мин.
- Профилактическое применение антиаритмических препаратов позволяет снизить частоту реперфузионных аритмий в 3,5 раза и предотвратить развитие фатальных аритмий (фибрилляции желудочков). Однако многие антиритмики способны существенно увеличивать процент внезапных асистолий. Кроме антиритмиков, при синдроме «реперфузии», вероятно, следует применять и антиоксиданты, препараты, уменьшающие ПОЛ и накопление гидроперекисей (токоферол, клофелин, мексидол, предуктал, цитофлавин и др.).
Диагностика ИМ:

Средимногочисленныхинструментальныхметодовисследования ведущееместопринадлежитэлектрокардиографии. Этот метод является незаменимым в диагностике ИБС, ОИМ, нарушений ритма и проводимости, гипертрофии желудочков и предсердий, других заболеваний сердца. В ПИТ как можно раньше следует начать ЭК-скопический мониторинг работы сердца.
ВпервыечасыЭКГчастонеподдаетсяоднозначнойинтерпретацииинаЭКГможетнебытьклассическихпризнаковИМ. Всомнительныхслучаяхбольшеезначениеприобретаетопределениесывороточныхмаркеров, эхокардиографияикоронароангиография.Реже (при так называемой вариантной стенокардии Принцметала) наблюдается смещение сегмента RST выше изолинии, что свидетельствует о развитии трансмуральной ишемии и кратковременного повреждения сердечной мышцы. В отличие от мелкоочагового ИМ смещение сегмента RST и (или) патологические изменения зубца Т исчезают уже через несколько минут или часов после приступа стенокардии.

ЭКГ признаки инфаркта миокарда
БольприИМ отличается интенсивностью и продолжительностью, иногда не снимается повторным введением наркотиков. Характерной особенностью боли при ИМ является выраженнаяэмоциональнаяокраска. Некоторые больные во время приступа испытывают чувство страха, смерти, возбуждены, беспокойны. В дальнейшем обычно развивается резкая слабость.
Могут отмечаться бледность,цианоз,потливость. В самом остром периоде ИМ часто наблюдается брадикардия, которая сменяется нормальной ЧСС илитахикардией. В период болевого приступа АД может кратковременно повышаться. В некоторых случаях оно снижаетсяуже сразу. Проявляется ряд симптомов, обусловленных всасыванием продуктов аутолиза миокарда (резорптивно-некротический синдром). Книмотносятсялихорадка, увеличениечислалейкоцитов, ускорениеСОЭ, атакжеизменениеактивностирядаферментовкрови.
ПриИМпроисходятизменениявкрови, отражающиенарушенияуглеводного, белкового, липидногообмена, кислотно—щелочногосостояния, электролитногобаланса, гормональногопрофиля. Нарушенияуглеводногообмена в острой фазе ИМ проявляются гипергликемией, а иногда и глюкозурией. Повышение сахара в крови связано с активацией САС и надпочечников. Гипергликемия более выражена при обширном ИМ и удерживается 5-10 дней. Нарушениябелковогообмена при ИМ выражаются в увеличении глобулинов и фибриногена. Нередко повышается уровень остаточного азота.
Актуальность ранней и точной диагностики ОИМ не вызывает сомнений. Успешно используют определение в крови больных ряда ферментов. В частности, необходимо определять криатинфосфокиназу (КФК), особенно её МВ-фракцию, в ранние сроки, а также первую фракцию ЛДГ – в более поздние сроки.
Высоко информативен для ОИМ иммуноферментный тест на сердечный Тропанин Т (сТп-Т), белок тропанинового комплекса миокарда. Чувствительность сТп-Т теста превышает КФК-МВ и составляет через 3 часа после приступа 60%, а через 10 часов приближается к 100%. Достоинством сТп-Т является и продолжительное «диагностическое окно» – его концентрация повышается через 2,5 часа от начала приступа и сохраняется до 14-18 дней. Повышение уровня сТп-Т коррелирует с обширностью поражения миокарда (В.В.Родионов с соавт., 1999).
Читать продолжение «Лечение ОИМ»
Читайте также другие работы автора:
Книга «Усмирение боли»
Источник
Острый коронарный синдром — это группа клинических и лабораторно-инструментальных признаков, указывающих на наличие нестабильной стенокардии или инфаркта миокарда. Состояние проявляется загрудинной болью длительностью более 20 минут, которая сопровождается потливостью, одышкой, бледностью кожи. У 15-20% больных наблюдается атипичное клиническое течение синдрома. Для диагностики проводят анализ кардиоспецифических ферментов, регистрируют ЭКГ. Медикаментозное лечение предполагает использование тромболитиков, антиагрегантов и антикоагулянтов, антиангинальных препаратов. В тяжелых случаях показана хирургическая реваскуляризация.
Общие сведения
Острый коронарный синдром (ОКС) является предварительным диагнозом, который устанавливается во время первого обследования пациента врачом-терапевтом. Термин возник в связи с необходимостью выбора лечебной тактики при ургентных состояниях, не дожидаясь постановки окончательного диагноза. ОКС и его осложнения занимают первое место (около 48%) среди всех причин смертности взрослого населения. Неотложное состояние у мужчин в возрасте до 60 лет определяется в 3-4 раза чаще, чем у женщин. В группе пациентов 60-летнего возраста и старше соотношение мужчин и женщин составляет 1:1.
Острый коронарный синдром
Причины
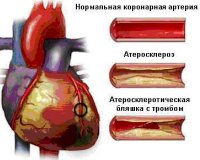
Все нозологические единицы, входящие в состав острого коронарного синдрома имеют общие этиологические факторы. Основной причиной заболевания служит тромбоз коронарного сосуда, возникающий при эрозии или разрыве атеросклеротической бляшки (атеротромбоз). Окклюзия венечной артерии тромбом встречается у 98% больных с выявленной клинической картиной ОКС. При тромбозе развитие коронарного синдрома связано как с механической закупоркой артерии, так и с выделением специфических вазоконстрикторных факторов.
Другая этиология острого процесса определяется крайне редко (около 2% случаев). Появление ОКС возможно при тромбоэмболии либо жировой эмболии коронарной артерии. Еще реже диагностируется переходящий спазм коронарных артерий — вариантная стенокардия Принцметала.
Факторы риска
Поскольку большинство эпизодов связано с атеросклеротическими осложнениями, факторы риска коронарного синдрома идентичны таковым для атеросклероза. Различают:
- Немодифицируемые факторы: мужской пол, пожилой возраст, наследственная предрасположенность;
- Корригируемые факторы: избыточная масса тела, вредные привычки, гиподинамия.
Наибольшую опасность из предпосылок представляет артериальная гипертензия. Повышенное артериальное давление способствует более раннему началу и быстрому прогрессированию атеросклероза.
Патогенез
Патофизиологической основной болезни служит острое снижение кровотока в одном из венечных сосудов. В результате этого нарушается баланс между потребностью мышечных волокон в кислороде и притоком артериальной крови. При остром коронарном синдроме возникает переходящая или стойкая ишемия, которая при прогрессировании вызывает органические изменения миокарда (некрозы, дистрофию).
При разрыве фиброзного покрова атеросклеротической бляшки происходит отложение тромбоцитов и фибриновых нитей — образуется тромб, перекрывающий просвет сосуда. В патогенезе синдрома существенную роль играют гемостатические нарушения, которые обуславливают формирование микротромбов в сосудах, питающих миокард. Выраженная клиническая симптоматика наблюдается при сужении просвета коронарной артерии не менее, чем на 50-70%.
Классификация
В современной кардиологии используется классификация, которая учитывает ЭКГ-проявления коронарного синдрома. Такое разделение патологии наиболее удобно в неотложной ситуации, когда врачу необходимо принимать решение о назначении лекарственной терапии для лечения острого состояния. Согласно этой классификации выделяют 2 формы коронарного синдрома:
- ОКС с подъемом ST (ОКСП ST). При данной форме отмечается стойкая ишемия и полная окклюзия (закрытие просвета) одной из венечных артерий. Состояние соответствует окончательному диагнозу «инфаркт миокарда». Подъем ST выше изолинии на ЭКГ — прогностически неблагоприятный признак.
- ОКС без подъема ST (ОКСБП ST). У таких пациентов начинаются ишемические процессы в миокарде при сохраненном кровотоке в коронарных сосудах. На ЭКГ зачастую определяются патологические изменения зубца T. Такой диагноз соответствует нестабильной стенокардии либо мелкоочаговому инфаркту миокарда без зубца Q.
Симптомы ОКС
Основное проявление острого коронарного синдрома — характерный приступ загрудинной боли. Болевые ощущения локализуются по центру либо с левой стороны грудной клетки. Боль возникает при физической нагрузке (быстрая ходьба, подъем по ступенькам) либо после эмоциональных стрессов. Боли могут быть жгучими, давящими, сжимающими. Типична иррадиация в левую руку, межлопаточную область, шею. Длительность приступа от 20 минут до получаса и более.
На развитие острого кислородного голодания сердечной мышцы указывает учащение и увеличение продолжительности сердечных болей при стабильной стенокардии. При этом снижается эффективность нитроглицерина для купирования острого болевого приступа. Кроме загрудинных болей типична бледность кожных покровов, иногда появляется холодный пот. Беспокоят одышка, резкая слабость и головокружение.
Для молодых (до 40 лет) и пожилых пациентов (старше 75 лет), а также больных сахарным диабетом характерно атипичное течение острого коронарного синдрома. В таких случаях возможны сильные боли в эпигастрии, которые сочетаются с расстройством пищеварения. Реже начинается односторонняя пульсирующая боль в грудной клетке. На фоне острого ухудшения состояния может наступить обморок.
Осложнения
В остром периоде данного состояния существует высокий риск внезапной сердечной смерти: около 7% при ОКС с элевацией сегмента ST, 3-3,5% при коронарном синдроме с нормальным ST. Ранние осложнения выявляются в среднем у 22% пациентов. Наиболее распространенное последствие заболевания — кардиогенный шок, который вдвое чаще диагностируется у мужчин. У больных старше 50 лет, как правило, развиваются тяжелые нарушения ритма и проводимости.
При успешном купировании острого сердечного приступа у 6-10% пациентов сохраняется риск поздних осложнений, которые развиваются спустя 2-3 недели после манифестации синдрома. Вследствие замещения участка мышечных волокон соединительной тканью есть вероятность развития хронической сердечной недостаточности, аневризмы сердца. При сенсибилизации организма продуктами аутолиза возникает синдром Дресслера.
Диагностика
С учетом типичных проявлений острого ангинозного приступа врач-кардиолог может поставить предварительный диагноз. Физикальное обследование необходимо для исключения внесердечных причин боли и кардиальных патологий неишемического происхождения. Для дифференцировки разных вариантов коронарного синдрома и выбора лечебной тактики проводятся три основных исследования:
- Электрокардиография. «Золотым стандартом» диагностики считается регистрация ЭКГ в течение 10 минут от начала острого приступа. Для коронарного синдрома характерна элевация ST более 0,2-0,25 мВ либо его депрессия в грудных отведениях. Первый признак ишемии миокарда — остроконечный высокий зубец Т.
- Биохимические маркеры. Чтобы исключить инфаркт, анализируется содержание кардиоспецифических энзимов — тропонинов I и Т, креатинфосфокиназы-МВ. Наиболее ранним маркером является миоглобин, который повышается уже в первые часы заболевания.
- Коронарная ангиография. Инвазивный метод исследования венечных сосудов используется после выявления подъема сегмента ST на кардиограмме. Коронарография применяется на этапе подготовки к реваскуляризации пораженной тромбом артерии.
После стабилизации состояния и ликвидации острого коронарного синдрома специалист назначает дополнительные методы диагностики. Для оценки риска пациентам с установленным диагнозом ИБС рекомендуют неинвазивные стресс-тесты, которые показывают функциональные возможности сердца. ЭхоКГ выполняют для измерения фракции выброса левого желудочка и визуализации магистральных сосудов.
Лечение острого коронарного синдрома
Консервативная терапия
Лечение больных с ОКС проводится только в специализированных кардиологических стационарах, пациентов в тяжелом состоянии госпитализируют в реанимационные отделения. Терапевтическая тактика зависит от варианта коронарного синдрома. При наличии на кардиограмме подъема ST устанавливают диагноз острого инфаркта миокарда. В таком случае показана интенсивная и тромболитическая терапия по стандартной схеме.
Пациентам, у которых не обнаружено стойкой элевации ST, назначают комбинированную медикаментозную терапию без тромболитиков. Чтобы купировать приступ, используют нитраты. Дальнейшее лечение направлено на ликвидацию ишемических процессов в миокарде, нормализацию реологических свойств крови и коррекцию артериального давления. В этих целях рекомендуется несколько групп лекарственных средств:
- Антиагреганты. Для профилактики тромбообразования принимают препараты на основе ацетилсалициловой кислоты или тиенопиридиновые производные. После начальных нагрузочных доз переходят на длительный прием медикаментов в средних терапевтических дозировках. В первые 2-5 дней схему дополняют антикоагулянтами.
- Антиишемические средства. Для улучшения кровоснабжения сердца и снижения потребности сердечной мышцы в кислороде применяют ряд препаратов: блокаторы кальциевых каналов, нитраты, бета-адреноблокаторы. Некоторые из этих лекарств обладают гипотензивным действием.
- Гиполипидемические препараты. Всем пациентам назначаются статины, которые снижают уровень общего холестерина и атерогенных ЛПНП в крови. Терапия уменьшает риск повторного развития острого коронарного синдрома, значительно улучшает прогноз, продлевает жизнь больных.
Хирургическое лечение
Реваскуляризация миокарда эффективна при инфаркте и рецидивирующей ишемии, рефрактерной к медикаментозной терапии. Методом выбора является малоинвазивная эндоваскулярная ангиопластика, которая быстро восстанавливает кровоток в пораженном сосуде, имеет короткий восстановительный период. При невозможности ее проведения показано коронарное шунтирование.
Прогноз и профилактика
Своевременное начало интенсивной терапии значительно сокращает риск ранних и поздних осложнений, снижает показатель летальности. Прогноз определяется клиническим вариантом острого коронарного синдрома, наличием сопутствующих кардиологических болезней. У 70-80% больных перед выпиской устанавливают низкую или среднюю степень риска, что соответствует сохраненной функции левого желудочка.
Неспецифическая профилактика заболевания включает модификацию факторов риска — нормализацию массы тела, отказ от вредных привычек и жирной пищи. Медикаментозная профилактика повторных эпизодов ОКС включает длительную (более 12 месяцев) антитромбоцитарную терапию и прием липидоснижающих препаратов. Пациенты, перенесшие острый коронарный синдром, находятся на диспансерном учете кардиолога.
Источник
