Общий анализ крови с геморрагическим синдромом это
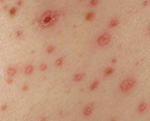
Геморрагическая болезнь новорожденных — патология неонатального периода, которая проявляется избыточной кровоточивостью, возникающей на фоне дефекта в работе факторов свертывания крови. Напрямую связана с дефицитом витамина К в организме ребенка.
Классификация
Современная классификация выделяет три формыгеморрагической болезни новорожденных, отличающиеся как предрасполагающими факторами, так и временем возникновения:
ранняя форма развивается в первые 24 часа на фоне изначально недостаточного уровня витамина К у ребенка;
классическая форма выявляется в первую неделю жизни и развивается в связи с недостаточным поступлением витамина К с грудным молоком, а также отсутствием нормальной флоры для его синтеза;
поздняя форма проявляется в период с 2 по 12 неделю жизни ребенка и чаще всего развивается на фоне вторичных патологий, приводящих к нарушению образования факторов свертывания крови.
Формы геморрагической болезни отличаются не только причинами формирования, но и клиническими проявлениями. Также различается прогноз заболевания.
Геморрагическая болезнь новорожденных, нахождение ребенка в кювезе
Причины развития
Геморрагическая болезнь новорожденных, помимо нехватки витамина К, может развиваться на фоне следующих состояний:
нехватка альфа-1 антитрипсина;
гепатит;
недоразвитие желчевыводящих путей;
муковисцидоз;
целиакия;
дисбактериоз.
Факторами риска могут служить:
- гестоз;
гипоксия и асфиксия плода;
родовая травма;
недоношенность;
отсутствие грудного вскармливания;
проведение парентерального питания;
антибиотикотерапия.
Вышеуказанные состояния опосредованно ведут к нарушению образования факторов свертывания крови, что приводит к формированию позднего варианта геморрагической болезни. Основными факторами развития классической формы заболевания в большей мере является неправильное грудное вскармливание или же его отсутствие.
Зачем нужен витамин К?
Витамин К в человеческом организме принимает участие в ряде физиологических процессов:
образование факторов свертывания крови;
участие в обмене кальция;
укрепление сосудов.
В том случае, если в организме отмечается избыток данного вещества, наблюдаются следующие нарушения:
повышение вязкости крови;
усиление риска формирования тромбов;
утолщение сосудистой стенки.
Поэтому избыточное потребление витамина К не рекомендуется тучным людям, варикозным больным и тем, кто страдает от мигреней.
Факторы риска
Предположить возможное развитие заболевания можно у тех детей, для которых характерно наличие одного или нескольких факторов риска. К таковым можно отнести:
применение во время беременности препаратов из группы неодикумарина;
беременность на фоне гестоза;
асфиксия плода;
роды путем кесарева сечения;
недостаточное грудное вскармливание;
недоношенность;
использование антибактериальных препаратов в течение длительного времени;
наличие патологий печени.
Изучение факторов риска необходимо для своевременной диагностики заболевания. Их устранение позволяет значительно снизить вероятность формирования патологии.
Клиническая картина
Симптомы заболевания напрямую зависят от его формы. Так, для раннего варианта геморрагической болезни характерны следующие проявления:
мелена — черный полужидкий стул;
кефалогематомы — особые кровоизлияния на голове;
геморрагическая сыпь;
кровотечение в легких;
- гематемезис — кровавая рвота.
Самым главным проявлением, в свою очередь, является начало заболевания в первые сутки жизни ребенка. Классический вариант геморрагической болезни характеризуется следующими симптомами:
возникновение кровотечений со 2 по 7 день жизни;
длительное кровотечение после отпадения пуповины;
рвота с кровью;
кровоизлияния в головной мозг.
Поздний вариант заболевания, возникающий после 14 дней жизни, протекает с таким грозным осложнением, как геморрагический шок. Также при данном варианте течения болезни возможно выявление следующих симптомов:
частые внутричерепные кровоизлияния;
экхимозы;
после инъекций отмечаются длительные кровотечения.
За несколько дней до появления первого внутричерепного кровоизлияния на коже или слизистых оболочках появляются характерные геморрагические высыпания. Чаще всего они локализуются в области нижних конечностей.
Витамин К2 продуцируется бактериями нормальной микрофлоры кишечника. Поэтому при дисбактериозе может отмечаться значительный дефицит данной формы витамина.
Предшественником внутричерепного кровоизлияния является внезапный, болезненный, однако непродолжительный плач. Сразу после этого начинается рвота. В некоторых случаях в рвотных массах может присутствовать кровь. Постепенно дети становятся апатичными и не реагируют на воздействие извне. Возможно развитие судорожного синдрома. Таким образом, клиническая картина заболевания достаточно разнообразна, однако самым главным проявлением являются частые кровотечения.
Лабораторные и инструментальные исследования
Для точной диагностики заболевания, а также своевременного выявления осложнений и начала лечебных мероприятий, могут быть назначены следующие исследования:
общий анализ крови;
коагулограмма;
нейросонография;
УЗИ;
- МРТ/КТ.
В коагулограмме отмечается удлинение протромбинового времени, а также активированного частичного тромбопластинового времени. Тромбиновое время при этом остается в пределах нормы. В общем анализе крови будет снижен общий уровень тромбоцитов. Нейросонография и УЗИ нужны при подозрении на наличие нарушений в работе внутренних органов. МРТ и КТ применяются не всегда и в основном нужны для определения локализации кровоизлияния. Однако их проведение очень затруднено на фоне тяжелого состояния детей.
Коагулограмма при поздней форме геморрагической болезни
Дифференциальная диагностика
Геморрагический синдром может выявляться на фоне ряда заболеваний, с которыми специалистам приходится проводить дифференциальную диагностику при подозрении на геморрагическую болезнь. К таким состояниям можно отнести:
гемофилии;
коагулопатии на фоне тяжелых патологий печени, сочетанных с холестазом;
синдром Вискотта-Олдрича;
тромбоцитопатии;
ДВС-синдром.
Поскольку одним из проявлений заболевания является мелена, необходимо исключить «синдром проглоченной крови». Для этого проводится так называемая проба Апта-Даунера, основанная на выявлении материнского гемоглобина. Если вместо него в анализе обнаруживается гемоглобин ребенка, это свидетельствует о мелене. В целом при дифференциальной диагностике не должно возникать никаких сложностей из-за характерной клинической картины геморрагической болезни.
Лечение
Главными целями лечения геморрагической болезни являются остановка кровотечения и стабилизация общего состояния ребенка. Терапия исключительно медикаментозная. Существуют клинические рекомендации по ведению ребенка с данной патологией. Можно выделить определенные моменты неотложной помощи при геморрагической болезни:
если у новорожденного имеются нарушения гемостаза, однако ему не был введен витамин К во время рождения, рекомендуется немедленно ввести стартовую дозу витамина;
если в коагулограмме отмечается повышение АЧТВ и протромбинового времени, необходимо внутривенно ввести свежезамороженную плазму;
если эффекта после введения плазмы не отмечается, использовать криопреципитат;
- повторная коагулограмма;
если сохраняются нарушения работы системы свертывания, повторить введение криопреципитата.
Стоит отметить, что анализы необходимо сдавать 2 раза в сутки. Кроме того, специалисты рекомендуют показать ребенка гематологу. Также необходимо определить причину, которая привела к коагулопатии. В некоторых случаях это может быть сепсис или гипоксическое повреждение. Очень важно не допустить формирования внутричерепного кровоизлияния. Для этого нужно еще на стадии появления сыпи госпитализировать ребенка в реанимационное отделение.
При использовании препаратов витамина К важно помнить, что высокие дозы, а также продолжительное применение могут привести к формированию гипербилирубинемии. Даже при правильно подобной дозировке усиливается гемолиз и повышается уровень билирубина.
Профилактическое введение витамина К беременной во время родов или до них считается неэффективным и не отменяет профилактики в период новорожденности.
В том случае, если на фоне заболевания отмечается развитие гиповолемического шока, после того как было проведено переливание свежезамороженной плазмы, необходима инфузионная терапия, а затем, при наличии показаний, переливание эритроцитарной массы.
Витамин К — основная клиническая рекомендация в профилактике геморрагической болезни
Профилактика
Основным профилактическим мероприятием по предотвращению развития заболевания является внутримышечное введение витамина К. Во многих странах эта процедура проводится всем детям после рождения. Однако отечественные специалисты рекомендуют проведение профилактики только детям из группы риска.
Геморрагическая болезнь новорожденных — тяжелое состояние неонатального периода, которое при отсутствии лечения может закончиться летальным исходом. Профилактическое введение витамина К после рождения ребенка значительно снижает вероятность развития данного заболевания.
Смотрите также: свиной грипп у детей
Источник
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 30 декабря 2019;
проверки требует 1 правка.
Постгеморрагическая анемия — развивается после кровопотери. Постгеморрагические анемии подразделяются на острые и хронические. Острая постгеморрагическая анемия развивается после обильных, остро возникающих кровотечений(кровотечение органов) Хронические постгеморрагические анемии развиваются после длительных необильных кровотечений(язвы).
История заболевания[править | править код]
Этиология[править | править код]
- травмы
- геморрагические заболевания (тромбоцитопатии, коагулопатии, ДВС-синдром, геморрагический васкулит, лейкозы, апластические анемии, дизовариальные меноррагии у девушек).
- легочное кровотечение, ЖК кровотечения
Патогенез[править | править код]
При быстрой кровопотере уменьшается объём циркулирующей крови (олигемическая фаза). В ответ на уменьшение объёма циркулирующей крови возникает компенсаторная реакция : возбуждение симпатического отдела нервной системы и рефлекторный спазм сосудов, артериально-венозное шунтирование, что первоначально способствует поддержанию артериального давления, адекватному венозному притоку и сердечному выбросу. Пульс ускорен и ослаблен. Максимально сужены сосуды в коже и мышцах, минимально — сосуды мозга, коронарные, что обеспечивает лучшее кровоснабжение жизненно-важных органов. С продолжением процесса начинаются явления постгеморрагического шока.
Клиника[править | править код]
При постгеморрагической анемии клинически на первый план выходят явления острой сосудистой недостаточности вследствие резкого опустошения сосудистого русла (гиповолемии): — это сердцебиение, одышка, ортостатический коллапс. Тяжесть состояния определяется не только количеством, но и скоростью кровопотери. Наблюдается снижение диуреза соответственно степени кровопотери. Уровень гемоглобина и количество эритроцитов не являются надежным критерием степени кровопотери.
В первые минуты содержание Hb из-за уменьшения ОЦК может быть даже высоким. При поступлении тканевой жидкости в сосудистое русло эти показатели снижаются даже при прекращении кровотечения. Цветовой показатель, как правило, нормален, так как происходит одновременная потеря и эритроцитов и железа, то есть анемия нормохромная. На вторые сутки увеличивается количество ретикулоцитов, достигающее максимума на 4 — 7 день, то есть анемия является гиперрегенераторной.
Диагностика[править | править код]
В диагностике постгеморрагической анемии учитывают сведения о произошедшей острой кровопотере при внешнем кровотечении; в случае массивного внутреннего кровотечения диагноз основывается на клинических признаках в сочетании с лабораторными пробами (Грегерсена, Вебера), повышении уровня остаточного азота при кровотечении из верхних отделов желудочно-кишечного тракта.
При внешнем кровотечении диагноз поставить несложно. При внутреннем кровотечении из органа надо исключать коллапс иного генеза.
Лечение[править | править код]
Самое главное — устранить источник кровотечения. Затем восполняют кровопотерю (в зависимости от степени тяжести анемии — эритроцитарная масса, на фоне введения гепарина). Общий объём гемотрансфузии не должен превышать 60 % дефицита объёма циркулирующей крови. Остальной объём восполняется кровезаменителями (5 % раствором альбумина, реополиглюкином, раствором Рингера и т. д.). Пределом гемодилюции считают гематокрит 30 и эритроциты более
3*10¹²/л. По окончании острого периода необходимо лечение препаратами железа, витаминами группы В, С, Е.
После ликвидации анемии препараты железа назначают в половинной дозе до 6-ти месяцев.
Прогноз[править | править код]
Прогноз зависит от причины кровотечения, скорости, объёма кровопотери, рациональной терапии. При кровопотере с дефицитом объёма циркулирующей крови более 50 % прогноз неблагоприятный.
См. также[править | править код]
- Анемия
- Кровотечение
Примечания[править | править код]
Ссылки[править | править код]
- Постгеморрагические анемии
- Неотложная помощь при постгеморрагической анемии
Литература[править | править код]
- У. Россе, Ф. Бонн. ГЕМОЛИТИЧЕСКИЕ И ОСТРАЯ ПОСТГЕМОРРАГИЧЕСКАЯ АНЕМИИ. From Harrison’s Principles of Internal Medicine. 14-th edition.
- Н. Н. Зайко, Ю. В. Быць, А. В. Атаман и др. К.: «Логос», 1996 Патологическая физиология
Источник

Геморрагическая лихорадка с почечным синдромом — зоонозная хантавирусная инфекция, характеризующаяся тромбогеморрагическим синдромом и преимущественным поражением почек. Клинические проявления включают острую лихорадку, геморрагическую сыпь, кровотечения, интерстициальный нефрит, в тяжелых случаях — острую почечную недостаточность. К специфическим лабораторным методам диагностики геморрагической лихорадки с почечным синдромом принадлежат РИФ, ИФА, РИА, ПЦР. Лечение заключается во введении специфического иммуноглобулина, препаратов интерферона, проведении дезинтоксикационной и симптоматической терапии, гемодиализа.
Общие сведения
Геморрагическая лихорадка с почечным синдромом (ГЛПС) — природно-очаговое вирусное заболевание, характерными признаками которого являются лихорадка, интоксикация, повышенная кровоточивость и поражение почек (нефрозонефрит). На территории нашей страны эндемичными районами являются Дальний Восток, Восточная Сибирь, Забайкалье, Казахстан, европейская территория, поэтому ГЛПС известна под различными названиями: корейская, дальневосточная, уральская, ярославская, тульская, закарпатская геморрагическая лихорадка и др. Ежегодно в России регистрируется от 5 до 20 тыс. случаев заболеваний геморрагической лихорадкой с почечным синдромом. Пик заболеваемости ГЛПС приходится на июнь-октябрь; основной контингент заболевших (70-90%) составляют мужчины в возрасте 16-50 лет.
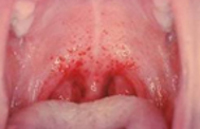
Геморрагическая лихорадка с почечным синдромом
Причины ГЛПС
Возбудителями болезни являются РНК-содержащие вирусные агенты рода Hantavirus (хантавирусы), относящиеся к семейству Bunyaviridae. Для человека патогенны 4 серотипа хантавирусов: Hantaan, Dubrava, Puumala, Seoul. Во внешней среде вирусы относительно долго сохраняют стабильность при отрицательной температуре и малоустойчивы при температуре 37°C. Вирусы имеют сферическую или спиральную форму, диаметр 80-120 нм; содержат одноцепочечную РНК. Хантавирусы обладают тропностью к моноцитам, клеткам почек, легких, печени, слюнных желез и размножаются в цитоплазме инфицированных клеток.
Переносчиками возбудителей геморрагической лихорадки с почечным синдромом служат грызуны: полевые и лесные мыши, полевки, домовые крысы, которые инфицируются друг от друга через укусы клещей и блох. Грызуны переносят инфекцию в форме латентного вирусоносительства, выделяя возбудителей во внешнюю среду со слюной, фекалиями и мочой. Попадание инфицированного выделениями грызунов материала в организм человека может происходить аспирационным (при вдыхании), контактным (при попадании на кожу) или алиментарным (при употреблении пищи) путем. К группе повышенного риска по заболеваемости геморрагической лихорадкой с почечным синдромом относятся сельскохозяйственные и промышленные рабочие, трактористы, водители, активно контактирующие с объектами внешней среды. Заболеваемость человека напрямую зависит от численности инфицированных грызунов на данной территории. ГЛПС регистрируется преимущественно в виде спорадических случаев; реже – в виде локальных эпидемических вспышек. После перенесенной инфекции остается стойкий пожизненный иммунитет; случаи повторной заболеваемости единичны.
Патогенетическую сущность геморрагической лихорадки с почечным синдромом составляют некротизирующий панваскулит, ДВС-синдром и острая почечная недостаточность. После заражения первичная репликация вируса происходит в эндотелии сосудов и эпителиальных клетках внутренних органов. Вслед за накоплением вирусов наступает вирусемия и генерализация инфекции, которые клинически проявляются общетоксическими симптомами. В патогенезе геморрагической лихорадки с почечным синдромом большую роль играют образующиеся аутоантитела, аутоантигены, ЦИК, оказывающие капилляротоксическое действие, вызывающие повреждение стенок сосудов, нарушение свертываемости крови, развитие тромбогеморрагического синдрома с повреждением почек и других паренхиматозных органов (печени, поджелудочной железы, надпочечников, миокарда), ЦНС. Почечный синдром характеризуется массивной протеинурией, олигоанурией, азотемией, нарушением КОС.
Симптомы ГЛПС
Геморрагическая лихорадка с почечным синдромом характеризуется циклическим течением с последовательной сменой нескольких периодов:
- инкубационного (от 2-5 дней до 50 суток — в среднем 2-3 недели)
- продромального (2-3 дня)
- лихорадочного (3-6 дней)
- олигоурического (с 3-6-го по 8-14-й день ГЛПС)
- полиурического (с 9-13 дня ГЛПС)
- реконвалесцентного (раннего – от 3-х недель до 2 месяцев, позднего — до 2-3-х лет).
В зависимости от выраженности симптомов, тяжести инфекционно-токсического, геморрагического и почечного синдромов различают типичные, стертые и субклинические варианты; легкие, среднетяжелые и тяжелые формы геморрагической лихорадки с почечным синдромом.
По истечении инкубационного периода наступает короткий продромальный период, во время которого отмечаются утомляемость, недомогание, головные боли, миалгии, субфебрилитет. Лихорадочный период развивается остро, с повышения температуры тела до 39-41°С, озноба и общетоксических симптомов (слабости, головной боли, тошноты, рвоты, расстройства сна, артралгии, ломоты в теле). Характерны боли в глазных яблоках, затуманенное зрение, мелькание «мушек», видение предметов в красном цвете. В разгар лихорадочного периода появляются геморрагические высыпания на слизистых оболочках полости рта, коже грудной клетки, подмышечных областей, шеи. При объективном осмотре выявляется гиперемия и одутловатость лица, инъекция сосудов конъюнктив и склер, брадикардия и артериальная гипотония вплоть до коллапса.
В олигоурический период геморрагической лихорадки с почечным синдромом температура тела снижается до нормы или субфебрильных цифр, однако это не приводит к улучшению состояния пациента. В эту стадию еще более усиливаются симптомы интоксикации и возникают признаки поражения почек: нарастают боли в пояснице, резко снижается диурез, развивается артериальная гипертензия. В моче выявляется гематурия, протеинурия, цилиндрурия. При нарастании азотемии развивается ОПН; в тяжелых случаях — уремическая кома. У большинства больных отмечается неукротимая рвота и диарея. Геморрагический синдром может быть выражен в различной степени и включать в себя макрогематурию, кровотечения из мест инъекций, носовые, маточные, желудочно-кишечные кровотечения. В олигоурический период могут развиваться тяжелые осложнения (кровоизлияния в головной мозг, гипофиз, надпочечники), служащие причиной летального исхода.
Переход геморрагической лихорадки с почечным синдромом в полиурическую стадию знаменуется субъективными и объективными улучшениями: нормализацией сна и аппетита, прекращением рвоты, исчезновением боле в пояснице и т. д. Характерными признаками данного периода служит увеличение суточного диуреза до 3-5 л и изогипостенурия. В период полиурии сохраняется сухость во рту и жажда.
Период реконвалесценции при геморрагической лихорадке с почечным синдромом может затягиваться на несколько месяцев и даже лет. У больных долго сохраняется постинфекционная астения, характеризующаяся общей слабостью, снижением работоспособности, быстрой утомляемостью, эмоциональной лабильностью. Синдром вегетативной дистонии выражается гипотонией, инсомнией, одышкой при минимальной нагрузке, повышенной потливостью.
Специфическими осложнениями тяжелых клинических вариантов ГЛПС могут являться инфекционно-токсический шок, кровоизлияния в паренхиматозные органы, отек легких и головного мозга, кровотечения, миокардит, менингоэнцефалит, уремия и др. При присоединении бактериальной инфекции возможно развитие пневмонии, пиелонефрита, гнойных отитов, абсцессов, флегмон, сепсиса.
Диагностика ГЛПС
Клиническая диагностика ГЛПС основывается на цикличности течения инфекции и характерной смене периодов. При сборе эпидемиологического анамнеза обращается внимание на пребывание пациента в эндемичной местности, возможный прямой или косвенный контакт с грызунами. При проведении неспецифического обследования учитывается динамика изменения показателей общего и биохимического анализа мочи, электролитов, биохимических проб крови, КОС, коагулограммы и др. С целью оценки тяжести течения и прогноза заболевания выполняется УЗИ почек, ФГДС, рентгенография органов грудной клетки, ЭКГ и др.
Специфическая лабораторная диагностика геморрагической лихорадки с почечным синдромом проводится с помощью серологических методов (ИФА, РНИФ, РИА) в динамике. Антитела в сыворотке крови появляются в конце 1-ой недели болезни, к концу 2-й недели достигают максимальной концентрации и сохраняются в крови 5–7 лет. РНК вируса может быть выделена с помощью ПЦР-исследования. ГЛПС дифференцируют с лептоспирозом, острым гломерулонефритом, пиелонефритом и энтеровирусной инфекцией, прочими геморрагическими лихорадками.
Лечение ГЛПС
Больные геморрагической лихорадкой с почечным синдромом госпитализируются в инфекционный стационар. Им назначается строгий постельный режим и диета №4; проводится контроль водного баланса, гемодинамики, показателей функционирования сердечно-сосудистой системы и почек. Этиотропная терапия геморрагической лихорадки с почечным синдромом наиболее эффективна в первые 3-5 суток от начала заболевания и включает введение донорского специфического иммуноглобулина против ГЛПС, назначение препаратов интерферона, противовирусных химиопрепаратов (рибавирина).
В лихорадочном периоде проводится инфузионная дезинтоксикационная терапия (внутривенные вливания глюкозы и солевых растворов); профилактика ДВС-синдрома (введение препаратов-дезагрегантов и ангиопротекторов); в тяжелых случаях применяются глюкокортикостероиды. В олигурическом периоде осуществляется стимуляция диуреза (введение ударных доз фуросемида), коррекция ацидоза и гиперкалиемии, профилактика кровотечений. При нарастающей ОПН показано переведение пациента на экстракорпоральный гемодиализ. При наличии бактериальных осложнений назначается антибиотикотерапия. В полиурическую стадию основной задачей является проведение оральной и парентеральной регидратации. В период реконвалесценции проводится общеукрепляющая и метаболическая терапия; рекомендуется полноценное питание, физиотерапия (диатермия, электрофорез), массаж и ЛФК.
Прогноз и профилактика ГЛПС
Легкие и среднетяжелые формы геморрагической лихорадки с почечным синдромом в большинстве случаев заканчиваются выздоровлением. Резидуальные явления (постинфекционная астения, боли в пояснице, кардиомиопатия, моно- и полиневриты) длительно наблюдаются у половины переболевших. Реконвалесценты нуждаются в ежеквартальном диспансерном наблюдении инфекциониста, нефролога и окулиста на протяжении года. Тяжелое течение сопряжено с высоким риском осложнений; смертность от ГЛПС колеблется в пределах 7-10%.
Профилактика геморрагической лихорадки с почечным синдромом заключается в уничтожении мышевидных грызунов в природных очагах инфекции, предупреждении загрязнения жилищ, водоисточников и продуктов питания выделениями грызунов, дератизации жилых и производственных помещений. Специфической вакцинации против ГЛПС не разработано.
Источник
