Оап код по мкб
Откры́тый артериа́льный прото́к (ОАП) — врождённый порок сердца, при котором артериальный проток новорождённого (Боталлов проток) не зарастает после рождения. Относится к белым порокам. Ранние симптомы встречаются редко, но в первый год жизни могут наблюдать усиление работы дыхания и плохой набор веса. С возрастом ОАП может привести к остановке сердца, при отсутствии коррекционной терапии.
Этиология[править | править код]
Открытый артериальный проток может быть идиопатическим (то есть без установления причины) или вторичным по отношению к другим состояниям. К предрасполагающим факторам относят:
- Недоношенность
- Синдром врождённой краснухи
- Хромосомные заболевания, например синдром Дауна
Закрытие артериального протока в норме[править | править код]
У развивающегося плода артериальный проток соединяет лёгочную артерию и аорту, что позволяет снабжать наполненные жидкостью сжатые лёгкие плода оксигенированной кровью из правого желудочка и при этом не перегружать его. В период внутриутробного развития, этот шунт защищает правый желудочек от перегрузок путём сброса избыточной крови (которая не может пройти в легочные артерии из-за высокого сопротивления в сжатых лёгких) в аорту в обход малого круга кровообращения. Внутриутробное закрытие этого протока может привести к правожелудочковой недостаточности.
Когда новорождённый делает свой первый вдох, лёгкие расправляются и сопротивление сосудов лёгких уменьшается. После рождения лёгкие высвобождают брадикинин, который сокращает гладкие мышцы стенок артериального протока и уменьшает кровоток через него. Артериальный проток обычно сужается и полностью зарастает в течение 15-20 часов жизни, но не более 2-8 недель (в редких случаях до 15 недель при положительной динамике закрытия). Основной стимул закрытия протока — увеличение содержания кислорода в крови новорождённых. Выделение материнских циркулирующих простагландинов препятствует закрытию протока. В современной практике препараты, тормозящие образование простагландинов, используются как терапевтические средства для закрытия артериального протока у новорожденных при врожденном дефекте его закрытия. Рубец из фиброзных остатков артериального протока называют артериальной связкой, которая остаётся в нормальном сердце взрослого человека.
Клиническая картина[править | править код]
Общие симптомы:
- Тахикардия
- Дыхательные проблемы
- Одышка
- Длительный «машинный» шум, выслушиваемый во втором-третьем межреберье
- Увеличение размеров сердца
- Высокое пульсовое давление
- Замедленный рост и развитие[3]
Прогноз[править | править код]
Без лечения заболевание может прогрессировать из белого порока (со сбросом слева-направо) в синий порок (со сбросом справа-налево).
На ранних этапах развития недоношенного новорожденного функционирование ОАП может считаться нормой, необходимо оценить его гемодинамическую значимость[источник не указан 1805 дней].
Дополнительные изображения[править | править код]
Открытый артериальный проток
Примечания[править | править код]
Mosalli R, AlFaleh K, Paes B. Role of prophylactic surgical ligation of patent ductus arteriosus in extremely low birth weight infants: Systematic review and implications for clinical practice. Ann Pediatr Card 2009;2:120-6. Available from: https://www.annalspc.com/text.asp?2009/2/2/120/58313
Источник
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Дополнительные факты
- Причины
- Классификация
- Симптомы
- Диагностика
- Дифференциальная диагностика
- Лечение
- Течение и стадии
- Прогноз
- Основные медицинские услуги
- Клиники для лечения
Названия
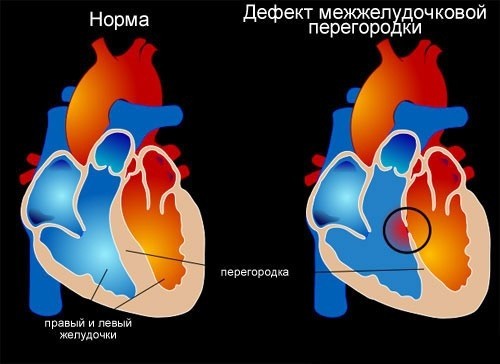
Q21,0 Дефект межжелудочковой перегородки.

Наличие дефекта между правым и левым желудочками сердца.
Описание
Дефект межжелудочковой перегородки. Врожденная внутрисердечная аномалия, характеризующаяся наличием сообщения между правым и левым желудочками. Дефект межжелудочковой перегородки проявляется одышкой, отставанием в физическом развитии, быстрой утомляемостью, учащенным сердцебиением, наличием «сердечного горба». Инструментальная диагностика дефекта межжелудочковой перегородки включает проведение ЭКГ, ЭхоКГ, рентгенографии органов грудной клетки, вентрикулографии, аортографии, катетеризации камер сердца, МРТ. При дефектах межжелудочковой перегородки проводят радикальные (закрытие дефекта) и паллиативные (сужение легочной артерии) вмешательства.
Дополнительные факты
Дефект межжелудочковой перегородки (ДМЖП) – отверстие в перегородке, разделяющей полости левого и правого желудочка, наличие которого приводит к патологическому шунтированию крови. В кардиологии дефект межжелудочковой перегородки – наиболее часто встречающийся врожденный порок сердца (9–25% от всех ВПС). Частота критических состояний при дефекте межжелудочковой перегородки составляет около 21%. С одинаковой частотой порок обнаруживается у новорожденных мальчиков и девочек.
Дефект межжелудочковой перегородки может быть единственной внутрисердечной аномалией (изолированный ДМЖП) или входить в структуру сложных пороков (тетрады Фалло, общего артериального ствола, транспозиции магистральных сосудов, атрезии трехстворчатого клапана и тд ). В ряде случаев межжелудочковая перегородка может отсутствовать полностью — такое состояние характеризуется как единственный желудочек сердца.
Особенности гемодинамики при дефекте межжелудочковой перегородки.
Межжелудочковая перегородка образует внутренние стенки обоих желудочков и составляет примерно 1/3 площади каждого из них. Межжелудочковая перегородка представлена мембранозным и мышечным компонентами. В свою очередь, мышечный отдел состоит из 3-х частей — приточной, трабекулярной и отточной (инфундибулярной).
Межжелудочковая перегородка, наряду с другими стенками желудочков, принимает участие в сокращении и расслаблении сердца. У плода она полностью формируется к 4-5-ой неделе эмбрионального развития. Если этого по каким-либо причинам не происходит, в межжелудочковой перегородке остается дефект. Нарушения гемодинамики при дефекте межжелудочковой перегородки обусловлены сообщением левого желудочка с высоким давлением и правого желудочка с низким давлением (в норме в период систолы давление в левом желудочке в 4 — 5 раз выше, чем в правом).
После рождения и установления кровотока в большом и малом кругах кровообращения из-за дефекта межжелудочковой перегородки возникает лево-правый сброс крови, объем которого зависит от размеров отверстия. При небольшом объеме шунтируемой крови давление в правом желудочке и легочных артериях остается нормальным либо незначительно повышается. Однако при большом поступлении крови через дефект в малый круг кровообращения и ее возврате в левые отделы сердца, развивается объемная и систолическая перегрузка желудочков.
Значительное повышение давления в малом круге кровообращения при больших дефектах межжелудочковой перегородки способствует возникновению легочной гипертензии. Повышение легочно-сосудистого сопротивления взывает развитие сброса крови из правого желудочка в левый (обратного или перекрестного шунтирования), что приводит к артериальной гипоксемии (синдром Эйзенменгера).
Многолетняя практика кардиохиругов показывает, что наилучших результатов закрытия дефекта межжелудочковой перегородки можно добиться при сбросе крови слева направо. Поэтому при планировании операции тщательно учитываются гемодинамические параметры (давление, сопротивление и объем сброса).
Причины
Чаще всего дефект межжелудочковой перегородки является следствием нарушения эмбрионального развития и формируется у плода при нарушениях закладки органов. Поэтому дефекту межжелудочковой перегородки часто сопутствуют другие сердечные пороки: открытый артериальный проток (20%), дефект межпредсердной перегородки (20%), коарктация аорты (12%), стеноз устья аорты (5%), аортальная недостаточность (2,5—4,5%), недостаточность митрального клапана (2%), реже — аномальный дренаж легочных вен, стеноз легочной артерии и тд.
В 25-50% случаев дефект межжелудочковой перегородки сочетается с пороками развития внесердечной локализации — болезнью Дауна, аномалиями развития почек, расщелиной твердого неба и заячьей губой.
Непосредственными факторами, вызывающими нарушение эмбриогенеза, выступают вредные воздействия на плод в I триместре гестации: заболевания беременной (вирусные инфекции, эндокринные нарушения), алкогольная и лекарственная интоксикации, ионизирующая радиация, патологическое течение беременности (выраженные токсикозы, угроза самопроизвольного прерывания беременности и пр. ). Имеются данные о наследственной этиологии дефекта межжелудочковой перегородки. Приобретенные дефекты межжелудочковой перегородки могут являться осложнением инфаркта миокарда.
Классификация
Размер дефекта межжелудочковой перегородки оценивается, исходя из его абсолютной величины и сопоставления с диаметром аортального отверстия: маленький дефект составляет 1-3 мм (болезнь Толочинова–Роже), средний – равен примерно 1/2 диаметра аортального отверстия, большой – равен или превышает его диаметр.
С учетом анатомического расположения дефекта выделяют:
• перимембранозные дефекты межжелудочковой перегородки — 75% (приточные, трабекулярные, инфундибулярные) расположены в верхней части перегородки под аортальным клапаном, могут закрываться самопроизвольно;
• мышечные дефекты межжелудочковой перегородки – 10% (приточные, трабекулярные) — расположены в мышечном отделе перегородки, на значительном удалении от клапанной и проводящей систем;
• надгребневые дефекты межжелудочковой перегородки — 5% — расположены выше наджелудочкового гребня (мышечного пучка, отделяющего полость правого желудочка от его выносящего тракта), самопроизвольно не закрываются.
Симптомы
Клинические проявления больших и малых изолированных дефектов межжелудочковой перегородки различны. Малые дефекты межжелудочковой перегородки (болезнь Толочинова—Роже) имеют диаметр менее 1 см и встречаются в 25-40% от числа всех ДМЖП. Проявляются нерезко выраженной утомляемостью и одышкой при нагрузке. Физическое развитие детей, как правило, не нарушено. Иногда у них определяется слабо выраженное куполообразное выпячивание грудной клетки в области сердца — «сердечный горб». Характерным клиническим признаком малых дефектов межжелудочковой перегородки служит аускультативно выявляемое наличие грубого систолического шума над областью сердца, который фиксируется уже на первой неделе жизни.
Большие дефекты межжелудочковой перегородки, имеющие размеры более 1/2 диаметра устья аорты или более 1 см, проявляются симптоматически уже в первые 3 месяца жизни новорожденных, приводя в 25-30% случаев к развитию критического состояния. При больших дефектах межжелудочковой перегородки отмечается гипотрофия, одышка при физической нагрузке или в покое, повышенная утомляемость. Характерны затруднения при кормлении: прерывистое сосание, частые отрывы от груди, одышка и бледность, потливость, пероральный цианоз. В анамнезе у большинства детей с дефектом межжелудочковой перегородки — частые респираторные инфекции, затяжные и рецидивирующие бронхиты и пневмонии.
В возрасте 3-4-лет, по мере нарастания сердечной недостаточности, у таких детей появляются жалобы на сердцебиение и боли в области сердца, склонность к носовым кровотечениям и обморокам. Транзиторный цианоз сменяется постоянным пероральным и акроцианозом; беспокоит постоянная одышка в покое, ортопноэ, кашель (синдром Эйзенменгера). На наличие хронической гипоксии указывают деформация фаланг пальцев и ногтей («барабанные палочки», «часовые стекла»).
Диагностика
К методам инструментальной диагностики дефекта межжелудочковой перегородки относятся ЭКГ, ФКГ, рентгенография грудной клетки, ЭхоКС, катетеризация камер сердца, ангиокардиография, вентрикулография.
Электрокардиограмма при дефекте межжелудочковой перегородки отражает перегрузку желудочков, наличие и степень выраженности легочной гипертензии. У взрослых больных могут регистрироваться аритмии (экстрасистолия, мерцание предсердий), нарушения проводимости (блокада правой ножки пучка Гиса, синдром WPW). Фонокардиография фиксирует высокочастотный систолический шум с максимумом в III-IV межреберье слева от грудины.
Эхокардиография позволяет выявить дефект межжелудочковой перегородки или заподозрить его по характерным нарушениям гемодинамики. Рентгенография органов грудной клетки при больших дефектах межжелудочковой перегородки обнаруживает усиление легочного рисунка, усиленную пульсацию корней легких, увеличение размеров сердца. Зондирование правых полостей сердца выявляет повышение давления в легочной артерии и правом желудочке, возможность проведения катетера в аорту, повышенную оксигенацию венозной крови в правом желудочке. Аортография проводится для исключения сопутствующих ВПС.
Дифференциальная диагностика
Дифференциальная диагностика дефекта межжелудочковой перегородки проводится с открытым атриовентрикулярным каналом, общим артериальным стволом, дефектом аортолегочной перегородки, изолированным стенозом легочной артерии, стенозом аорты, врожденной митральной недостаточностью, тромбоэмболией.
Лечение
Асимптомное течение дефекта межелудочковой перегородки при его небольших размерах позволяет воздержаться от хирургического вмешательства и осуществлять динамическое наблюдение за ребенком. В ряде случаев возможно спонтанное закрытие дефекта межжелудочковой перегородки к 1-4 годам жизни или в более позднем возрасте. В остальных случаях показано хирургическое закрытие дефекта межжелудочковой перегородки, как правило, после достижения ребенком 3-х лет.
При развитии сердечной недостаточности и легочной гипертензии проводится консервативное лечение с помощью сердечных гликозидов, мочегонных препаратов, ингибиторов ангиотензинпревращающего фермента, кардиотрофиков, антиоксидантов.
Кардиохирургическое лечение дефекта межжелудочковой перегородки может быть радикальным и паллиативным. К радикальным операциям относятся ушивание малых дефектов межжелудочковой перегородки П-образными швами; пластика больших дефектов синтетической (тефлон, дакрон и тд ) заплатой или биологической (консервированный ксеноперикард, аутоперикард) тканью; рентгенэндоваскулярная окклюзия дефекта межжелудочковой перегородки.
У грудных детей с выраженной гипотрофией, большим лево-правым шунтированием крови и множественными дефектами предпочтение отдается паллиативной операции, направленной на создание искусственного стеноза легочной артерии с помощью манжетки. Данный этап позволяет подготовить ребенка к радикальной операции по устранению дефекта межжелудочковой перегородки в более старшем возрасте.
Течение и стадии
Женщины с небольшим дефектом межжелудочковой перегородки, как правило, в состоянии нормально выносить и родить ребенка. Однако, при больших размерах дефекта, аритмии, сердечной недостаточности или легочной гипертензии риск осложнений во время беременности значительно повышается. Наличие синдрома Эйзенменгера является показанием для искусственного прерывания беременности. У женщин с дефектом межжелудочковой перегородки имеется повышенная вероятность рождения ребенка с аналогичным или другим врожденным пороком сердца.
Перед планированием беременности пациентке с пороком сердца (оперированным или нет) необходимо проконсультироваться с акушером-гинекологом, кардиологом, генетиком. Ведение беременности у категории женщин с дефектом межжелудочковой перегородки требует повышенного внимания.
Прогноз
Естественное течение дефекта межжелудочковой перегородки в целом не позволяет надеяться на благоприятный прогноз. Продолжительность жизни при данном пороке зависит от величины дефекта и составляет в среднем около 25 лет. При больших и средних дефектах 50-80% детей умирают в возрасте до 6 мес. Или 1 года от сердечной недостаточности, застойной пневмонии, бактериального эндокардита, нарушений ритма сердца, тромбоэмболических осложнений.
В редких случаях ДМЖП не оказывает существенного влияния на продолжительность и качество жизни. Спонтанное закрытие дефекта межжелудочковой перегородки наблюдается в 25-40% случаев, преимущественно при его малом размере. Однако даже в этом случае больные должны находиться под наблюдением кардиолога в связи с возможными осложнениями со стороны проводящей системы сердца и высоким риском возникновения инфекционного эндокардита.
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Включен: острый перикардиальный выпот
Исключен: ревматический перикардит (острый) (I01.0)
Исключены:
- некоторые текущие осложнения острого инфаркта миокарда (I23.-)
- посткардиотонический синдром (I97.0)
- травма сердца (S26.-)
- болезни, уточненные как ревматические (I09.2)
Исключен:
- острый ревматический эндокардит (I01.1)
- эндокардит БДУ (I38)
Исключены: митральная (клапанная):
- болезнь (I05.9)
- недостаточность (I05.8)
- стеноз (I05.0)
при неустановленной причине, но с упоминанием ее
- болезни аортального клапана (I08.0)
- митральном стенозе или обструкции (I05.0)
поражения, уточненные как врожденные (Q23.2-Q23.9)
поражения, уточненные как ревматические (I05.-)
последние изменения: январь 2015
Исключены:
- гипертрофический субаортальный стеноз (I42.1)
- при неустановленной причине, но с упоминанием о болезни митрального клапана (I08.0)
- поражения, уточненные как врожденные (Q23.0, Q23.1, Q23.4-Q23.9)
- поражения, уточненные как ревматические (I06.-)
последние изменения: январь 2015
Исключенs:
- без уточнения причины (I07.-)
- поражения, уточненные как врожденные (Q22.4, Q22.8, Q22.9)
- уточненные как ревматические (I07.-)
последние изменения: январь 2005
Исключены:
- поражения, уточненные как врожденные (Q22.1, Q22.2, Q22.3)
- нарушения, уточненные как ревматические (I09.8)
последние изменения: январь 2005
I38
Эндокардит, клапан не уточнен
Включены:
Эндокардит (хронический) БДУ
Клапанная(ый):
Вульвит (хронический) неуточненного клапана | БДУ или уточненной причины, кроме ревматической или врожденной |
Исключены:
- эндокардиальный фиброэластоз (I42.4)
- случаи, уточненные как ревматические (I09.1)
- врожденная недостаточность клапанов аорты БДУ (Q24.8)
- врожденный стеноз аортального клапана БДУ (Q24.8)
последние изменения: январь 2005
Включены: поражение эндокарда при:
- кандидозной инфекции (B37.6†)
- гонококковой инфекции (A54.8†)
- болезни Либмана-Сакса (M32.1†)
- менингококковой инфекции (A39.5†)
- ревматоидном артрите (M05.3†)
- сифилисе (A52.0†)
- туберкулезе (A18.8†)
- брюшном тифе (A01.0†)
Исключены:
- кардиомиопатия, осложняющая:
- беременность (O99.4)
- послеродовой период (O90.3)
- ишемическая кардиомиопатия (I25.5)
Исключены:
- кардиогенный шок (R57.0)
- осложняющая:
- аборт, внематочную или молярную беременность (O00-O07, O08.8)
- акушерские хирургические вмешательства и процедуры (O75.4)
Исключен:
- осложняющая:
- аборт, внематочную или молярную беременность (O00-O07, O08.8)
- акушерские хирургические вмешательства и процедуры (O75.4)
- тахикардия:
- БДУ (R00.0)
- синоаурикулярная БДУ (R00.0)
- синусовая БДУ (R00.0)
последние изменения: январь 2006
последние изменения: январь 2013
Исключены:
- брадикардия:
- БДУ (R00.1)
- синоатриальная (sinoatrial) (R00.1)
- синусовая (sinus) (R00.1)
- вагальная (vagal) (R00.1)
- состояния, осложняющие:
- аборт, внематочную или молярную беременность (O00-O07, O08.8)
- акушерские хирургические вмешательства и процедуры (O75.4)
- нарушение ритма сердца у новорожденного (P29.1)
последние изменения: январь 2006
Исключены:
- состояния, осложняющие:
- аборт, внематочную или молярную беременность (O00-O07, O08.8)
- акушерские хирургические вмешательства и процедуры (O75.4)
- состояния, обусловленные гипертензией (I11.0)
- заболеванием почек (I13.-)
- последствия операции на сердце или при наличии сердечного протеза (I97.1)
- сердечная недостаточность у новорожденного (P29.0)
Исключены:
- любые состояния, указанные в рубриках I51.4-I51.9, обусловленные гипертензией (I11.-)
- любые состояния, указанные в рубриках I51.4-I51.9, обусловленные гипертензией
- с заболеванием почек (I13.-)
- осложнения, сопровождающие острый инфаркт (I23.-)
- уточненные как ревматические (I00-I09)
Исключены: сердечно-сосудистые нарушения БДУ при болезнях, классифицированных в других рубриках (I98*)
Источник
