О миелобластный лейкоз код по мкб 10 у детей
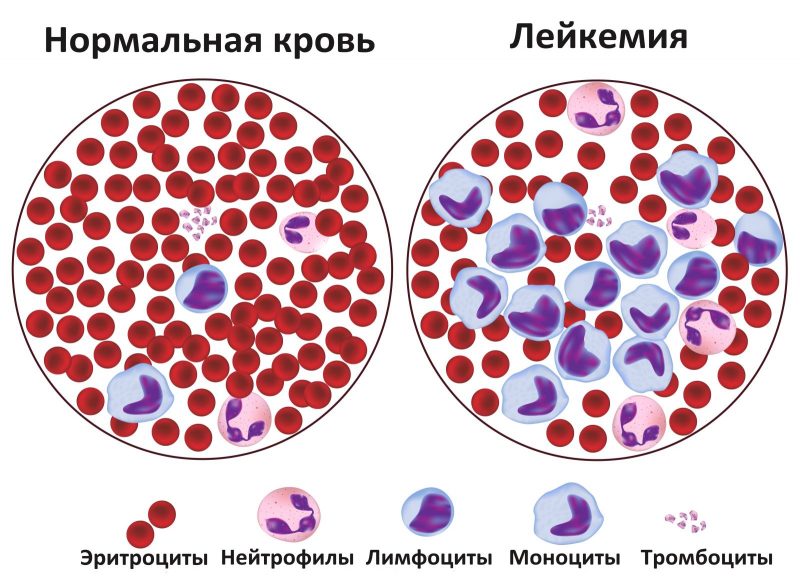
MKБ 10 или международная классификация всех заболеваний 10 созыва имеет в себе практически все короткие обозначения известных патологий, в том числе и онкологических. Лейкоз коротко по МКБ 10 имеет две точные кодировки:
- С91 — Лимфоидная форма.
- С92 — Миелоидная форма или миелолейкоз.
Но также нужно учитывать и характер заболевания. Для обозначения используют подгруппу, которая пишется после точки.
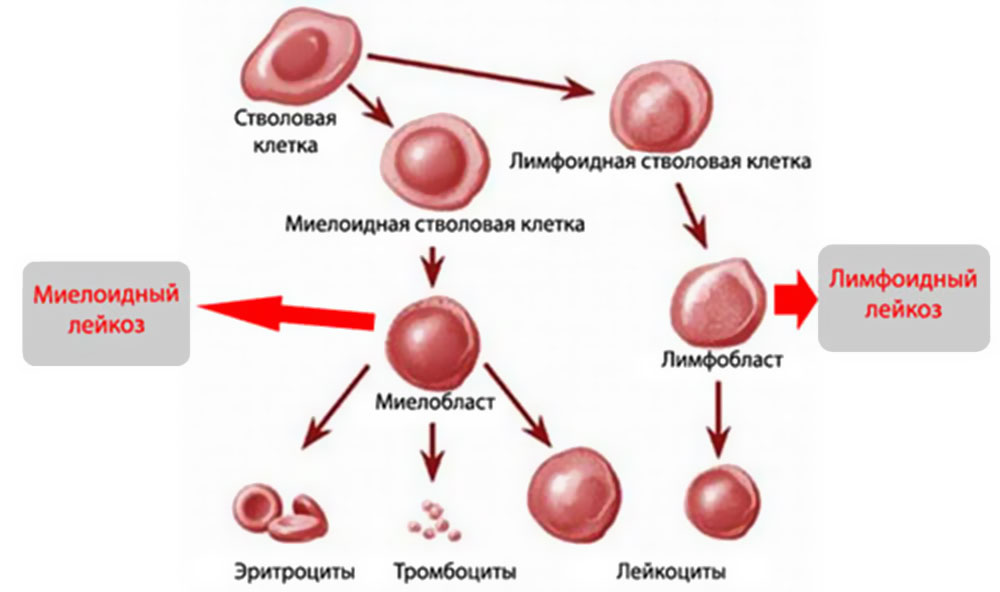
Лимфолейкоз
| Кодировка | Лимфоидный лейкоз |
| C 91.0 | Острый лимфобластный лейкоз при Т или В клеток предшественников. |
| C 91.1 | Лимфоплазматическая форма, Синдром Рихтера. |
| C 91.2 | Подострый лимфоцитарный (в данной время код не используется) |
| C 91.3 | Пролимфоцитарный В-клеточный |
| C 91.4 | Волосатоклеточный и лейкемический ретикулоэндотелиоз |
| C 91.5 | Т-клеточная лимфома или лейкемия взрослых с параметром HTLV-1-ассоциированная. Варианты: Тлеющий, острый, лимфоматоидный, тлеющий. |
| C 91.6 | Пролимфоцитарный T-клеточный |
| C 91.7 | Хронический из больших зернистых лимфоцитов. |
| C 91.8 | Зрелый B-клеточный (Беркитта) |
| C 91.9 | Неутонченная форма. |
Миелолейкоз
Включает в себя гранулоцитарный и миелогенный.
| Коды | Миелоидный лейкоз |
| C 92.0 | Острый миелобластный лейкоз (ОМЛ) с низким показателем дифференцировки, а также форма с созреванием. (AML1/ETO, AML M0, AML M1, AML M2, AML с t (8 ; 21), AML ( без FAB классификации ) БДУ) |
| С 92.1 | Хроническая форма (ХМЛ) [CML], BCR/ABL-положительный. Филадельфийская хромосома (Ph1) положительная. t (9 : 22) (q34 ;q11). С бластным кризом. Исключения: неклассифицированное миелопролиферативное заболевание; атипичный, BCR / ABL-отрицательный; Хронический миеломоноцитарный лейкоз. |
| C 92.2 | Атипичный хронический, BCR/ABL-отрицательный. |
| С 92.3 | Миелоидная саркома в которой новообразование состоит из незрелыз атипичных мелеоилных клеточек. Также в нее входит гранулоцитарная саркома и хлорома. |
| C 92.4 | Острый промиелоцитарный лейкоз [PML] с параметрами: AML M3 и AML M3 с t (15 ; 17). |
| С 92.5 | Острый миеломоноцитарный с параметрами AML M4 и AML M4 Eo с inv (16) or t(16;16) |
| C 92.6 | С 11q23-аномалией и с вариацией MLL хромосомы. |
| С 92.7 | Другие формы. Исключение — гиперэозинофильный синдром или хронический эозинофильный. |
| C 92.8 | С многолинейной дисплазией. |
| С 92.9 | Неутонченные формы. |
Причины
Напомним, что точной причины из-за чего происходит развитие рака крови не известно. Именно поэтому врачам, так сложно бороться с этим недугом и предотвращать его. Но есть ряд факторов, которые могут увеличивать шанс возникновения онкологии красной жидкости.
- Повышенная радиация
- Экология.
- Плохое питание.
- Ожирение.
- Чрезмерное употребление лекарственных средств.
- Лишний вес.
- Курение, алкоголь.
- Вредная работа, связанная с пестицидами и химическими реагентами, которые могут влиять на кроветворную функцию.

Симптомы и аномалии
- Анемия возникает в результате угнетения эритроцитов из-за чего кислород до здоровых клеток доходит не в полном объеме.
- Сильные и частые головные боли. Начинается с 3 стадии, когда возникает интоксикация из-за злокачественной опухоли. Также может быть результатом запущенной анемии.
- Постоянная простуда и инфекционные и вирусные заболевания с продолжительным периодом. Бывает, когда здоровые лейкоциты заменяются на атипичные. Они не выполняют свою функцию и организм становится менее защищенным.
- Боль в суставах и ломка.
- Слабость, утомляемость, сонливость.
- Систематическая субфебрильная температура без причины.
- Изменение запаха, вкусов.
- Потеря веса и аппетита.
- Долгие кровотечения при снижении количество тромбоцитов в крови.
- Болезненность воспаление лимфатических узлов по всему телу.
Диагностика
Точный диагноз можно поставить, только после проведения тщательного обследования и сдачи определенного перечня анализов. Чаще всего людей ловят на аномальных показателях при биохимическом и общем анализе крови.
Для более точного диагноза делают пункцию костного мозга из тазовой кости. Позже клетки отправляют на биопсию. Также врач-онколог проводит полный осмотри тела: МРТ, УЗИ, КТ, рентген, для выявления метастазов.
Лечение, терапия и прогноз
Основным типом лечения используется химиотерапия, когда в кровь вводят химические яды, которые направлены на уничтожение аномальных клеток крови. Опасность и малоэффективность данного типа лечения в том, что также уничтожаются и здоровые клетки крови, коих и так мало.
При выявлении первичного очага, врач может назначить химию для полного уничтожения костного мозга в данной зоне. После проведения процедуры также могут проводить и облучение для уничтожения остатков раковых клеток. В процессе происходит пересадка стволовых клеток от донора.
(1 оценок, среднее: 5,00 из 5)
Загрузка…
Источник
Рубрика МКБ-10: C92.0
МКБ-10 / C00-D48 КЛАСС II Новообразования / C00-C97 Злокачественные новообразования / C81-C96 Злокачественные новообразования лимфоидной, кроветворной и родственных им тканей / C92 Миелоидный лейкоз миелолейкоз
Определение и общие сведения[править]
Острый миелоидный лейкоз
Синонимы: острый нелимфобластный лейкоз (ОНЛЛ), острый миелобластный лейкоз (ОМЛ)
Гетерогенная группа опухолевых заболеваний системы крови, характеризуемая повышенным уровнем предшественников миелоидных, моноцитарных, эритроидных или мегакариоцитарных клеток в костном мозге.
Эпидемиология
ОМЛ в детском возрасте встречают в 15-20% случаев среди всех лейкозов, заболеваемость составляет 5,6 случаев на 1 млн детского населения в год.
Этиология и патогенез[править]
Известны довольно частые случаи развития ОМЛ и хронического миелолейкоза (ХМЛ) у людей, перенёсших атомную бомбардировку Хиросимы. У этой группы больных было выявлено достоверно более высокое содержание субклонов с моносомией 7 и делецией 20q13.3 участка. Среди популяции, проживавшей около Чернобыля во время аварии на атомной станции, чаще стали диагностировать FAB M4 и M5 варианты. Исследуют влияние длительного воздействия пестицидов, принимаемых с пищей, прием алкоголя и ингибиторов топоизомеразы II во время беременности матери, развитие у детей вторичного лейкоза или миелодиспластического синдрома (МДС) при лечении другой опухоли вследствие приема алкилирующих агентов или ингибиторов топоизомеразыII. Риск развития ОМЛ связан также со спленомегалией, суммарной дозой алкилирующих агентов, дозой и объёмом лечебного облучения и возрастом. Дети, получавшие химиотерапию во время лечения другой опухоли, рискуют заболеть вторичным ОМЛ в большей степени, чем другие дети. Наибольший риск (23%) развития вторичных лейкозов отмечен у больных с метастатической саркомой Юинга, подвергнутых интенсивному лечению с использованием ифосфамида, циклофосфамида и радиотерапии.
Патогенез
ОМЛ возникает при трансформации гемопоэтической клетки — родоначальницы клональной популяции опухолевых клеток, которая замещает при этом нормальные клетки костного мозга, а также может поражать экстрамедуллярные ткани. Точное количество генных мутаций, участвующих в возникновении и патогенезе ОМЛ, до сих пор не известно. Несмотря на расширение знаний о природе человека, точные цели этих мутаций не вполне ясны. В большинстве случаев ОМЛ нельзя определить клеткуродоначальницу опухолевого клона.
В настоящее время известны, как минимум, три потенциальные механизма, посредством которых лейкозные клетки могут аккумулироваться в костном мозге. Один из них способствует более быстрой пролиферации опухолевых клеток по сравнению с нормальными клетками костного мозга. Другой потенциальный механизм клеточной трансформации — выход из нормального пути апоптоза. Третий механизм развития ОМЛ состоит в блокировке нормальной дифференцировки клеток — предшественников гемопоэза.
Молекулярный механизм до сих пор ясно не представлен.
Одним из его примеров служит острый промиелоцитарный лейкоз (ОПЛ), при котором в результате транслокации t(15;17) возникает аномальный ген PML/RARα и клетка начинает синтез аномального белка PML/RARα, который блокирует клеточную дифференцировку путем ингибирования рецептора к ретиноидам. Лейкозные клетки нормально дифференцируются до промиелоцитов, после чего возникает полный блок дифференцировки клеточной линии. Этот блок может быть преодолен назначением полностью — трансретиноевой кислоты (ATRA). Такой пример иллюстрирует возможность лечения ОМЛ посредством агентов клеточной дифференцировки.
Клинические проявления[править]
Клиническая картина ОМЛ выражена следующими синдромами: анемическим, геморрагическим, токсическим, которые отражают снижение продукции эритроцитов, тромбоцитов и гранулоцитов. Первыми симптомами ОМЛ у детей могут быть лейкозные экстрамедуллярные поражения. Повышенная утомляемость, бледность кожных покровов, выраженная слабость, головокружение, головная боль, одышка, тахикардия — проявления анемии, которая обычно бывает нормохромной. Уровень гемоглобина в периферической крови в пределах 27-140 г/л, в среднем составляет 70 г/л. Часто родители не обращают внимания на повышенную утомляемость, бледность кожных покровов, объясняя эти симптомы большими нагрузками в школе и недостаточным нахождением ребёнка на свежем воздухе. Тромбоцитопения обычно вызывает развитие геморрагического синдрома, который может быть представлен как кожными проявлениями (петехии, пурпура, экхимозы, гематомы), так и различными кровотечениями (носовыми, кишечными, из полости матки, из слизистой дёсен и полости рта). На момент диагностики уровень тромбоцитов, по данным анализов периферической крови, составляет не более 50×109/л приблизительно у 50% детей, больных ОМЛ. Кроме того, геморрагический синдром часто бывает проявлением синдрома диссеменированного внутрисосудистого свёртывания (ДВС), который может возникнуть при любом варианте ОМЛ, но особенно характерен для ОПЛ. Активированный тромбопластин из гранул опухолевых промиелоцитов выходит в сосудистое русло при их лизисе, который происходит под воздействием индуктивной цитостатической терапии, что усиливает ДВС-синдром.
Как правило, в дебюте заболевания у детей с ОМЛ снижено абсолютное количество гранулоцитов (менее 1×109/л в анализе периферической крови); у больных часто возникают инфекции, вызванные сапрофитными микроорганизмами полости рта, кишечника, параректальной области, лёгких, кожи. Чаще повышение температуры обусловлено инфекционным процессом. В связи с этим фебрильную температуру до начала цитостатической терапии необходимо рассматривать как признак инфекции, для диагностики которой проводят бактериологическое исследования крови, кала, мочи, мазков из полости рта, носа и с поверхности кожи, а также назначают эмпирическую антибактериальную терапию с последующей её коррекцией в зависимости от результатов высевов.
Гепатоспленомегалию встречают более чем в половине всех случаев ОМЛ у детей. Выраженный гепатолиенальный синдром обнаруживают у 25% больных ОМЛ, что более характерно для пациентов с моноцитоидным компонентом опухолевых клеток (М4 и М5 FABварианты).
Лимфатические узлы у большинства больных небольших размеров, безболезненные, не спаяны с кожей и друг с другом. В редких случаях наблюдают увеличенные лимфатические узлы размером 2,5-5 см с образованием конгломератов в шейнонадключичной области.
Проявлениями изменений в костносуставной системе в некоторых случаях служат выраженные оссалгии в нижних конечностях и в области позвоночного столба, что сопровождается нарушением движений и походки.
На рентгенограммах костной системы отмечают деструктивные изменения различной локализации, периостальные реакции, явления остеопороза. Проявления экстрамедуллярных опухолевых поражений чаще выражены гингивитом и экзофтальмом, в том числе двусторонним. В редких случаях отмечают опухолевую инфильтрацию мягких тканей, гипертрофию нёбных миндалин, поражение носоглотки и лицевого нерва. Экстрамедуллярные проявления ОМЛ объединяет термин гранулоцитарная (миелоидная) саркома, включая классическую хлорому и непигментированные опухоли.
По данным аутопсии, миелоидную саркому диагностируют у больных ОМЛ в 3-8% случаев. Она может предшествовать поражению костного мозга или сочетаться с признаками ОМЛ, а также возникать при рецидиве заболевания. Орбитальная ткань и внутренние структуры черепа — наиболее частые зоны локализации опухолевого роста. Бластные клетки чаще представлены FAB М2 вариантом и транслокацией t(8;21), а у детей в возрасте до 1 года — М4 и М5 вариантами ОМЛ. Ряд авторов указывают на более плохой прогноз у этих больных, чем у детей с ОМЛ без экстрамедуллярной инфильтрации.
Поражение ЦНС может быть как локальным, представленным миелоидной саркомой этой зоны, так и диссеминированным поражением оболочек головного мозга. Клинически отмечают головную боль, тошноту, рвоту, фотофобию. Поражение ЦНС должно быть подтверждено анализом цитологических препаратов, приготовленных путём центрифугирования ликвора. Вовлечение в лейкозный процесс ЦНС отмечают у 5-15% детей с ОМЛ в сочетании с высоким лейкоцитозом или возрастом пациентов менее 2 лет на момент диагностики ОМЛ, а также у детей с М4Ео и М5 вариантами.
Острый миелоидный лейкоз: Диагностика[править]
Анамнез
При ретроспективном анализе родители пациента обычно отмечают появление симптомов ОМЛ за 2-4 нед, иногда за 1-2 мес до установления диагноза.
Физикальное обследование
При осмотре обращают внимание на анемию, геморрагический синдром, увеличение печени, селезёнки, периферических лимфатических узлов, а также возможное экстрамедулярное поражение мягких тканей (кожа, периорбитальная клетчатка и др.).
Лабораторные исследования
Уровень гемоглобина в периферической крови подвержен колебаниям от 27 до 140 г/л, в среднем составляет 70 г/л, увеличено количество лейкоцитов (у 25% больных более 100×109/л). Количество бластных клеток в анализе периферической крови может быть как выраженным (более 80%), так и незначительным, вплоть до их полного отсутствия.
При оценке миелограммы диагноз ОМЛ устанавливают при наличии более 25-30% бластных клеток, классифицируемых по FABклассификации.
Моноклональные антитела используют при иммунофенотипировании для определения линейноспецифических и стадия специфических антигенов лимфоидной и миелоидной дифференцировки бластов. Моноклональные антитела помогают установить диагноз ОМЛ и дифференцировать его от ОЛЛ, если это затруднительно при морфоцитохимическом исследовании. Некоторые миелоидные маркёры могут определять и на лимфобластах, тогда диагноз ОМЛ не может быть установлен только на основе результатов иммунофенотипирования.
Клональные хромосомные аномалии определяют в большинстве случаев ОМЛ, что способствует более точной диагностике. Существуют хромосомные аномалии, характерные для определённых морфологических вариантов ОМЛ: t(15;17), t(8;21) для М2 ОНЛЛ и inv(16) для М4 ОМЛ. Но в то же время другие аномалии, например, вовлекающие ген MLL, локализованный на 11q23, могут определяться не только при различных морфологических вариантах ОМЛ, но и при ОЛЛ. Исследование с помощью FISH даёт возможность определить генетические аномалии при ограниченных возможностях стандартного цитогенетического исследования. Применяя FISHисследование, можно выявить хромосомные аберрации не только на метафазных, но и на интерфазных ядрах, что особенно важно для обнаружения остаточного клона клеток после химиотерапии. Для выявления ДВСсиндрома необходимы данные коагулограммы.
Инструментальные тсследования
В целях диагностики поражения ЦНС необходимы дополнительные методы исследования: МРТ, КТ, ЭЭГ и ЭхоЭГ.
Дифференциальный диагноз[править]
Апластическая анемия, тромбоцитопеническая пурпура, миелодиспластический синдром, ОЛЛ (острый лимфобластный лейкоз), ХМЛ (хронический миелобластный лейкоз), нейробластома, ретинобластома.
Острый миелоидный лейкоз: Лечение[править]
Цель лечения
Максимальная эрадикация лейкозного клона.
Показания к госпитализации
Проведение интенсивной ПХТ и лечение осложнений.
Немедикаментозное лечение
Лучевая терапия при инициальном поражении ЦНС и для профилактики её лейкозного поражения при inv(16)/t(16;16).
Медикаментозное лечение
При проведении индуктивного и консолидирующего курсов химиотерапии необходима максимальная интенсификация, что приводит к наиболее быстрому достижению полной ремиссии. Следствие такой терапии — аплазия костного мозга, во время которой резко возрастает опасность возникновения инфекционных и геморрагических осложнений. В связи с этим больным необходимо массивное сопроводительное лечение, включающее в себя заместительную, антибактериальную и дезинтоксикационную инфузионную терапию с ежедневной коррекцией электролитов и белка. Основные препараты, входящие в используемые программы ПХТ, цитарабин в сочетании с антрациклиновыми антибиотиками: этопозидом, флударабином, кладрибином. Аллогенная трансплантация гемопоэтических стволовых клеток показана у больных с очень медленным ответом на проведённую химиотерапию (отсутствие ремиссии после курса индукции ремиссии).
Хирургическое лечение
Не показано.
Профилактика[править]
Прочее[править]
Показания к консультации других специалистов
При появлении определённой симптоматики.
Примерные сроки нетрудоспособности
В течение 6 мес интенсивной ПХТ.
Дальнейшее ведение
Наблюдение врачом онкогематологом один раз в 2 нед в течение 2 лет, затем один раз в 2 мес (3 года), далее один раз в 6 мес (5 лет).
Информация для пациента
Охранительный режим (ограничить физические нагрузки, избегать прямых солнечных лучей), полноценное питание.
Прогноз
В первую очередь прогноз зависит от кариотипа опухолевых клеток. Так, к благоприятному кариотипу относят следующие аномалии: t(8;21), t(15;17), inv(16), t(9;11) и другие аномалии 11q23, исключая t(10;11), к промежуточному кариотипу — нормальный кариотип и к кариотипу с высоким риском развития рецидива — 5, 7, 5q, более 5 различных аномалий, исключая стандартные. До сих пор нет определённых данных о значении инициального уровня лейкоцитов, размеров паренхиматозных органов для прогноза ОМЛ. Возможно, это связано с различной по интенсивности терапией, используемой различными исследовательскими группами и гетерогенностью ОМЛ. Отмечают неблагоприятное течение ОМЛ при FAB М4 без inv(16), М5, М6 и М7 морфологических вариантах. Довольно часто прогностически неблагоприятные генетические аномалии сочетаны с прогностически неблагоприятными морфологическими вариантами.
Источники (ссылки)[править]
Онкология [Электронный ресурс] / Под ред. Чиссова В.И., Давыдова М.И. — М. : ГЭОТАР-Медиа, 2013. — https://www.rosmedlib.ru/book/ISBN9785970423684.html
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
- Азацитидин
- Гилтеритиниб
- Гласдегиб
- Даунорубицин
- Даунорубицин/цитарабин
- Доксорубицин
- Гемтузумаб озогамицин
- Меркаптопурин
- Мидостаурин
- Митоксантрон
- Циклофосфамид
- Цитарабин
- Энасидениб
- Этопозид
Источник
- Описание
- Симптомы (признаки)
- Диагностика
Краткое описание
Острый лейкоз — злокачественное заболевание кроветворной системы; морфологический субстрат — бластные клетки.
Код по международной классификации болезней МКБ-10:
- C91.0 Острый лимфобластный лейкоз
- C92 Миелоидный лейкоз [миелолейкоз]
- C93.0 Острый моноцитарный лейкоз
Частота. 13,2 случаев на 100 000 населения среди мужчин и 7,7 случаев на 100 000 населения среди женщин.
КЛАССИФИКАЦИЯ
FAB классификация (франко американо британская) основана на морфологии лейкемических клеток (строение ядра, соотношение размеров ядра и цитоплазмы) • Острый миелобластный (нелимфобластный) лейкоз (ОМЛ) •• М0 — без созревания клеток, миелогенная дифференцировка доказывается только иммунологически •• М1 — без созревания клеток •• М2 — ОМЛ с дифференцировкой клеток, •• М3 — промиелоцитарный •• М4 — миеломоноцитарный •• М5 — монобластный лейкоз •• М6 — эритролейкоз •• М7 — мегакариобластный лейкоз • Острый лимфобластный лейкоз (ОЛЛ): •• L1 — без дифференцировки клеток (морфологически гомогенные клетки) •• L2 — с дифференцировкой клеток (морфологически гетерогенная популяция клеток) •• L3 — беркеттоподобные лейкозы • Недифференцируемый лейкоз — к этой категории относят лейкозы, клетки которых невозможно идентифицировать как миелобластные или лимфобластные (ни химическими, ни иммунологическими методами) • Миелопоэтическая дисплазия •• Рефрактерная анемия без бластоза (в костном мозге бласты и промиелоциты <10%) •• Рефрактерная анемия с бластозом (в костном мозге бласты и промиелоциты 10 30%) •• Рефрактерная анемия с избытком бластов в трансформации •• Хронический миеломоноцитарный лейкоз.
REAL классификация (Revised Europian American classification of Lymphoid neoplasms), пересмотренная (Европейско Американская) классификация лимфоидных гемобластозов • Пре B клеточные опухоли •• Пре B лимфобластный лейкоз/лимфома • Пре T клеточные опухоли •• Пре T лимфобластный лейкоз/лимфома • Опухоли периферических B клеток •• хронический лимфолейкоз/лимфома из малых лимфоцитов •• Лимфоплазмоцитарная лимфома •• Лимфома из плащевых клеток •• Фолликулярная лимфома •• Лимфома из клеток краевой зоны •• Волосато клеточный лейкоз •• Плазмоцитома/миелома плазмоцитарная •• Диффузная лимфома из больших лимфоцитов•• Лимфома Беркетта • Опухоли периферических T клеток и NK клеток •• T клеточный хронический лимфолейкоз •• Лейкоз из крупных зернистых лимфоцитов •• Грибовидный микоз и синдром Сезари T клеточная лимфома •• Ангиоиммунобластическая T клеточная лимфома •• Ангиоцентрическая лимфома (лимфома из NK и T клеток) •• Кишечная T клеточная лимфома •• Лейкоз/лимфома T клеточная взрослых •• Анапластическая крупноклеточная лимфома
Варианты ОМЛ (классификация ВОЗ, 1999) • ОМЛ с t(8;21)(q22;q22) • ОМЛ с t(15;17) (q22;q11 12) • Острый миеломонобластный лейкоз • ОМЛ с патологической костномозговой эозинофилией (inv(16)(p13q22) или t(16;16) (p13;q11) • ОМЛ с 11q23 (MLL) дефектами • Острый эритроидный лейкоз • Острый мегакариоцитарный лейкоз • Острый базофильный лейкоз • Острый панмиелоз с миелофиброзом • Острые бифенотипические лейкозы • ОМЛ с мультилинейной дисплазией • Вторичный ОМЛ.
Иммуногистохимическое исследование (определение клеточного фенотипа) необходимо для уточнения иммунологического варианта лейкоза, влияющего на схему лечения и клинический прогноз
• Острый лимфобластный лейкоз (247640, , мутация соматических клеток) — 85% всех случаев, составляет до 90% всех лейкозов детского возраста У взрослых развивается достаточно редко. Цитохимические реакции: положительная на терминальную дезоксинуклеотидил трансферазу; отрицательные на миелопероксидозу, гликоген. Использование маркёров клеточной мембраны позволило выделить подвиды •• В — клеточные — 75% всех случаев •• С отсутствием розеткообразования •• Т — клеточые •• Другие варианты (редко). Дифференциальная диагностика подвидов важна для прогноза, т.к. Т — клеточные варианты плохо поддаются лечению.
• Острый миелобластный лейкоз чаще возникают у взрослых, подтип зависит от уровня дифференцировки клеток. В большинстве случаев клон миелобластов исходит из стволовых кроветворных клеток, способных к множественной дифференцировке в колониеобразующие единицы гранулоцитов, эритроцитов, макрофагов или мегакариоцитов, поэтому у большинства больных злокачественные клоны не имеют признаков лимфоидных или эритроидных ростков •• ОМЛ наблюдают наиболее часто; имеет четыре варианта (М0 — М3) •• М0 и М1 — острый лейкоз без дифференцировки клеток •• М2 — острый с дифференцировкой клеток •• М3 — промиелоцитарный лейкоз, характеризуется наличием аномальных промиелоцитов с гигантскими гранулами; часто сочетается с ДВС, обусловленным тромбопластическим эффектом гранул, что подвергает сомнению целесообразность применения гепарина при терапии. Прогноз при М3 менее благоприятен, чем при М0–М1 •• Миеломонобластный и монобластный лейкозы (соответственно М4 и М5) характеризуются преобладанием неэритроидных клеток типа монобластов. М4 и М5 составляют 5–10% всех случаев ОМЛ. Частый признак — образование внекостномозговых очагов кроветворения в печени, селезёнке, дёснах и коже, гиперлейкоцитоз, превышающий 50–100109/л. Чувствительность к терапии и выживаемость ниже, чем при других вариантах острых миелобластных лейкозов •• Эритролейкоз (М6). Вариант острого миелобластного лейкоза, сопровождающийся усиленной пролиферацией эритроидных предшественников; характерно наличие аномальных бластных ядросодержащих эритроцитов. Эффективность лечения эритролейкоза сходна с результатами терапии других подтипов или несколько ниже •• Мегакариобластный лейкоз (М7) — редкий вариант, сочетающийся с фиброзом костного мозга (острый миелосклероз). Плохо поддаётся терапии. Прогноз неблагоприятный.
Патогенез обусловлен пролиферацией опухолевых клеток в костном мозге и их метастазированием в различные органы. Угнетение нормального кроветворения связано с двумя основными факторами: • повреждение и вытеснение нормального ростка кроветворения низкодифференцированными лейкемическими клетками • выработка бластными клетками ингибиторов, подавляющих рост нормальных кроветворных клеток.
Стадии острого лейкоза • Первично — активная фаза • Ремиссия (при лечении) — полная клинико — гематологическая •• Содержание бластов в костном мозге менее 5% при нормальной клеточности •• В клинической картине отсутствует пролиферативный синдром • Рецидив (ранний и поздний) •• Изолированный костномозговой — содержание бластов в костном мозге более 25% •• Внекостномозговой ••• Нейролейкоз (неврологическая симптоматика, цитоз более 10 клеток, бласты в ликворе) ••• Тестикулярный (увеличение размеров одного или двух яичек, наличие бластов подтверждено цитологическим и гистологическим исследованиями) •• Смешанный • Терминальная фаза (при отсутствии лечения и резистентность к проводимой терапии)
Симптомы (признаки)
Клиническая картина острых лейкозов определяется степенью инфильтрации костного мозга бластными клетками и угнетения ростков кроветворения • Угнетение костномозгового кроветворения •• Анемический синдром (миелофтизная анемия) •• Геморрагический синдром (вследствие тромбоцитопении отмечают кожные геморрагии — петехии, экхимозы; кровотечения из слизистых оболочек — носовые кровотечения, внутренние кровотечения) •• Инфекции (нарушение функции лейкоцитов) • Лимфопролиферативный синдром •• Гепатоспленомегалия •• Увеличение лимфатических узлов • Гиперпластический синдром •• Боли в костях •• Поражения кожи (лейкемиды), мозговых оболочек (нейролейкоз) и внутренних органов • Интоксикационный синдром •• Снижение массы тела •• Лихорадка •• Гипергидроз •• Выраженная слабость.
Диагностика
Диагноз острого лейкоза подтверждают наличием бластов в костном мозге. Для идентификации подтипа лейкоза применяют гистохимические, иммунологические и цитогенетические методы исследования.
Лабораторные исследования • В периферической крови уровень лейкоцитов может варьировать от выраженной лейкопении (ниже 2,0109/л) до гиперлейкоцитоза; анемия, тромбоцитопения; наличие бластных клеток вплоть до тотального бластоза • Гиперурикемия вследствие ускоренного жизненного цикла клеток • Гипофибриногенемия и повышение содержания продуктов разрушения фибрина вследствие сопутствующего ДВС. Влияние ЛС. ГК не следует назначать до постановки окончательного диагноза. Высокая чувствительность к преднизолону бластных клеток приводит к их разрушению и трансформации, затрудняющим диагностику.
Лечение комплексное; цель — достижение полной ремиссии. В настоящее время в гематологических центрах используют различные протоколы химиотерапии, основанные на принципах полихимиотерапии и интенсификации лечения.
• Химиотерапия состоит из нескольких этапов •• Индукция ремиссии ••• При ОЛЛ — одна из схем: комбинации винкристина в/в еженедельно, преднизолона внутрь ежедневно, даунорубицина и аспарагиназы в течение 1–2 мес непрерывно ••• При ОМЛ — сочетание цитарабина в/в капельно или п/к, даунорубицина в/в, иногда в сочетании с тиогуанином. Более интенсивная постиндукционная химиотерапия, уничтожающая оставшиеся лейкозные клетки, увеличивает длительность ремиссии •• Консолидация ремиссии: продолжение системной химиотерапии и профилактика нейролейкоза при ОЛЛ (эндолюмбальное введение метотрексата при ОЛЛ в сочетании с лучевой терапией на головной мозг с захватом спинного мозга [C1–C2]) •• Поддерживающая терапия: периодические курсы реиндукции ремиссии.
• При ОМЛ М3 проводят лечение препаратами ретиноевой кислоты (третиноин).
• Трансплантация костного мозга — метод выбора при острых миелобластных лейкозах и при рецидивах всех острых лейкозов. Главное условие для проведения трансплантации — полная клинико — гематологическая ремиссия (содержание бластов в костном мозге менее 5%, отсутствие абсолютного лимфоцитоза). Перед операцией можно провести химиотерапию в сверхвысоких дозах, изолированно или в сочетании с лучевой терапией (с целью полного уничтожения лейкозных клеток) •• Оптимальный донор — однояйцовый близнец или сибс; чаще используют доноров с 35% — совпадением по Аг HLA. При отсутствии совместимых доноров используют аутотрансплантацию костного мозга, взятого в период ремиссии •• Главное осложнение — реакция трансплантат против хозяина. Развивается вследствие пересадки Т — лимфоцитов донора, распознающих Аг реципиента как чужеродные и вызывающих иммунную реакцию против них. Острая реакция развивается в течение 20–100 дней после трансплантации, отсроченная — через 6–12 мес ••• Основные органы — мишени — кожа (дерматит), ЖКТ (диарея) и печень (токсический гепатит) ••• Лечение длительное, обычно ограничено назначением комбинаций преднизолона, циклоспорина и малых доз азатиоприна •• На течение посттрансплантационного периода влияют также подготовительные схемы лечения, развитие интерстициальной пневмонии, отторжение трансплантата (редко).
• Заместительная терапия •• Трансфузия эритроцитарной массы для поддержание уровня Hb не ниже 100 г/л. Условия трансфузий: неродственный донор, использование лейкоцитарных фильтров •• Трансфузия свежей тромбоцитарной массы (снижает риск кровотечений). Показания: содержание тромбоцитов менее 20109/л; геморрагический синдром при содержании тромбоцитов менее 50109/л.
• Профилактика инфекций — главное условие выживания пациентов с нейтропенией, возникшей вследствие химиотерапии •• Полная изоляция пациента •• Строгий санитарно — дезинфекционный режим — частые влажные уборки (до 4–5 р/сут), проветривание и кварцевание палат; использование одноразового инструментария, стерильной одежды медицинского персонала •• Профилактическое применение антибиотиков, противогрибковых и противовирусных препаратов (при содержании сегментоядерных нейтрофилов менее 0,5109/л показана профилактика пневмоцистной пневмонии) ••• При повышении температуры тела проводят клиническое и бактериологическое исследования и немедленно начинают лечение комбинациями бактерицидных антибиотиков широкого спектра действия: цефалоспоринов, аминогликозидов и полусинтетических пенициллинов ••• При вторичных подъёмах температуры тела, возникших после лечения антибиотиками широкого спектра действия, эмпирически применяют противогрибковые средства (амфотерицин В) •• Для профилактики и лечения нейтропении можно назначить колониестимулирующие факторы (например, молграмостим).
Прогноз • Прогноз у детей с острым лимфолейкозом хороший: у 95% и более наступает полная ремиссия. У 70–80% больных проявлений болезни нет в течение 5 лет, их считают излечившимися. При возникновении рецидива в большинстве случаев можно достичь второй полной ремиссии. Больные со второй ремиссией — кандидаты на трансплантацию костного мозга с вероятностью долговременного выживания 35–65% • Прогноз у больных острым миелобластным лейкозом неблагоприятный. 75% больных, получающих адекватное лечение с использованием современных химиотерапевтических схем, достигают полной ремиссии, 25% больных погибают (длительность ремиссии — 12–18 мес). Есть сообщения об излечении в 20% случаев при продолжении интенсивной терапии после ремиссии. Прогноз при М3 — варианте ОМЛ улучшается при лечении препаратами ретиноевой кислоты. Больным моложе 30 лет после достижения первой полной ремиссии можно проводить трансплантацию костного мозга. У 50% молодых больных, подвергшихся аллогенной трансплантации, развивается длительная ремиссия. Обнадёживающие результаты получены и при пересадках аутологичного костного мозга.
Возрастные особенности
• Дети •• 80% всех острых лейкозов — ОЛЛ •• Неблагоприятные прогностические факторы при ОЛЛ ••• Возраст ребёнка младше 1 года и старше 10 лет ••• Мужской пол ••• Т — клеточный вариант ОЛЛ ••• Содержание лейкоцитов в момент диагностики более 20109/л ••• Отсутствие клинико — гематологической ремиссии на фоне проводимой индукции •• Прогноз и течение. 80% выхода в клинико — гематологическую ремиссию. 5 — летняя выживаемость — 40–50%.
• Пожилые. Снижена толерантность к аллогенному костному мозгу. Максимальный возраст для трансплантации — 50 лет. Аутологичную трансплантацию можно проводить пациентам старше 50 лет при отсутствии органных поражений и общем соматическом благополучии.
Сокращения • МДС — миелодиспластический синдром • ОЛЛ — острый лимфобластный лейкоз • ОМЛ — острый миелобластный лейкоз.
МКБ-10 • C91.0 Острый лимфобластный лейкоз • C92 Миелоидный лейкоз [миелолейкоз] •• C93.0 Острый моноцитарный лейкоз
Лекарственные средства и Медицинские препараты применяемы для лечения и/или профилактики «Лейкоз острый».
Источник
