Нарушение гемостаза при геморрагических диатезах и двс синдромах
Геморрагические диатезы – общее название ряда гематологических синдромов, развивающихся при нарушении того или иного звена гемостаза (тромбоцитарного, сосудистого, плазменного). Общими для всех геморрагических диатезов, независимо от их происхождения, являются синдром повышенной кровоточивости (рецидивирующие, длительные, интенсивные кровотечения, кровоизлияния различных локализаций) и постгеморрагический анемический синдром. Определение клинической формы и причин геморрагических диатезов возможно после всестороннего обследования системы гемостаза — проведения лабораторных тестов и функциональных проб. Лечение включает гемостатическую, гемотрансфузионную терапию, местную остановку кровотечений.
Общие сведения
Геморрагические диатезы – болезни крови, характеризующиеся наклонностью организма к возникновению спонтанных или неадекватных травмирующему фактору кровоизлияний и кровотечений. Всего в литературе описано свыше 300 геморрагических диатезов. В основе патологии лежат количественные либо качественные дефекты одного или нескольких факторов свертывания крови. При этом степень кровоточивости может варьировать от мелких петехиальных высыпаний до обширных гематом, массивных наружных и внутренних кровотечений.
По приблизительным данным, в мире около 5 млн. населения страдает первичными геморрагическими диатезами. С учетом вторичных геморрагических состояний (например, ДВС-синдрома), распространенность геморрагических диатезов поистине велика. Проблема осложнений, связанных с геморрагическими диатезами, находится в поле зрения различных медицинских специальностей – гематологии, хирургии, реаниматологии, травматологии, акушерства и гинекологии и мн. др.

Геморрагические диатезы
Классификация геморрагических диатезов
Геморрагические диатезы принято различать в зависимости от нарушения того или иного фактора гемостаза (тромбоцитарного, коагуляционного или сосудистого). Этот принцип положен в основу широко используемой патогенетической классификации и в соответствии с ним выделяют 3 группы геморрагических диатезов: тромбоцитопатии, коагулопатии и вазопатии.
Тромбоцитопении и тромбоцитопатии, или геморрагические диатезы, связанные с дефектом тромбоцитарного гемостаза (тромбоцитопеническая пурпура, тромбоцитопении при лучевой болезни, лейкозах, геморрагической алейкии; эссенциальная тромбоцитемия, тромбоцитопатии).
Коагулопатии, или геморрагические диатезы, связанные с дефектом коагуляционного гемостаза:
- с нарушением первой фазы свертывания крови – тромбопластинообразования (гемофилия)
- с нарушением второй фазы свертывания крови – превращения протромбина в тромбин (парагемофилия, гипопротромбинемии, болезнь Стюарта Прауэр и др.)
- с нарушением третьей фазы свертывания крови – фибринообразования (фибриногенопатии, врожденная афибриногенемическая пурпура)
- с нарушением фибринолиза (ДВС-синдром)
- с нарушением коагуляции в различных фазах (болезнь Виллебранда и др.)
Вазопатии, или геморрагические диатезы, связанные с дефектом сосудистой стенки (болезнь Рандю-Ослера-Вебера, геморрагический васкулит, авитаминоз С).
Причины геморрагических диатезов
Различают наследственные (первичные) геморрагические диатезы, манифестирующие в детском возрасте, и приобретенные, чаще всего являющиеся вторичными (симптоматическими). Первичные формы являются семейно-наследственными и связаны с врожденным дефектом или дефицитом обычно одного фактора свертывания. Примерами наследственных геморрагических диатезов служат гемофилия, тромбостения Гланцмана, болезнь Рандю-Ослера, болезнь Стюарта Прауэр и др. Исключение составляет болезнь Виллебранда, являющаяся полифакторной коагулопатией, обусловленной нарушением фактора VIII, сосудистого фактора и адгезивности тромбоцитов.
К развитию симптоматических геморрагических диатезов обычно приводит недостаточность сразу нескольких факторов гемостаза. При этом может отмечаться уменьшение их синтеза, повышение расходования, изменение свойств, повреждение эндотелия сосудов и пр. Причинами повышенной кровоточивости могут служить различные заболевания (СКВ, цирроз печени, инфекционный эндокардит), геморрагические лихорадки (лихорадка денге, Марбург, Эбола, Крымская, Омская и др.), дефицит витаминов (С, К и др.). В группу ятрогенных причин входит длительная или неадекватная по дозе терапия антикоагулянтами и тромболитиками.
Чаще всего приобретенные геморрагические диатезы протекают в форме синдрома диссеминированного внутрисосудистого свертывания (тромбогеморрагического синдрома), осложняющего самые различные патологии. Возможно вторичное развитие аутоиммунных, неонатальных, посттрансфузионных тромбоцитопений, геморрагического васкулита, тромбоцитопенической пурпуры, геморрагического синдрома при лучевой болезни, лейкозах и т. д.
Симптомы геморрагических диатезов
В клинике различных форм гемостазиопатий доминируют геморрагический и анемический синдромы. Выраженность их проявлений зависит от патогенетической формы геморрагического диатеза и сопутствующих нарушений. При различных видах геморрагических диатезов могут развиваться разные типы кровотечений.
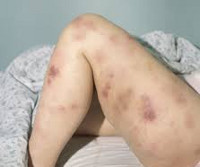
Микроциркуляторный (капиллярный) тип кровоточивости встречается при тромбоцитопатиях и тромбоцитопениях. Проявляется петехиально-пятнистыми высыпаниями и синяками на коже, кровоизлияниями в слизистые оболочки, кровотечениями после экстракции зуба, десневыми, маточными, носовыми кровотечениями. Геморрагии могут возникать при незначительном травмировании капилляров (при надавливании на кожу, измерении АД и пр.).
Гематомный тип кровоточивости характерен для гемофилии, возможен при передозировке антикоагулянтов. Характеризуется образованием глубоких и болезненных гематом в мягких тканях, гемартрозов, кровоизлияний в подкожно-жировую и забрюшинную клетчатку. Массивные гематомы приводят к расслоению тканей и развитию деструктивных осложнений: контрактур, деформирующих артрозов, патологических переломов. По происхождению такие кровотечения могут быть спонтанными, посттравматическими, послеоперационными.
Капиллярно-гематомные (смешанные) геморрагии сопровождают течение ДВС-синдрома, болезни Виллебранда, наблюдаются при превышении дозы антикоагулянтов. Сочетают петехиально-пятнистые кровоизлияния и гематомы мягких тканей.
Микроангиоматозный тип кровоточивости встречается при геморрагическом ангиоматозе, симптоматических капилляропатиях. При этих геморрагических диатезах возникают упорные рецидивирующие кровотечения одной или двух локализации (обычно носовые, иногда — желудочно-кишечные, легочные, гематурия).
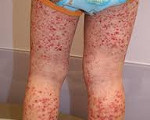
Васкулитно-пурпурный тип кровоточивости отмечается при геморрагических васкулитах. Представляет собой мелкоточечные геморрагии, как правило, имеющие симметричное расположение на конечностях и туловище. После исчезновения кровоизлияний на коже длительно сохраняется остаточная пигментация.
Частые кровотечения вызывают развитие железодефицитной анемии. Для анемического синдрома, сопровождающего течение геморрагических диатезов, характерны слабость, бледность кожных покровов, артериальная гипотония, головокружения, тахикардия. При некоторых геморрагических диатезах может развиваться суставной синдром (припухлость сустава, артралгии), абдоминальный синдром (тошнота, схваткообразные боли), почечный синдром (гематурия, боли в пояснице, дизурия).

Кожный геморрагический синдром
Диагностика
Целью диагностики геморрагических диатезов служит определение его формы, причин и степени выраженности патологических сдвигов. План обследования пациента с синдромом повышенной кровоточивости составляется гематологом совместно с лечащим специалистом (ревматологом, хирургом, акушером-гинекологом, травматологом, инфекционистом и др.).
В первую очередь исследуются клинические анализы крови и мочи, количество тромбоцитов, коагулограмма, кал на скрытую кровь. В зависимости от полученных результатов и предполагаемого диагноза назначается расширенная лабораторная и инструментальная диагностика (биохимическое исследование крови, стернальная пункция, трепанобиопсия). При геморрагических диатезах, имеющих иммунный генез, показано определение антиэритроцитарных антител (тест Кумбса), антитромбоцитарных антител, волчаночного антикоагулянта и др. Дополнительные методы могут включать функциональные пробы на ломкость капилляров (пробы жгута, щипка, манжеточную пробу и др.), УЗИ почек, УЗИ печени; рентгенографию суставов и др. Для подтверждения наследственной природы геморрагических диатезов рекомендуется консультация генетика.
Лечение геморрагических диатезов
При подборе лечения практикуется дифференцированный подход, учитывающий патогенетическую форму геморрагического диатеза. Так, при повышенной кровоточивости, вызванной передозировкой антикоагулянтов и тромболитиков, показана отмена данных препаратов или коррекция их дозы; назначение препаратов витамина К (викасола), аминокапроновой кислоты; переливание плазмы. Терапия аутоиммунных геморрагических диатезов основана на применении глюкокортикоидов, иммунодепрессантов, проведении плазмафереза; при нестабильном эффекте от их применения требуется проведение спленэктомии.
При наследственном дефиците того или иного фактора свертываемости показано проведение заместительной терапии их концентратами, трансфузий свежезамороженной плазмы, эритроцитарной массы, гемостатической терапии. С целью местной остановки небольших кровотечений практикуется наложение жгута, давящей повязки, гемостатической губки, льда; проведение тампонады носа и пр. При гемартрозах выполняются лечебные пункции суставов; при гематомах мягких тканей – их дренирование и удаление скопившейся крови.
Основные принципы лечения ДВС-синдрома включают активное устранение причины данного состояния; прекращение внутрисосудистого свертывания, подавление гиперфибринолиза, проведение заместительной гемокомпонентной терапии и т. д.
Осложнения и прогноз
Наиболее частым осложнением геморрагических диатезов служит железодефицитная анемия. При рецидивирующих кровоизлияниях в суставы может развиться их тугоподвижность. Сдавление массивными гематомами нервных стволов чревато возникновением парезов и параличей. Особую опасность представляют профузные внутренние кровотечения, кровоизлияния в головной мозг, надпочечники. Частое повторное переливание препаратов крови является фактором риска развития посттрансфузионных реакций, заражения гепатитом В, ВИЧ-инфекцией.
Течение и исходы геморрагических диатезов различны. При проведении адекватной патогенетической, заместительной и гемостатической терапии прогноз относительно благоприятный. При злокачественных формах с неконтролируемыми кровотечениями и осложнениями исход может быть фатальным.
Источник
ДВС-синдром (диссеминированнное внутрисосудистое свертывание крови) — приобретенное нарушение свертывающей системы крови, возникающее в результате чрезмерного образования факторов свертывания в периферической крови, которые вызывают образование тромбов в мелких кровеносных сосудах, сопровождающееся повреждением органов и тканей, а затем повышенной кровоточивостью.
Существует около ста клинических ситуаций, при которых развивается ДВС-синдром. Наиболее частые причины возникновения:
- * генерализованная инфекция, септические состояния;
- * все виды шока (травматический, ожоговый, анафилактический, септический);
- * обширные травматические хирургические вмешательства;
- * несовместимые переливания крови и другие виды внутрисосудистого гемолиза;
- • акушерская патология (преждевременное отделение последа, тяжелая эклампсия, внутриутробная гибель плода и др.);
- * опухоли, особенно гемобластозы;
- * деструктивные процессы в печени, поджелудочной железе, почках;
- * гемолитико-уремический синдром;
- * термические и химические ожоги;
- * системные заболевания соединительной ткани и другие иммунокомплексные заболевания (СКВ, СВ, гломерулонефрит и др.);
- * различные, значительно выраженные аллергические реакции;
- * тромботическая тромбоцитопеническая пурпура (болезнь Мошковиц);
- * отравление змеиным ядом;
- * массивные гемотрансфузии;
- * интенсивное лечение препаратами, повышающими агрегацию тромбоцитов и свертывание крови (аминокапроновая кислота, прогестины и др.);
- * лечение фибринолитиками и антикоагулянтами в больших дозах, истощающих резерв антитромбина III и антифибринолитической системы;
- * множественные и гигантские ангиомы;
- * трансплантация органов и тканей.
Основные факторы патогенеза синдрома ДВС (З.С. Баркаган, 1988):
- • активация свертывающей системы крови и тромбоцитарного гемостаза эндогенными (продуктами распада клеток крови и тканей, поврежденным эндотелием) и / или экзогенными факторами (околоплодными водами и пр.);
- • поражение эндотелия и снижение его антитромботического потенциала;
- • рассеянное внутрисосудистое свертывание крови и агрегация тромбоцитов и эритроцитов с образованием множества микросгустков и блокадой ими кровообращения в органах;
- • глубокие дистрофические и деструктивные нарушения в органах, нарушение их функции;
- • глубокие циркуляторные нарушения, гипоксия тканей, гемокоагуляционный шок, ацидоз, нарушения микроциркуляции;
- • коагулопатия потребления (вплоть до полной несвертываемости крови) с истощением противосвертывающих механизмов (дефицит антитромбина III и протеина С), компонентов фибринолитической и калликреин-кининовой систем (вслед за их интенсивной активацией), резкое повышение антиплазминовой активности;
- • вторичная тяжелая эндогенная интоксикация продуктами протеолиза и деструкции тканей.
Центральное место в патогенезе синдрома ДВС занимают образование в сосудистом русле тромбина и истощение как гемокоагуляционного потенциала, так и механизмов, препятствующих свертыванию крови и агрегации тромбоцитов.
Выделяют 4 стадии синдрома ДВС (Е. П. Иванов, 1991 и др.)
Стадия I — гиперкоагуляция и агрегация тромбоцитов.
Стадия II — переходная с нарастающей коагулопатией и тромбоцитопенией, разнонаправленными сдвигами в общих коагуляционных тестах.
Стадия III — глубокая гипокоагуляция (вплоть до полного несвертывания крови).
Стадия IV — восстановительная (или при неблагоприятном течении фаза исходов и осложнений).
По клиническому течению различают:
- * острый синдром ДВС, развивающийся внезапно в течение 24 ч;
- * подострый синдром ДВС, продолжающийся в течение 1-3 недель;
- * хронический синдром ДВС, продолжающийся более 1 месяца;
- * латентный синдром ДВС, протекающий без клинических проявлений, диагностирующийся лабораторно.
Клиническая картина ДВС-синдрома складывается из симптомов основного заболевания, признаков гемокоагуляционного или смешанного шока, глубокого нарушения всех звеньев системы гемостаза, тромбозов и геморрагий, гиповолемии и анемии, дисфункции и дистрофических изменений в органах и тканях, метаболических нарушений. Наиболее тяжелое и опасное течение характерно для острого синдрома ДВС.
Гемокоагуляционный шок обусловлен нарушением микроциркуляции в органах и их гипоксией, образованием в крови и поступлением в нее извне токсических продуктов протеолиза. Часто трудно проследить за трансформацией шока, послужившего причиной ДВС-синдрома, в гемокоагуляционный, поскольку они сливаются в общий острый срыв гемодинамики с катастрофическим падением артериального и центрального венозного давления, нарушением микроциркуляции в органах с развитием их острой недостаточности.
Нарушение микроциркуляции в органах в результате тромбогеморрагий в них с их дисфункцией и дистрофией определяет клиническую картину, тяжесть, исход и осложнение ДВС-синдрома. При этом могут страдать то одни, то другие органы, обозначаемые как «органы-мишени».
К «органам-мишеням» относятся легкие, в сосуды которых заносится огромное количество микросгустков фибрина, агрегатов клеток крови и продуктов протеолиза. В результате развивается острая легочно-циркуляторная недостаточность — одышка, цианоз, снижение рО2, а затем повышение рСО2 в артериальной крови, появляется интерстициальный отек, инфаркты легкого и др. признаки «шокового» легкого.
Острая почечная недостаточность проявляется снижением диуреза вплоть до полной анурии, появлением в моче белка, цилиндров, эритроцитов, нарушением водно-электролитного баланса и кислотно-основного состояния, нарастанием в сыворотке уровня мочевины и креатинина.
Реже развивается поражение печени с развитием паренхиматозной желтухи, а иногда и острыми болями в правом подреберье, увеличением печени с цитолитическим лабораторным синдромом (повышение АЛТ, АСТ).
Поражение желудка и кишечника сопровождается глубокой дистрофией слизистой оболочки двенадцатиперстной кишки, желудка, микротромбированием и стазом в их сосудах, появлением множественных геморрагий, образованием острых язв и эрозий.
Нарушение церебральной циркуляции, тромбозы и геморрагии в этой области дают разнообразную симптоматику — от головной боли, головокружения, спутанности сознания до типичных тромботических или геморрагических инсультов.
Поражение надпочечников и гипофиза, приводящие к типичной картине острой надпочечниковой недостаточности (затяжной коллапс, понос, электролитные нарушения, обезвоживание) и несахарному мочеизнурению, наблюдаемые при ДВС-синдроме септического и шокогенного генеза. Они связаны либо с тромбозами сосудов, питающих эти железы, либо с кровоизлияниями в них.
Геморрагический синдром — частое и опасное, но не обязательное проявление ДВС-синдрома. Важно разграничивать кровотечения локального типа, связанные с повреждением или деструктивными изменениями в органах, которые из-за нарушения гемостаза становятся катастрофическими, и распространенный геморрагический синдром, обусловленный общими сдвигами в системе гемостаза.
Локальные кровотечения — геморрагии из ран, послеродовые кровотечения, профузные геморрагии из язв желудка и 12-перстной кишки, гематурия вследствии инфаркта почек и т.д.
Общая кровоточивость характеризуется появлением синяков, кровоподтеков и гематом, подкожной и забрюшиной клетчатке, носовыми, желудочно-кишечными, легочными, почечными и другими кровотечениями в различные органы.
При подостром и затяжном ДВС-синдроме процесс часто начинается с длительного периода гиперкоагуляции, флеботромбозов с тромбоэмболиями и шемическими явлениями в органах. Затяжной ДВС-синдром наблюдается при большинстве онкологических, иммунокомплексных заболеваниях, при сердечной недостаточности, при циррозе печени, протезировании сосудов и др.
Диагностика. Разработана 3-х этапная система диагностики ДВС-синдрома (Лычев В.Г.). На первом этапе распознавание ДВС большое значение имеет ситуационная диагностика. Она основывается на тщательном анализе ситуации и знании круга основных заболеваний, при которых наблюдается наиболее частое и закономерное развитие ДВС-синдрома. На втором этапе выявляются и анализируются клинические симптомы и выделяются наиболее типичные для ДВС-синдрома симптомы. Особенно важны комбинированные нарушения органов (острая дыхательная недостаточность, ОПН, надпочечниковая недостаточность и др.), множественные геморрагии, сочетание тромбоза с кровоточивостью. Третий этап включает анализ наиболее информативных тестов коагулограммы: количество тромбоцитов, АПТВ, АКТ, протромбиновое время, паракоагуляционные тесты, концентрация фибриногена, антитромбина III. Изменения в системе гемокоагуляции, определяемые с помощью лабораторных методов, сохраняются дольше, чем клинические. Поэтому лабораторная диагностика ДВС-синдрома имеет первостепенное значение: позволяет более точно установить степень или фазу синдрома и выбрать правильное лечение. Вместе с тем следует учесть, что нет патогномоничных лабораторных признаков ДВС-синдрома и этот вид патологии диагностируется лишь на основании учета результатов определения нескольких параметров коагулограммы. При этом нарушения гемостаза проходят разные фазы — от гиперкоагуляции до более или менее глубокой гипокоагуляции.
Лечение
Своевременная коррекция нарушений в системе гемостаза при самой различной патологии может способствовать не только снижению дальнейшей активации протеолитических систем, профилактике тромбогеморрагического синдрома, но и более эффективному лечению основного заболевания. В ряде случаев лечение основного заболевания и ДВС-синдрома совпадают.
Основными направлениями лечения ДВС-синдрома следует считать:
Адекватное лечение основного заболевания и его осложнений (шок, интоксикация, бактериемия, инфаркт и др.)
Коррекция нарушений свертывающей функции крови: 1) антикоагулянтная; 2) тромболитическая; 3) антипротеолитическая; 4) трансфузионная терапия; 5) плазмоцитаферез.
Лечение и профилактика ДВС-синдрома должны проводиться с учетом вида процесса:
При латентном ДВС-синдроме целенаправленной медикаментозной коррекции системы гемостаза, как правило, не требуется;
При хроническом ДВС-синдроме назначают:
- · антиагреганты (тиклопидин 500-750 мг/сут, пентоксифиллин 300-600 мг/сут или дипиридамол 75-150 мг/сут);
- · при угрозе тромбозов — антивитамины К (неодикумарин 200-300 мг/сут) под контролем ПТИ (не ниже 40-50%) или профилактические дозы гепарина (2500-5000 ЕД каждые 6 часов) п/кожно в течение 7-10 сут с последующим переходом на непрямые антикоагулянты;
- · В ряде случаев (например, при остром коронарном синдроме) лечение начинают с инфузий гепарина 1000 ЕД/ч 1,5-2,5 раза) с последующим переходом на подкожное введение в течение 7-10 сут;
При подостром ДВС-синдроме назначают антиагреганты, реополиглюкин, гепарин п/к 5000-10 000 ЕД каждые 6 ч в течение 7-10 сут, концентраты АТ III, при необходимости повторно нативную, СЗП 200-400 мл;
Лечение острого ДВС синдрома проводится обязательно в отделении интенсивной терапии
Лечение I (гиперкоагуляционной) стадии. Должно проводиться лечение основного заболевания и коррекция гемодинамики: внутривенная инфузионная терапия (солевых растворов, реополиглюкина, альбумина) под контролем центрального венозного давления. При шоке: в/венно вводят большие дозы ГКС (гидрокортизона гемисукцинат или фосфат — 1000-1500 мг/сут; преднизолон до 600 мг/сут или дексаметазон до 150-200 мг в сутки). Способность ГКС повышать свертывание крови нивелируется гепарином. При шоке не рекомендуется применение симпатомиметиков из-за их способности повышать свертывание крови и агрегацию тромбоцитов, кроме допмина. Для лечения шока 200 мг (5 мл) допмина растворяют в 400 мл реополиглюкина или 5% р-ра глюкозы и вводят в/в, кап.
Гепаринотерапия и лечение криоплазмой являются базисными методами лечения гиперкоагуляционной стадии синдрома ДВС. Гепарин по рекомендациям 3. С. Баркагана (1990) должен вводиться в умеренных дозах — до 20 тыс. ЕД в сутки, из которых первые 10 тыс. ЕД вводят в/в струйно; оставшуюся часть в/в капельно по 1000 ЕД-500 ЕД в час или под кожу живота по 5 тыс. ЁД через 6-8 ч. П. А. Воробьев (1994) считает, что в большинстве случаев достаточно вводить 10 тыс. ЕД гепарина в 2-4 приема под кожу живота. Побочные действия гепарина: вторичное («рикошетное») тромбообразование при снижении уровня антитромбина III; тромбоцитопения в связи с увеличением убыли функционально активных тромбоцитов из кровяного русла.
Свежезамороженная плазма (криоплазма) служит источником антитромбина III, плазминогена, факторов свертывания крови и естественных антиагрегантов и необходима для восстановления антипротеолитической активности крови и объема циркулирующей крови. Криоплазму вводят внутривенно струйно 600-800 мл, а затем по 300-400 мл через каждые 6-8 ч. В начале каждого введения вводят внутривенно по 2500-5000 ЕД гепарина.
Антиагреганты — важный компонент терапии синдрома ДВС. Трентал 0,1 г в 250 мл 5%- глюкозы в/венно капельно; курантил по 0,1 г 3 раза в день внутрь; тиклопидин по 0,3 г 3 раза в день внутрь. Аспирин, по мнению 3. С. Баркагана (1988), при ДВС синдроме не назначается (из-за ульцерогенного действия и снижения антитромбоген-ного потенциала сосудистой стенки).
Для активации фибринолиза рекомендуют введение: в/в капельно 1% раствора никотиновой кислоты — 7-10 мл в 300 мл физиологического раствора, тканевого (эндотелиального) активатора плазминогена (лизирует фибрин, деблокирует микроциркуляцию).
Применение стрептокиназы, урокиназы не рекомендуется, поскольку они вызывают интенсивную деструкцию фибрина, фибриногена, резкое снижение активности факторов V и VIII, нарастание в крови ПДФ.
Плазмаферез — обязательный метод, применяемый в 1 стадии ДВС, необходимый для удаления избыточного количества факторов свертывания, токсических веществ и пр. Удаляют около 1,000 мл плазмы (с замещением СЗП в том же объеме) для получения хорошего клинического эффекта. Процедура проводится ежедневно и при необходимости 2 раза в сутки.
Ингибиторы протеолитических ферментов устраняют влияние продуктов белкового распада (высокотоксичных, повреждающих сосудистую стенку, усугубляющих нарушение микроциркуляции, усиливающих свертывание крови). Они наиболее показаны в гипокоагуляционной фазе, но, по мнению 3. С. Баркагана (1990), должны применяться и в I стадии. Рекомендуется вводить ингибиторы протеолиза внутривенно капельно (например, контрикал — 20 тыс. — 60 тыс. ЕД в сутки, гордокс 200 тыс. -500 тыс. КИЕ) под прикрытием 60-120 мг преднизолона.
При развитии острой почечной недостаточности при ДВС рекомендуется капельное внутривенное вливание допмина, который повышает сократительную способность миокарда и расширяет сосуды почек, увеличивает почечный кровоток. Кроме того, проводится лечение фуросемидом внутривенно, продолжаются инфузии гепарина и криоплазмы.
Лечение во II (промежуточной) стадии аналогично лечению в I стадии, но в зависимости от показателей коагулограммы возможно введение гепарина в меньшей дозе. Основой лечения по-прежнему являются плазмаферез и переливание криоплазмы.
Лечение в III (гипокоагуляционной) стадии
Криоплазма вводится в/венно струйно, при тяжелом кровотечении — 1000 мл, затем каждые 12 ч — по 500 мл. При отсутствии СЗП — антигемофильную плазму, нативную плазму, криопреципитат.
Ингибиторы протеолитических ферментов снижают высокую фибринолитическую активность и интенсивность кровотечений. Трасилол вводят от 50 до 150 тыс. ЕД в сутки, контрикал 20-60 тыс. ЕД/сут.
Плазмаферез назначается при тяжелом геморрагическом синдроме для удаления из крови ПДФ и других веществ, обладающих антикоагулянтным действием.
Переливание концентрата тромбоцитов патогенетически обосновано в связи с развитием тромбоцитопении.
Препараты, действующие на сосудистый гемостаз, резко снижают проницаемость сосудистой стенки, вызывают сужение капилляров и способствуют остановке кровотечения. Дицинон 2-4 мл в/мышечно, адроксон 1-2 мл 0,025% в/имышечно 2-3 раза в день. На локальный гемостаз воздействуют (через фиброгастроскоп) путем применения кровоостанавливающего клея, орошения аминокапроновой кислотой.
Купирование анемического синдрома проводят при снижении Нв< 50-60 г/л у лиц молодого и среднего возраста и < 80-70 г/л у лиц пожилого возраста. Переливают эритроцитарную массу не более 300 мл в сутки до уровня гематокрита 0,22.
В III (гипокоагуляционной) стадии не рекомендуется применение гепарина и антиагрегантов.
Источник
