Национальные рекомендации синдром раздраженного кишечника
Существует множество хронических и рецидивирующих гастроинтестинальных функциональных расстройств, которые не могут быть объяснены структурными или биохимическими отклонениями. Такие расстройства наблюдаются в глотке, пищеводе, желудке, желчных путях, кишечнике, аноректальной зоне.
Синдром раздраженного кишечника (СРК) относится к группе функциональных расстройств именно кишечника, куда также входят: функциональный метеоризм, функциональный запор, функциональная диарея и неспецифические функциональные расстройства кишечника. Главной особенностью СРК, отличающей его от других функциональных расстройств, является обязательное наличие абдоминальной боли [1].
СРК – функциональное расстройство ЖКТ, характеризующееся абдоминальными болями, метеоризмом и нарушением транзита кишечника при отсутствии специфических и уникальных органических изменений, хотя в некоторых случаях может быть выявлено микроскопическое воспаление (при постинфекционном СРК) [2].
Популяционные исследования оценивают распространенность синдрома раздраженного кишечника в 10–20%, однако имеются значительные географические и социально-экономические различия. СРК может появляться в любом возрасте, в т. ч. у детей (при среднем возрасте больных 24−41 год). Женщины страдают СРК примерно в 2 раза чаще, чем мужчины (например, в странах Азии, Индии, Шри-Ланке ситуация обратная и чаще к врачу обращаются именно мужчины). У женщин, как правило, симптомы более выраженные и в большей степени влияют на повседневную активность [3, 4].
СРК – это классическое психосоматическое заболевание. Психические симптомы и заболевания встречаются у таких пациентов в 3 раза чаще, чем у лиц с органическими заболеваниями кишечника. Чаще других симптомов выявляются тревожность и депрессия, но могут встречаться пациенты с фобиями, навязчивыми состояниями, нарушениями сна, паническими атаками и пр. Показательно, что распространенность СРК в психиатрических клиниках достигает 71% [5].
Клиническая картина
В соответствии с действующими в настоящее время Римскими критериями IV [6–8], чтобы отличить СРК от преходящих нарушений со стороны ЖКТ, абдоминальная боль должна отмечаться по меньшей мере 1 день в неделю за последние 3 мес.
СРК как функциональную патологию устанавливают при наличии у больного рецидивирующей боли, ассоциированной с 2 и более следующими обстоятельствами и симптомами:
1) дефекация;
2) изменение частоты дефекации;
3) изменение формы стула;
4) изменение частоты стула – менее 3-х дефекаций в неделю или более 3-х дефекаций за день;
5) патологическая форма стула (комковатый/твердый стул или жидкий водянистый);
6) натуживание при дефекации, императивные позывы, ощущение неполного опорожнения кишечника;
7) выделение слизи с калом;
8) вздутие живота.
Критерии валидны при их наличии в течение последних 3-х мес. и начале симптомов не менее 6 мес. назад [8]. Диагностические критерии 4−8 считаются дополнительными [9].
Таким образом, исходя из Римских критериев манифестацию СРК можно подразделить на 3 клинически формы:
I. Нарушение транзита.
II. Абдоминальные боли.
III. Вздутие живота.
I. Нарушение транзита. Нарушения кишечной моторики при СРК включают диарею, запор или их чередование. В такие периоды в стуле часто присутствует слизь, что связывают с перестройкой слизистой оболочки дистальных отделов толстой кишки с преобладанием бокаловидных клеток над обычными энтероцитами. Требуется тщательный сбор анамнеза, чтобы определить, что пациент называет запором, а что – диареей [10].
Диарея. Пациенты могут часто жаловаться на относительно нормальный стул, однако учащенный и водянистый в утренние часы, без дальнейших расстройств в течение остальной части суток. Другие пациенты, жалуясь на диарею, подразумевают частое посещение туалета с отхождением небольшого количества слизи, нормального кала или даже вовсе без кала. Наиболее выраженные нарушения стула бывают в утренние часы, часто после приема пищи, в оставшуюся часть дня состояние больного остается удовлетворительным [11].
Запор. Пациенты могут жаловаться на запор, если фактически при сохранении частоты дефекации выделяется небольшое количество твердых фекальных масс (овечий или ленточный стул). Необходимость натуживаться и ощущение неполного опорожнения кишечника пациенты могут также назвать запором.
Чередование симптомов. Часто у одного и того же больного наблюдается чередование симптомов. Изменения стула могут быть связаны с изменением жизненной ситуации или привычного образа жизни. Обучение выявлению факторов, приводящих к изменению стула, и их устранению поможет пациенту успешно управлять симптомами своего заболевания [12]. Однако нельзя исключать появление интеркуррентного соматического заболевания при указанных состояниях.
II. Абдоминальные боли. Боль в животе – главный симптом СРК, она может заметно варьировать по интенсивности и частоте. Появляются дискомфорт в животе, колики, острые интенсивные или тупые ноющие боли. Одни пациенты жалуются на ежедневные симптомы, другие сообщают о периодических болях с интервалом в недели и даже месяцы [13]. Боль после еды (очень частая жалоба) сочетается со вздутием, метеоризмом или обострением диареи, после дефекации, как правило, уменьшается. Боль появляется сразу после пробуждения или после приема пищи, может быть вызвана физическим напряжением или стрессовым событием [14].
Таким образом, для болевого синдрома или дискомфорта при СРК характерны следующие состояния:
1) усиление болей после приема пищи, а также уменьшение (но не полное исчезновение) боли или дискомфорта после дефекации или отхождения газов;
2) отсутствие прогресса болей с течением времени;
3) боли чаще не постоянные, а периодические, эпизоды острой боли накладываются на постоянную тупую боль;
4) боли чаще наблюдаются в левой подвздошной области, но могут носить диффузный характер, либо не имеют четкой локализации;
5) отсутствие ночной симптоматики [15].
Любое изменение такого «стабильного» течения может служить предупреждением для врача о появлении другой, возможно органической, патологии.
III. Вздутие живота. Многие пациенты ощущают дискомфорт от вздутия и растяжения кишечника, одежда становится для них тесной и неудобной. Нарушают покой повышенное кишечное газообразование, урчание, газоотделение.
Причина вздутия заключается в том, что часть невсосавшейся пищи может подвергаться брожению в рамках физиологической нормы, способствуя газообразованию. При этом ускорение транзита пищи в тонкой кишке при СРК может усилить процессы брожения с образованием газа и осмотически активных веществ типа короткоцепочечных жирных кислот, стул меняет свою консистенцию, становится более жидким или кашицеобразным.
Внекишечные проявления СРК
Здесь нужно сказать, что обращающихся за медицинской помощью пациентов с СРК можно условно разделить на 2 группы. В 1-ю группу (85–90%) входит категория лиц, которые хорошо приспосабливаются к своему заболеванию, не обращались к врачу, либо же однократно проходили обследование и лечение и благополучно справляются с проявлениями СРК самостоятельно. Вторая группа (10–15%) пациентов часто обращается к врачам, прибегает к инструментальным методам исследования, госпитализируется и даже подвергается оперативным вмешательствам. Для пациентов этой группы характерны длительные (не менее месяца) обострения, частые рецидивы симптомов на протяжении года. Зачастую у этих больных имеется отягощенный психосоциальный анамнез (физические, сексуальные домогательства, тяжелый стресс и т. д.), сопутствующая психопатология и необходимость психоневрологического лечения. Качество жизни таких больных значительно ухудшено [16, 17].
Именно для этих пациентов наиболее характерно проявление внекишечных симптомов СРК, а именно: слабость, утомляемость, головные боли по типу мигрени, ощущение кома в горле, неудовлетворенность вдохом, невозможность спать на боку из-за появляющихся неприятных ощущений в области сердца, диспепсические симптомы (тошнота, изжога, раннее насыщение), мочевые симптомы (дизурия, никтурия, частое мочеиспускание, императивные позывы, чувство неполного опорожнения), сексуальная дисфункция (в т. ч. диспареуния, слабость либидо), боли в спине [18].
Симптомы тревоги
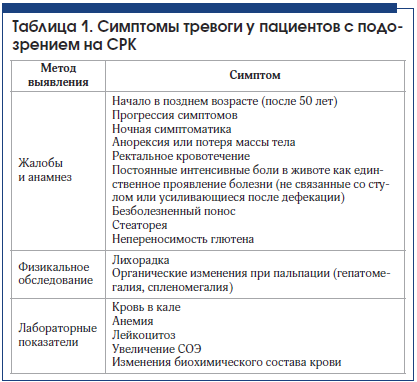
Одним из основных дифференциально-диагностических отличий СРК считается отсутствие симптомов в ночное время [19]. Есть ряд симптомов, которые не согласуются с синдромом раздраженного кишечника и которые должны насторожить врача относительно возможной органической патологии, так называемые симптомы тревоги (табл. 1) [20].
Классификация
После постановки диагноза необходимо классифицировать СРК по преобладающему признаку, чтобы в дальнейшем определить лечебную тактику. Классификация СРК происходит именно по форме стула [18], а не по частоте дефекаций, общепринятой является Бристольская шкала формы стула (рис. 1), где типы 1–2 относят к запору, а типы 6–7 – к диарее.
Выделяют 4 типа СРК (рис. 1):
1) с преобладанием запора – твердый или комковатый стул (типы 1–2 Бристольской шкалы) более 25% и жидкий или водянистый стул (типы 6–7) менее 25% дефекаций;
2) с преобладанием диареи – жидкий или водянистый стул (типы 6–7) более 25% и твердый или комковатый стул (типы 1–2) менее 25% дефекаций;
3) смешанный СРК – твердый или комковатый стул (типы 1–2) более 25% и жидкий или водянистый стул (типы 6–7) более 25% дефекаций;
4) неспецифический СРК – патологическая консистенция стула, не соответствующая предыдущим критериями.

Примечательно, что в течение года у 75% больных изменяется тип СРК.
Диагностика
Беспроигрышный путь к постановке диагноза СРК подразумевает целый ряд лабораторных и инструментальных исследований, чтобы подтвердить диагноз методом исключения. Этот подход требует времени и больших затрат, неудобен для пациента и может вызвать у него тревожный синдром.
Фактически у пациентов до 50 лет СРК уверенно может быть диагностирован на основании типичных симптомов, выявленных путем тщательного сбора анамнеза (в т. ч. оценив психологические факторы), объективного осмотра и при отсутствии симптомов тревоги [20].
Так, при обследовании проводят следующие основные исследования:
– общий анализ крови для выявления анемии, признаков воспаления, инфекции;
– биохимический анализ крови для оценки метаболических нарушений, в т. ч. электролитного дисбаланса у больных с диареей;
– копрологическое исследование на яйца гельминтов, скрытую кровь, патологические примеси, простейших, кишечных патогенов, лейкоцитов, токсинов Clostridium defficile.
Из инструментальных методов исследования кишечника определяющими служат эндоскопические (колоноскопия, ректороманоскопия) и рентгенконтрастное исследование – ирригоскопия, а также УЗИ органов брюшной полости, КТ, МРТ [4–5, 21–22].
По показаниям проводятся следующие исследования:
– определение скорости транзита по кишечнику, манометрия разных отделов толстой кишки;
– балонно-дилатационный тест с введением в прямую кишку латексного баллона с переходником длиной 3–4 см, через который в баллон вводят воздух [23];
– определение вегетативного статуса (метод интервалокардиографии) с определением вегетативного тонуса, вегетативной реактивности и вегетативного обеспечения различных форм деятельности, как правило, у больных с СРК определяются различные вегетативные дисфункции [24];
– для объективной оценки психологического статуса используют: 1) Госпитальную шкалу тревоги и депрессии (Hospital Anxiety-Depression Scale – HADS) – опросник из 14 пунктов, предназначенный для оценки уровня тревожности и депрессии; 2) тест на «чувство близости» (SOC); 3) опросник о состоянии здоровья (PHQ-15) из 15 вопросов, ответы на которые помогают выявить наличие множественных соматических симптомов; 4) Гиссенский соматический и личностный опросник; 5) опросник Леонгарда – Смишека для определения структуры личности [25].
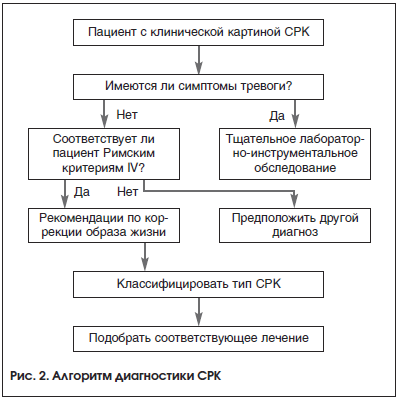
Дифференциальную диагностику проводят со многими заболеваниями, применяя при необходимости дополнительные исследования: воспалительные заболевания кишечника (ректальные кровотечения, изменения в анализах крови, патология при колоноскопии), лактазная недостаточность (связь симптомов с приемом молочных продуктов, дыхательный тест), целиакия (хроническая диарея, синдром мальабсорбции, наличие антител к тканевой трансглютаминазе, атрофия ворсинок и гипертрофия крипт по данным биопсии слизистой оболочки тонкого кишечника), хронический панкреатит, поражение, обусловленное приемом медикаментов (например, после приема слабительных, магнийсодержащих антацидов), острая инфекционная диарея (острое начало, позитивные результаты бактериологических исследований), паразитарные инфекции, синдром избыточного бактериального роста (СИБР) (водородный дыхательный тест), антибиотикоассоциированная диарея и псевдомембранозный колит, микроскопические колиты, спаечная болезнь толстой кишки, рак толстой кишки, дивертикулез, ишемический колит (наличие атеросклеротического стенозирования по данным ангиографии брыжеечных сосудов), психические расстройства (депрессия), метаболические нарушения (сахарный диабет, тиреотоксикоз, патология паращитовидной железы), гормонпродуцирующие опухоли [4, 26]. Алгоритм диагностики СРК представлен на рисунке 2.

Лечение
Важно объяснить пациенту значение психоэмоциональных факторов, во избежание тревожности представить медицинскую документацию с отсутствием отклонений от нормы в лабораторных и инструментальных методах исследования. Терапию назначают в зависимости от преобладания тех или иных симптомов [27].
Вылечить СРК в настоящее время невозможно. Терапия направлена на уменьшение симптомов и достижение длительной ремиссии. Залогом успеха лечения является индивидуальный подход к пациенту. Прежде всего, лекарственные препараты должны устранять доминирующие симптомы болезни, одновременно проводится коррекция психоэмоционального напряжения и образа жизни пациента. Существенной частью терапии является правильное построение беседы врача и больного, которая призвана создать атмосферу доверия и уверенности. Врачу необходимо уделить такому пациенту достаточное время, чтобы он мог изложить все жалобы. Только при полном взаимопонимании можно перейти к медикаментозной терапии (табл. 2). К сожалению, терапия СРК на сегодняшний день несовершенна. Препарат, который улучшает один симптом, может усугублять другой. Так, лоперамид, устраняя диарею, зачастую усиливает абдоминальную боль и вздутие. Примеров подобного несовершенства лечения множество [4, 5].

Из лекарственных препаратов хорошо зарекомендовал себя Иберогаст – препарат растительного происхождения. Препарат обладает выраженным противовоспалительным действием, а также нормализует тонус гладкой мускулатуры ЖКТ: способствует устранению спазма без влияния на нормальную перистальтику, а при пониженном тонусе и моторике оказывает тонизирующее, прокинетическое действие [28–30].
Иберогаст понижает афферентную чувствительность при раздражении кишечника серотонином или в случае чрезмерного перерастяжения, таким образом, исчезает повышенная висцеральная чувствительность. Этот эффект объясняется тем, что вещества, составляющие основу препарата, вступают во взаимодействие со специальными белками – рецепторами серотонина, и с опиоидными и мускариновыми рецепторами 3-го типа. Следовательно, Иберогаст обладает регулирующим перистальтику и чувствительность органов ЖКТ действием [28–30].
Иберогаст принимают до 20 капель 3 раза в течение суток, запивая незначительным количеством жидкости (2–3 столовые ложки воды). Препарат можно назначать уже на первом приеме у врача, до постановки окончательного диагноза, т. к. он характеризуется хорошей переносимостью и высоким профилем безопасности [28–30].
Относительно недавно в США зарегистрирован ряд новых препаратов для лечения СРК, которые хорошо зарекомендовали себя в рандомизированных клинических исследованиях. К этим лекарствам относятся: линаклотид, алосетрон и любипростон (не разрешены к применению в РФ).
Любипростон – производное простагландинов, но без системного действия. Действуя как селективный активатор хлорных каналов, любипростон усиливает cекрецию эпителиальных клеток слизистой оболочки кишечника, стимулируя вторично кишечный транзит содержимого. Препарат эффективен в лечении хронического функционального запора и СРК с запором. Линаклотид – селективный агонист гуанилатциклазы энтероцитов. Он увеличивает секрецию воды и электролитов энтероцитами и вторично стимулирует моторику кишечника. Показано, что применение линаклотида у больных с СРК с запором уменьшает боль в животе, увеличивает частоту дефекации, улучшает консистенцию стула, уменьшает напряжение при дефекации. Алосетрон – антагонист 5-НТ3-рецепторов. Эти рецепторы находятся на энтеральных нейронах ЖКТ. Их стимуляция вызывает гиперчувствительность и гиперреактивность кишечника. Алосетрон имеет строгие показания к назначению, что связано с его побочными действиями. Он показан женщинам с СРК и диареей более 6 мес., не имеющих анатомических аномалий ЖКТ, и не отвечающих на другую терапию [31–33].
Применение данных препаратов в клинической практике имеет широкие перспективы и будет большой помощью врачам в терапии синдрома раздраженного кишечника.
Источник
Brian E. Lacy, Ferm»n Mearin, Lin Chang, William D. Chey, Anthony J.
Lembo, Magnus Simren,Robin Spiller. Gastroenterology 2016;150:1393–1407.Ивашкин В.Т., Полуэктова Е.А. Сочетание синдрома функциональной
диспепсии и синдрома раздраженного кишечника. Российский журнал
гастроэнтерологии, гепатологии, колопроктологии, 2011, № 4. С. 75-81.Yarandi SS, Christie J. Functional Dyspepsia in Review:
Pathophysiology and Challenges in the Diagnosis and Management due to
Coexisting Gastroesophageal Reflux Disease and Irritable Bowel Syndrome.
Gastroenterol Res Pract., 2013.C.K. Nagasako, Garcia Montes C, Silva Lorena SL, Mesquita MA.
Irritable bowel syndrome subtypes: Clinical and psychological features,
body mass index and comorbidities. Rev Esp Enferm Dig. 2016
Feb;108(2):59-64.Cho HS, Park JM, Lim CH, Cho YK, Lee IS, Kim SW, Choi MG, Chung IS,
Chung YK. Anxiety, depression and quality of life in patients with
irritable bowel syndrome. Gut Liver., 2011 Mar;5(1):29-36.Mark Pimentel, Laura Hwang, Gil Y. Melmed, et.al. New Clinical
Method for Distinguishing D-IBS from Other Gastrointestinal Conditions
Causing Diarrhea: The LA/IBS Diagnostic Strategy. Digestive Diseases and
Sciences January 2010, Volume 55, Issue 1, pp 145-149.ПолуэктоваЕ.А. Некоторые особенности патогенеза, клиники,
диагностики и лечения синдрома раздражённого кишечника. Диссертация на
соискание ученой степени кандидата медицинских наук. Москва, 2001 г.Shalaby SA, Sayed MM, Ibrahim WA, Abdelhakam SM, Rushdy M. The
prevalence of coeliac disease in patients fulfilling Rome III criteri|
for irritable bowel syndrome. Arab J Gastroenterol. 2016 Jun 24. pii:
S1687-1979(16)30028-4.Шульпекова Ю.О., Баранская Е.К. Дифференциальная диагностика
синдрома раздраженного кишечника и глютеновой энтеропатии. Российский
журнал гастроэнтерологии, гепатологии, колопроктологии. 2009, Т.19. № 6,
С. 39-48.Jian-Feng Yang, Mark Fox, Hua Chu, Xia Zheng, Yan-Qin Long, Daniel
Pohl, Michael Fried, Ning Dai. Four-sample lactose hydrogen breath test
for diagnosis of lactose malabsorption in irritable bowel syndrome
patients with diarrhea. World J Gastroenterol. 2015 Jun 28; 21(24):
7563–7570.Leeds JS, Hopper AD, Sidhu R, Simmonette A, Azadbakht N, Hoggard N,
Morley S, Sanders DS. Some patients with irritable bowel syndrome may
have exocrine pancreatic insufficiency. Clin Gastroenterol Hepatol. 2010
May;8(5):433-8.Рациональная фармакотерапия заболеваний органов пищеварения
(руководство для практикующих врачей) под общей редакцией В.Т.Ивашкина,
Москва «Издательство «Литерра» 2011, стр. 506-516.Guagnozzi D, Arias Á, Lucendo AJ. Systematic review with
meta-analysis: diagnostic overlap of microscopic colitis and functional
bowel disorders. Aliment Pharmacol Ther. 2016 Feb 24.ИвашкинВ.Т., ШептулинА.А., ШифринО.С., ГалимоваС.Ф., ЮрмановаЕ.Н.
Микроскопический колит: клинические формы, диагностика, лечение.
Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2006,
Т.16, № 6, С. 56-60.Chachu KA, Osterman MT. How to Diagnose and Treat IBD Mimics in the
Refractory IBD Patient Who Does Not Have IBD. Inflamm Bowel Dis. 2016
May;22(5):1262-74.Shah E.D., Basseri R.J., Chong K., Pimentel M. Abnormal breath
testing in IBS: a meta-analysis // Dig. Dis. Sci. – 2010. – Vol. 55. – P. 2441-9.Кучумова С.Ю. Патогенетическое и клиническое значение кишечной
микрофлоры у больных с синдромом раздраженного кишечника. Диссертация на
соискание ученой степени кандидата медицинских наук. Москва, 2016 г.Longstreth GF, Tieu RS. Clinically Diagnosed Acute Diverticulitis in
Outpatients: Misdiagnosis in Patients with Irritable Bowel Syndrome. Dig
Dis Sci. 2016 Feb;61(2):578-88.Cuomo R, Barbara G, Andreozzi P et.al. Symptom patterns can
distinguish diverticular disease from irritable bowel syndrome. Eur J
Clin Invest. 2013 Nov;43(11):1147-55.Wu CY, Chang WP, Chang YH, Li CP, Chuang CM. The risk of irritable
bowel syndrome in patients with endometriosis during a 5-year follow-up:
a nationwide population-based cohort study. Int J Colorectal Dis. 2015
Jul;30(7):907-12.Mathur R, Ko A, Hwang LJ, Low K, Azziz R, Pimentel M. Polycystic
ovary syndrome is associated with an increased prevalence of irritable
bowel syndrome. Dig Dis Sci. 2010 Apr;55(4):1085-9.Layer P., Andresen V., Pehl C., et al. Guideline Irritable Bowel
Syndrome: Definition, Pathophysiology, Diagnosisand Therapy. Joint
Guideline of the German Society for Digestive and Metabolic Diseases
(DGVS) and the German Society for Neurogastroenterology and Motility
(DGNM). Z Gastroenterol 2011; 49:237-93.Moayyedi P, Quigley EM, Lacy BE, et al. The effect of dietary
intervention on irritable bowel syndrome: a systematic review. Clin
Transl Gastroenterol 2015:e107.Johannesson E, Ringström G, Abrahamsson H, Sadik R. Intervention to
increase physical activity in irritable bowel syndrome shows long-term
positive effects. World J Gastroenterol. 2015 Jan 14;21(2):600-8.Sackett DL, Strauss SE, Richardson WS, et al. Evidence-Based
Medicine: How to Practice and Teach EBM. Philadelphia, Pa:
Churchill-Livingstone; 2000.Ruepert et al. Bulking agents, antispasmodics and antidepressants
for the treatment of irritable bowel syndrome. The Cochrane
Collaboration The Cochrane Library 2013, Issue 3Ford AC, Moayyedi P, Lacy BE, et.al. American College of
Gastroenterology monograph on the management of irritable bowel syndrome
and chronic idiopathic constipation. Am J Gastroenterol. 2014 Aug;109
Suppl 1:S2-26.Hou X, Chen S, Zhang Y, Sha W, Yu X, Elsawah H. et al. Quality of
life in patients with Irritable Bowel Syndrome (IBS), assessed using the
IBS-Quality of Life (IBS-QOL) measure after 4 and 8 weeks of treatment
with mebeverine hydrochloride or pinaverium bromide: results of an
international prospective observational cohort study in Poland, Egypt,
Mexico and China. Clin Drug Investig. 2014;34(11):783-93.Boisson J, Coudert Ph, Dupuis J, Laverdant Ch, Toulet J Tolerance de
la mebeverine a long terme. Act Ther 1987;16(4):289-92.Шептулин А.А., Визе-Хрипунова М.А. Сравнительная оценка
американских, немецких, французских и российских рекомендаций по ведению
больных с синдромом раздраженного кишечника. РЖГГК он-лайн –
www.gastro-j.ru.Chang F.Y., Lu C.L., Chen C.Y., Luo J.C. Efficacy of dioctahedral
smectite in treating patients of diarrhea-predominant irritable bowel
syndrome // J. Gastroenterol. Hepatol. – 2007. – Vol. 22 (12). – P.
2266-72.Menees SB, Maneerattannaporn M, Kim HM, Chey WD. The efficacy and
safety of rifaximin for the irritable bowel syndrome: a systematic
review and meta-analysis // Am J Gastroenterol.2012 Jan;107(1):28-35.Schindlbeck NE, Müller-Lissner SA. Dietary fiber. Indigestible
dietary plant constituents and colon function. // Med Monatsschr Pharm.
1988 Oct;11(10):331-6.Müller-Lissner SA, Kaatz V, Brandt W, Keller J, Layer P. The
perceived effect of various foods and beverages on stool consistency.
Eur J Gastroenterol Hepatol. 2005 Jan;17(1):109-12.Bijkerk CJ, de Wit NJ, Muris JW., et al. Soluble or insoluble fibre
in irritable bowel syndrome in primary care? Randomised placebo
controlled trial. BMJ 2009; 339 : b3154.Tack J, Müller-Lissner S et al. Diagnosis and treatment of chronic
constipation – a European perspective. // NeurogastroenterolMotil.2011
Aug;23(8):697-710.Ивашкин В.Т., Алексеенко С.А., Колесова Т.А., Корочанская Н.В.,
Полуэктова Е.А., Симаненков В.И., Ткачев А.В., Трухманов А.С., Хлынов
И.Б., Шептулин А.А., Шифрин О.С. Резолюция Экспертного совета,
посвященного проблемам диагностики и лечения функциональных заболеваний
желудочно-кишечного тракта. РЖГГК. — 2016. — Т.26. — №4. — С.109-110.Mueller-Lissner S, Kamm MA et al. Multicenter, 4-week, double-blind,
randomized, placebo-controlledtrial of sodium picosulfate in patients
with chronic constipation // Am J Gastroenterol. 2010
Apr;105(4);897-903.Bengtsson M, Ohlsson B. Psychological well-being and symptoms in
women with chronic constipation treated with sodium picosulphate. //
Gastroenterol Nurs. 2005 Jan-Feb;28(1):3-12.А.А. Шептулин. Прукалоприд в лечении хронических запоров
функциональной природы. РЖГГиК – 2012. — Т. 22 — №1. — С.9-13.Muhammad S Sajid, Madhu Hebbar, Mirza K Baig, Andy Li, Zinu
Philipose. Use of Prucalopride for Chronic Constipation: A Systematic
Review and Meta-analysis of Published Randomized, Controlled Trials J
Neurogastroenterol Motil. 2016 Apr 29Delvaux M, Wingate D. Trimebutine: mechanism of action, effects on
gastrointestinal function and clinical results // J Int Med Res.1997
Sep-Oct;25(5):225-46.Zhong YQ et al. A randomized and case-control clinical study on
trimebutine maleate in treating functional dyspepsia coexisting with
diarrhea-dominant irritable bowel syndromе // ZhonghuaNeiKeZaZhi.2007
Nov;46(11):899-902.В.Т. Ивашкин, А.А. Шептулин, Е.А. Полуэктова, Д.В. Рейхарт, А.В.
Белостоцкий, А.А. Дроздова, В.С. Арнаутов. Возможности применения
Опросника «7×7»( 7 симптомов за 7 дней) для оценки динамики симптомов
функциональной диспепсии и синдрома раздраженного кишечника. РЖГГК. — 2016. — Т.26. — №3. — С.24.В.Т.Ивашкин, Е.А.Полуэктова, Д.В.Рейхарт, А.А.Шептулин, О.С.Ляшенко,
А.Г.Бениашвили, А.В.Белостоцкий. Эффективность наиболее часто
назначаемых групп препаратов у пациентов с функциональными
расстройствами желудочно-кишечного тракта (синдромом функциональной
диспепсии и синдромом раздраженного кишечника) (Результаты
наблюдательного исследования). РЖГГК. — 2016. — Т.26. — №4. — С.7-14.Ottillinger B, Storr M, Malfertheiner P, Allescher HD. STW 5
(Iberogast®)—a safe and effective standard in the treatment of
functional gastrointestinal disorders. Wien Med Wochenschr. 2013
Feb;163(3-4):65-72.Шептулин А.А., Кайбышева В.О. Эффективность применения растительного
препарата STW 5 в многоцелевой терапии функциональной диспепсии. РЖГГК.2015. — Т.25. — №5. — С.101-106.
Ивашкин В. Т., Маев И. В., Шептулин А. А. и соавт. Резолюция
Экспертного совета «Как улучшить результаты лечения больных с
функциональной диспепсией и синдромом раздраженного кишечника»?
Российский журнал гастроэнтерологии, гепатологии, колопроктологии, 2016,
№2, С. 101-104.Francisco Guarner, Aamir G. Khan, James Garisch et.al World
Gastroenterology Organisation Global Guidelines Probiotics and
prebiotics October 2011.Ford AC, Quigley EMM, Lacy BE, et al. Efficacy of prebiotics,
probiotics, and synbiotics in irritable bowel syndrome and chronic
idiopathic constipation: systematic review and meta-analysis. Am J
Gastroenterol 2014; 109:1547–1561.Tiequn B, Guanqun C, Shuo Z. Therapeutic effects of Lactobacillus in
treating irritable bowel syndrome: a meta-analysis. Intern Med.
2015;54(3):243-9.Dragana Skokovic-Sunjic Clinical Guide to PROBIOTIC SUPPLEMENTS
AVAILABLE IN CANADA: 2015 Еdition. Indications, Dosage Forms, and
Clinical Evidence to Date. TSteer T., Carpenter H., Tuohy K., Gibson G.R. Perspectives on the
role of the human gut microbiota and its modulation by pro- and
prebiotics // Nutrition Research Reviews. – 2000. – Vol. 13. – P.
229–54.Urbanska A.M., Bhathena J., Martoni C., Prakash S. Estimation of the
potential antitumor activity of microencapsulated Lactobacillus
acidophilus yogurt formulation in the attenuation of tumorigenesis in
Apc (Min/+) mice // Dig. Dis. Sci. – 2009. – Vol. 54. – P. 264–73.В. Т. Ивашкин, О. М. Драпкина, А. А. Шептулин, О. С. Шифрин, Е. А.
Полуэктова, С. Ю. Кучумова. Сравнительная эффективность композиции
Bifidobacterium bifidum, Bifidobacterium longum, Bifidobacterium
infantis, Lactobacillus rhamnosus и Saccharomyces boulardii в лечении
больных с диарейным вариантом синдрома раздраженного кишечника. РЖГГК. — 2015. — Т.25. — №2. — С.10.В. Т. Ивашкин, О. М. Драпкина, А. А. Шептулин, О. С. Шифрин, Е. А.
Полуэктова, С. Ю. Кучумова. Сравнительная эффективность композиции
Bifidobacterium bifidum, Bifidobacterium longum, Bifidobacterium
infantis, Lactobacillus rhamnosus и прукалоприда в лечении больных с
обстипационным вариантом синдрома раздраженного кишечника. РЖГГК. — 2015. — Т.25. — №3. — С.21-32.Ivashkin V., Drapkina O., Poluektova Ye., Kuchumova S., Sheptulin
A., Shifrin O. The Effect of a Multi-strain Probiotic on the Symptoms
and Small Intestinal Bacterial Overgrowth in Constipation-predominant
Irritable Bowel Syndrome: A Randomized, Simple-blind, Placebo-controlled
Trial. American Journal of Clinical Medicine Research, 2015, Vol. 3, No.
2, 18-23.Osler W. The principles and practice of medicine: designed for the
use of practitioners and students of medicine (1892), New York: D
Appleton and companyCreed F. Relationship between IBS and psychiatric disorder //
Irritable bowel syndrome (Ed. M. Camilleri, R. C. Spiller), 2002. –
p.45-54.Dekel R, Drossman DA, Sperber AD. The use of psychotropic drugs in
irritable bowel syndrome. Expert Opin Investig Drugs. 2013
Mar;22(3):329-39.Xie C, Tang Y, Wang Y, Yu T, Wang Y, Jiang L, Lin L. Efficacy and
Safety of Antidepressants for the Treatment of Irritable Bowel Syndrome:
A Meta-Analysis. PLoS One. 2015 Aug 7;10(8):e0127815.eCollection 2015.A.W. Bundeff, Woodis CB. Selective Serotonin Reuptake Inhibitors for
the Treatment of Irritable Bowel Syndrome. The Annals of
pharmacotherapy. 2014;48(6):777–84.Pae CU, Lee SJ, Han C, Patkar AA, Masand PS. Atypical antipsychotics
as a possible treatment option for irritable bowel syndrome. Expert Opin
Investig Drugs. 2013 May;22(5):565-72.Wouters MM et al. Histamine receptor H1–mediated sensitization of
TRPV1 mediates visceral hypersensitivity and symptoms in patients with
irritable bowel syndrome. Gastroenterology 2016 Apr; 150:875.Annaházi A, R-ka R, Roszt-czy A, Wittmann T. Role of antispasmodics
in the treatment of irritable bowel syndrome. World J Gastroenterol.
2014 May 28;20(20):6031-43.Albert U, Carmassi C, Cosci F, De Cori D, Di Nicola M, Ferrari S,
Poloni N, Tarricone I, Fiorillo A. Role and clinical implications of
atypical antipsychotics in anxiety disorders, obsessive-compulsive
disorder, trauma-related, and somatic symptom disorders: a systematized
review. Int Clin Psychopharmacol. 2016 Mar 11.Н.Н. Яхно, В.А. Парфенов, Д.В. Рейхарт, А.В. Белостоцкий, В.С.
Арнаутов. Многоцентровая неинтервенционная проспективная наблюдательная
программа изучения практики назначения препарата тералиджен у больных с
диагнозом вегетативного расстройства (СТАРТ-2: российский опыт
применения русскоязычной валидированной версии опросника 4DSQ.
Промежуточный анализ). Журнал неврологии и психиатрии им. С.С.
Корсакова. 2015;115(5): 27-33Constanze Hausteiner-Wiehle, Peter Henningsen. Irritable bowel
syndrome: Relations with functional, mental, and somatoform disorders.
World J Gastroenterol. 2014 May 28; 20(20): 6024–6030.Greenwood-Van Meerveld B, Moloney RD, Johnson AC, Vicario M.
Mechanisms of stress-induced visceral pain: implications in irritable
bowel syndrome. J Neuroendocrinol. 2016 Jan 8.Юрманова Е.Н. «Отдаленные результаты лечения и прогноз пациентов с
синдромом раздражённого кишечника» Диссертация на соискание ученой
степени кандидата медицинских наук. Москва, 2007 год.
Источник
