Мукополисахаридоз синдром моркио 4 а
В отличие от остальных типов мукополисахариодозов, синдром Моркио не связан со снижением интеллекта.
Как и большинство болезней накопления, Синдром Моркио (мукополисахаридоз 4 типа, МПС-IV) передается по аутосомно-рецессивному принципу. То есть проявляется у детей с вероятностью 25%, если оба родителя являются носителями одинаковой генетической мутации. Если мутация в гене есть только у одного родителя, то ребенок родится здоровым, но существует вероятность, что он также является носителем и передаст генетический дефект через поколение. МПС-IV встречается у 1 из 250 000 новорожденных.
На фоне этого генетического заболевания в организме снижена или вовсе прекращена выработка лизосомных ферментов: либо галактозамин-6-сульфат-сульфатазы (тогда развивается МПС-IV типа А), либо β-галактозидазы (развивается развивается МПС-IV типа В). В результате кислые мукополисахариды (правильнее называть их гликозамингликаны, ГАГ), которые должны расщепляться под их воздействием, не расщепляются. Их обмен нарушается, их количество становится избыточным – и это приводит к развитию патологии тех органов и тканей, где скапливается ГАГ (потому мукополисахаридозы и называют болезнями накопления).
Существуют разные группы ГАГ. Галактозамин-6-сульфат-сульфатаза и β-галактозидаза ответственны за обмен кератансульфатов, которые входят в состав костной и соединительной ткани. Соответственно, их накопление со временем приводит к поражению именно этих «мишеней» — костей и суставов, в меньшей степени – сосудов, мышц и роговицы глаза. Накопительный эффект становится заметен к полутора-трем годам и прогрессирует очень быстро.
Диагностика
Синдрома Моркио может быть диагностирован по результатам анализа мочи на уровень гликозамингликанов (ГАГ). Их выделение повышено при мукополисахаридозах всех типов, но только при Синдроме Моркио ГАГ в моче представлены исключительно в виде кератансульфатов. Однако при легких формах МПС-IV может наблюдаться нормальный уровень ГАГ, что приводит к задержке в постановке диагноза (часто ошибочно ставится диагноз «нанизм»). Поэтому предпочтительны:
- Анализ активности ферментов галактозамин-6-сульфат-сульфатазы и β-галактозидазы в лейкоцитах крови.
- ДНК-диагностика (можно провести по слюне ребенка в генетической лаборатории) для выявления мутаций в генах GALNS (для МПС IVA) и GBS (для МПС IVB).
В расширенную диагностическую программу при постановке диагноза «МПС-IV» включаются также:
- УЗИ органов брюшной полости, селезенки, почек. При Синдроме Моркио печень и селезенка не обязательно будут выражено увеличены, как при других типах МПС,
- Рентгенография скелета. При МПС-IV выявляются деформации грудной клетки, а также уплощение и расширение тел позвонков, чем объясняется характерное укорочение туловища и необычно короткая шея. Рентген длинных трубчатых костей выявляет укорочение костей предплечья: локтевая кость не достигает лучезапястного сустава. Контуры всех костей неровные.
- Электромиография (ЭМГ) и электронейромиография (ЭНМГ). Они позволяют оценить функциональное состояние мышечных тканей, нервов и нервно-мышечной передачи.
- Исследование функции внешнего дыхания (ФВД). Из-за патологии соединительной ткани при всех мукополисахаридозах возникает сужение трахеи.
- ЭКГ и ЭхоКГ, холтеровский мониторинг ЭКГ, суточный мониторинг артериального давления. Эти обследования проводятся ежегодно, т.к. у больных МПС-IV с детства отмечаются сердечно-сосудистые нарушения.
- МРТ головы и шеи – для выявления компрессии спинного мозга.
Пренатальная диагностика возможна путем измерения активности ферментов в биоптате ворсин хориона на 9-11 неделе беременности. Для семей с известным генотипом возможно проведение ДНК-диагностики при планировании беременности.
Симптомы
Дети рождаются без признаков болезни. Первые симптомы появляются в возрасте 1-3 года; к 7-8 годам клиническая картина уже полностью выражена.
Первое, на что следует обратить внимание родителям:
- Дисплазия тазобедренных суставов, не диагностированная в первые месяцы жизни, обнаруживается ближе к году.
- Существенная задержка роста тоже проявляется на втором году жизни. Дети с тяжелой формой заболевания обычно к восьми годам вырастают до 80—100 см и прекращают расти. При менее тяжелых формах заболевания продолжают расти до подросткового возраста и достигают 125 см.
- Тело развивается непропорционально: короткое туловище, короткая шея, маленькая голова.
- Зубы растут неровно, на большом расстоянии друг от друга. И даже молочные зубы склонны к кариесу и истончению эмали.
- С возрастом все заметнее проявляется Х-образная деформация ног.
Из-за повреждения костной ткани, суставов и межпозвоночных дисков детей могут беспокоить боли в спине и ногах, онемение или покалывание рук и ног, «мурашки». Из-за нарушения передачи нервных импульсов ребенок может с возрастом утратить контроль над функциями тазовых органов.
Лечение
В 2014 году Управление по контролю за продуктами и лекарствами (FDA) США одобрило препарат Вимизим (Vimizim) компании Биомарин Фармасьютикал для лечения MPS-IVA.
Действующее вещество препарата – альфа-элосульфаза, очищенный человеческий фермент, полученный с помощью генинженерных технологий. Такая фермент-заместительная терапия, предназначена только для лечения Синдрома Моркио типа А.
Вимизим представляет собой раствор для внутривенного введения. Рекомендуемая доза составляет 2 мг на кг веса, препарат вводится 1 раз в неделю с предварительным введением антигистаминых препаратов и антипиретиков, поскольку может вызывать сильные аллергические реакции и лихорадку. Терапия должна быть пожизненной.
Данные клинических исследований подтверждают, что Вимизим может улучшить выносливость и позволяет пациентам сохранить способность к самостоятельному передвижению, однако он не способен обратить вспять уже произошедшие изменения костной системы и не отменяет необходимости хирургической коррекции. Эффективность применения Вимизима у детей младше 5 лет (то есть при первых признаках заболевания) мало изучена, и ее результаты в долгосрочной перспективе вызывают настолько большие сомнения, что в большинстве стран Евросоюза пока отказались от применения альфа-элосульфазы у детей. В России препарат также не сертифицирован. Однако постклинические исследования продолжаются, и российские НИИ и больницы могут принимать в них участие – так что у детей с синдромом Моркио есть шанс попасть в программу исследований. Сейчас несколько пациентов получают лечение и находятся под наблюдением в Екатеринбурге, Ростовской области и Республике Саха. Информацию о наборе пациентов в исследовательские программы можно искать на сайте Союза пациентов и пациентских организаций по редким заболеваниям.
Препараты для ферментозаместительной терапии МПС-IV типа В находится в стадии тестирования на животных.
Перспективным методом, но также малоизученным, с точки зрения отложенных последствий, считается трансплантация стволовых клеток. Впервые такая процедура при МПС-IV была проведена в 1982 году. В мировой медицинской практике подтверждены несколько успешных операций, после которых мобильность пациентов улучшилась и сохранялась более 10 лет наблюдения, однако риски подобной операции очень высоки, поэтому решение о ее целесообразности остается за родителями. Стволовые клетки для трансплантации предпочтительно получать от родственных доноров (обычно из пуповинной крови или костного мозга), их вводят внутривенно пациенту. Иммунный ответ предполагает ранние и поздние эффекты. Ранние побочные эффекты связаны с иммуно-конфликтом, развитием сепсиса, тромбозами вен. Потенциальные поздние эффекты подразумевают застойную сердечную недостаточность, эндокринные заболевания и повышенный риск развития злокачественных образований. Однако в случае успеха трансплантация способствует улучшению двигательных навыков, слуха, функции сердца, улучшает функцию дыхания и предотвращает деформации кости. Прогноз особенно благоприятен, если провести трансплантацию ребенку до 2 лет. В более позднем возрасте деформации уже не могут быть устранены, но рост все равно улучшается. Поэтому так важна ранняя диагностика.
При невозможности трансплантации или отказе от нее остается симптоматическая терапия:
- При развитии сдавления спинного мозга рекомендовано хирургическое вмешательство на позвоночнике.
- После декомпрессии будет возможна хирургическая коррекция деформаций рук и ног.
- Несмотря на то, что пороки сердца при синдром Моркио развиваются реже, чем при других типах мукополисахариоза, ребенок должен находиться на диспансерном учете у кардиолога.
- Дважды в год требуется контроль со стороны отоларинголога и офтальмолога.
- Разрабатывается реабилитационная программа, включающая ЛФК и физиопроцедуры.
Как с этим жить
Поскольку у детей с синдромом Моркио сохранный интеллект, им, как и здоровым детям, нужны развивающие и обучающие программы. Есть смысл рассмотреть возможности инклюзивного образования.
Поскольку основные проблемы у этих детей связаны с патологией опорно-двигательного аппарата и трудностями передвижения, то для повышения качества их жизни нужно современное обрудование: электрокресла, выпрямители, ходунки. Имеет смысл закрепить поручни вдоль стен дома – чтобы ребенок мог самостоятельно передвигаться в помещении.
Полезные ссылки
https://spiporz.ru/ — Союз пациентов и пациентских организаций по редким заболеваниям.
https://www.everydayhealth.com/drugs/vimizim — Вимизим, доступная информация для пациентов
https://www.pediatr-russia.ru/sites/default/files/file/kr_mps4.pdf — Мукополисахаридоз IV типа, клинические рекомендации
https://www.mps-russia.org/ — Межрегиональная Благотворительная Общественная Организация «Общество инвалидов, страдающих синдромом Хантера, другими формами мукополисахаридоза и иными редкими генетическими заболеваниями»
Куда обратиться
- Центр молекулярной генетики (Молекулярно-генетический научный центр РАМН) med-gen.ru
- Генетическая лаборатория Генотек — https://www.genotek.ru/
- Медицинская компания ИНВИТРО — https://www.invitro.ru
- адаптивно-бытовое оборудование для инвалидов – invaprom.ru
- Городской центр орфанных и других редких заболеваний у детей и подростков — https://xn--90adclrioar.xn--p1ai/gorodskoy-tsentr-orfannykh-i-drugikh-redkikh-zabolevaniy-u-detey-i-podrostkov/
- ФГБУ «Научно-исследовательский детский ортопедический институт имени Г.И. Турнера» Министерства здравоохранения РФ (Санкт-Петербург, Пушкин) — https://www.rosturner.ru/
Источник
Мукополисахаридо́зы сокращённо МПС, или англ. MPS (от мукополисахариды + -ōsis) — группа метаболических заболеваний соединительной ткани, связанных с нарушением обмена кислых гликозаминогликанов (GAG, мукополисахаридов), связанных недостаточностью лизосомных ферментов обмена гликозаминогликанов. Заболевания вызваны наследственными аномалиями обмена, проявляются в виде лизосомной болезни накопления: различных дефектов костной, хрящевой, соединительной тканей.
Классификация[править | править код]
Современная классификация, в зависимости от характера ферментативного дефекта, выделяет несколько основных типов мукополисахаридозов:
- I тип — синдром Гурлер (мукомполисахаридоз I H — Hurler[3]), синдром Шейе (мукополисахаридоз I S — Scheie[4]), синдром Гурлер-Шейе (мукополисахаридоз I H/S — Hurler-Scheie[5]). Обусловлен дефицитом альфа-L-идуронидазы (фермент катаболизма мукополисахаридов). Заболевание постепенно приводит к накоплению в тканях гепарансульфата и дерматансульфата. Выделяют три фенотипа: синдром Гурлер, синдром Шейе и синдром Гурлер-Шейе.
- II тип — синдром Хантера[6]
- III тип — синдром Санфилиппо: A[7], B[8], C[9], D[10]
- IV тип — синдром Моркио: A[11], B[12]
- VI тип — синдром Марото—Лами[13]
- VII тип — синдром Слая (дефицит β-глюкуронидазы)[14]
Встречающийся в литературе термин «гаргоилизм», введенный в клинику английским врачом Эллисом (англ. R. W.В. Ellis) в 1936 году до открытия биохимической основы патологического процесса, объединяет мукополисахаридозы типа I (Н, S, H/S) и типа II (синдром Хантера)[15].
Патогенез[править | править код]
В зависимости от недостаточности одного из ферментов лизосом, накапливаются мукополисахариды одного из трёх классов: гепаран-, дерматан- или кератансульфаты[15].
Наследование[править | править код]
Подавляющее большинство мукополисахаридозов (практически все) наследуются по аутосомно-рецессивному типу. Исключение составляет болезнь Хантера (мукополисахаридоз II типа), которая наследуется по X-сцепленному рецессивному механизму[15].
Клиническая картина[править | править код]
В клинической практике все 12 известных мукополисахаридозов согласно фенотипу делят на две группы: Гурлер-подобный (10) и Моркио-подобный фенотип (2: синдром Моркио A и B)[16]:
| Фенотипы мукополисахаридоза[16]: | |
|---|---|
Гурлер-подобный фенотип: | Моркио-подобный фенотип: |
низкий рост с диспропорциональным строением скелета (относительно длинными конечностями, короткими туловищем и шеей); | диспропорциональная карликовость; |
грубые черты лица (запавшее переносье, нередко экзофтальм, густые сросшиеся брови, полные губы, большой, нередко не помещающийся в полости рта язык); | грубоватые черты лица; |
костные деформации (кифосколиоз, воронкообразная деформация грудной клетки); | килевидная деформация грудной клетки; |
контрактуры крупных и мелких суставов; | гипермобильность межфаланговых и тугоподвижность крупных суставов; |
мышечная гипотония; | «браслетки», «чётки», увеличение объёма коленных суставов и их вальгусная деформация; |
наличие пупочной и пахово-мошоночной грыжи; | |
гипертрофия лимфатического глоточного кольца; | |
гипертрихоз; | |
гепатоспленомегалия. | |
| Типична патология: | |
центральной нервной системы (снижение интеллекта, обычно довольно грубое); | нормальный интеллект. |
органов зрения (помутнение роговицы, глаукома); | Патология других органов и систем идентична изменениям у пациентов с Гурлер-подобным фенотипом мукополисахаридоза. |
слуха (тугоухость различной степени выраженности); | |
сердечно-сосудистой системы (недостаточность клапанов сердца, гипертрофия миокарда, нарушения сердечного ритма); | |
бронхолёгочной системы (синусобронхопатии с образованием обильного количества слизисто-гнойного отделяемого, снижение показателей функции внешнего дыхания, апноэ). | |
Диагностика[править | править код]
- Определение активности лизосомальных гидролаз.
- Исследование мочи на ГАГ.
См. также[править | править код]
- Генные болезни
- Лизосомные болезни накопления
Примечания[править | править код]
Литература[править | править код]
- Harrison’s Principles of Internal Medicine
Ссылки[править | править код]
- Все о синдроме Хантера и других формах мукополисахаридоза
- Мукополисахаридозы
- Белорусская организация больных мукополисахаридозом и другими редкими генетическими заболеваниями
- Справочник химика 21: Лизосомные болезни накопления
Источник
Мукополисахаридоз – наследственное заболевание соединительной ткани, связанное с нарушением обмена гликозаминогликанов, для которого характерен специфический внешний вид лица, аномалии глаз, костей, селезенки, печени. В некоторых случаях заболевание может сопровождаться задержкой умственного развития.
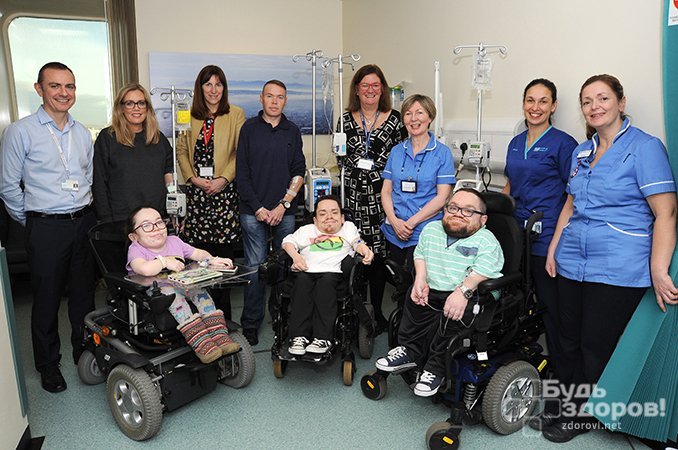
Существуют различные типы мукополисахаридоза, развитие каждого из которых обусловлено определенной генетической аномалией, которая оказывает влияние на синтез специфического фермента.
Существующие методы лечения мукополисахаридоза имеют низкий уровень эффективности.
Причины мукополисахаридоза
Причиной развития мукополисахаридоза является нарушение ферментативного катализа гликозаминогликанов в лизосомах. При мукополисахаридозе нарушается процесс расщепления и сохранения мукополисахаридов, которые являются основными компонентами соединительной ткани. Избыток мукополисахаридов проникает в кровь и накапливается в тканях. Поэтому данное заболевание относят к болезням накопления.
В настоящее время выявлено 10 генетических типов мукополисахаридоза, четыре из которых возникают при нарушении активности гликозидаз, пять – сульфатаз, один развивается в случае дефицита трансферазы.
Заболевание наследуется по аутосомно-рецессивному и рецессивному, сцепленному с Х-хромосомой типам.
Типы и симптомы мукополисахаридоза
Выделяют следующие типы мукополисахаридоза:
- I тип или синдром Гурлера;
- II тип или синдром Гунтера;
- III тип или синдром Санфилиппо;
- IV тип или синдром Моркио;
- V тип или синдром Шейе;
- VI тип или синдром Марото-Лами;
- VII тип или синдром Слая;
- VIII тип или синдром Ди Ферранте.
Симптомы мукополисахаридоза обнаруживаются у ребенка на первом году жизни и уже к 12-24 месяцам они становятся довольно выраженными.
У таких детей наблюдаются:
- Череп в форме лодочного киля;
- Шумное дыхание ртом;
- Грубые черты лица;
- Отставание в росте;
- Деформации скелета;
- Постепенное развитие сгибательных контрактур;
- Увеличение размеров живота;
- Пупочные и паховые грыжи;
- Гидроцеле;
- Изменения со стороны глаз: помутнение и увеличение размеров роговицы, врожденная глаукома, атрофия сосков зрительных нервов, застойные явления на глазном дне, пигментная дистрофия сетчатки;
- Снижение слуха;
- Изменения со стороны сердца;
- Умственная отсталость;
- Повышенный тонус мышц, нарушение координации движений, параличи.
При I типе заболевания симптомы мукополисахаридоза при рождении отсутствуют. Первые симптомы мукополисахаридоза в виде ограниченного разгибания пальцев на руках наблюдаются только в 3-6 лет. Со временем уменьшается объем движений в других суставах рук. К периоду полового созревания все симптомы проявляются особенно ярко.
II тип мукополисахаридоза чаще встречается у мальчиков. Для больных характерны: скафоцефалия, грубые черты лица, низкий грубый голос, шумное дыхание, частые ОРВИ. В 3-4 года возникают нарушения координации движений. Наблюдается прогрессирующая тугоухость, остеоартриты, узелковые поражения кожи спины.
При наличии синдрома Санфилиппо (III тип) ребенок в течение 3-5 лет нормально развивается, хотя иногда могут наблюдаться затрудненное глотание и неуклюжая походка. После трех лет у ребенка начинает развиваться апатия, возникает задержка психомоторного развития, нарушается речь, грубеют черты лица, возникает недержание кала и мочи, ребенок перестает узнавать окружающих. Такие дети умирают в возрасте 10-20 лет из-за интеркуррентных инфекций.
IV тип мукополисахаридоза характеризуется появлением первых симптомов в 1-3 года. Наблюдаются: резкая задержка роста, непропорциональное телосложение, грубые черты лица, кифоз или сколиоз, деформация грудной клетки; контрактуры в плечевых, локтевых, коленных суставах; плоскостопие; снижение мышечной силы; снижение слуха; дистрофия роговицы. Больные не доживают до 20-летнего возраста по причине сердечно-легочной недостаточности.
Для синдрома Шейе (V тип) характерен низкий рост, уплощенная переносица, короткая шея, контрактуры суставов, гипотония мышц конечностей, вегетативная лабильность, снижение сухожильных рефлексов, значительное помутнение роговиц.
Синдром Марото-Лами (VI тип) впервые проявляется после 2 лет. Он характеризуется отставанием в росте, грубыми чертами лица, бочкообразной грудной клеткой, малыми размерами верхней челюсти, короткой шеей, сгибательными контрактурами суставов рук. Интеллект больных не страдает.
Мукополисахаридоз VII типа устанавливают лишь при детальном биохимическом исследовании.
Синдром Ди Ферранте (VIII тип) схож с синдромом Моркио, но отличается выраженной задержкой интеллектуального и психомоторного развития.
Диагностика мукополисахаридоза
Диагностика мукополисахаридоза основывается на его характерных проявлениях, результатах рентгенологического исследования, установления экскреции гликозаминогликанов с мочой, исследования активности ферментов в фибробластах кожи.
Диагностировать мукополисахаридоз можно еще до рождения ребенка, используя для анализа амниотическую жидкость или ворсины хориона.

Лечение мукополисахаридоза
В настоящее время специфического лечения мукополисахаридоза не разработано.
Как правило, терапия мукополисахаридоза носит симптоматический характер. Пациента при этом наблюдают врачи различных специализаций: педиатр (по причине частых острых респираторных вирусных инфекций), хирург (в связи с наличием грыж), ортопед (в связи с нарушениями опорно-двигательного аппарата), отоларинголог (в связи с хроническими синуситами и отитами, нарушениями слуха), офтальмолог, невропатолог, нейрохирург.
В лечении мукополисахаридоза используются различные гормональные препараты (глюкокортикоиды, кортикотропин, тиреоидин), витамин А, цитостатики, сердечные препараты, переливания лейкоцитарной массы, крови, плазмы. Но все это вызывает лишь временные улучшения.
При синдроме Гурлера может проводиться трансплантация костного мозга. При ранних сроках ее проведения (до 1,5 лет) она может в значительной мере улучшить прогноз болезни, но данная процедура может вызывать ряд осложнений.
В США, странах Европы и Японии для лечения мягких форм мукополисахаридоза I типа применяется препарат альдуразим, который замещает недостающий в организме пациента фермент и приводит к улучшению состояния дыхательной системы, костей и суставов. Но внутривенное введение препарата не останавливает поражения ЦНС, поскольку альдуразим не проникает из крови в мозг. Данное средство применяется в случаях, когда трансплантация невозможна или непосредственно перед трансплантацией костного мозга, чтобы улучшить состояния больного и замедлить развитие болезни.
Таким образом, мукополисахаридоз – это редкое заболевание с неблагоприятным прогнозом для жизни пациента, поскольку с течением времени проявления болезни только усиливаются, а эффективного способа ее лечения пока нет. Единственный способ предотвратить заболевание – это обнаружить его еще в неонатальном периоде и предпринять соответствующие меры.
Источник
