Мкб 10 код метаболический синдром
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Причины
- Симптомы
- Диагностика
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Названия
Метаболический синдром.

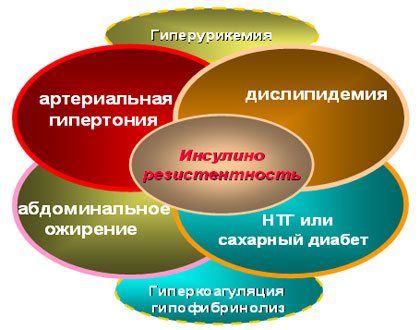
Основные звенья патогенеза метаболического синдрома
Описание
Метаболический синдром (МС, синдром X, синдром инсулинорезистентности) — совокупность метаболических нарушений, включающая избыточную массу тела с формированием ожирения по абдоминальному типу, ин- сулинорезистентности, дислипидемии и/или артериальной гипертензии. Наблюдаются и другие симптомы МС: микроальбуминурия, нарушения системы гемостаза.
Частота МС в зависимости от критериев включения несколько различна. Однако чётко установлена зависимость от возраста. В США МС был диагностирован у 6,7% обследованных в возрасте 20-29 лет, у 43,6% — 60-69 лет и у 42% — от 70 лет и старше. По данным исследования ВОЗ в популяции г. Новосибирска в возрасте 25-64 лет частота МС составила 40%.
Причины
Этиология неизвестна. Имеются исследования, которые указывают на роль следующих факторов развития МС:
1. Генетическая предрасположенность. У некоторых людей нечувствительность к инсулину заложена на генетическом уровне. Ген, который несет ответственность за развитие метаболического синдрома, находится в 19 хромосоме. Его мутации могут привести к тому, что.
У клеток недостаточно рецепторов, отвечающих за связывание инсулина;
Рецепторы не чувствительны к инсулину;
Иммунная система вырабатывает антитела, которые блокируют инсулиночувствительные рецепторы;
Поджелудочная железа вырабатывает аномальный инсулин.
Существует теория, согласно которой сниженная чувствительность к инсулину результат эволюции. Это свойство помогает организму благополучно пережить голод. Но у современных людей при потреблении калорийной и жирной пищи у таких людей развивается ожирение и метаболический синдром.
2. Диета с высоким содержанием жиров и углеводов – самый важный фактор развития метаболического синдрома. Насыщенные жирные кислоты, поступающие с животными жирами в большом количестве, способствуют развитию ожирения. Кроме того жирные кислоты вызывают изменения в оболочках клеток, делая их нечувствительными к действию инсулина. Чрезмерно калорийное питание приводит к тому, что в кровь поступает много глюкозы и жирных кислот. Их избыток откладывается в жировых клетках в подкожной жировой клетчатке, а также в других тканях. Это приводит к снижению их чувствительности к инсулину.
3. Малоподвижный образ жизни. Уменьшение физической активности влечет за собой снижение скорости всех обменных процессов, в том, числе и расщепления и усвоения жиров. Жирные кислоты блокируют транспорт глюкозы в клетку и снижают чувствительность ее мембраны к инсулину.
4. Длительная не леченная артериальная гипертония. Вызывает нарушение периферического кровообращения, которое сопровождается снижением чувствительности тканей к инсулину.
5. Пристрастие к низкокалорийным диетам. Если калорийность суточного рациона составляет менее 300 ккал, это приводит к необратимым нарушениям обмена веществ. Организм «экономит» и наращивает запасы, что приводит к усиленному жироотложению.
6. Стрессы. Длительные психические нагрузки нарушают нервную регуляцию органов и тканей. В результате нарушается производство гормонов, в том числе инсулина, и реакция клеток на них.
7. Приём препаратов-антагонистов инсулина: глюкагон, кортикостероиды, пероральные контрацептивы, тиреоидные гормоны.
Эти лекарственные препараты уменьшают поглощение тканями глюкозы, что сопровождается снижением чувствительности к инсулину.
8. Передозировка инсулина при лечении сахарного диабета. Неправильно подобранное лечение приводит к тому, что в крови находится большое количество инсулина. Это вызывает привыкание рецепторов. Инсулинорезистентность в этом случае является своеобразной защитной реакцией организма от высокой концентрации инсулина.
9. Гормональные нарушения. Жировая ткань является эндокринным органом и выделяет гормоны, которые снижают чувствительность к инсулину. Причем, чем более выражено ожирение, тем ниже чувствительность. У женщин при повышенной выработке тестостерона и сниженной эстрогена жиры накапливаются по «мужскому» типу, нарушается работа сосудов и развивается артериальная гипертензия. Снижение уровня гормонов щитовидной железы при гипотиреозе также способно вызвать повышение уровня липидов (жиров) в крови и развитие инсулинорезистентности.
10. Возрастные изменения у мужчин. С возрастом снижается выработка тестостерона, что приводит к инсулинорезистентности, ожирению и гипертонии.
11. Апное во сне. Задержка дыхания во сне вызывает кислородное голодание мозга и усиленную выработку соматотропного гормона. Это вещество способствуют развитию нечувствительности к инсулину.
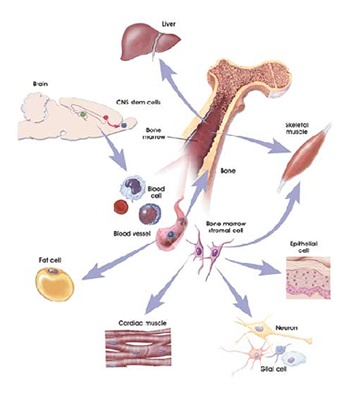
Органы-мишени при метаболическом синдроме
Симптомы
Субъективные ощущения при метаболическом синдроме.
Приступы плохого настроения в голодном состоянии. Плохое поступление глюкозы в клетки головного мозга вызывает раздражительность, приступы агрессии и плохого настроения.
Повышенная утомляемость. Упадок сил вызван тем, что несмотря на высокие показатели сахара в крови, клетки не получают глюкозу, остаются без питания и источника энергии. Причина «голодания» клеток в том, что не работает механизм, транспортирующий глюкозу через клеточную оболочку.
Избирательность в еде. Мясо и овощи не вызывают аппетит, хочется сладкого. Это связано с тем, что клетки мозга испытывают потребность в глюкозе. После потребления углеводов кратковременно улучшается настроение. Овощи и белковая пища (творог, яйца, мясо) вызывают сонливость.
Приступы учащенного сердцебиения. Повышенный уровень инсулина ускоряет сердцебиение и увеличивает выброс крови сердцем при каждом сокращении. Это поначалу приводит к утолщению стенок левой половины сердца, а потом к изнашиванию мышечной стенки.
Боли в сердце. Отложения холестерина в коронарных сосудах вызывают нарушения питания сердца и болезненные ощущения.
Головная боль связана с сужением сосудов головного мозга. Спазм капилляров появляется при повышении артериального давления или из-за сужения сосудов атеросклеротическими бляшками.
Тошнота и нарушение координации вызваны повышением внутричерепного давления в связи с нарушением оттока крови из мозга.
Жажда и сухость во рту. Это результат угнетения симпатическими нервами слюнных желез при высокой концентрации инсулина в крови. Храп.
Склонность к запорам. Ожирение внутренних органов и высокий уровень инсулина замедляют работу кишечника и ухудшают выделение пищеварительных соков. Поэтому пища надолго задерживается в пищеварительном тракте.
Повышенная потливость, особенно в ночные часы – результат стимуляции инсулином симпатической нервной системы.
Внешние проявления метаболического синдрома.
Абдоминальное ожирение, отложение жира в районе живота и плечевого пояса. Появляется «пивной» живот. Жировая клетчатка скапливается не только под кожей, но и вокруг внутренних органов. Она не только сдавливает их, затрудняя их работу, но и играет роль эндокринного органа. Жир выделяет вещества, способствующие появлению воспаления, повышению уровня фибрина в крови, что повышает риск развития тромбов. Абдоминальное ожирение диагностируют, если окружность талии превышает:
У мужчин более 102 см;
У женщин более 88.
Красные пятна на груди и шее. Это признаки повышения давления связанного со спазмом сосудов, который вызван избытком инсулина.
Артериальная гипертензия. Показатели артериального давления (без применения гипотензивных препаратов).
Систолическое (верхнее) давление крови превышает 130 мм.
Диастолическое (нижнее) давление превышает 85 мм.
Диагностика
Лабораторные симптомы метаболического синдрома.
При биохимическом исследовании крови у людей с метаболическим синдромом обнаруживаются значительные отклонения от нормы.
•Триглицериды – жиры, лишенные холестерина. У больных метаболическим синдромом их количество превышает 1,7 ммоль/л. Уровень триглициридов повышается в крови вследствие того, что при внутреннем ожирении в воротную вену выделяются жиры.
•Липопротеины высокой плотности (ЛПВП) или «хороший» холестерин. Концентрация уменьшается в связи с недостаточным потреблением растительных масел и малоподвижным образом жизни.
Женщины – менее 1,3 ммоль/л.
Мужчины – менее 1,0 ммоль/л.
•Холестерол, липопротеины низкой плотности (ЛПНП) или «плохой» холестерин повышение уровня свыше 3,0 ммоль/л. В воротную вену попадает большое количество жирных кислот из жировой ткани, окружающей внутренние органы. Эти жирные кислоты стимулируют печень синтезировать холестерол.
•Уровень глюкозы в крови натощак повышен более 5,6-6,1 ммоль/л. Клетки тела плохо усваивают глюкозу, поэтому ее концентрации в крови высокие даже после ночного голодания.
•Толерантность к глюкозе. Перорально принимают 75 г глюкозы и через 2 часа определяют уровень глюкозы в крови. У здорового человека глюкоза за это время усваивается, и ее уровень возвращается к норме, не превышает 6,6 ммоль/л. При метаболическом синдроме концентрация глюкозы 7,8-11,1 ммоль/л. Это говорит о том, что глюкоза не усваивается клетками и остается в крови.
•Мочевая кислота повышена более 415 мкмоль/л. Ее уровень повышается вследствие нарушения пуринового обмена. При метаболическом синдроме мочевая кислота образуется при гибели клеток и плохо выводится почками. Она свидетельствует об ожирении и высоком риске развития подагры.
•Микроальбуминурия. Появление молекул белка в моче говорит об изменениях в работе почек, вызванных сахарным диабетом или гипертонической болезнью. Почки недостаточно хорошо фильтруют мочу, в результате в нее попадают молекулы белка.
•Наличие стрий (растяжек) на коже. При резком наборе веса разрывается сетчатый слой кожи, и мелкие кровеносные капилляры. Эпидермис при этом остается неповрежденным. В результате на коже появляются красные полосы шириной 2-5 мм, которые со временем заполняются соединительными волокнами и светлеют.
•Лабораторная диагностика метаболического синдрома.
•Общий холестерин повышен ≤5,0 ммоль/л. Это вызвано нарушением липидного обмена и неспособностью организма должным образом усваивать жиры. Высокая концентрация холестерина связна с перееданием и высоким уровнем инсулина.
•Высокомолекулярные липопротеины (ЛПВП или холестерин высокой плотности) снижен меньше 1 ммоль/л — у мужчин и меньше 1,3 ммоль/л — у женщин. ЛПВП – это «хороший» холестерин. Он хорошо растворим, поэтому не откладывается на стенках сосудов и не вызывает атеросклероза. Высокая концентрация глюкозы и метилглиоксаля (продукта распада моносахаров) приводит к разрушению ЛПВП.
•Низкомолекулярные липопротеиды (ЛПНП или холестерин низкой плотности) концентрация повышена ≤3,0 ммоль/л. «Плохой холестерин» образуется в условиях избытка инсулина. Он слаборастворим, поэтому осаждается на стенках сосудов и формирует атеросклеротические бляшки.
•Триглицериды повышены >1,7 ммоль/л. Эфиры жирных кислот, которые используются организмом для транспортировки жиров. Они попадают в венозную систему из жировой ткани, поэтому при ожирении их концентрация повышается.
•Уровень глюкозы в крови натощак повышен >6,1 ммоль/л. Организм не в состоянии усвоить глюкозу и ее уровень остается высоким даже после ночного голодания.
•Инсулин повышен >6,5 ммоль/л. Высокий уровень этого гормона поджелудочной железы вызван нечувствительностью тканей к инсулину. Повышая выработку гормона, организм пытается воздействовать на инсулиночувствительные рецепторы клеток, и обеспечить усвоение глюкозы.
•Лептин повышен >15-20 нг/мл. Гормон, вырабатываемый жировой тканью, который вызывает инсулинорезистентность. Чем больше жировой ткани, тем выше концентрация этого гормона.
Лечение
Цель лечения: безопасное снижение массы тела, восстановление репродуктивных функций при их нарушении.
Эффективное леченияе метаболического синдрома включает в себя :
А. Формирование и поддержание внутренней мотивации пациентки к снижению массы тела;
Б. Постоянный контакт с пациенткой с постановкой и согласование промежуточных целей лечения и контроля их достижения.
Немедикаментозное лечение:
- Лекции для больных.
- Рациональное гипо- и эукалорийное питание.
- Увеличение физической активности.
- Нормализация образа жизни.
- Оперативное лечение, направленное на уменьшение объёма желудка.
Медикаментозная терапия:
- Селективный ингибитор обратного захвата серотонина и норадреналина (сибутрамин) по 10-15 мг в сутки: вызывает быстрое возникновение и пролонгирование чувства насыщения и, как следствие, уменьшение объёма потребляемой пищи. Начальная доза сибутрамина 10 мг в сутки. При потере массы тела менее 2 кг в течение 4 нед дозу увеличивают до 15 мг в сутки. Препарат противопоказан при артериальной гипертензии.
- Препарат периферического воздействия — орлистат ингибирует ферментативные системы кишечника, снижая количество свободных жирных кислот и моноглицеридов в тонком кишечнике. Наиболее эффективная дозировка — 120 мг 3 раза в день. Наряду со снижением веса на фоне лечения ксеникалом отмечены нормализация или достоверное снижение артериального давления, уровня общего холестерина, ХС- ЛПНП, триглицеридов, что свидетельствует об уменьшении риска развития сердечно-сосудистых заболеваний. Ксеникал обладает хорошей переносимостью и безопасен.
- Антидепрессанты — селективные ингибиторы обратного захвата серотонина показаны больным с тревожно-депрессивными расстройствами, паническими атаками и невротической булимией: флуоксетин — суточная доза от 20 до 60 мг в течение 3 мес или флувоксамин по 50—100 мг в сутки в течение 3 мес.
Патогенетическая медикаментозная терапия менопаузального МС — заместительная гормонотерапия.
Снижение массы тела в конечном итоге способствует снижению риска развития сердечно-сосудистых заболеваний, рака, профилактике сахарного диабета 2 типа, снижению частоты апноэ и остеоартрита. Механизмы достижения конечного результата после снижения массы тела довольно сложные и включают:
- нормализацию обмена липидов;
- снижение АД, концентрации инсулина, провоспалительных цитокинов, риска тромбообразования, оксидативного стресса.
Поскольку у женщин репродуктивного возраста, страдающих МС, нередко наблюдают олигоменорею, как правило, снижение массы тела на 10% и более способствует нормализации менструальных циклов у 70% женщин и восстановлению овуляции — у 37% женщин без гормональных препаратов. ЗГТ при ММС способствует снижению массы тела, уменьшению индекса окружность талии/окружность бёдер, нормализации уровня инсулина и липидного спектра крови.
Сохраняющийся избыток массы тела повышает риск сердечно-сосудистых заболеваний, поражения опорно-двигательного аппарата, а также некоторых акушерских и гинекологических заболеваний (гиперплазия эндометрия, ДМК, слабость сократительной деятельности матки в родах).
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Большинство авторов сходятся во мнении о существовании нескольких механизмов, обусловливающих наличие связи артериальной гипертензии и инсулинорезистентности.
Еще в 80-х годах прошлого века ученые пришли к выводу, что сочетание артериальной гипертензии с метаболическими факторами риска – это не механическое скопление, а закономерное проявление единой цепи целого ряда сложных биохимических нарушений на тканевом уровне. В 1985 г. Было высказано предположение, что гиперинсулинемия может служить связывающим звеном между артериальной гипертензией, ожирением и нарушением толерантности к глюкозе (НТГ). В ряде исследований по прямому определению инсулинорезистентности было показано, что больные с артериальной гипертензией в среднем утилизируют на 40% меньше глюкозы, чем лица с нормальным артериальным давлением.
В эпидемиологических исследованиях продемонстрировано также, что 64% больных с артериальной гипертензией имели инсулинорезистентности и только у половины пациентов она клинически манифестировала с нарушением углеводного обмена. С другой стороны, у 36% больных, имевших гиперлипопротеидемию (ГЛП) или избыточную массу тела (ИМТ), не было выявлено инсулинорезистентности. Таким образом, даже на фоне имеющегося в настоящее время огромного интереса к метаболическому синдрому было бы ошибочным связывать каждый случай эссенциальной артериальной гипертензии с проявлениями тканевой инсулинорезистентности.
Хроническая гиперинсулинемия как проявление тканевой инсулинорезистентности способствует задержке в организме натрия путем ускорения его реабсорбции, что приводит к увеличению объема жидкости и общего периферического сосудистого сопротивления. Повышение активности Na-K-, H- и Ca-Mg-АТФазы под непосредственным воздействием инсулина вызывает увеличение содержания внутриклеточного натрия и кальция, что способствует вазоконстрикции гладкой мускулатуры сосудов. При этом усиливается и чувствительность сосудов к прессорным агентам, таким как адреналин и ангиотензин.
Гиперинсулинемия также способствует активации симпатической нервной системы (СНС), в результате чего возрастает сердечный выброс и стимулируется вазоконстрикция периферических кровеносных сосудов. Симпатическая стимуляция почек запускает мощный механизм развития артериальной гипертензии – ренин-ангиотензин-альдостероновую систему. Исследования показывают, что при сочетании артериальной гипертензии с инсулинорезистентностью активность АПФ является достоверно более высокой по сравнению с больными артериальной гипертензией без проявлений инсулинорезистентности. Ангиотензин 11 – главный действующий компонент ренин-ангиотензин-альдостероновой системы – прямо и косвенно (опосредованно через активацию симпатической нервной системы) повышает давление в клубочковом аппарате, вызывает пролиферацию гладкомышечных стенок артерий, гипертрофию кардиомиоцитов и нарушает функцию эндотелия, что способствует системной артериальной и венозной вазоконстрикции.
Особую роль в ассоциации артериальной гипертензии и инсулинорезистентности играет ожирение абдоминального типа, характерное для метаболиского синдрома. В адипоцитах брыжейки и сальника идет синтез метаболически активных веществ, ингибирующих выработку эндогенного оксида азота, соответственно стимулируя вазоконстрикцию. В последние годы также активно обсуждается роль лептина в усилении активности симпатической нервной системы. Артериальная гипертензия развивается примерно у 60% больных ожирением.
В последнее десятилетие получило развитие учение о роли функции эндотелия в формировании и прогрессировании артериальной гипертензии. Показано, что в патогенезе артериальной гипертензии, связанном с метаболическими нарушениями, эндотелиальная функция является интегральным аспектом синдрома инсулинорезистентности и способствует ее углублению, увеличению реактивности сосудов и дальнейшему формированию артериальной гипертензии.
Источник
