Митохондриальная энцефалопатия код мкб

Митохондриальная энцефалопатия (также именуемая нейрогастроинтестинальная энцефаломиопатия) является частным случаем более широкой группы митохондриальных болезней ─ редких наследственных патологий, связанных с нарушением функционирования важных клеточных органелл (митохондрий).
Патологические состояния, связанные с дисфункцией митохондрий обусловлены генетическими, биохимическими и структурными дефектами в этих клеточных органеллах, чьей основной задачей в организме является обеспечение энергетического обмена.

Митохондрия имеет собственную ДНК
Особенностями митохондриальных болезней является:
- разнообразие клинических проявлений;
- поражение одновременно нескольких органов и систем;
- вариабельная реакция на проводимое лечение;
- прогрессирование.
Подобные заболевания могут проявить себя практически в любое время, но чаще всего это происходит в детском возрасте.
В зависимости от того, какие клетки организма пострадали более всего, о митохондриальном заболевании могут говорить клинические признаки со стороны различных органов и систем: утомляемость и мышечная слабость, нарушения дыхания и ритма сердца, поражения нервной системы (эпилептические приступы, нарушения зрения и слуха), болезни пищеварительного тракта, эндокринопатии (сахарный диабет, гипопаратиреоз).
В данной статье речь пойдет о таком явлении, как митохондриальная энцефалопатия у детей: о том, что это такое, как проявляется, а также о том, что известно о лечении данной патологии.
Специалисты внесли митохондриальную энцефалопатию в Международную классификацию болезней 10-го пересмотра (МКБ-10) под кодом G93-4 ─ «энцефалопатия неуточненная».
Причины болезни
Заболевания, связанные с нарушениями в работе митохондрий развиваются по причине возникновения мутаций в митохондриальной ДНК (мтДНК) или генах внутри клеточных ядер.
Всего на настоящий день науке известно несколько сотен видов возможных мутаций, с каждым годом описываются все новые.
В одной семье, среди детей, унаследовавших похожие гены, могут быть различные клинические проявления или же они могут не болеть вовсе, а быть только носителями поврежденных генов, что проявится только в последующих поколениях.
Клиническая картина
Как правило, первые симптомы появляются до 20 лет. У многих пациентов проявления касаются системы пищеварения, а именно:
- плохой аппетит и быстрая насыщаемость;
- тошнота и рвота;
- боли в животе;
- метеоризм, урчание;
- неустойчивый стул;
- иногда признаки кишечной непроходимости.

Клинически митохондриальная энцефалопатия может проявляться поражением органов ЖКТ
Со стороны нервной системы наблюдаются:
- Полиневропатия с нарушением поверхностной чувствительности по типу «носков» и «перчаток».
- Снижение мышечной силы в дистальных отделах верхних и нижних конечностей, плохая переносимость физических нагрузок и мышечная слабость.
- Развитие нейросенсорной глухоты.
- Дегенерация сетчатки.
- Поражение глазодвигательных нервов (опущение века, «паралич взора»).
- Эпилептические припадки.
- Мозжечковый синдром (нарушения равновесия, дрожание).
- Мигренеподобные головные боли.
- Интеллектуальные нарушения, задержка в развитии.
Клинические проявления, степень их тяжести индивидуальны для каждого больного. Возможно поражение других органов (сердце, почки, печень), поэтому все пациенты нуждаются в подробном обследовании.
Диагностика

В диагностике митохондриальной энцефалопатии используются определенные клинические критерии
Далее о том, какие диагностические мероприятия помогут установить у ребенка диагноз митохондриальной энцефалопатии:
- консультация невролога, определение подробного неврологического статуса;
- КТ головного мозга;
- МРТ головного мозга;
- офтальмологический прием, осмотр глазного дна;
- электронейромиография (ЭНМГ);
- определение лактата в крови, а также отношения лактата и пирувата;
- биопсия мышцы/кожи;
- молекулярно-генетический анализ. ДНК-диагностика проводится лаборатории наследственных болезней обмена веществ МГНЦ РАМН.
Выполнение каждого пункта из приведенного списка обследований, к сожалению, может осуществить далеко не каждая больница в России, но часто этого и не нужно.
Немаловажное значение в диагностике имеет семейный анамнез. Определение заболевания осуществляется врачом-генетиком.
Пренатальная диагностика
Задумываться о преимплантационной диагностике митохондриальных заболеваний стоит семьям, у которых есть предрасположенность (есть причины думать о генетической предрасположенности).
Подтверждение заболевания у ребенка до рождения проводится у тех детей, которым ранее был определен этот диагноз в ходе преимплантационной диагностики. Мутации в генах клеточных ядер можно заметить еще на сроке в 8-12 недель.

Для выявления патогенных мутаций в митохондриальной ДНК проводят пренатальную диагностику
Подходы к лечению
Специфического лечения и профилактики на настоящий момент не разработано. Есть данные о применении с лечебной целью препаратов, повышающих продукцию АТФ путем активации транспорта субстратов митохондрий, а также снижающих лактат-ацидоз.
Кроме того, врачи проводят симптоматическую терапию.
Острые состояния
Больные митохондриальной энцефалопатией особенно чувствительны к таким стрессовым факторам, как инфекционные заболевания, оперативные вмешательства, применение анестетиков, повышенная температура тела, длительное голодание. Их воздействие приводит к острым метаболическим нарушениям, которые в центральной нервной системе, вызывая ишемию головного мозга, провоцирует появление инсультоподобных состояний, проявляющихся гемианопсией, парезами, нарушениями равновесия и т.п.
Очаговая неврологическая симптоматика в большинстве случаев полностью регрессирует в течение месяца.
Основной принцип лечения подобного криза ─ поддержание кислотно-щелочного равновесия в крови, назначение необходимых витаминов. В то же время необходимо избегать употребления лекарственных веществ, которые оказывают токсическое действие на митохондрии.
Препараты, негативно влияющие на митохондрии

Некоторые лекарственные препараты отрицательно влияют на состояние митохондрий
Пациентам, страдающим от митохондриальных заболеваний противопоказаны лекарственные средства следующих групп:
- противоэпилептические средства (вальпроаты);
- статины;
- эритромицин;
- антибиотики аминогликозидного ряда.
Особенности диеты
Питание больных митохондриальными заболеваниями также имеет свои особенности. Прежде всего в диете следует ограничить и даже исключить те продукты питания, которые могут вызвать обострение.
Кроме того, диета таких пациентов должна быть обогащена витаминами группы В, Е, аскорбиновой кислотой, карнитином, фолиевой кислотой, селеном и т.п.
Обострение митохондриальной энцефаломиопатии может быть спровоцировано длительным голоданием, а также употреблением:
- большого количества жиров и белков;
- крахмала;
- сахарозы;
- кофеина;
- алкогольных напитков.

Спиртные напитки могут спровоцировать обострение митохондриальных заболеваний
Прогноз при данном заболевании может быть различным, ведь митохондриальная энцефаломиопатия это не означает инвалидность. Все зависит тяжести основных проявлений болезни.
Грамотная симптоматическая терапия, а также регулярный прием препаратов, улучшающих функцию дыхательной цепи митохондрий (идебенон, кудесан) и антиоксидантов (мексидол) позволяет стабилизировать состояние пациентов с митохондриальными заболеваниями.
Источник
Связанные заболевания и их лечение
Описания заболеваний
Стандарты мед. помощи
Содержание
- Описание
- Причины
- Симптомы
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Названия
Митохондриальные заболевания.
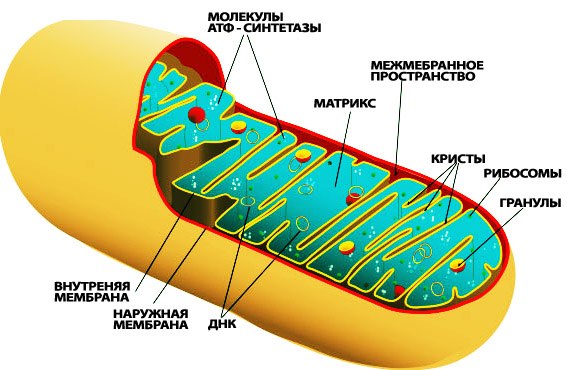
Строение митохондрии
Описание
Митохондриальные заболевания — группа наследственных заболеваний, связанных с дефектами в функционировании митохондрий, приводящими к нарушениям энергетических функций в клетках эукариот, в частности, человека.
Митохондриальные заболевания обусловлены генетическими, структурными, биохимическими дефектами митохондрий, приводящими к нарушениям тканевого дыхания. Они передаются только по женской линии к детям обоих полов, так как сперматозоиды передают зиготе половину ядерного генома, а яйцеклетка поставляет и вторую половину генома, и митохондрии. Патологические нарушения клеточного энергетического обмена могут проявляться в виде дефектов различных звеньев в цикле Кребса, в дыхательной цепи, процессах бета-окисления.
Не все ферменты и другие регуляторы, необходимые для эффективного функционирования митохондрий, кодируются митохондриальной ДНК. Большая часть митохондриальных функций контролируется ядерной.
Можно выделить две группы митохондриальных заболеваний:
Ярко выраженные наследственные синдромы, обусловленные мутациями генов, ответственных за митохондриальные белки (синдром Барта, синдром Кернса-Сейра, синдром Пирсона, синдром MELAS, синдром MERRF и другие).
Вторичные митохондриальные заболевания, включающие нарушение клеточного энергообмена как важное звено формирования патогенеза (болезни соединительной ткани, синдром хронической усталости, гликогеноз, кардиомиопатия, мигрень, печёночная недостаточность, панцитопения, а также гипопаратиреоз, диабет, рахит и другие).
Причины
Повреждение митохондрий в основном возникаетиз-за воздействия реактивных форм кислорода (РФК). В настоящее время считают, что большинство РФК образуется комплексами I и III, вероятно, вследствие высвобождения электронов под воздействием НАД-Н и ФАД-Н в ЦПЭ. Митохондрии используют приблизительно 85% кислорода, потребляемого клеткой, в процессе образования АТФ. В ходе нормального процессаОФ от 0,4% до 4,0% всего употребляемого кислорода преобразуется в митохондриях в супероксидные радикалы (О2-). Супероксид трансформируется до пероксида водорода (Н2О2) с помощью ферментов детоксикации-марганцевой супероксиддисмутазы (Mn-СОД) или цинк/медь- супероксиддисмутазы (Cu/Zn СОД),- а затем до воды с помощью глутатионпероксидазы (ГП) или пероксидредоксина III (ПР III). Однако, если эти ферменты не способны достаточно быстроконвертировать РФК, такие как супероксид-радикал, до воды, происходит оксидативное повреждение и аккумулируется в митохондриях. Глутатион в ПР является одним из основных антиоксидантов в организме. Глутатион представляет собой трипептид, содержащий глутамин, глицин и цистеин. ГП требует селен в качестве кофактора.
Показано, сто супероксид in vitro повреждает железо-серный кластер, находящийся в в активном центре аконитазы, фертента цикла ТКК. Из-за этого железо вступает в реакцию с Н2О2 с образованием гидроксильных радикалов через реакцию Фентона (Fenton). Кроме того, оксид азота (NO) образуется в митохондриях с помощью митохондриальной синтазы оксида азота (МтСОА), а также свободно диффундирует в митохондрии из цитозоля. NO реагирует с O2 с образованием другого радикала- пероксинитрита (ONOO-). Вместе эти два радикала и другие радикалы могут нанести существенное повреждение митохондриям и другим компонентам клетки.
В митохондриях элементами, которые особенно подвержены воздействию свободных радикалов, являются липиды, белки, окислительно-восстановительные ферменты и мтДНК. Прямое повреждение митохондриальных белков снижает их аффинность к субстратам или коферментам и таким образом нарушают их функцию. Проблема осложняется тем, что если повреждение митохондрии произошло, то функция митохондрии может быть скомпрометирована увеличением потребностей клетки для процессов репарации энергии. Митохондриальная дисфункция может привести к цепному процессу, при котором митохондриальное повреждение влечет за собой дополнительное повреждение.
Комплекс I особенно чувствителен к воздействию оксида азота (NO). У животных, которым вводили природные и синтетические антагонисты комплекса I, как правило, наблюдается гибель нейронов. Нарушение функции комплекса I было ассоциировано с наследственной оптической нейропатией Лебера, болезнью Паркинсона и другими нейродегенеративными состояниями.
Гипергликемия индуцирует образование супероксида в митохондриях эндотелиальными клетками, который является важным медиатором диабетических осложнений, таких как сердечно- сосудистые заболевания. Образование супероксида в эндотелии также способствует развитию атеросклероза, гипертензии, сердечной недостаточности, старения, сепсиса, ишемически- реперфузионных повреждений и гиперхолестеринемии.
Медиаторы воспаления, такие как фактор некроза опухолей α (ФНОα) in vitro были связаны с митохондриальной дисфункциейи повышали образование ФРК. В модели застойной сердечной недостаточностидобавление ФНОα к культуре кардиомиоцитов повышало образование РФК и гипертрофию миоцитов. ФНОα вызывает митохондриальную дисфункциюпутем восстановления активности комплекса III в ЦПЭ, увеличивая образование РФК и повреждение мтДНК.
Дефицит питательных веществ или их избыток также может привести к митохондриальной дисфункции. Витамины, минералы и другие метаболиты работают как необходимые кофакторы для синтеза и функционирования митохондриальных ферментов и других составляющих, которые поддерживают функцию митохондрий, и диета с недостатком микрокомпонентов можетускорять старение митохондрий и способствовать нейродегенерации. Например, ферменты участвующие в цепи синтеза гемма, требуют достаточных количеств пиридоксина, железа, меди, цинка и рибофлавина. Недостаток питательных веществ, необходимых для каких- либо компонентов цикла ТКК или ЦПЭ, может привести к увеличению образования свободных радикалов и повреждению мтДНК.
Хорошо известно, что недостаток питательных веществ является широко распространенной причиной патогенеза многих заболеваний и является главным предметом спора в здравоохранении. Недостаток железа главным посредником в развитии общего груза заболеваний, затрагивающих приблизительно 2 миллиарда людей, преимущественно женщин и детей. Это наиболее распространенный тип дефицита питательных веществ. Низкий статус содержания железа снижает активность митохондрийпутем выключения комплекса IV и увеличенияоксидативного стресса. Механизмы, лежащие в основе процесса влияния дефицита питательных веществ (и в некоторых случаях избыток, как при перегрузке железом) на возникновение, развитие и прогрессирование заболеваний, возникающих вследствие нарушения митохондриальных функций, к настоящему времени уже изучены.
Наследование митохондриальных болезней:
Митохондрии наследуются иначе, чем ядерные гены. Ядерные гены в каждой соматической клетке обычно представлены двумя аллелями (за исключением большинства сцепленных с полом генов у гетерогаметного пола). Один аллель унаследован от отца, другой от матери. Однако митохондрии содержат собственную ДНК, причем в каждой митохондрии человека обычно содержится от 5 до 10 копий кольцевой молекулы ДНК ( Гетероплазмия), и все митохондрии наследуются от матери. Когда митохондрия делится, копии ДНК случайным образом распределяются между ее потомками. Если только одна из исходных молекул ДНК содержит мутацию, в результате случайного распределения такие мутантные молекулы могут накопиться в некоторых митохондриях. Митохондриальная болезнь начинает проявляться в тот момент, когда заметное число митохондрий во многих клетках данной ткани приобретают мутантные копии ДНК (пороговая экспрессия).
Мутации в митохондриальной ДНК происходят, по разным причинам, намного чаще, чем в ядерной. Это означает, что митохондриальные болезни достаточно часто проявляются из-за спонтанных вновь возникающих мутаций. Иногда темп мутирования увеличивается из-за мутаций в ядерных генах, кодирующих ферменты, которые контролируют репликацию ДНК митохондрий.
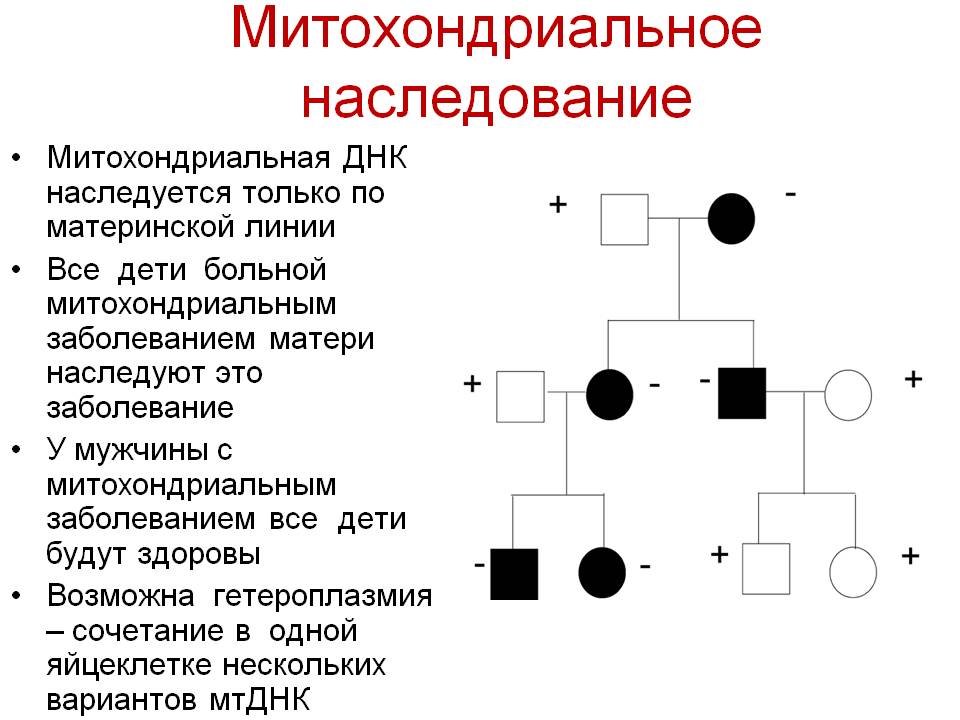
Генетические аспекты митохондриальных болезней
Симптомы
Эффекты митохондриальных заболеваний очень разнообразны. Из-за различного распределения дефектных митохондрий в разных органах мутация у одного человека может привести к заболеванию печени, а у другого — к заболеванию мозга. Величина проявления дефекта может быть большой или малой, и она может существенно изменяться, медленно нарастая во времени. Некоторые небольшие дефекты приводят лишь к неспособности пациента выдерживать физическую нагрузку, соответствующую его возрасту, и не сопровождаются серьёзными болезненными проявлениями. Другие дефекты могут быть более опасны, приводя к серьёзной патологии.
В общем случае митохондриальные заболевания проявляются сильнее при локализации дефектных митохондрий в мышцах, мозге, нервной ткани, поскольку эти органы требуют больше всего энергии для выполнения соответствующих функций.
Несмотря на то, что протекание митохондриальных заболеваний сильно отличаются у разных пациентов, на основании общих симптомов и конкретных мутаций, вызывающих болезнь, выделено несколько основных классов этих заболеваний.
Помимо относительно распространённой митохондриальной миопатии, встречаются:
1. Митохондриальный сахарный диабет, сопровождающийся глухотой (DAD, MIDD, синдром MELAS) — это сочетание, проявляющееся в раннем возрасте, может быть вызвано мутацией митохондриального гена MT-TL1, но сахарный диабет и глухота могут быть вызваны как митохондриальными заболеваниями, так и иными причинами;
2. Наследственная оптическая нейропатия Лебера, характеризующийся потерей зрения в раннем пубертатном периоде;
3. Синдром Вольфа-Паркинсона-Уайта;
4. Рассеянный склероз и подобные ему заболевания;
5. Синдром Лея (Leigh) или подострая некротизирующая энцефаломиопатия : после начального нормального постнатального развития болезнь проявляется обычно в конце первого года жизни, иногда — во взрослом возрасте. Болезнь сопровождается быстрой потерей функций организма и характеризуется судорогами, нарушенным состоянием сознания, деменцией, остановкой дыхания;
6. Нейропатия, атаксия, retinitis pigmentos и птоз: прогрессирующие симптомы нейропатии, атаксии, туннельное зрение и потеря зрения, птоз, деменция;
7. Митохондриальная нейрогастроинтенстинальная энцефалопатия: гастроинтестинальная псевдообструкция и кахексией, нейропатия, энцефалопатия с изменениями белого вещества головного мозга.
Лечение
В настоящее время лечение митохондриальных заболеваний находится в стадии разработки, но распространённым терапевтическим методом служит симптоматическая профилактика с помощью витаминов. В частности, в лечении синдрома MELAS у ряда пациентов оказались эффективными кофермент Q, который применяется как цитопротектор и антиоксидант при кардиомиопатиях и хронической сердечной недостаточности, рибофлавин и никотинамид. Также в качестве одного из методов применяются пируваты.
В настоящее время проводятся экспериментальные работы по изучению возможности экстракорпорального (in vitro) оплодотворения с использованием химерной яйцеклетки, ядро которой получено из яйцеклетки пациентки с митохондриальным заболеванием, а цитоплазму из другой яйцеклетки от женщины с нормально функционирующими митохондриями (замена ядра).
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
