Миеломная по мкб код
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Причины
- Симптомы
- Диагностика
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Названия
Миеломная болезнь.
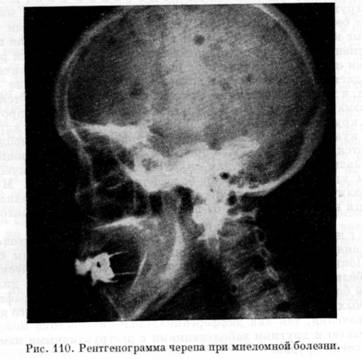
Рентгенограмма черепа при миеломе
Описание
Миеломная болезнь — это злокачественное новообразование системы крови, относящееся к группе парапротеинемических гемобластозов, возникающее в результате бесконтрольной пролиферации в костном мозге плазматических клеток, имеющих способность продуцировать большое количество моноклонального иммуноглобулина (IgG, IgA, IgD, IgE) или легких цепей каппа или лямбда.
Эпидемиология. Заболеваемость миеломной болезнью составляет примерно 40 случаев на миллион населения. Средний возраст пациентов на момент установления диагноза — 60-65 лет, около 2% больных старше 40 лет. Мужчины болеют чаще женщин.
Причины
Этиология миеломной болезни не известна. К потенциальным факторам риска относят контакт с радиоактивными веществами, пестицидами, бензолом, некоторыми органическими растворами.
Как правило, миелома проявляется множественными литическими опухолями в костях, остеопорозом и диффузным плазмоцитозом в костном мозге. Значительное количество патологического моноклонального иммуноглобулина (миеломные белки), который продуцируется плазматически клетками, циркулирует в плазме, вследствие чего может увеличиваться ее объем и общая вязкость крови. Миеломные белки взаимодействуют с факторами свертывания крови и, обволакивая тромбоциты, влияют на их функцию и усиливают кровоточивость.
Кроме миеломных белков, плазматические клетки имеют способность также производить различные цитотоксические факторы, например фактор, который активирует функцию остеокластов. Остеокласты обусловливают резорбцию костной ткани, в результате чего появляются боли в костях, патологические переломы и возникает гиперкальциемия. Следствием инфильтрации костного мозга плазматическими клетками являются анемия различной степени тяжести, лейкопения и / или тромбоцитопения. Уменьшение количества лейкоцитов и нарушения синтеза нормальных иммуноглобулинов может вызвать депрессию гуморального и в меньшей степени, клеточного иммунитета, что делает таких больных очень чувствительными ко многим инфекциям (преимущественно бактериальных).
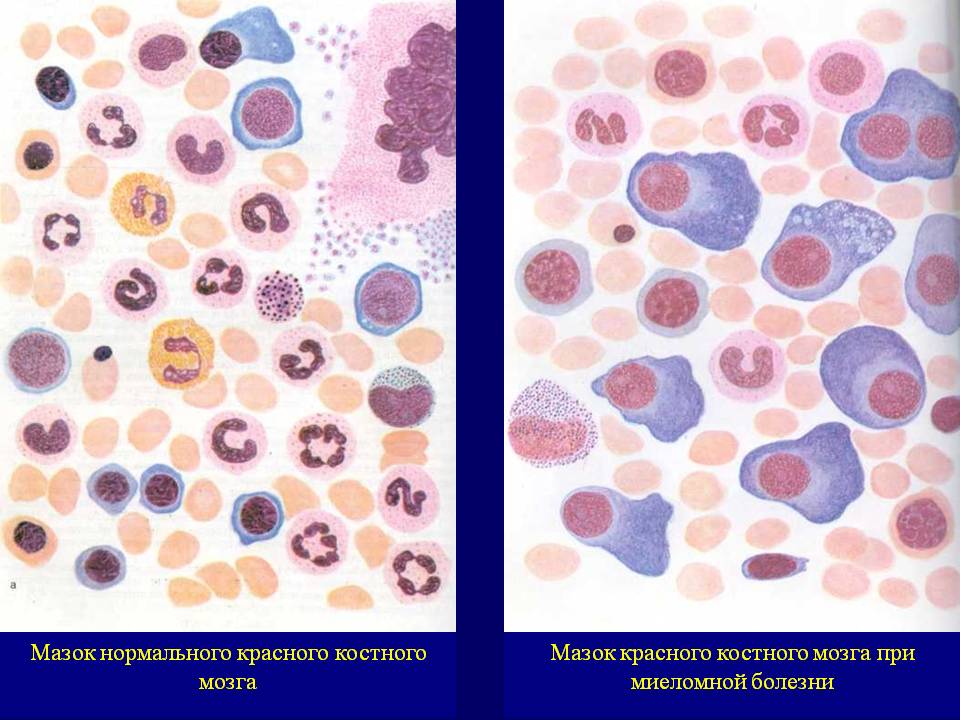
Клетки костного мозга при миеломной болезни
Симптомы
Клинические признаки заболевания достаточно разнообразны. Больные, как правило, жалуются на постоянные боли в костях, спине и пояснице, что сочетается с уменьшением роста и остеопорозом (особенно у мужчин и у женщин до периода менопаузы). Возможна компрессия спинного мозга и спинномозговых нервов с возникновением соответствующей неврологической симптоматики (парапарез и нарушение функции тазовых органов). Обычным явлением для пациентов являются патологические переломы.
Больные миеломной болезнью страдают от частых инфекционных осложнений (вызванных преимущественно Streptococcus pneumonie, Staphylococcus aureus, граммотрицательными микроорганизмами), чувствуют слабость, одышку, головокружение, связанные с анемией и опухолевой интоксикации, возможно наличие симптомов, характерных для почечной недостаточности. Следствием коагулопатии и тромбоцитопении могут быть проявления повышенной кровоточивости. У части пациентов наблюдается бессимптомное течение миеломы, и заболевания выявляется при исследовании анализа крови, которое проводится по другому поводу.
Боль в шейном отделе позвоночника. Вялость. Гиперкальциемия. Рвота. Слабость мышц (парез). Тошнота. Увеличение СОЭ.
Диагностика
В общем анализе крови может отмечаться эритроцитопения, лейкопения и тромбоцитопения. Особое диагностическое значение имеет увеличение СОЭ. При исследовании сыворотки крови нередко привлекает внимание выраженная протеинемия, которая возникает за счет увеличенной продукции плазматическими клетками моноклональних иммуноглобулинов определенного класса. В моче больных миеломной болезнью можно обнаружить протеинурию, часто положительную реакцию на белок Бенс-Джонса (отметим, что эта реакция не является патогномоничной для миеломы и может наблюдаться при других патологических состояний).
Рентгенологическое исследование костей скелета (грудной клетки, таза, черепа, плечевой и бедренной кости, позвоночника) позволяет обнаружить в них очаги резорбции костной ткани и остеопороза. Про это следует помнить, что специфических рентгенологических признаков, характерных для миеломной болезни, не существует. Отсутствие остеодеструкций не исключает заболевания, а их наличие считается недостаточной для подтверждения диагноза.
Для верификации диагноза миеломной болезни необходимо проведение стернальной пункции с последующим подсчетом миелограммы, позволяющий установить плазмоклеточных инфильтрацию костного мозга. Однако при множественно-очаговых формах заболевания, когда не наблюдается диффузного поражения костного мозга, миелограма может быть нормальной. При наличии других признаков миеломной болезни (остеодеструкиия, моноклональная имуноглобулинопатия) для подтверждения диагноза следует назначать повторные проколы грудины в разных местах, трепанобиопсию подвздошной кости, проводить пункции в местах костных опухолей, при спорных вопросах возможно проведение резекции пораженной кости (ребра, лопатки).
Диагноз миеломной болезни считается достоверным при совокупности следующих признаков:
1. Количество плазматических клеток в костном мозге> / = 10% и / или установлено присутствие солитарной плазмоцитомы, которая подтверждена с помощью биопсии.
2. Выявление моноклонального белка в плазме крови и / или моче (если моноклональный протеин не обнаружен, то количество плазматических клеток в костном мозге должна превышать 30%).
3. Уровень кальция в крови — на верхней границе нормы или выше, почечная недостаточность (креатинин> 20 мкмоль / л), анемия (гемоглобин менее 100 г / л), очаги деструкции в костях или остеопороз (если присутствует только остеопороз, то для подтверждения диагноза необходимо иметь более 30% плазматических клеток в костном мозге).

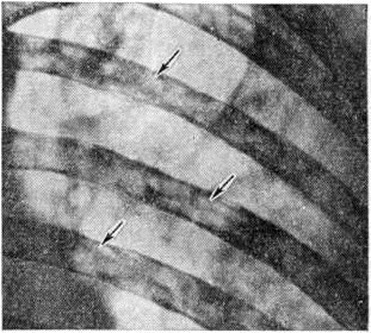
Повреждения ребер при миеломной болезни
Лечение
Лечение пациентов с миеломной болезнью заключается в проведении химиотерапии, направленной на борьбу с опухолевым клоном, и в коррекции осложнений, связанных с течением болезни (синдром анемии, синдром резорбции костной ткани, почечная недостаточность и ).
Следует отметить, что состояние пациентов, у которых отсутствуют клинические симптомы заболевания, нормальный уровень гемоглобина и кальция в плазме, нет нарушений в функции почек и синдрома резорбции костей, может оставаться стабильным в течение длительного времени («тлеющая», или «ленивая» миелома) и не требовать специфического лечения. Таким больным, однако, необходимо проходить тщательный врачебный осмотр и исследование парапротеина в плазме и моче каждык 3 месяца.
Больным, у которых заболевание имеет выраженные клинические признаки или наблюдается прогрессирование заболевания, следует проводить курсы химиотерапии.
Чаще всего на первом этапе лечения пациентам назначается комбинация мелфалана с преднизолоном. Как правило, такая схема приемлема для пациентов пожилого возраста, которым не планируется проведение высокодозной терапии с аутотрансплантацией костного мозга. Мелфалан применяют в дозе 6-8 мг/м2 в сутки вместе с преднизолоном в дозе 40-60 мг / сут в течение 4-7 дней с 4-6-недельными интервалами. Лечение продолжается до достижения максимального ответа на лечение (всего 9-12 месяцев). Такая лечебная схема позволяет достичь уменьшения уровня парапротеина на 50% у 50% больных в течение нескольких месяцев. Продолжительность положительного эффекта от лечения равна 18-24 месяца, средняя продолжительность жизни пациентов, лечащихся по этой схемеувеличивается на 2-4 года. Продолжение химиотерапии после достижения стабильной фазы заболевания (фаза плато) не влияет на продолжительность ремиссии. Полные ремиссии достигаются редко. Следует учитывать, что мелфалан нужно применять с осторожностью у больных с почечной недостаточностью.
Достаточно широко используемых является протокол VAD. При лечении по этому протоколу используют винкристин и адриамицин в течение 4 дней непрерывной инфузией в сочетании с пероральным приемом дексаметазона в большой дозе. Taкоe лечение позволяет достичь значительного процента полных ремиссий (60-70% за короткий промежуток времени). Протокол VAD имеет незначением влияние на стволовые клетки и является идеальным режимом, применяется перед аутотрансплантацией. В то же время проведение такого лечения имеет значительные недостатки, связанные с необходимостью использования для инфузии химиопрепаратов центрального венозного катетера, что может обусловить возникновение катетер-ассоциированной инфекции и коагуляционных осложнений.
Пульсовая терапия дексаметазоном в дозе 40 мг в день в течение 4 дней с 4-дневным перерывом в лечении также считается достаточно эффективным методом лечения впервые выявленной миеломной болезни. Лечебный ответ составляет 40-50% и более, позитивный ответ наблюдается после нескольких циклов. Однако пульсовая терапия дексаметазоном имеет много побочных эффектов, аналогических тем, которые возникают при применении высоких доз глюкокортикостероидних гормонов (нарушение настроения, бессонница, раздражительность, нарушения внимания, задержка жидкости в организме, увеличение веса, стероидный диабет, гастроинтестинальные расстройства, инфекционные осложнения, слабость проксимальных мышц, снижение зрения, включая развитие катаракты).
В некоторых случаях пациентам назначается комбинированная полихимиотерапия (протоколы М2, АВСМ и ). Как правило, использования комбинации из нескольких химиопрепаратов не имеет значительных преимуществ перед указанными выше схемами, но повышает токсическое воздействие на организм пациентов.
Пациенты, которые не ответили положительно на терапию первой линии, рассматриваются как потенциальные кандидаты на проведение аутотрансплантации периферических стволовых клеток.
Высокодозной химиотерапии с последующей аутотрансплантацией считается одним из достаточно эффективных современных методов лечения миеломной болезни (полная ремиссия достигнута у 24-75% больных, частичная ремиссия — у 76-90%), однако этот метод окончательно не излечивает данную патологию (в более 90% больных в будущем подвергается рецидивам болезни). Средняя продолжительность жизни у больных после проведенной высокодозной терапии составляет 4-5 лет, безрецедивный период длится примерно 18-24 месяца. Смертность, связанная с процедурой трансплантации, низкая (около 1%). Аутотрансплантация не показана пациентам пожилого возраста (старше 70 лет) и тем, кто имеет серьезную сопутствующую патологию.
В наше время не существует четких рекомендаций о назначении терапии больным, которые достигли ремиссии. В рамках исследовательских протоколов с этой целью чаще всего применяют преднизолон, альфа-интерферон, ведется изучение эффективности использования талидомида.
Для эффективного лечения костных поражений при миеломной болезни чрезвычайно важным является назначение с самого начала адекватной химиотерапии и, при необходимости, облучения костей. Облучение костей назначается при компрессии спинного мозга, длительном сильном болевом синдроме, для лечения и предупрждения патологических переломов.
С целью ускорения процесса репарации костной ткани рекомендуется назначение бисфосфонатов — памидроната (Аредиа), золедроновой кислоты (Зомета), клодроната (Бонефос). Аредиа применяется внутривенно один раз в 3-4 недели в дозе 120 мг и считается самым безопасным препаратом для больных с нарушением функции почек. Одним из лучших препаратов среди представителей этой группы для коррекции гиперкальциемии является Зомета. Препарат применяется в дозе 4 мг в виде 15-минутной инфузии раз в 3 — 4 недели. Бонефос применяют в виде внутривенной 2-часовой инфузии в дозе 300 мг в день в течение 7 дней, как альтернативный метод лечения может использоваться пероральный прием препарата — 1600 мг в сутки.
Новым методом лечения деструкций позвоночника является применение кофопластики с введением жидкого цемента, что позволяет укрепить позвоночный столб и уменьшить болевой синдром. Больным, у которых не выявлено патологических переломов, рекомендуются умеренные физические нагрузки, особенно плавание и ходьба.
Для коррекции синдрома анемии, сопровождающего миеломной болезнью, применяют препараты железа, витамина В12 (в случаях сопутствующего дефицита этих элементов), проводят переливание эритроцитарной массы. Также для лечения анемии патогенетически обоснованным является назначение эритропоэтина (Эпрекс, Рекормон и ). На первом этапе при лечении эритропоэтинами применяется «нагрузка дозой», когда препарат вводят в дозе 40 000 единиц в неделю. Если после 4 недель приема препарата в указанной дозе не произошло повышения гемоглобина, доза эритропоэтина повышается до 60 000 единиц. Терапия продолжается до тех пор, пока уровень гемоглобина не возрастет до 120 г/л, и прекращается при гемоглобине 140 г/л. Поддерживающая терапия эритропоэтином проводится трижды в неделю в дозе 10 000 единиц с повышением дозы в случае необходимости до 20 000 единиц.
Важной составляющей лечения пациентов с миеломной нефропатией является достаточная гидратация, переливания щелочных растворов и плазмафарез. У пациентов с почечной недостаточностью следует ограничить использование нефротоксических препаратов (внутривенные контрасты, аминогликозиды, ванкомидин, амфотерицин В, ацикловир, циклофосфамид, диуретики, бисфосфонаты — за исключением аредиа).
При проведении химиотерапии у больных с почечной недостатнистью преимущество в лечении следует предоставлять протоколам и дексаметазону в качестве монотерапии, поскольку они обеспечивают быстрый лечебный эффект без дополнительного токсического влияния на почки, как это можно наблюдать в случае с мелфаланом.
Причиной инфекционных осложнений у больных с впервые установленной миеломой, как правило, Streptococcus pneumoniae, Hemophilus inflrnse, Herpes zoster Установлено, что инфекционные осложнения чаще встречаются в первые 3 месяца от начала лечения и во время рецидива заболевания. В этот период больным миеломой возможно назначение антибиотиков и сульфаниламидов (например, бисептол) с целью профилактики инфекционных осложнений. Лечения бактериальной инфекции проводится по общим принципам рациональной антибиотикотерапии с учетом нефротоксичности отдельных препаратов.
Современная терапия способствует продлению жизни больных миеломой. Средняя продолжительность жизни при адекватном лечении составляет 50 месяцев.
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Связанные заболевания и их лечение
Описания заболеваний
Национальные рекомендации по лечению
Стандарты мед. помощи
Содержание
- Описание
- Симптомы
- Причины
- Лечение
- Основные медицинские услуги
- Клиники для лечения
Названия
Множественная миелома.
Описание
Множественная миелома — злокачественная опухоль системы В-лимфоцитов, возникающая на уровне пре-В-клеточных стадий моноклонального развития и сохраняющих способность к дифференцировке до конечной стадии — плазмоцита. Определение множественной миеломы как плазмоклеточной опухоли с парапротеинемией не совсем точно, так как выделен вариант заболевания, при котором патологические клетки синтезируют иммуноглобулины, но не секретируют их в кровь (так называемая несекретирующая миелома).
Имеются сведения о значительных колебаниях стандартизованных показателей заболеваемости множественной миеломой в различных странах. В нашей стране по данным выборочных исследований множественной миеломы встречается в 5,3% случаев всех заболеваний гемобластозами. Среднегодовые стандартизованные показатели заболеваемости на различных территориях колебались от 0,3 до 1,1.
Множественная миелома наблюдается одинаково часто у мужчин и женщин. Чаще заболевают люди в возрасте старше 50 лет.
Симптомы
Развернутой клинической картине заболевания обычно предшествует бессимптомный период различной длительности.
В клинической картине имеет место:
1. Поражение скелета. Рентгенологически обнаруживаются миеломатозные опухоли различных размеров в ребрах, грудине, позвоночнике, ключице, черепе, конечностях, проявляющиеся болями, вначале носящими летучий характер, затем они становятся более интенсивными и продолжительными. Нередко возникают патологические переломы с деформацией грудной клетки, компрессией тел поясничных и грудных позвонков.
2. Поражения нервной системы. Они связаны в большинстве случаев с опухолевым поражением костей свода черепа и позвоночника, в результате чего могут развиться параплегии, синдром сдавления корешков спинномозговых нервов, гемиплегии или гемипарез. В ряде случаев наблюдаются диэнцефально-гипофизарные и психические расстройства, гиперкальциемическая энцефалопатия.
3. Почечная патология. Миеломная нефропатия, возникающая у 60—90% больных, характеризуется протеинурией, почечной недостаточностью, ангиоретинопатией, отеками и гематурией. Вследствие деструкции костей наблюдается гиперкальциемия и гиперкальциурикемия. У 1/3 больных азотемия является причиной смерти.
4. Гипервязкостный синдром. Обусловлен высоким содержанием в сыворотке протеинов, встречается при миеломе IgG и IgA. С повышенной вязкостью крови связаны изменения глазного дна и возможное развитие тяжелых нарушений центральной нервной системы.
5. Геморрагический синдром. Нарушения тромбоцитарных, плазменных и сосудистых факторов гемостаза. Парапротеины оседают на мембранах тромбоцитов. Они образовывают комплексы с V, VII, VIII факторами свертывания, протромбином, фибриногеном.
6. Нарушения гемопоэза. Чаще развивается нормохромная анемия. При кровотечениях она носит железодефицитный характер, в случаях дефицита витамина B12 и фолиевой кислоты в костном мозге выявляются черты мегалобластического кроветворения. У 86—90% больных при исследованиях костномозгового кроветворения обнаруживается миеломоноклеточная инфильтрация.
7. Депрессия иммунитета. Снижение содержания в сыворотке крови уровня нормальных иммуноглобулинов (часто менее 20%), нарушение антителообразоваиия, уменьшение количества гранулоцитов и их функциональная дефектность обусловливают предрасположенность больных к инфекциям.
Причины
Происхождение парапротеинемических гемобластозов из одной клетки подтверждается однородностью парапротеинов по классу, типу L-цепей, алло- и идиотипу, соответствием количества секретируемых иммуноглобулинов массе опухоли.
Результаты иммуноморфологических исследований убеждают в том, что опухолевый процесс при множественной миеломе и макроглобулинемии Вальденстрема возникает на уровне В-клеток-предшественниц и не зависит от антигенного стимула.
На терминальном этапе течения этих заболеваний наряду с общими проявлениями, характерными для гемобластозов, обнаруживают изменения продукции моноклональных Ig.
Лечение
У больных множественной миеломой соматически и гематологически компенсированных (стадии IA и НА) воздерживаются от цитостатической терапии под контролем ежемесячного исследования гемограммы и уровня патологического иммуноглобулина (Pig). У части пациентов в течение нескольких лет может выявляться вялотекущая форма болезни. При появлении признаков прогрессирования процесса (нарастание опухолевой массы, наличие болевого синдрома, анемии, нарастание количества Pig) прибегают к цитостатической терапии. Широкое применение получили алкилирующие препараты: сарколизин, мельфалан (левовращающий изомер сарколизина), циклофосфан (эндоксан), производные нитрозомочевины.
Основные медуслуги по стандартам лечения | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
