Механизм гиперлипидемии при нефротическом синдроме
Ярким признаком HC является гиперлипидемия. Для нефротической гиперлипидемии характерно в первую очередь увеличение общего и эстерифицированного холестерина (липопротеиды низкой плотности, апоВ). При выраженном HC повышается и уровень триглицеридов (липопротеиды очень низкой плотности). Содержание липопротеидов высокой плотности (ЛВП) чаще нормально или снижено.
Концентрация неэстерифицированных жирных кислот обычно не изменена. Однако в целом их метаболизм, по всей видимости, нарушен, так как в результате гипоальбуминемии значительная часть жирных кислот транспортируется несвязанными, что в свою очередь отражается на обмене липопротеинов.
Тяжесть нефротической гиперлипидемии нередко определяется нозологической формой ГН (например, менее выражена при НС, обусловленном люпус-нефритом), течением HC (особенно высока при персистирующем течении), приемом глюкокортикостероидов.
Механизм развития нефротической гиперлипидемии полностью не выяснен. Наиболее распространенной в настоящее время является теория о ведущей роли гипоальбуминемии, стимулирующей при HC увеличение синтеза как белка, так и липопротеинов. В дальнейшем белок теряется с мочой, а гиперлипопротеинемия сохраняется. Эта теория подтверждается обнаруживаемой многими авторами связью выраженности нефротической гиперлипидемии с гипоальбуминемией. В реализации этого механизма имеет значение изменение двух факторов на пути синтеза в печени холестерина — увеличения активности ГМГ-КоА-редуктазы и снижения катаболизма мевалоната.
Наряду с мнением о гиперпродукции липопротеинов существует теория, отводящая основную роль нарушению их катаболизма, что связывают в первую очередь со снижением активности липопротеин-липазы вследствие потери с мочой ее активаторов. Это подтверждается снижением содержания липидов в крови, сопровождающим уменьшение протеинурии при неизменном уровне альбумина крови у больных с НС, леченных иАПФ.
Клиническое значение нефротической гиперлипидемии определяется ее атерогенным эффектом и вкладом в прогрессирование повреждения почек. Возможность ускоренного развития атеросклероза на фоне нефротической гиперлипидемии до настоящего времени подвергается сомнению ввиду отсутствия убедительных проспективных исследований. Вместе с тем существуют клинические подтверждения атеросклеротического повреждения аорты даже у 5-месячных детей. Представляют интерес результаты J.D. Ordonez и соавт., сопоставивших частоту тяжелых проявлений ишемической болезни сердца в группе из 142 больных с HG, каждый из которых имел пару среди 142 лиц контрольной группы. Авторами установлено, что при HC частота инфарктов миокарда (11 случаев) и смертей от осложнений ишемической болезни сердца (7 случаев) была значительно выше, чем в контрольной группе (соответственно 4 и 3 случая).
Морфологические маркеры липидогенных воздействий на почки представлены крупными внутриклеточными липидными включениями в ряде случаев с формированием пенистых клеток. По данным Н.И. Неверова, помимо гиперлипидемии, появление гломерулярных липидогенных маркеров определяется морфологической картиной нефропатии. Так, они почти всегда обнаруживаются в случаях нефротической гиперлипидемии, обусловленной так называемыми невоспалительными нефропатиями (минимальные изменения клубочков, мембранозная нефропатия, ФСГС). Внутриклеточное и внеклеточное накопление липидов в структурах клубочка стимулирует пролиферативные и склеротические процессы. Вероятность такого механизма подтверждена корреляциями между выраженностью липидогенных морфологических изменений и интенсивностью склеротических (избыточное накопление коллагена IV типа, появление коллагенов I и III типов) и пресклеротических (утолщение ГБМ, накопление мезангиального матрикса) процессов в клубочке.
Характерным признаком HC является нарушение метаболизма витамина D и связанного с ним фосфорно-кальциевого обмена. Эти нарушения выражаются в гипокальциемии (главным образом за счет белковосвязанного кальция, но также и его ионизированной фракции), гипокальциурии с клиническими признаками тетании (чаще у детей), остеопороза и остеомаляции. В основе этих нарушений лежит дефицит одного или нескольких метаболитов витамина D. Один из метаболитов (25-гидроксивитамин D) циркулирует в крови вместе с а-глобулином, витамин-D-связывающим белком и при нарушенной проницаемости ГБМ выходит в клубочковый фильтрат. Дигидроксилированные метаболиты [в основном 1,25а(ОH)2D3] образуются в проксимальных канальцах, и при массивной протеинурии, ведущей к поражению канальцев, их синтез снижается. Дефицит метаболитов витамина D ведет к развитию резистентности скелета к кальциймобилизующему действию паратгормона и нарушению всасывания кальция в кишечнике и тем самым к снижению ионизированного кальция. Большое значение имеет снижение связанного с белком кальция, обусловленное гипоальбуминемией. Снижение содержания ионизированного кальция стимулирует активность паращитовидных желез с развитием вторичного гиперпаратиреоза.
У части больных с HC выявляется диабетоподобный ответ на нагрузку глюкозой, а также повышение экскреции инсулина, а в крови — количества гормона роста. Эти расстройства чаще наблюдались у больных мембранозной нефропатией и фокально-гломерулярным склерозом. Нередко обнаруживается гипогликемия натощак одновременно с базальной гиперинсулинемией; гликемические кривые у этих больных уплощенные, резко замедленные.
В наших наблюдениях уровень иммунореактивного инсулина (ИРИ) был максимально высоким (24,0 мкед U/мл) в сыворотке крови больных с нефротическим синдромом по сравнению с показателем ИРИ у доноров (17,0 мкед U/мл), у больных с изолированным мочевым синдромом (19,0 мкед U/мл) и у больных с ХПН (22,0). Это позволило предположить, что при НС, характеризующемся усиленным липолизом, гиперлипидемией и катаболизмом, имеет место реактивный усиленный синтез инсулина как важнейшего гормона антилиполиза, липогенеза и анаболизма — своего рода адаптивная реакция поджелудочной железы. Тот факт, что базальная гиперинсулинемия при HC была достоверно выше (30) у больных с благоприятным прогнозом по сравнению с больными, имевшими плохой прогноз (21,0 мкед U/мл), позволяет рассматривать ее как компенсаторный позитивный признак.
При HC изменяются состав и количественное соотношение основных микроэлементов как в плазме крови, так и в клеточных элементах. В частности, могут выявляться резко выраженная гипоцинкемия, пониженное содержание железа и кобальта, на фоне чего развиваются анемия, тяжелые дистрофические изменения кожи и ее дериватов, отставание в росте детей с длительно существующим НС.
У больных с массивной протеинурией иногда могут быть различные расстройства функции проксимальных канальцев — аминоацидурия, глюкозурия, фосфатурия, почечный канальцевый ацидоз; в редких случаях эти расстройства сочетаются, давая клиническую картину синдрома Фанкони.
Источник
Этим термином обозначается симптомокомплекс, характеризующийся массивной протеинурией(более 3 г белка/сутки), гипо- и диспротеинемией, гиперлипидемией, гиперхолестеринемией, распространенными отеками и водянкой серозных полостей.
По этиологииразличают первичный и вторичный нефротический синдром. Причиной развития первичного нефротического синдромаявляются первично возникающие заболевания почек, такие, как гломерулопатия с минимальными изменениями в виде слияния малых ножек подоцитов (липоидный нефроз), мембранозный гломерулонефрит, фокально-сегментарный гломерулосклероз, мембранозно-пролиферативный гломерулонефрит.
Вторичный нефротический синдромвозникает при многих заболеваниях, в основном системного характера, при которых почки поражаются вторично. К числу таких заболеваний относятся сахарный диабет (диабетическая нефропатия), амилоидоз, злокачественные опухоли, коллагенозы (системная красная волчанка, склеродермия, ревматизм, узелковый периартериит), хронические инфекционные процессы в организме, паразитарные заболевания
(токсоплазмоз, шистоматоз и др.), аллергические заболевания (сывороточная болезнь и др.). Кроме этого вторичный нефротический синдром возникает при интоксикациях (золото, ртуть, висмут, пенициламин, нестероидные противовоспалительные средства, яды насекомых и змей), нефропатии беременных, тромбозе почечных сосудов и др.
Этиология нефротического синдрома в значительной степени зависит от возраста. Наиболее частой причиной развития этого синдрома у детей является нефропатия с минимальными изменениями; у взрослых среди причин развития нефротического синдрома на первом месте стоит мембранозный гломерулонефрит; у людей старше 60 лет, наряду с мембранозным гломерулонефритом, развитие нефротического синдрома во многих случаях связано с диабетической нефропатией и другими системными заболеваниями, вторично нарушающими функцию почек.
Патогенез.Во всех случаях нефротического синдрома имеет место повышенная проницаемость базальной мембраны капилляров клубочков для белка. Протеинурияможет иметь как селективный, так и неселективный характер. При нефротическом синдроме с минимальными изменениями повышение клубочковой проницаемости связано с уменьшением постоянного электрического заряда стенки капиллярных петель, что обусловлено исчезновением из нее сиалопротеида, в норме тонким слоем покрывающего эндотелий и отростки подоцитов, лежащих на базальной мембране. При мембранозном гломерулонефрите главную роль играет потеря функции барьера, зависящего от размера пор в базальной мембране, которые в норме ограничивают прохождение плазменных белков с молекулярной массой более 150 кД.
Повышение проницаемости фильтрующих мембран клубочков связывают с повреждающим действием откладывающихся на них иммунных комплексов, а также лизосомальных ферментов и активных форм кислорода, выделяемых нейтрофилами и моноцитами. Кроме того, в плазме крови больных с нефротическим синдромом обнаружен фактор, предположительно образуемый лимфоцитами, который повышает проницаемость клубочкового барьера. При любом механизме повреждения происходит повышенное поступление белков плазмы крови, преимущественно альбуминов, в клубочковый фильтрат, и развивается резко выраженная протеинурия (более 3 г белка/сутки, в отдельных случаях — до 50 г белка/сутки). Следствием этого является гипопротеинемия(менее 60 г белка/л),
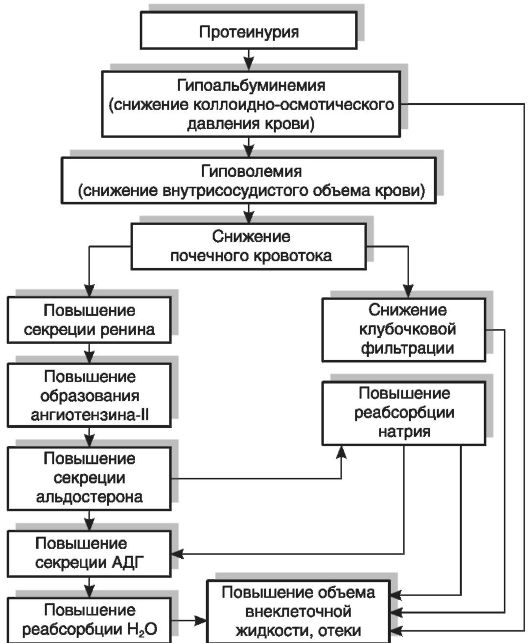
главным образом за счет снижения содержания альбуминов. Вызываемое гипопротеинемией падение коллоидно-осмотического давления сопровождается усиленным выходом жидкости из сосудов в межклеточное пространство и серозные полости тела и развитием гиповолемии, что, в свою очередь, вызывает повышение активности РААС и усиление продукции альдостерона; последний снижает экскрецию натрия с мочой и увеличивает его концентрацию в крови. При проведении ряда клинических и экспериментальных исследований было установлено, что, кроме описанного механизма, развитию гипернатриемии при нефротическом синдроме способствует снижение реакции почек на действие предсердного натрийдиуретического пептида, стимулирующего выведение натрия с мочой. Установлено, что пониженная реакция нефротической почки на предсердный натрийуретический пептид обусловлена пострецепторным дефектом в механизме действия этого фактора на уровне канальцевого эпителия. Возникающее при этом повышение осмотического давления стимулирует секрецию АДГ, который усиливает задержку в организме воды, что ведет к развитию отеков (рис. 19-2).
Стимуляция секреции АДГ под действием гипернатриемии сопровождается увеличением объема плазмы крови, но происходит ее разжижение, гипопротеинемия и гипоонкия возрастают. Вследствие этого избыточная вода не задерживается в кровеносном русле, а перемещается в ткани, что способствует дальнейшему нарастанию отеков, т.е. возникает «порочный круг».
Развитию гипопротеинемии при нефротическом синдроме, кроме протеинурии, способствуют повышенный выход белка в ткани в составе транссудата и потеря его через отечную слизистую кишечника. Гипопротеинемия сочетается с диспротеинемией,так как наряду с альбуминами нередко снижается содержание в крови γ-глобулинов, которые также могут поступать в мочу. Вместе с тем развивается гиперлипидемияза счет повышения содержания липопротеинов низкой и очень низкой плотности (ЛПОНП) при нормальном или пониженном уровне липопротеинов высокой плотности. В плазме крови повышается содержание холестерина и триацилглицеролов. За развитие гиперлипидемии ответственны два механизма: повышение продукции липопротеинов в печени и нарушение катаболизма хиломикронов и ЛПОНП. Предполагается, что пониженный катаболизм липопротеинов может быть обусловлен потерей с мочой некоторых субстанций (например, ли-
 Рис. 19-2.Механизм развития отеков при нефротическом синдроме. АДГ — антидиуретический гормон
Рис. 19-2.Механизм развития отеков при нефротическом синдроме. АДГ — антидиуретический гормон
попротеиновой липазы). Однако ни один из компонентов, выделенных из мочи этих больных, полностью не устраняет нарушения обмена липопротеинов. Гиперхолестеринемия и гиперлипидемия повышают риск развития у таких пациентов сердечно-сосудистых нарушений.
При нефротическом синдроме многие транспортные белки, связывающие эндогенные и экзогенные субстанции, теряются с мочой. В связи с этим в плазме крови у больных с нефротическим синдромом понижен уровень ряда микроэлементов (Fe, Cu
и Zn), метаболитов витамина D, тареоидньгх и стероидных гормонов. Многие лекарства в плазме крови связаны с альбуминами, поэтому при гипоальбуминемии повышается количество свободно циркулирующих форм, что может повысить их токсичность.
Развитие обширных отеков(вплоть до отека легких и мозга) и накопление транссудата в серозных полостях могут сопровождаться тяжелыми нарушениями функции жизненно важных органов и стать причиной летального исхода. Наряду с этим при нефротическом синдроме возникает ряд осложнений, являющихся факторами риска для таких больных.
Главную опасность при нефротическом синдроме составляют тромбоэмболические осложнения.У больных мембранозным гломерулонефритом часто возникает тромбоз почечной вены (у 20-30% взрослых пациентов); нередко происходит тромбоз глубоких вен голени. Другим опасным осложнением является эмболия легочной артерии. Артериальные тромбозы менее часты, но они могут привести к нарушению коронарного кровообращения, что повышает риск развития инфаркта миокарда. Главными факторами, ответственными за состояние гиперкоагуляции при нефротическом синдроме, являются повышение содержания прокоагулянтов — фибриногена и плазменных факторов V и VIII, снижение содержания антикоагулянта антитромбина III, ослабление активности фибринолитической системы вследствие снижения содержания плазминогена и повышение активности а2-антиплазмина; кроме того, происходит увеличение количества тромбоцитов и повышается их способность к адгезии и агрегации, что способствует нарушению микроциркуляции в различных органах и тканях.
Другую опасность для больных с нефротическим синдромом представляют инфекционные осложнения. Ранее дети с этим синдромом умирали от бактериальной инфекции, в частности от пневмококкового перитонита. Повышенная чувствительность к бактериальной инфекции обусловлена снижением уровня иммуноглобулинов А и G вследствие потери их с мочой.
Нередко происходит развитие гипокалыщемии,что обусловлено потерей с мочой связанного с белком кальция и метаболитов витамина D и снижением продукции этого витамина в проксимальных канальцах нефронов. Следствием гипокальциемии является развитие гиперпаратиреоза и остеопороза.Из других осложнений следует указать на возможность развития острой почечной недостаточности в связи с резко выраженной гиповолемией.
Ренальные показатели при нефротическом синдроме в значительной степени зависят от заболевания, на фоне которого он развился. В наиболее чистом виде они выражены при нефропатии с минимальными изменениями. При этом состоянии развивается олигурия,относительная плотность мочи повышена (1030-1050); кроме массивной протеинурии, регистрируется липидурия;в осадке мочи обнаруживаются гиалиновые, восковидные и эпителиальные цилиндры с жировыми включениями. При других вариантах нефротического синдрома в осадке мочи могут присутствовать эритроциты и лейкоциты. Массивная протеинурия повреждает эпителий канальцев, и это может сопровождаться развитием глюкозурии, гипераминоацидурии, фосфатурии, почечного канальцевого ацидоза; возникает состояние, подобное синдрому де Тони- Дебре-Фанкони.
Считается, что прогноз нефротического синдрома благоприятен при нефропатии с минимальными изменениями (при условии своевременно начатого лечения). При нефротическом синдроме другой этиологии исход зависит от вида заболевания, возникших осложнений, возраста пациента, своевременности и правильности лечения.
Источник
Нефротический синдром — состояние, характеризующееся генерализованными отеками, массивной протеинурией (выше 50 мг*кг/сут или выше 3,5 г/сутки), гипопротеинемией и гипоальбуминемией (менее 20 г/л), гиперлипидемией
(холестерин выше 6,5 ммоль/л). Термин предложен Е. М. Тареевым в 1923 году.
Характерен для поражения клубочкового аппарата почек.
Классификация[править | править код]
Гистологическая классификация[править | править код]
| Нефротический синдром | |||||||||||||||||||||||||||||||||||||||||
| Болезнь минимальных изменений | Фокальный сегментарный гломерулосклероз | Мембранозная нефропатия | Мембранопролиферативный гломерулонефрит | ||||||||||||||||||||||||||||||||||||||
Диагностика[править | править код]
Диагностика основывается на выявленных изменениях в анализах крови и мочи (протеинурия, гиперлипидемия, гипопротеинемия), на клинических данных.
Клиника МИНС(НС с минимальными изменениями) развертывается постепенно, причём преобладают экстраренальные симптомы, особенно отечный: появляются нарастающие отеки, вначале век, лица, поясничной области (в дальнейшем могут достигать степени анасарки — распространённый отёк подкожной клетчатки), половых органов, асцит, гидроторакс, реже — гидроперикард. Характерна значительная гепатомегалия вследствие дистрофии печени. Кожа становится бледной («перламутровая» бледность) при отсутствии анемии, сухой, появляются признаки гиповитаминозов А, С, В1, В2, дистрофические изменения. Могут наблюдаться ломкость и потускнение волос, на коже — трещины, из которых вытекает жидкость, striae distensae. Ребёнок вялый, плохо ест, развивается одышка, тахикардия, систолический шум на верхушке («гипопротеинемическая кардиопатия»).
Тяжёлым осложнением у больных анасаркой, то есть выраженной гипопротеинемией, может быть гиповолемический шок, которому предшествуют анорексия, рвота, резкие боли в животе. В наблюдениях Н. Д. Савенковой и А. В. Папаяна (1997) абдоминальный болевой синдром развивается у 23,5 % детей с гипоальбуминемией менее 15 г/л, а мигрирующие рожеподобные эритемы у 33,3 %, тромботические эпизоды у 12,5 %, ОПН у 3,3 % детей с той же выраженностью гипоальбуминемии, тогда как нефротический гиповолемический шок отмечен лишь при уровне белка в сыворотке менее 10 г/л (у 5 %). По мере схождения отеков становится все заметнее уменьшение массы скелетных мышц.
Артериальное кровяное давление обычно нормальное, лишь у до10% детей может быть кратковременная артериальная гипертензия. Уровень альбумина в сыворотке крови у таких детей менее 10 г/л.
Содержание общего белка в плазме (сыворотке) крови снижено иногда до 40 г/л.
Особенно резко снижена концентрация альбуминов и g-глобулина, тогда как уровень a2-глобулинов повышен, то есть наблюдается резкая диспротеинемия. Сыворотка крови имеет молочный цвет, в ней находят высокий уровень липидов, холестерина, фибриногена. Уровень азотистых шлаков крови, как правило, нормальный, а содержание калия и натрия снижено. СОЭ резко увеличена (до 50-70 мм/час).
Ренальная симптоматика — олигурия с высокой относительной плотностью (1,026-1,030) мочи и выраженная протеинурия. При исследовании клубочковой фильтрации по эндогенному креатинину получают нормальные и даже повышенные показатели, но это ложное впечатление. Если учесть степень протеинурии, то клубочковая фильтрация при МИНС всегда снижена.
Клиническая картина, течение и исход НС, осложнившего диффузный гломерулонефрит, отличаются от клиники МИНС.
Мочевой синдром при МИНС слагается из следующих симптомов:
1. протеинурия,
2. олигурия с высокой относительной плотностью мочи,
3. цилиндрурия.
Протеинурия при МИНС, как правило, селективная, то есть в моче находят белки плазмы крови с молекулярной массой менее 85 000 (альбумин и его полимеры, преальбумины, сидерофилин, гаптоглобин, трансферрин, a1- и b-глобулины, a1- и a2-гликопротеины и др.). В большинстве случаев у детей с селективной протеинурией прогноз лучше, и они чувствительны к терапии глюкокортикоидами. В генезе протеинурии имеет значение и нарушение реабсорбции белка в почечных канальцах. Неселективная протеинурия, когда в моче есть много крупномолекулярных белков, как правило, следствие фибропластического процесса, склероза, то есть для МИНС нехарактерна. Напомним, что у здорового ребёнка старше 4 лет в суточной моче может быть до 100—150 мг белка.
Олигурия связана с гиповолемией, гиперальдостеронизмом, поражением канальцев. Из-за протеинурии относительная плотность мочи увеличена, достигает 1,040. Высока активность в крови больных и АДГ.
Иногда при НС отмечается массивная лейкоцитурия, обусловленная иммунопатологическим процессом в почках. Лейкоцитурия чаще кратковременная и не связана с бактериальной инфекцией, то есть пиелонефритом. Частота выявления лейкоцитурий и эритроцитурий при МИНС по данным разных авторов не превышает 10 %.
При большом количестве белка в моче он может свернуться ещё в канальцах, принимая их форму; на этот слепок наслаивается жироперерожденный почечный эпителий — так образуются гиалиновые, зернистые и восковые цилиндры.
Отеки. Массивная и длительная альбуминурия у больного с НС в конце концов неизбежно вызывает гипопротеинемию, так как потери белка превышают интенсивность его синтеза. Гипопротеинемия ведёт к нарушению старлингова равновесия между гидродинамическим, фильтрационным и коллоидно-осмотическим давлением. Это приводит к преобладанию оттока жидкости из артериального русла над притоком. Отеки начинают появляться, когда уровень альбумина снижается ниже 27 г/л плазмы и развиваются всегда, если гипоальбуминемия достигает 18 г/л.
В патогенезе отеков важную роль играет и вторичный гиперальдостеронизм, типичный для НС. В результате его в организме задерживается натрий, а следовательно, и вода, хотя в крови имеется гипонатриемия.
Гипопротеинемия. Основной причиной гипопротеинемии у больных с НС являются большие потери альбуминов с мочой и перемещение их в ткани. Кроме того, имеют значение повышенный катаболизм альбуминов, нарушение белоксинтезирующей функции печени. Уменьшение содержания g-глобулинов в крови больных прежде всего с нарушением их синтеза. Гипоальбуминемия и гиповолемия, дефицит антикоагулянтов — антитромбина III и протеинов С и S, гиперфибриногенемия, гиперлипидемия создают угрозу для тромботических нарушений у больных МИНС.
Гиперлипидемия. Некоторые авторы связывают увеличение уровня липопротеинов низкой и очень низкой плотности, холестерина и липидов (свободные жирные кислоты, триглицериды, фосфолипиды и др.) при НС с нарушением функции печени, другие объясняют это явление понижением функции щитовидной железы. В связи с тем, что внутривенное введение раствора альбумина препятствует нарастанию гиперхолестеринемии, предполагают, что увеличение уровня холестерина в крови происходит компенсаторно вследствие уменьшения содержания альбуминов. Поскольку липидемию в эксперименте можно получить после перевязки мочеточников, высказывают мысль о том, что гиперхолестеринемия и липидемия при МИНС имеют почечное происхождение и зависят от повреждения интермедиарного обмена в ферментной системе канальцев. В генезе гиперлипидемии имеет значение также низкий уровень в крови лецитин-холестеринацетилтрансферазы, в больших количествах выделяющейся с мочой, и низкая активность липопротеидлипазы. При МИНС обычно диагностируют IIа и IIб типы гиперлипидемий.
Нарушения фосфорно-кальциевого обмена (гипокальциемия, остеопороз, остеомаляция) обусловлены нарушением функции почек, а также метаболизма витамина D.
Нарушения обмена железа и микроэлементов с низкими уровнями в крови как железа, так и цинка, меди, кобальта определяют в значительной степени склонность таких больных к анемиям, трофическим расстройствам кожи, задержке роста, а возможно — иммунодефицитам.
Вязкость крови при МИНС повышена за счёт гиперлипидемии, повышенной адгезивности тромбоцитов. В то же время уровни факторов свертывания крови (прокоагулянтов) и антисвертывания (антитромбин III, протеины С и S) снижены, что и объясняет сравнительно низкую частоту декомпенсированного ДВС-синдрома при МИНС.
Инфекции — прежде одно из очень частых осложнений МИНС. Особенно часто были перитониты, которые в большинстве случаев вызывались пневмококками, но в 25-50 % случаев — кишечной палочкой.
Диагноз[править | править код]
Характерная клинико-лабораторная картина МИНС в подавляющем большинстве случаев (90-95 %) у детей 2-7 лет позволяет поставить диагноз без биопсии почек. Хороший и быстрый ответ на терапию глюкокортикоидами подтверждает диагноз. В то же время, целесообразно у любого ребёнка с НС определить уровень IgE, выяснить наличие хронических персистирующих вирусных инфекций (гепатит B, цитомегалия, герпес-вирусные инфекции и др.), так как положительные результаты существенно дополняют и модифицируют терапию. О рецидивирующем течении НС свидетельствуют 2 рецидива в год, а о часто рецидивирующем — 3 и более рецидивов в год. Ремиссию констатируют при отсутствии протеинурии или её значении менее 4 мг/м2 в час и достижении уровня альбумина сыворотки 35 г/л. Биопсия показана детям с НС в возрасте до года и старше 12 лет, ибо у них очень мала частота МИНС.
Дифференциальная диагностика[править | править код]
Прежде всего Нефротический синдром необходимо дифференцировать от гломерулонефрита, СКВ, амилоидоза почек, интерстициального нефрита, тромбоза печеночных вен.
Лечение[править | править код]
- Диета — при нарушении функции почек ограничение приема жидкости, бессолевая, оптимальное по возрасту количество белка
- Инфузионная терапия (альбумин, реополиглюкин и др)
- Диуретики
мочегонные средства играют большую роль в лечении заболевания почек, однако при бесконтрольном и длительном их применении могут наступить резкая потеря натрия и снижение объема циркулирующей крови, гипокалиемия и метаболический ацидоз. Форсированный диурез с помощью больших доз диуретиков, как и ультрафильтрация, в условиях резкой гипоальбуминемии или выраженной почечной недостаточности может осложниться трудноуправляемым гиповолемическим шоком или дальнейшим снижением клубочковой фильтрации. Поэтому лечение диуретиками рекомендуется проводить максимально кратковременно и возобновлять только в случаях заметного снижения диуреза и нарастания отеков.
Для лечения нефротических отеков обычно применяют фуросемид — 20 — 400 мг внутрь, 20 — 1200 мг внутривенно), который оказывает достаточно мощное и быстрое, хотя и кратковременное, действие. Подобно фуросемиду действует и этакриновая кислота (50 — 200 мг/сут). Слабее действует гипотиазид, диуретический эффект которого наблюдается через 1 — 2 ч после приема 25 — 100 мг препарата. Важную роль в борьбе с отеками играют калийсберегающие диуретики — триамтерен, амилорид, особенно спиронолактоны (альдактон, верошпирон). Верошпирон применяют в дозе от 25 до 200—300 мг в сутки, Он наиболее эффектииен в сочетании с тиазидовыми диуретиками, фуросемидом. Отеки — при нефротическом синдроме, обусловленном амилоидозом, отличаются большой резистентностью к мочегонным средствам.
- Гепарин
- Антибактериальная терапия
- Кортикостероиды
Глюкокортикоиды (ГК) — преднизолон (ПЗ) (медопред, преднизол, преднизолон) и метилпреднизолон (МП) (метипред, солу-медрол) — являются первыми препаратами выбора при иммуносупрессивном лечении ГН. ГК влияют на перераспределение иммунокомпетентных и воспалительных клеток, препятствуя их поступлению в очаг воспаления, подавляют их чувствительность к медиаторам воспаления, угнетают секрецию таких провоспалительных цитокинов, как ФНО-α, ИЛ-1, ИЛ-2, ИЛ-6. ГК запускают процессы глюконеогенеза, способствуя включению антител в углеводный обмен и тем самым снижая их количество, тонизируют капиллярную стенку и снижают гиперемию за счёт активации и набухания перицитов. Введение больших доз ГК в виде «пульсов» МП угнетает образование ДНК-антител, приостанавливает образование иммунных комплексов, уменьшает их массу и способствует выходу из субэндотелиальных слоёв гломерулярной базельной мембраны, повышает клубочковую фильтрацию и почечный кровоток.
ГК назначаются детям во всех случаях впервые возникшего НС, при рецидивах гормоночувствительного НС (как правило, НСМИ), при прогрессирующем течении ГН, в сочетании с другими иммунодепрессантами и пр.
На практике применяются три режима ГК терапии.
Постоянный пероральный прием ПЗ в дозе 1-2 мг/кг в 2-4 приема с учетом суточной активности коры надпочечников (максимальные дозы препарата в утренние часы с последующим снижением, последний прием не позднее 16.00) назначается в начале лечения для достижения ремиссии.
Альтернирующий (альтернативный) режим приема ПЗ используется при переходе на поддерживающую терапию. Заключается в приеме суточной дозы ПЗ через день, что позволяет при сохранении клинического эффекта значительно снизить побочные явления: острые — бессонницу, эйфорию, психоз, повышение аппетита; хронические — отеки, ожирение, миопатию, стрии, атрофию кожи, гирсутизм, aкне, остеопороз, катаракту, повышение АД, стероидный диабет; адреналовый криз — острую надпочечниковую недостаточность при резкой отмене препарата. Также существует вариант альтернирующего режима с приемом ПЗ ежедневно в течение 3 дней, затем 3-4 дня перерыва. По эффективности оба режима альтернирующего приема ПЗ примерно одинаковы.
Пульс-терапия МП используется для достижения очень высоких концентраций ГК в плазме. Заключается во внутривенном капельном введении в течение 20-40 мин около 30 мг/кг МП (не более 1 г на пульс) один раз в 48 ч. Количество введений, а также разовая и суммарная доза определяются выбранной схемой терапии данной патологии.
Побочные эффекты глюкокортикоидов могут быть следующими: бессонница, эйфория, психоз, повышение аппетита, отеки, ожирение, миопатия, стрии, атрофия кожи, гирсутизм, акне, остеопороз, катаракта, повышение АД, стероидный диабет, адреналовый криз (острая надпочечниковая недостаточность при резкой отмене препарата)
- Цитостатики
Цитостатические (цитотоксические) препараты (ЦС). Алкилирующие агенты: циклофосфамид (циклофосфан, цитоксан) и хлорамбуцил (хлорбутин, лейкеран) — нарушают деление клеток за счёт связывания с нуклеиновыми кислотами ядерной ДНК. Поступают в организм в неактивном состоянии, активизируются в печени. Действуют неизбирательно на все делящиеся клетки (неселективные иммуносупрессанты).
Циклофосфамид назначается внутрь или в виде «пульсов». Внутрь препарат назначается из расчёта 2,0-2,5 мг/кг/сут на 8-12 нед при лечении гормонозависимого или часторецидивирующего НС на фоне постепенного снижения дозы альтернирующего режима ПЗ, а также при гормонорезистентности.
Пульс-терапия циклофосфамидом проводится на фоне альтернирующего курса ПЗ при гормонозависимом и гормонорезистентном НС из расчёта 12-17 мг/кг внутривенно капельно. Количество «пульсов» и временной интервал между ними зависят от выбранной схемы терапии. Другой вариант — «пульс» 1 раз в месяц в течение 6-12 мес, в кумулятивной дозе не выше 250 мг/кг.
Хлорамбуцил принимается per os в дозе 0,15-0,2 мг/кг/сут в течение 8-10 нед для лечения гормонозависимого и часторецидивирующего НС, реже при гормонорезистентном НС, на фоне альтернирующего курса ПЗ с постепенным снижением.
Антиметаболиты — азатиоприн и метотрексат — в настоящее время при лечении ГН используются редко. Из побочных действий цитостатиков возможны: при применении циклофосфана — тошнота, рвота, лейкопения, геморрагический цистит, недостаточность гонад; хлорбутина — лёгочный фиброз, дерматит, судороги, гепатопатия, лейкопения.
Ссылки[править | править код]
- Нефротический синдром
- Нефротический синдром (недоступная ссылка)
- Нефротический синдром у детей
Источник
