Малоинвазивная терапия болевого синдрома от
30 апреля 2019 г.
Просмотров: 541
В лечении болевых синдромов наряду с фармакотерапией используются малоинвазивные способы. К ним относят нейромодуляцию и лечебно-медикаментозные блокады. Оптимальность мультидисциплинарного подхода в терапии хронической боли не подлежит сомнению, но вместе с тем очевидно, что каждый из указанных методов в определенных случаях может оказаться важным и результативным способом лечения.
Проведение малоинвазивных процедур требует определенного оснащения и специфических навыков, в связи с чем уступает по доступности фармако-терапевтическому подходу, но знать о терапевтических возможностях этих методик, их потенциальных преимуществах и вероятных осложнениях должны как узкие специалисты, так и врачи общей практики, так или иначе связанные с лечением пациентов, страдающих острой и хронической болью.
Хирургическая нейромодуляция представлена методами лечения, основанными на электрическом или медиаторном воздействии на структуры нервной системы. Ее подразделяют на нейростимуляцию и длительное эпидуральное или интратекальное введение лекарственных средств.
Нейростимуляции лучше поддается боль, имеющая нейрогенную природу. Для лечения ноцигенной боли более действенным оказывается эпидуральное или интратекальное введение опиоидных анальгетиков. Каждый из этих методов имеет теоретическое обоснование.
Эпидуральное применение опиоидов
Существенный прогресс в понимании механизма анальгетического действия опиоидов произошел в начале 70-х годов ХХ столетия. Вначале был выделен класс высоко специфичных опиоидных рецепторов, а затем обнаружена высокая плотность нахождения этих рецепторов в местах межсинаптической передачи в спинном и головном мозге. В экспериментах на животных была подтверждена возможность обеспечения селективной анальгезии после введения морфина в субарахноидальное пространство.
На рубеже 70–80-х годов прошлого столетия начались клинические исследования эффективности подоболочечного (субарахноидального) и эпидурального использования морфина для купирования боли у пациентов с прогрессирующим раком, сопровождающимся трудно купируемым болевым синдромом.
Подведение опиоидов к спинномозговым структурам, контролирующим проведение сигналов от периферии в головной мозг, позволяет существенно увеличить их концентрацию в рецепторной зоне, поэтому эффект анальгезии достигается использованием малого количества наркотического анальгетика. Рандомизированные клинические исследования показали преимущество такого способа перед традиционным парентеральным введением максимальных доз опиоидов как по выраженности обезболивания, так и по частоте развития побочных эффектов.
Первоначально к выведенному через кожу концу эпидурального катетера присоединялся бак фильтр с целью снижения частоты инфекционных осложнений. Катетер крепили к коже с помощью прозрачного пластыря. Эффективное функционирование такой системы составляло от 1 недели до 2-3 месяцев. Одним из лимитирующих факторов их использования являлся риск развития инфекции и близость входных ворот (места пункции) к эпидуральному пространству (4-5 см). Поэтому начали использовать методики подкожной туннелизации катетера, что удлиняло реальные сроки относительно безопасной его эксплуатации до нескольких месяцев.

При высокой эффективности анальгезии и существенном уменьшении суточной дозы морфина (по сравнению с подкожными инъекциями) выявился существенный недостаток: методика введения морфина требовала участия в процедуре медработника или самого пациента. Поэтому со временем стали использоваться полностью имплантируемые системы с помпой и подкожным портом, доступ к которому для «дозаправки» осуществлялся с помощью чрескожной иглы.
Субарахноидальное введение опиоидов
Следующим шагом в совершенствовании методики явилась установка катетера в субарахноидальное пространство: расход морфина для получения желаемого эффекта обезболивания сокращался на порядок — суточная доза морфина снижалась до 1 мг. Внедрение такого способа обезболивания подразумевало не только использование микрокатетеров, но и специальных устройств-дозаторов (помп) — резервуаров с активным веществом с постоянным или регулируемым режимами введения препарата. В этом случае скорость введения обеспечивается при помощи специального радиопередатчика — программатора.
Как и в случае использования подобных эпидурально устанавливаемых систем, помпа и катетер полностью имплантируются под кожу (помпа — обычно на уровне передней поверхности грудной клетки на уровне 12-го ребра). Заправка такой системы анальгетиком производится раз в несколько недель и сводит к минимуму участие пациента.
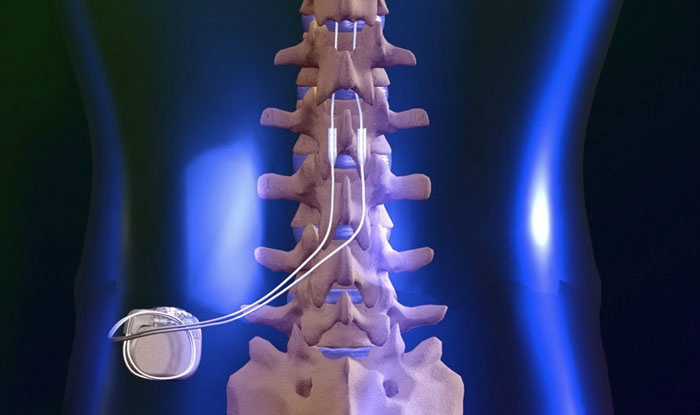
Хроническая стимуляция спинного мозга
Наиболее распространенной формой нейростимуляции (существует электростимуляция периферических нервов, задних столбов спинного мозга, глубоких структур и коры головного мозга) является хроническая стимуляция спинного мозга.
Объяснить получаемый при помощи такой методики анальгетический эффект можно при помощи теории «воротного контроля», предложенной П. Уоллом и Р. Мелзаком в 1965 году. Авторы предположили, что в спинном мозге на уровне 2-го нейрона через вставочные интернейроны желатинозной субстанции осуществляется подавление ноцигенной информации, приходящей с периферии. Модуляторами этого «болевого» потока выступают антиноцицептивная система и поступающая к тому же нейрону сенсорная «неболевая» информация.
Таким образом, легкое потирание поврежденного участка или электрическая стимуляция нервов и задних колонн «закрывают ворота» для ноцигенного стимула. Ввиду низкой силы генерируемых импульсов, повреждения нервных структур не происходит, формируемые ощущения в виде тепла или легкой вибрации не приносят беспокойства пациенту, но их вполне достаточно, чтобы блокировать ощущение боли. При этом происходит не только конкурентное подавление восходящей ноцицептивной информации, но и стимуляция антиноцицептивных механизмов, значительно подавленных при хроническом болевом синдроме. Таким образом, происходит восстановление баланса между болевой и противоболевой активностью, клинически проявляющегося купированием или значительным ослаблением боли.

Схема имплантируемого под кожей устройства похожа на описанную выше катетерную эпидуральную методику обезболивания при помощи помпового механизма, только вместо катетера используются специальные электроды, а вместо помпы с лекарственным веществом — программируемый генератор. Развитие технологий привело к созданию тонких электродов, программируемых нейростимуляторов, возможности полностью имплантировать системы и осуществлять их настройку с помощью программатора. Методика показала высокую эффективность в лечении периферической нейропатической боли. Важным сдерживающим фактором ее широкого применения у пациентов с рефрактерными болевыми синдромами является достаточно высокая стоимость.
Блокады нервных стволов
Одним из важных методов лечения болевых синдромов являются блокады нервных стволов, сплетений, ганглионарных структур. Далеко не каждое инъекционное воздействие следует считать медикаментозной блокадой. Блокада — это малоинвазивное высокоселективное воздействие на определенные структуры, генерирующие или транслирующие события, воспринимаемые как локализованная боль. Для ее успешного проведения специалист должен обладать не только базовыми знаниями по патологии, которую собирается лечить, но и хорошо представлять топографическую анатомию области манипуляции, фармакологию средств, которыми предполагает работать, а также прогнозировать возможные осложнения (порой довольно драматичные) и в случае их развития использовать приемы интенсивной терапии и жизнеобеспечения.
В настоящее время с целью купирования болевых синдромов преимущественно применяются паравертебральные, эпидуральные, внутри суставные и внутрикостные блокады. Необходимо понимать, что эффективность лечебных блокад основана не на временном выключении ноцицепторов с помощью местного анестетика, а на прерывании болевой импульсации, которая поддерживает нейрональную гиперактивность.
Блокады бывают двух типов: диагностические и лечебные. Цель диагностической блокады — уточнение локализации источника боли и определение предполагаемой эффективности процедуры. Терапевтическая блокада — по возможности должна быть этиопатогенетической.
Нередко для усиления действия местного анестетика используют комбинацию лекарственных препаратов с противовоспалительным действием. Бывают ситуации, когда для эффективной анальгезии может потребоваться стойкое выключение нейрональной структуры посредством подведения раствора нейролептика или проведения радиочастотной абляции. В качестве примера остановимся на некоторых вариантах блокад. Одной из важнейших медико-социальных проблем является боль в спине — наиболее распространенная причина ограничения физической активности у лиц молодого и среднего возраста. Среди причинных факторов ведущее значение имеют поражение фасеточных суставов и радикулопатии.
Селективные блокады корешков спинномозговых нервов
Основным показанием для селективной корешковой блокады является радикулопатия. При этом клиническая картина болевого синдрома не всегда позволяет четко определить локализацию поражения, а существующие методы визуальной диагностики (МРТ, КТ) могут выявить многоуровневый характер поражения. Для невролога, выбирающего фармакотерапию, возможно, точность локализации генератора боли не повлияет на лечебную тактику. Но для специалиста, проводящего лечебно-медикаментозную блокаду, а тем более собирающегося проводить оперативное лечение, безошибочное определение «мишени», т.е. очага поражения, имеет первостепенное значение.
Поэтому в затруднительных ситуациях первоначально осуществляется диагностическая блокада местным анестетиком. Эта процедура, заключающаяся в высокоточном подведении малого количества местного анестетика к «подозрительному» корешку (предпочтительно в условиях лучевой или ультразвуковой визуализации), позволяет селективно блокировать его.
Блокада фасеточных (дугоотросчатых) суставов
Кому не знакомы схваткообразные боли в поясничной области, иррадиирующие в ягодицы и бедра, усиливающиеся при длительном сидении, при наклонах, разгибании и ротации туловища, чувство скованности в пояснице, уменьшающееся при ходьбе?
Так характеризуются ощущения при патологии парных дугоотросчатых суставов, образованных суставными отростками соседних позвонков. В структуре боли в спине данная патология достигает 50%. Внутрисуставная инъекция малого количества местного анестетика (объем сустава — 0,5-1,0 мл) или блокада медиальной ветви задней порции спинномозгового нерва на уровне поражения и сегментом выше — основная диагностическая процедура при патологии фасеточного сустава. Стойкий эффект возможен при острой ситуации — люмбаго.
В случаях хронической люмбалгии часто эффект ограничен длительностью действия анестетика. Добавление к смеси глюкокортикоида (0,5 мл) может существенно удлинить аналгезию, однако стойкое улучшение состояния может быть достигнуто при помощи радиочастотной абляции медиальной ветви.
Манипуляции должны выполняться под рентген контролем. Осложнения могут включать разрыв сустава, непреднамеренную корешковую блокаду, случайное интратекальное введение, неврит при проведении абляции.
Симпатические блокады
Среди лечебно-медикаментозных блокад, используемых в лечении болевых синдромов, особое место занимают симпатические блокады, прерывающие симпатические эфферентные влияния, играющие важную роль в патогенезе ряда заболеваний (плексопатиях, КРБС, постгерпетической невралгии, сосудистых поражениях, висцеральных болевых синдромах). В своей практике врачи анестезиологи-реаниматологи нередко используют преимущества симпатического блока для устранения, например, послеоперационного пареза кишечника, устанавливая для обезболивания катетер в эпидуральное пространство. К сожалению, возникающий в таких ситуациях блок неселективен, поскольку вместе с симпатическими волокнами выключаются и сенсорные нервы.
Изолированные симпатические блокады имеют четкие показания:
- Заболевания внутренних органов. Не случайно вегетативную нервную систему раньше называли висцеральной: по сути, висцеральные волокна, ответственные за афферентацию, имеют тесную анатомическую связь с симпатическими структурами — чревным, верхним подчревным сплетением, спланхническими нервами, ганглиями симпатической цепочки. Блокада (временная или стойкая) этих образований способна прервать болевой поток от внутренних органов.
- Ишемические поражения конечностей. Способность симпатических волокон участвовать в регуляции тонуса периферических сосудов с успехом используется при лечении ряда заболеваний (синдром и болезнь Рейно, облитерирующий эндартериит, атеросклероз, ангиопатии при сахарном диабете). Симпатическая блокада в таких случаях способна улучшить периферический кровоток, уменьшить трофические нарушения и существенно уменьшить болевые ощущения в конечностях.
- Симпатически поддерживаемая боль.
В многопрофильной клинике «Медицина 24/7» принимают пациентов любой степени тяжести, в том числе с онкологическими диагнозами III и IV стадий. Инкурабельным пациентам наши врачи могут помочь паллиативным лечением, направленным на продление качественной жизни пациента. Паллиативное лечение включает в себя не только уход за пациентом, но и проведение оперативных вмешательств с целью снятия болезненных симптомов. В частности, в клинике проводят: циторедуктивные операции, радиочастотную аблацию метастатического поражения печени и костей, фотодинамическую терапию, стентирование при стенозах внутренних органов, гастростомия, колостомию и др.
Литература:
- Браун Д.Л. Атлас регионарной анестезии / Пер. с англ.под ред. акад. В.К. Гостищева. М., 2009.
- Ван Роенн Д.Х., Пэйс Д.А., Преодер М.И. Диагностика и лечение боли / Пер. с англ. под ред. проф. М.Л. Кукушкина. М., 2012.
- Каннер Р.М. Секреты лечения боли / Пер. с англ. под ред. проф. А.М. Овечкина. М., 2006.
- Benzon H.T. Complications associated with neurolytic blocks // Complications in regional anesthesia and painmedicine. / Eds. J.M. Neal, J.P. Rathmell. Philadelphia:Saunders Elsevier. 2007. P. 273-286.
Источник: Научно-практический журнал «Паллиативная медицина и реабилитация» № 2. 2018.
Источник
