Липидный обмен при метаболическом синдроме

Большинство авторов сходятся во мнении о существовании нескольких механизмов, обусловливающих наличие связи артериальной гипертензии и инсулинорезистентности.
Еще в 80-х годах прошлого века ученые пришли к выводу, что сочетание артериальной гипертензии с метаболическими факторами риска – это не механическое скопление, а закономерное проявление единой цепи целого ряда сложных биохимических нарушений на тканевом уровне. В 1985 г. Было высказано предположение, что гиперинсулинемия может служить связывающим звеном между артериальной гипертензией, ожирением и нарушением толерантности к глюкозе (НТГ). В ряде исследований по прямому определению инсулинорезистентности было показано, что больные с артериальной гипертензией в среднем утилизируют на 40% меньше глюкозы, чем лица с нормальным артериальным давлением.
В эпидемиологических исследованиях продемонстрировано также, что 64% больных с артериальной гипертензией имели инсулинорезистентности и только у половины пациентов она клинически манифестировала с нарушением углеводного обмена. С другой стороны, у 36% больных, имевших гиперлипопротеидемию (ГЛП) или избыточную массу тела (ИМТ), не было выявлено инсулинорезистентности. Таким образом, даже на фоне имеющегося в настоящее время огромного интереса к метаболическому синдрому было бы ошибочным связывать каждый случай эссенциальной артериальной гипертензии с проявлениями тканевой инсулинорезистентности.
Хроническая гиперинсулинемия как проявление тканевой инсулинорезистентности способствует задержке в организме натрия путем ускорения его реабсорбции, что приводит к увеличению объема жидкости и общего периферического сосудистого сопротивления. Повышение активности Na-K-, H- и Ca-Mg-АТФазы под непосредственным воздействием инсулина вызывает увеличение содержания внутриклеточного натрия и кальция, что способствует вазоконстрикции гладкой мускулатуры сосудов. При этом усиливается и чувствительность сосудов к прессорным агентам, таким как адреналин и ангиотензин.
Гиперинсулинемия также способствует активации симпатической нервной системы (СНС), в результате чего возрастает сердечный выброс и стимулируется вазоконстрикция периферических кровеносных сосудов. Симпатическая стимуляция почек запускает мощный механизм развития артериальной гипертензии – ренин-ангиотензин-альдостероновую систему. Исследования показывают, что при сочетании артериальной гипертензии с инсулинорезистентностью активность АПФ является достоверно более высокой по сравнению с больными артериальной гипертензией без проявлений инсулинорезистентности. Ангиотензин 11 – главный действующий компонент ренин-ангиотензин-альдостероновой системы – прямо и косвенно (опосредованно через активацию симпатической нервной системы) повышает давление в клубочковом аппарате, вызывает пролиферацию гладкомышечных стенок артерий, гипертрофию кардиомиоцитов и нарушает функцию эндотелия, что способствует системной артериальной и венозной вазоконстрикции.
Особую роль в ассоциации артериальной гипертензии и инсулинорезистентности играет ожирение абдоминального типа, характерное для метаболиского синдрома. В адипоцитах брыжейки и сальника идет синтез метаболически активных веществ, ингибирующих выработку эндогенного оксида азота, соответственно стимулируя вазоконстрикцию. В последние годы также активно обсуждается роль лептина в усилении активности симпатической нервной системы. Артериальная гипертензия развивается примерно у 60% больных ожирением.
В последнее десятилетие получило развитие учение о роли функции эндотелия в формировании и прогрессировании артериальной гипертензии. Показано, что в патогенезе артериальной гипертензии, связанном с метаболическими нарушениями, эндотелиальная функция является интегральным аспектом синдрома инсулинорезистентности и способствует ее углублению, увеличению реактивности сосудов и дальнейшему формированию артериальной гипертензии.
Источник
Содержание
- Метаболический синдром
- Причины метаболического синдрома
- Симптомы метаболического синдрома
- Осложнения
- Диагностика
- Лечение метаболического синдрома
- Прогноз и профилактика
Метаболический синдром – симптомокомплекс, проявляющийся нарушением обмена жиров и углеводов, повышением артериального давления. У больных развивается артериальная гипертензия, ожирение, возникает резистентность к инсулину и ишемия сердечной мышцы. Диагностика включает осмотр эндокринолога, определение индекса массы тела и окружности талии, оценку липидного спектра, глюкозы крови. При необходимости проводят УЗ-исследование сердца и суточное измерение АД. Лечение заключается в изменении образа жизни: занятиях активными видами спорта, специальной диете, нормализации веса и гормонального статуса.
Метаболический синдром
Метаболический синдром (синдром Х) – коморбидное заболевание, включающее сразу несколько патологий: сахарный диабет, артериальную гипертензию, ожирение, ишемическую болезнь сердца. Термин «синдром Х» впервые был введен в конце ХХ века американским ученым Джеральдом Ривеном. Распространённость заболевания колеблется от 20 до 40%. Болезнь чаще поражает лиц в возрасте от 35 до 65 лет, преимущественно страдают пациенты мужского пола. У женщин риск возникновения синдрома после наступления менопаузы увеличивается в 5 раз. За последние 25 лет количество детей с данным расстройством возросло до 7% и продолжает увеличиваться.
Причины метаболического синдрома
Синдром Х – патологическое состояние, которое развивается при одновременном воздействии нескольких факторов. Главной причиной является нарушение чувствительности клеток к инсулину. В основе инсулинорезистентности лежит генетическая предрасположенность, заболевания поджелудочной железы. К другим факторам, способствующим возникновению симптомокомплекса, относят:
- Нарушение питания. Повышенное потребление углеводов и жиров, а также переедание приводят к увеличению веса. Если количество потребленных калорий превосходит энергетические затраты, накапливаются жировые отложения.
- Адинамия. Малоактивный образ жизни, «сидячая» работа, отсутствие спортивной нагрузки способствуют замедлению метаболизма, ожирению и появлению инсулинорезистентности.
- Гипертоническая болезнь. Длительно протекающие неконтролируемые эпизоды гипертензии вызывают нарушение кровообращения в артериолах и капиллярах, возникает спазм сосудов, нарушается метаболизм в тканях.
- Нервное напряжение. Стресс, интенсивные переживания приводят к эндокринным расстройствам и перееданию.
- Нарушение гормонального баланса у женщин. Во время менопаузы повышается уровень тестостерона, снижается выработка эстрогена. Это становится причиной замедления обмена веществ в организме и увеличения жировых отложений по андроидному типу.
- Гормональный дисбаланс у мужчин. Снижение уровня тестостерона после 45 лет способствует набору массы тела, нарушению метаболизма инсулина и повышению артериального давления.
Симптомы метаболического синдрома
Первыми признаками метаболических нарушений становятся утомляемость, апатия, немотивированная агрессия и плохое настроение в голодном состоянии. Обычно пациенты избирательны в выборе пищи, предпочитают «быстрые» углеводы (торты, хлеб, конфеты). Потребление сладкого вызывает кратковременные подъемы настроения. Дальнейшее развитие болезни и атеросклеротические изменения в сосудах приводят к периодическим болям в сердце, приступам сердцебиения. Высокий уровень инсулина и ожирение провоцируют расстройства работы пищеварительной системы, появление запоров. Нарушается функция парасимпатической и симпатической нервной системы, развивается тахикардия, тремор конечностей.
Для заболевания характерно увеличение жировой прослойки не только в области груди, живота, верхних конечностей, но и вокруг внутренних органов (висцеральный жир). Резкий набор веса способствует появлению бордовых стрий (растяжек) на коже живота и бедер. Возникают частые эпизоды повышения АД выше 139/89 мм рт. ст., сопровождающиеся тошнотой, головной болью, сухостью во рту и головокружением. Отмечается гиперемия верхней половины туловища, обусловленная нарушением тонуса периферических сосудов, повышенная потливость за счет сбоев в работе вегетативной нервной системы.
Осложнения
Метаболический синдром приводит к возникновению гипертонической болезни, атеросклероза коронарных артерий и сосудов головного мозга и, как следствие, инфаркту и инсульту. Состояние инсулинорезистентности вызывает развитие сахарного диабета 2 типа и его осложнений – ретинопатии и диабетической нефропатии. У мужчин симптомокомплекс способствует ослаблению потенции и нарушению эректильной функции. У женщин синдром Х является причиной возникновения поликистоза яичников, эндометриоза, снижения либидо. В репродуктивном возрасте возможно нарушение менструального цикла и развитие бесплодия.
Диагностика
Метаболический синдром не имеет явной клинической симптоматики, патология часто диагностируется на поздней стадии после возникновения осложнений. Диагностика включает:
- Осмотр специалиста. Врач-эндокринолог изучает анамнез жизни и заболевания (наследственность, распорядок дня, режим питания, сопутствующие болезни, условия жизни), проводит общий осмотр (параметры АД, взвешивание). При необходимости больной направляется на консультацию к диетологу, кардиологу, гинекологу или андрологу.
- Определение антропометрических показателей. Андроидный тип ожирения диагностируется путем измерения окружности талии. При синдроме Х данный показатель у мужчин составляет более 102 см, у женщин – 88 см. Лишний вес выявляется подсчетом индекса массы тела (ИМТ) по формуле ИМТ = вес (кг)/рост (м)². Диагноз «ожирение» ставят при ИМТ больше 30.
- Лабораторные анализы. Нарушается липидный обмен: повышается уровень холестерина, ЛПНП, триглицеридов, снижается уровень ЛПВП. Расстройство углеводного обмена ведет к увеличению глюкозы и инсулина в крови.
- Дополнительные исследования. По показаниям назначается суточный мониторинг АД, ЭКГ, ЭХО-КГ, УЗИ печени и почек, гликемический профиль и глюкозотолерантный тест.
Метаболические нарушения следуют дифференцировать с болезнью и синдромом Иценко-Кушинга. При появлении затруднений выполняют определение суточной экскреции кортизола с мочой, дексаметазоновую пробу, томографию надпочечников или гипофиза. Дифференциальная диагностика метаболического расстройства также проводится с аутоиммунным тиреоидитом, гипотиреозом, феохромоцитомой и синдромом стромальной гиперплазии яичников. В этом случае дополнительно определяют уровень АКТГ, пролактина, ФСГ, ЛГ, тиреотропного гормона.
Лечение метаболического синдрома
Лечение синдрома Х предполагает комплексную терапию, направленную на нормализацию веса, параметров АД, лабораторных показателей и гормонального фона.
- Режим питания. Пациентам необходимо исключить легкоусвояемые углеводы (выпечку, конфеты, сладкие напитки), фаст-фуд, консервированные продукты, ограничить количество потребляемой соли и макаронных изделий. Ежедневный рацион должен включать свежие овощи, сезонные фрукты, злаковые, нежирные сорта рыбы и мяса. Пищу следует употреблять 5-6 раз в день небольшими порциями, тщательно пережевывая и не запивая водой. Из напитков лучше выбирать несладкий зеленый или белый чай, морсы и компоты без добавления сахара.
- Физическая активность. При отсутствии противопоказаний со стороны опорно-двигательной системы рекомендуется бег трусцой, плавание, скандинавская ходьба, пилатес и аэробика. Физическая нагрузка должна быть регулярной, не менее 2-3 раз в неделю. Полезна утренняя зарядка, ежедневные прогулки в парке или лесополосе.
- Медикаментозная терапия. Лекарственные препараты назначаются с целью лечения ожирения, снижения давления, нормализации обмена жиров и углеводов. При нарушении толерантности к глюкозе применяют препараты метформина. Коррекцию дислипидемии при неэффективности диетического питания проводят статинами. При гипертензии используют ингибиторы АПФ, блокаторы кальциевых каналов, диуретики, бета-блокаторы. Для нормализации веса назначают препараты, уменьшающие всасывание жиров в кишечнике.
Прогноз и профилактика
При своевременной диагностике и лечении метаболического синдрома прогноз благоприятный. Позднее выявление патологии и отсутствие комплексной терапии вызывает серьезные осложнения со стороны почек и сердечно-сосудистой системы. Профилактика синдрома включает рациональное питание, отказ от вредных привычек, регулярные занятия спортом. Необходимо контролировать не только вес, но и параметры фигуры (окружность талии). При наличии сопутствующих эндокринных заболеваний (гипотиреоз, сахарный диабет) рекомендовано диспансерное наблюдение эндокринолога и исследование гормонального фона.
Источник
На рубеже веков демографическая ситуация в мире заметно меняется: в 2000 г. в популяции преобладали лица молодого возраста, тогда как через 30 лет ожидается заметное старение человеческой популяции. Эксперты ВОЗ прогнозируют увеличение темпов неинфекционных заболеваний, к числу которых относятся ССЗ, ИБС, нарушение мозгового кровообращения, СД типа 2 и онкологические заболевания. В развитии «заболеваний цивилизации» существенную роль играют факторы риска. Если в 60-х гг. XX в. основными факторами риска считались гиперхолестеринемия, курение и артериальная гипертония, то в настоящее время доминируют метаболические факторы риска, такие, как ожирение, метаболический синдром и сахарный диабет (1).
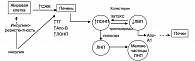
Рисунок 1. Механизм развития дислипидемии при МС

Таблица 1. Мета-анализ крупных исследований по влиянию статинов на риск сердечно-сосудистых осложнений в общей группе и субгруппе больных сахарным диабетом
В 2007 г. были опубликованы рекомендации Европейского общества кардиологов и Европейской ассоциации по изучению диабета, в которых анализируется роль метаболического синдрома (МС) в развитии сердечно-сосудистых заболеваний (ССЗ) и их осложнений. МС является сочетанием инсулинорезистентности, артериальной гипертонии, дислипидемии (гипертриглицеридемия, повышение холестерина ЛНП, низкий уровень холестерина ЛВП), микроальбуминурии, гиперурикемии, нарушения системы гемостаза и хронического субклинического воспаления. В настоящее время существует по крайнем мере 5 определений, предложенных: ВОЗ в 1998 г., Европейской группой по изучению инсулинорезистентности (ЕГИР) в 1999 г., Советом экспертов национальной образовательной программы по холестерину (ATP III NCEP) в 2001 г., Американской ассоциацией клинических эндокринологов в 2003 г. и Международной федерацией диабета в 2005 г. Критерии ВОЗ и ЕГИР были предназначены для исследовательских целей, а критерии NCEP и Международной федерации диабета нацелены на клиническую практику. В нескольких европейских проспективных исследованиях было показано, что МС ассоциируется с увеличением сердечно-сосудистой и общей смертности. Однако в американском исследовании NHANES II с участием 2341 взрослых американцев в возрасте 30-75 лет МС сопровождался умеренным увеличением риска сердечно-сосудистой смерти, но не оказывал достоверного влияния на риск смерти от любых причин или инсульта. Мета-анализ проспективных исследований показывает, что МС по сравнению с отдельными факторами риска ССЗ имеет более выраженный атерогенный потенциал, что способствует высокому риску развития ССЗ (2).
Особенности нарушений липидного обмена при МС
Термин дислипидемия более точно характеризует нарушения липидного обмена при МС, которые проявляются в виде увеличения апо-В-содержащих частиц, таких, как триглицериды, холестерин ЛОНП, мелкие и плотные частицы холестерина ХС ЛНП и снижения апо-А1-содержащих частиц холестерина ХС ЛВП. Эти нарушения имеют определенную последовательность или патогенетическую цепь развития (рисунок 1). При инсулинорезистентности в жировой клетке происходит липолиз, что приводит к выбросу большого количества свободных жирных кислот в кровоток через воротную вену. Они служат субстратом для синтеза триглицеридов печенью и избыточной продукции липопротеидов очень низкой плотности (ЛОНП). Под воздействием фермента печеночная липаза, ЛОНП превращаются в мелкие и плотные частицы ЛНП. Такие частицы подвергаются быстрому окислению и проникают в субэндотелиальное пространство, что усиливает процесс развития атеросклеротического поражения. В то же время увеличение активности белка, переносящего эфиры холестерина, приводит к переходу триглицеридов от ЛОНП к ЛВП (взамен на холестерин). В результате этого уменьшается концентрация ЛВП – основных частиц, осуществляющих обратный транспорт холестерина. Более того, они изменяются качественно (более мелкие частицы), что является причиной их быстрого выведения из кровообращения (9). Таким образом, нарушения липидного обмена при СД отличаются изменением соотношения «плохого» (ХС ЛНП и ХС ЛОНП) и «хорошего» (ХС ЛВП) холестерина, а также увеличением концентрации триглицеридов. В практической медицине эти нарушения именуется как липидная триада (3).
В 2007 г. завершено одномоментное российское исследование по выявлению МС в случайной выборке взрослой популяции в отдельно взятом городе Приволжского федерального округа (г. Чебоксары). В исследовании участвовали 1800 мужчин и женщин в возрасте 30-69 лет. Отклик составил 88,7% (n = 1718).Было показано, что 20,6% лиц имеют МС, причем у женщин он встречается в 2,4 раза чаще, а с возрастом число больных увеличивается. Так, в возрастном диапазоне 30-39 лет МС выявлен у 1%, в 40-49 лет – у 3,6%, в 50-59 лет – у 9%, а в возрасте 60-69 лет – у 7% респондентов. Для диагностики метаболического синдрома использовали критерии NCEP (наличие 3 и более компонентов, включая гипертриглицеридемию и низкий уровень холестерина ЛВП). В целом, у 78% пациентов с МС выявлен низкий уровень холестерина ЛВП, тогда как гипертриглицеридемия диагностирована у 44%. Несмотря на то, что гиперхолестеринемия не включена в критерии диагностики, у 76% пациентов с МС диагностирована мягкая и умеренная гиперхолестеринемия (52 и 24% соответственно) (4).
По данным Британского проспективного исследования по диабету (UKPDS), прогностическая значимость факторов риска в плане развития ИБС (стенокардия напряжения и/или инфаркт миокарда) составляет следующую последовательность: холестерин ЛНП, холестерин ЛВП, гликированный гемоглобин, систолическое АД. В исследовании определяли влияние на риск развития ИБС повышения уровней ключевых факторов риска на одну ступень. Так, повышение уровня холестерина ЛНП на 1 ммоль/л вызывало увеличение риска развития ИБС на 57%, а повышение уровня холестерина ЛВП на 0,1 ммоль/л приводило к снижению риска на 15% (5).
Учитывая сложное взаимодействие триглицеридов и других липопротеидов и вариабельность концентрации триглицеридов, очевидно, что подтвердить их прогностическое значение с помощью математических методов сложно. При мета-анализе популяционных исследований было показано, что при увеличении уровня триглицеридов на 1 ммоль/л сердечно-сосудистый риск повышается на 32% у мужчин и 76% у женщин. С поправкой на уровень холестерина ЛВП степень повышения сердечно-сосудистого риска уменьшилась вдвое, но сохранила статистическое значение (2).
Таким образом, повышенный уровень холестерина ЛНП и низкая концентрация холестерина ЛВП в крови является сильным предиктором развития ИБС у больных с МС.
Принципы лекарственной терапии при дислипидемии и МС
Поиск эффективных методов лечения дислипидемии берет свое начало с 70-х гг. XX в. Применение секвестрантов желчных кислот, никотиновой кислоты и в дальнейшем фибратов (в частности, гемфиброзил) показало, что имеется достоверная корреляция между снижением уровня холестерина и уменьшением частоты сердечно-сосудистых осложнений. По различным причинам эти группы препаратов не нашли широкого применения для коррекции дислипидемии у больных с метаболическими нарушениями и высоким сердечно-сосудистым риском. С появлением статинов открылись новые возможности эффективного и безопасного снижения смертности от сердечно-сосудистых заболеваний. Американский ученый W. Roberts определил значение статинов при лечении атеросклероза таким, каким было значение пенициллина в лечении инфекционных болезней. Основным механизмом действия статинов является умеренное снижение содержания холестерина в клетках печени за счет обратимого подавления ключевого фермента синтеза холестерина – ГМК-КоА редуктазы, что приводит к увеличению количества рецепторов для ЛНП и повышению выведения их из кровотока. В экспериментальных исследованиях было показано, что статины способствуют стабилизации атеросклеротической бляшки за счет уменьшения объема липидного ядра, укрепления оболочки (противовоспалительный эффект) и улучшения локальной функции эндотелия. В 90-х гг. были проведены масштабные клинические исследования, в которых изучалось влияние терапии статинами на различные конечные точки, характеризующие сердечно-сосудистую заболеваемость и смертность, обусловленных атеросклерозом (6). Мета-анализ результатов 4 крупных проспективных исследований показал, что применение статинов у больных с умеренной и выраженной гиперхолестеринемией привело к достоверному снижению сердечно-сосудистой и обшей смертности (таблица 1) (7-10). В большинстве исследований также отслеживалась эффективность статинов у больных СД типа 2 и метаболическими нарушениями (примерно 10-15% общего числа участников). Несмотря на одинаковые исходные уровни холестерина ЛНП, в субгруппе пациентов с СД риск сердечно-сосудистых осложнений снижается достоверно на 7% (от 2 до 10%) больше по сравнению с общей группой больных. Эти данные свидетельствуют о том, что применение статинов у больных СД в сочетании с гиперхолестеринемией приводит к заметному снижению общего риска сердечно-сосудистых осложнений. Более того, эти результаты превосходят таковые по сравнению с общей группой больных (с наличием или без ИБС) без СД. Эксперты Европейского общества кардиологов и Европейской ассоциации по изучению диабета на основании проспективных исследований с твердыми конечными точками статины рекомендуют средством первого ряда в лечении высокого уровня холестерина ЛНП у больных СД и метаболическими нарушениями (класс I, уровень А) (2).
Российский опыт применения статинов у лиц с МС
Одной из актуальных проблем первичной и вторичной профилактики ССЗ является выявление и коррекция нарушений липидного обмена в реальной клинической практике. По сравнению с европейскими странами (по данным исследования REALITY, 58223 пациентов из 10 стран Европы) в России липидснижающая терапия (в частности, статины) назначаются в 5-6 раз реже. В 2006 г. были представлены результаты двух российских исследований (MCC – Московское исследование по статинам и ОСКАР – Эпидемиология и особенности терапии пациентов высокого риска в реальной клинической практике), которые дали представление об адекватности терапии гиперлипидемии в учреждениях первичного здравоохранения. В частности, в исследовании ОСКАР, состоявшего из 2 этапов, было показано, что в клинической практике только 5,3% больных среди пациентов, имеющих факторы риска ССЗ, получают гиполипидемическую терапию статинами, причем только 4,3% достигают целевых уровней липидов. Во второй части программы ОСКАР всем 7098 пациентам рекомендована статинотерапия: большинство пациентов принимали симвастатин (Вазилип, 20 мг в сутки), 20% пациентам был рекомендован аторвастатин (Аторис, 10 мг в сутки). Через 8 недель терапии удалось достичь снижения уровня холестерина на 23%, при этом целевые уровни холестерина (
В двух крупных исследованиях, посвященных первичной профилактике ССЗ (ASCOT-LLA, n = 2532 и CARDS, n = 2838), показано, что терапия с применением аторвастатина в дозе 10 мг на протяжении не менее 3 лет способствует снижению кумулятивного показателя сердечно-сосудистых событий на 36 и 37% соответственно.
Недавно опубликованы результаты клинического исследования А.Л. Хохлова и соавт., посвященного изучению эффективности применения аторвастатина у лиц с дислипидемией и МС. В исследование были включены 40 пациентов в среднем возрасте 54,4 ± 5,0 лет с МС (АГ I-II ст., абдоминальное ожирение, СД типа 2 и дислипидемия). Исходно пациенты имели умеренную гиперхолестеринемию (7,5 ± 1,1 ммоль/л) и мягкую гипертриглицеридемию (2,4 ± 0,9 ммоль/л), при этом коэффициент атерогенности составил 6,1 ± 1,2. На фоне терапии с применением аторвастатина (Аторис, 10 мг в сутки) продолжительностью 5 месяцев общий холестерин снизился на 32%, холестерин ЛНП на 44%, триглицериды на 22,5%, а холестерин ЛВП увеличился на 15%. На фоне терапии целевые уровни общего холестерина достигнуты у 20%, ХС ЛНП у 25% и триглицериды у 55% пациентов с МС. Наряду с этим начальные дозы аторвастатина способствуют снижению уровня гликированного гемоглобина на 1,1%. По данным исследования UKPDS, снижение HbA1с на 1% сопровождается снижением риска ССЗ на 25%. В результатах исследования представлены данные о динамике уровня С-реактивного белка – маркера хронического воспаления. Так, высоко чувствительный С-реактивный белок снизился на 37% (12). Плеотропные эффекты аторвастатина доказаны в крупном российском исследовании ФАРВАТЕР. В частности, применение Аторис 10-20 мг у лиц с документированными ИБС и гиперлипидемией на протяжении 24 недель способствовало снижению С-реактивного белка на 20%, улучшение эндотелий-зависимой вазодилатации на 52%, увеличению растяжимости на 45% и уменьшение жесткости сосудистой стенки на 25% (13).
В целом применение аторвастатина у лиц с МС и ИБС, стенокардией напряжения приводит к снижению частоты ангинозных приступов (1,95 ± 1,76 до исследования и 0,8 ± 0,7 после лечения, p
Таким образом, включение аторвастатина в среднесуточной дозе в стандартную терапию пациентов с МС снижает уровень аторогенных частиц, снижает коэффициент атерогенности, а также достоверно уменьшает уровни гликированного гемоглобина и высоко чувствительного С-реактивного белка, что способствует снижению суммарного показателя сердечно-сосудистого риска.
Заключение
Таким образом, атерогенная дислипидемия является важным фактором развития сердечно-сосудистых осложнений у больных с метаболическими нарушениями.
Данные доказательной медицины убедительно показывают, что статины являются препаратами первого ряда для первичной и вторичной профилактики ССЗ. У больных с СД и ССЗ статины назначают независимо от исходного уровня холестерина ЛНП. У взрослых больных с СД и метаболическими нарушениями статины применяются, если уровень холестерина ЛНП превышает 3,5 ммоль/л.
В рекомендациях Европейского общества кардиологов целевые уровни липидов при первичной профилактике у больных с метаболическими нарушениями и СД соответствуют таковым у больных с ССЗ: общий холестерин 1 ммоль/л у мужчин и > 1,2 ммоль/л у женщин.
В некоторых случаях для снижения уровня холестерина не ЛВП требуется применение высоких доз статинов или комбинированная терапия с использованием эзетимиба, никотиновой кислоты или фибратов.
Источник
