Лечение болевого синдрома с позиции эффективности и безопасности
В статье дается анализ нестероидных противовоспалительных препаратов с позиций безопасности и эффективности. А
вторы рассматривают обоснованность выбора того или иного ингибитора ЦОГ в разных клинических ситуациях: при лечении пациентов, получающих низкие дозы аспирина с целью кардиопротекции, больных с высоким риском эрозивно-язвенного поражения ЖКТ, пациентов с переломом конечностей или в случае оперативного вмешательства у лиц, принимающих алкоголь.
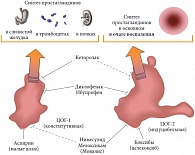
Рис. 1. Спектр эффектов НПВС определяется их способностью блокировать различные циклооксигеназы (ЦОГ)
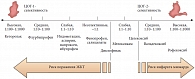
Рис. 3. Побочное действие ингибиторов ЦОГ-2 на сердечно-сосудистую систему (данные исследования VIGOR)

Рис. 2. Зависимость побочных эффектов НПВС от силы блокирования ЦОГ первого и второго типов
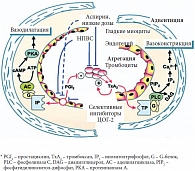
Рис. 4. Предполагаемые механизмы влияния НПВС, аспирина и селективных ингибиторов ЦОГ-2 на гемостаз и сосудистую стенку*
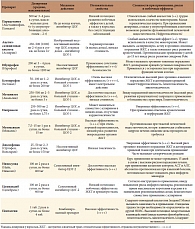
Таблица 1. Сравнительная характеристика наиболее часто применяемых в России неопиоидных анальгетиков
Сегодня, как и тысячи лет назад, большинство пациентов рассматривают нашу работу через призму облегчения боли. Именно боль или ожидание боли приводят пациента к хирургу, травматологу-ортопеду, ревматологу, стоматологу. Обычно врача в первую очередь интересует прогноз. При этом далеко не всегда лечебное пособие, улучшающее прогноз заболевания, параллельно приводит к быстрому повышению качества жизни, и задача по контролю болевого синдрома решается с помощью назначения анальгетиков.
Для хирурга, выполняющего сложную радикальную операцию, ревматолога, проводящего высокодозовую базисную терапию, и стоматолога, принявшего решение сохранить альвеолярный нерв, задача подбора анальгетической терапии естественным образом уходит на второй план, что нередко приводит к назначению одного из «самых сильных» анальгетиков, известных врачу. Проведение длительной терапии нестероидными противовоспалительными средствами (НПВС) – задача не менее сложная: риск развития побочных эффектов напрямую зависит от продолжительности лечения, и многие доктора имеют «любимые» препараты, которые продолжают назначаться, несмотря на новые свидетельства об их небезопасности. В настоящем обзоре мы рассмотрим аспекты лечения НПВС, в том числе в сложных клинических ситуациях, с точки зрения тонкого баланса эффективности и безопасности, основываясь на результатах последних исследований.
Фармакология НПВС: ключи к выбору оптимального препарата
Анальгетическое действие НПВС определяется их способностью ингибировать циклооксигеназы (ЦОГ) – ключевые ферменты синтеза простагландинов, обладающих мощными провоспалительными и гипералгезическими свойствами. ЦОГ-1 участвует в поддержании гомеостаза в различных органах и тканях; катализируя продукцию простациклина, она оказывается ответственной за защиту слизистой желудка, регуляцию почечного кровотока и эндотелиальную функцию (рис. 1). Продуцируемая в очаге воспаления ЦОГ-2 вызывает взрывную продукцию простагландина Е, что ведет к активации ноцицепторов и появлению боли. Исключая парацетамол, механизм действия которого до сих пор не вполне ясен, все НПВС можно разделить на три группы: ингибиторы ЦОГ-1, ингибиторы ЦОГ-2 и неселективные препараты.
Аспирин, применяемый в малых дозах, – селективный и необратимый ингибитор ЦОГ-1 – широко используется в кардиологической практике в качестве антиагреганта. Важно отметить, что аспирин подавляет образование не только проагрегантного тромбоксана, но и антиагрегантного простациклина, при этом его дезагрегантное действие определяется тем, что пулы ингибированной аспирином ЦОГ-1 эндотелиоцитов восстанавливаются посредством синтеза новых молекул этого фермента, в то время как в лишенных ядра тромбоцитах ее ресинтез оказывается невозможным [1].
Параллельное ингибирование ЦОГ-1 в слизистой органов желудочно-кишечного тракта служит непосредственной причиной диспепсии, боли в эпигастрии (до 20–30% пациентов), желудочнокишечных кровотечений (2–8%), а также поражения кишки. Учитывая системное действие аспирина, попытки использовать кишечнорастворимую оболочку, скорее, привели к росту распространенности резистентности к аспирину [2], чем к снижению числа побочных эффектов [3]. По той же причине не выдерживает критики и такой подход, как совместное использование аспирина с гидроксидом магния. Авторы данной работы используют в своей практике кишечнорастворимый аспирин, в первую очередь, с целью повышения приверженности к лечению.
Немаловажно, что тяжесть побочных эффектов на слизистой желудка, по всей видимости, напрямую связана с силой ингибирования ЦОГ-1 (рис. 2) [4]. Практикующим врачам хорошо известно, что в связи с риском развития гастропатии и желудочнокишечного кровотечения применение наиболее сильных ингибиторов ЦОГ-1 кеторолака и кетопрофена затруднено даже при параллельном назначении антисекреторных препаратов, особенно при необходимости парентерального введения этих средств в течение нескольких дней.
Нежелательные реакции, опосредуемые через ЦОГ-1, не ограничиваются слизистой органов ЖКТ. Хорошо известно, что применение аспирина может приводить к бронхообструкции1. Снижение продукции простагландина Е2 и простациклина в почках может приводить к ухудшению почечного кровотока и, соответственно, к ишемии и снижению скорости клубочковой фильтрации. Наконец, длительное применение НПВС (например, индометацина) способно ускорять дегенерацию хрящевой ткани суставных поверхностей2 [5], что впоследствии сильно затрудняет контроль болевого синдрома у пациентов с ревматоидным артритом и остеоартрозом.
Высокоселективные ингибиторы ЦОГ-2, действие которых ограничивается очагом воспаления, разрабатывались с целью решения проблемы негативного влияния НПВС на ЖКТ. Однако крупномасштабные рандомизированные исследования селективных НПВС зафиксировали развитие кардиоваскулярных осложнений при приеме этих препаратов [6].
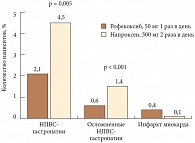
Впервые повышение сердечнососудистых осложнений на фоне приема ингибиторов ЦОГ-2 было отмечено в исследовании VIGOR (Vioxx Gastrointestinal Outcomes Research) (n = 8076), изучавшем рофекоксиб. Данное исследование задумывалось, для того чтобы доказать меньшую токсичность для ЖКТ ингибиторов ЦОГ-2 в сравнении с неселективными НПВС [7]. В то время как частота гастроэнтерологических осложнений на фоне рофекоксиба статистически достоверно снижалась более чем на 50%, в группе принимавших его больных отмечался четырехкратный рост частоты развития инфаркта миокарда (ИМ) в сравнении с группой напроксена (рис. 3) [7]. По всей видимости, такие результаты стали возможны благодаря кардиопротективному эффекту использовавшегося в контрольной группе напроксена, который обладает слабыми антиагрегантными свойствами [8].
Значительный и статистически достоверный рост риска инфаркта миокарда и инсульта отмечался и в исследованиях с другими селективными ингибиторами ЦОГ-2 – вальдекоксибом, парекоксибом, целекоксибом и люмиракоксибом, что резко ограничило применение по всему миру препаратов класса коксибов [6]. При этом есть основания полагать, что опасность в отношении развития сердечно-сосудистых
осложнений напрямую зависит от силы ингибирования ЦОГ-2 (или отношения активности ЦОГ-2/ЦОГ-1) (рис. 2) [4]: вальдекоксиб и рофекоксиб отозваны с рынка, целекоксиб (Целебрекс) и эторикоксиб (Аркоксиа) имеют очень ограниченное применение, а более мягкий ингибитор ЦОГ-2 мелоксикам, по всей видимости, не приводит к повышению риска инфаркта миокарда.
Эти данные имеют четкое теоретическое обоснование. Простациклин (простагландин I2) – преобладающий продукт деятельности циклооксигеназы эндотелия – ингибирует агрегацию тромбоцитов и опосредует вазодилатацию. Основным «поставщиком» простациклина является именно ЦОГ-2. Сердечно-сосудистые эффекты простациклина противоположны действию тромбоксана А2, главного продукта тромбоцитарной ЦОГ-1, который индуцирует их агрегацию, а также вазоконстрикцию.
Применение высокоселективных ингибиторов ЦОГ-2 ведет к ингибированию синтеза простациклина при сохраненном или увеличенном синтезе тромбоксана А2 (рис. 4) [9]. По сути, эти препараты представляют собой «антиаспирин», и принимающие их больные могут быть предрасположены к «взрывному» тромбообразованию в ответ на повреждение эндотелия или разрыв фиброзной покрышки атеросклеротической бляшки. При этом чем выше собственный сердечно-сосудистый риск пациента, тем выше вероятность, что данный механизм реализуется в форме сердечнососудистой катастрофы [1, 4, 6].
Тактика назначения НПВС в клинической практике
Как грамотно подобрать НПВС для вашего пациента с учетом того, что селективные ингибиторы ЦОГ-2 опасны в отношении развития инфаркта миокарда и инсульта, а «жесткие» ингибиторы ЦОГ-1 способны вызвать язву желудка или кровотечение? На наш взгляд, единственным выходом служит aurea mediocritas, то есть назначение НПВС из «светлого» промежутка на рисунке 2, с наиболее благоприятным соотношением риск/польза.
В этом ключе более подробного рассмотрения требуют имеющиеся на российском рынке нимесулид (Нимесил, Найз, Нимулид) и мелоксикам (Мовалис). Мелоксикам ингибирует ЦОГ-2 в три раза сильнее ЦОГ-1, а нимесулид – в 12 раз сильнее [10], что обусловливает низкий риск возникновения побочных эффектов как в отношении слизистой желудка, так и в отношении сердца (в особенности для более слабого ингибитора ЦОГ-2 мелоксикама).
Эффективность этих лекарственных препаратов достаточно высокая, что позволяет использовать их в качестве средств монотерапии при остеоартрите и ревматоидном артрите, а также для купирования болевого синдрома в послеоперационном периоде, в ортопедической и стоматологической практике. В прямых сравнительных исследованиях эти лекарственные препараты не уступают кетопрофену и напроксену [11]. Мовалис несколько более удобен в использовании ввиду того, что может применяться один раз в день.
В единственном на сегодняшний день прямом сравнительном рандомизированном исследовании, изучавшем нимесулид (100 мг/сут) и мелоксикам (15 мг/сут) у пациентов, перенесших экстракцию третьего моляра, не было обнаружено разницы в анальгетической эффективности этих препаратов. Нимесулид был несколько более эффективен в отношении устранения отечности и тризма [12]. Основным фактором, сильно ограничивающим сферу применения нимесулида (Нимесил, Найз), служит резко выраженная гепатотоксичность. Европейское медицинское агентство (EMEA) в своем постановлении от 21 сентября 2007 г. ограничило применение нимесулид-содержащих препаратов максимальным периодом в 15 дней и отозвало все упаковки, содержащие более 30 доз препарата [14].
Другими НПВС, опасными в отношении развития поражения печени, являются сулиндак (фатальное холестатическое поражение печени), ибупрофен, аспирин (синдром Рейе у детей), диклофенак (6 случаев гепатотоксичности на 100 тыс.) [13]. Применение парацетамола в США приводит к развитию 1600 эпизодов острой печеночной недостаточности в год, что составляет 41% всех случаев гепатотоксичности [15]. Здесь следует отметить, что парацетамол наиболее опасен при применении у лиц с алкоголизмом, ввиду высокой активности системы цитохрома Р450 и нуклеофильных протеинов гепатоцитов, которые и приводят к образованию токсичных метаболитов, в то же время при применении у детей препарат практически безопасен благодаря преимущественному метаболизму путем глюкуронирования, не приводящему к образованию токсических метаболитов.
Терапия НПВС в сложныхклинических ситуациях
Сильные и слабые стороны, а также «рабочие» дозировки наиболее широко применяемых в нашей стране НПВС приведены в таблице 1. При составлении комментариев учитывались важные для практикующих врачей аспекты. Ниже мы рассмотрим проблему рационального выбора НПВС, возникающую в сложных, но типичных для современной клинической практики ситуациях.
Необходимость применения НПВС у пациентов, получающих низкие дозы аспирина с целью кардиопротекции Сложность комбинированной терапии в данном случае определяется, с одной стороны, ростом риска кровотечений и эрозивноязвенных поражений органов ЖКТ, а с другой – снижением эффективности кардиопротективного эффекта аспирина [16]. Следует учитывать, что НПВС в высоких дозах в комбинации с аспирином могут повышать риск осложнений на ЖКТ до 13,3 раз [17]. В практическом ключе возможно предпринять следующие шаги.
- Обсудить с кардиологом целесообразность применения аспирина или возможность прекращения приема аспирина на время назначения НПВП. Здесь важно подчеркнуть: аспирин может быть назначен как по жизненным показаниям (острый коронарный синдром, инсульт или инфаркт миокарда в анамнезе), так и в рамках первичной профилактики (например, у больных с артериальной гипертензией без стенокардии). В последнем случае доказательная база в отношении эффективности профилактического применения аспирина достаточно слабая [18].
- Проводить терапию «под прикрытием» ингибитора протонной помпы (ИПП) или блокатора Н2-гистаминовых рецепторов. Эта стратегия применяется достаточно часто, однако следует помнить о том, что ИПП также не лишены побочных эффектов. Их применение может вызывать зависимость, а также приводить к росту риска перелома шейки бедренной кости [19].
- Рассмотреть вопрос использования НПВС совместно с мизопростолом. Здесь нужно отметить, что, во-первых, эффективность мизопростола может быть недостаточной для профилактики поражения ЖКТ и, вовторых, мизопростол сам может служить причиной появления боли в животе, тошноты, рвоты и гинекологических побочных эффектов.
Наконец, следует выбрать НПВС с наименьшим потенциалом влияния на ЖКТ. Наиболее подходящим в этом ключе представляется мелоксикам (Мовалис) [20]. Можно также использовать напроксен, диклофенак или парацетамол.
Необоснованные назначения
- «Переключение» с аспирина на клопидогрел сильно удорожает стоимость лечения, но навряд ли связано со снижением риска тяжелых побочных эффектов на ЖКТ [21].
- Снижение дозы аспирина до 50 мг (при использовании в дозировках менее 81 мг нет доказательств кардиопротективного эффекта).
- Применение кишечнорастворимых форм аспирина и кардиомагнила должно рассматриваться с точки зрения психологического комфорта, но не профилактики НПВС-ассоциированной гастропатии.
- Препараты из группы коксибов (Целебрекс, Аркоксиа) применять в данном случае не представляется возможным ввиду повышения риска инсульта, инфаркта миокарда и нивелирования кардиопротективных свойств аспирина [6].
Лечение пациентов с высоким риском эрозивно-язвенного поражения ЖКТ
Среди факторов, повышающих риск развития НПВС-гастропатии, можно выделить следующие [1, 6]:
- возраст > 65 лет (риск в 4 раза выше);
- наличие анамнеза, отягощенного по язвенной болезни (риск повышается в 14–17 раз);
- продолжительность приема НПВП;
- высокая доза и частый режим приема НПВС;
- одновременное лечение несколькими НПВП;
- прием оральных глюкокортикостероидов, антикоагулянтов;
- инфекция Helicobacter pylori (данные противоречивы).
В случае очень низкого риска сердечно-сосудистых осложнений и короткого курса приема возможно использовать высокоселективный ингибитор ЦОГ-2 целекоксиб. При планировании более длительного курса терапии, при необходимости парентерального введения препарата, а также с учетом высокой распространенности болезней сердца в нашей стране, следует применять мелоксикам (Мовалис). Риск развития НПВС-ассоциированной гастропатии возрастает в ряду: мелоксикам > парацетамол > диклофенак > напроксен > ибупрофен > кеторолак и кетопрофен.
Возможно проведение эрадикационной терапии и совместное назначение с антисекреторными препаратами. Несмотря на то что язвы на фоне приема НПВС часто бывают безболезненными, важен клинический контроль состояния органов ЖКТ. У наиболее тревожных пациентов оправдано проведение контрольной эзофагогастродуоденоскопии и анализа кала на скрытую кровь.
Необоснованные назначения
- Мелоксикам следует предпочесть пироксикаму ввиду наличия у пироксикама влияния на слизистую желудка, что было показано в прямом сравнительном исследовании [22]. Применение мелоксикама не было связано с изменением продукции простагландинов в слизистой оболочке желудка.
- За исключением мелоксикама, парентерально вводимые НПВС (особенно кетопрофен и кеторолак) в сравнении с таблетированными формами не только не снижают, но могут дополнительно повышать риск развития НПВС-ассоциированной гастропатии.
Перелом конечности или оперативные вмешательства у лиц, принимающих алкоголь
В данном случае осторожность должна быть продиктована возможным сочетанным поражением печени, повышенным риском развития кровотечений, а также ожидаемо низкой приверженностью к лечению. Препаратами выбора в данном случае могут быть мелоксикам и напроксен (следует использовать с осторожностью ввиду антиагрегантного действия). Можно использовать ибупрофен или диклофенак, но на фоне их приема описаны случаи гепатотоксичности, которая может «проявиться» у пациентов, злоупотребляющих алкоголем.
Необоснованные назначения
- Применение парацетамола ограничено в связи с ростом риска гепатотоксичности у лиц, принимающих алкоголь. Суточная доза не должна превышать 1,5–2 г.
- Использование нимесулида нежелательно ввиду высокой вероятности развития печеночной недостаточности.
Заключение
При выборе НПВС следует ориентироваться на соотношение эффективности и безопасности терапии, принимая во внимание как побочные эффекты на органы ЖКТ и печень, так и риск сердечно-сосудистых катастроф. При обилии на рынке самых разнообразных НПВС для применения в широкой клинической практике подходят далеко не все препараты, что требует от врача исключительной внимательности при выборе НПВС, особенно при лечении сложных пациентов.
Источник
В статье дается анализ нестероидных противовоспалительных препаратов с позиций безопасности и эффективности. А
вторы рассматривают обоснованность выбора того или иного ингибитора ЦОГ в разных клинических ситуациях: при лечении пациентов, получающих низкие дозы аспирина с целью кардиопротекции, больных с высоким риском эрозивно-язвенного поражения ЖКТ, пациентов с переломом конечностей или в случае оперативного вмешательства у лиц, принимающих алкоголь.

Рис. 1. Спектр эффектов НПВС определяется их способностью блокировать различные циклооксигеназы (ЦОГ)

Рис. 3. Побочное действие ингибиторов ЦОГ-2 на сердечно-сосудистую систему (данные исследования VIGOR)

Рис. 2. Зависимость побочных эффектов НПВС от силы блокирования ЦОГ первого и второго типов

Рис. 4. Предполагаемые механизмы влияния НПВС, аспирина и селективных ингибиторов ЦОГ-2 на гемостаз и сосудистую стенку*

Таблица 1. Сравнительная характеристика наиболее часто применяемых в России неопиоидных анальгетиков
Сегодня, как и тысячи лет назад, большинство пациентов рассматривают нашу работу через призму облегчения боли. Именно боль или ожидание боли приводят пациента к хирургу, травматологу-ортопеду, ревматологу, стоматологу. Обычно врача в первую очередь интересует прогноз. При этом далеко не всегда лечебное пособие, улучшающее прогноз заболевания, параллельно приводит к быстрому повышению качества жизни, и задача по контролю болевого синдрома решается с помощью назначения анальгетиков.
Для хирурга, выполняющего сложную радикальную операцию, ревматолога, проводящего высокодозовую базисную терапию, и стоматолога, принявшего решение сохранить альвеолярный нерв, задача подбора анальгетической терапии естественным образом уходит на второй план, что нередко приводит к назначению одного из «самых сильных» анальгетиков, известных врачу. Проведение длительной терапии нестероидными противовоспалительными средствами (НПВС) – задача не менее сложная: риск развития побочных эффектов напрямую зависит от продолжительности лечения, и многие доктора имеют «любимые» препараты, которые продолжают назначаться, несмотря на новые свидетельства об их небезопасности. В настоящем обзоре мы рассмотрим аспекты лечения НПВС, в том числе в сложных клинических ситуациях, с точки зрения тонкого баланса эффективности и безопасности, основываясь на результатах последних исследований.
Фармакология НПВС: ключи к выбору оптимального препарата
Анальгетическое действие НПВС определяется их способностью ингибировать циклооксигеназы (ЦОГ) – ключевые ферменты синтеза простагландинов, обладающих мощными провоспалительными и гипералгезическими свойствами. ЦОГ-1 участвует в поддержании гомеостаза в различных органах и тканях; катализируя продукцию простациклина, она оказывается ответственной за защиту слизистой желудка, регуляцию почечного кровотока и эндотелиальную функцию (рис. 1). Продуцируемая в очаге воспаления ЦОГ-2 вызывает взрывную продукцию простагландина Е, что ведет к активации ноцицепторов и появлению боли. Исключая парацетамол, механизм действия которого до сих пор не вполне ясен, все НПВС можно разделить на три группы: ингибиторы ЦОГ-1, ингибиторы ЦОГ-2 и неселективные препараты.
Аспирин, применяемый в малых дозах, – селективный и необратимый ингибитор ЦОГ-1 – широко используется в кардиологической практике в качестве антиагреганта. Важно отметить, что аспирин подавляет образование не только проагрегантного тромбоксана, но и антиагрегантного простациклина, при этом его дезагрегантное действие определяется тем, что пулы ингибированной аспирином ЦОГ-1 эндотелиоцитов восстанавливаются посредством синтеза новых молекул этого фермента, в то время как в лишенных ядра тромбоцитах ее ресинтез оказывается невозможным [1].
Параллельное ингибирование ЦОГ-1 в слизистой органов желудочно-кишечного тракта служит непосредственной причиной диспепсии, боли в эпигастрии (до 20–30% пациентов), желудочнокишечных кровотечений (2–8%), а также поражения кишки. Учитывая системное действие аспирина, попытки использовать кишечнорастворимую оболочку, скорее, привели к росту распространенности резистентности к аспирину [2], чем к снижению числа побочных эффектов [3]. По той же причине не выдерживает критики и такой подход, как совместное использование аспирина с гидроксидом магния. Авторы данной работы используют в своей практике кишечнорастворимый аспирин, в первую очередь, с целью повышения приверженности к лечению.
Немаловажно, что тяжесть побочных эффектов на слизистой желудка, по всей видимости, напрямую связана с силой ингибирования ЦОГ-1 (рис. 2) [4]. Практикующим врачам хорошо известно, что в связи с риском развития гастропатии и желудочнокишечного кровотечения применение наиболее сильных ингибиторов ЦОГ-1 кеторолака и кетопрофена затруднено даже при параллельном назначении антисекреторных препаратов, особенно при необходимости парентерального введения этих средств в течение нескольких дней.
Нежелательные реакции, опосредуемые через ЦОГ-1, не ограничиваются слизистой органов ЖКТ. Хорошо известно, что применение аспирина может приводить к бронхообструкции1. Снижение продукции простагландина Е2 и простациклина в почках может приводить к ухудшению почечного кровотока и, соответственно, к ишемии и снижению скорости клубочковой фильтрации. Наконец, длительное применение НПВС (например, индометацина) способно ускорять дегенерацию хрящевой ткани суставных поверхностей2 [5], что впоследствии сильно затрудняет контроль болевого синдрома у пациентов с ревматоидным артритом и остеоартрозом.
Высокоселективные ингибиторы ЦОГ-2, действие которых ограничивается очагом воспаления, разрабатывались с целью решения проблемы негативного влияния НПВС на ЖКТ. Однако крупномасштабные рандомизированные исследования селективных НПВС зафиксировали развитие кардиоваскулярных осложнений при приеме этих препаратов [6].
Впервые повышение сердечнососудистых осложнений на фоне приема ингибиторов ЦОГ-2 было отмечено в исследовании VIGOR (Vioxx Gastrointestinal Outcomes Research) (n = 8076), изучавшем рофекоксиб. Данное исследование задумывалось, для того чтобы доказать меньшую токсичность для ЖКТ ингибиторов ЦОГ-2 в сравнении с неселективными НПВС [7]. В то время как частота гастроэнтерологических осложнений на фоне рофекоксиба статистически достоверно снижалась более чем на 50%, в группе принимавших его больных отмечался четырехкратный рост частоты развития инфаркта миокарда (ИМ) в сравнении с группой напроксена (рис. 3) [7]. По всей видимости, такие результаты стали возможны благодаря кардиопротективному эффекту использовавшегося в контрольной группе напроксена, который обладает слабыми антиагрегантными свойствами [8].
Значительный и статистически достоверный рост риска инфаркта миокарда и инсульта отмечался и в исследованиях с другими селективными ингибиторами ЦОГ-2 – вальдекоксибом, парекоксибом, целекоксибом и люмиракоксибом, что резко ограничило применение по всему миру препаратов класса коксибов [6]. При этом есть основания полагать, что опасность в отношении развития сердечно-сосудистых
осложнений напрямую зависит от силы ингибирования ЦОГ-2 (или отношения активности ЦОГ-2/ЦОГ-1) (рис. 2) [4]: вальдекоксиб и рофекоксиб отозваны с рынка, целекоксиб (Целебрекс) и эторикоксиб (Аркоксиа) имеют очень ограниченное применение, а более мягкий ингибитор ЦОГ-2 мелоксикам, по всей видимости, не приводит к повышению риска инфаркта миокарда.
Эти данные имеют четкое теоретическое обоснование. Простациклин (простагландин I2) – преобладающий продукт деятельности циклооксигеназы эндотелия – ингибирует агрегацию тромбоцитов и опосредует вазодилатацию. Основным «поставщиком» простациклина является именно ЦОГ-2. Сердечно-сосудистые эффекты простациклина противоположны действию тромбоксана А2, главного продукта тромбоцитарной ЦОГ-1, который индуцирует их агрегацию, а также вазоконстрикцию.
Применение высокоселективных ингибиторов ЦОГ-2 ведет к ингибированию синтеза простациклина при сохраненном или увеличенном синтезе тромбоксана А2 (рис. 4) [9]. По сути, эти препараты представляют собой «антиаспирин», и принимающие их больные могут быть предрасположены к «взрывному» тромбообразованию в ответ на повреждение эндотелия или разрыв фиброзной покрышки атеросклеротической бляшки. При этом чем выше собственный сердечно-сосудистый риск пациента, тем выше вероятность, что данный механизм реализуется в форме сердечнососудистой катастрофы [1, 4, 6].
Тактика назначения НПВС в клинической практике
Как грамотно подобрать НПВС для вашего пациента с учетом того, что селективные ингибиторы ЦОГ-2 опасны в отношении развития инфаркта миокарда и инсульта, а «жесткие» ингибиторы ЦОГ-1 способны вызвать язву желудка или кровотечение? На наш взгляд, единственным выходом служит aurea mediocritas, то есть назначение НПВС из «светлого» промежутка на рисунке 2, с наиболее благоприятным соотношением риск/польза.
В этом ключе более подробного рассмотрения требуют имеющиеся на российском рынке нимесулид (Нимесил, Найз, Нимулид) и мелоксикам (Мовалис). Мелоксикам ингибирует ЦОГ-2 в три раза сильнее ЦОГ-1, а нимесулид – в 12 раз сильнее [10], что обусловливает низкий риск возникновения побочных эффектов как в отношении слизистой желудка, так и в отношении сердца (в особенности для более слабого ингибитора ЦОГ-2 мелоксикама).
Эффективность этих лекарственных препаратов достаточно высокая, что позволяет использовать их в качестве средств монотерапии при остеоартрите и ревматоидном артрите, а также для купирования болевого синдрома в послеоперационном периоде, в ортопедической и стоматологической практике. В прямых сравнительных исследованиях эти лекарственные препараты не уступают кетопрофену и напроксену [11]. Мовалис несколько более удобен в использовании ввиду того, что может применяться один раз в день.
В единственном на сегодняшний день прямом сравнительном рандомизированном исследовании, изучавшем нимесулид (100 мг/сут) и мелоксикам (15 мг/сут) у пациентов, перенесших экстракцию третьего моляра, не было обнаружено разницы в анальгетической эффективности этих препаратов. Нимесулид был несколько более эффективен в отношении устранения отечности и тризма [12]. Основным фактором, сильно ограничивающим сферу применения нимесулида (Нимесил, Найз), служит резко выраженная гепатотоксичность. Европейское медицинское агентство (EMEA) в своем постановлении от 21 сентября 2007 г. ограничило применение нимесулид-содержащих препаратов максимальным периодом в 15 дней и отозвало все упаковки, содержащие более 30 доз препарата [14].
Другими НПВС, опасными в отношении развития поражения печени, являются сулиндак (фатальное холестатическое поражение печени), ибупрофен, аспирин (синдром Рейе у детей), диклофенак (6 случаев гепатотоксичности на 100 тыс.) [13]. Применение парацетамола в США приводит к развитию 1600 эпизодов острой печеночной недостаточности в год, что составляет 41% всех случаев гепатотоксичности [15]. Здесь следует отметить, что парацетамол наиболее опасен при применении у лиц с алкоголизмом, ввиду высокой активности системы цитохрома Р450 и нуклеофильных протеинов гепатоцитов, которые и приводят к образованию токсичных метаболитов, в то же время при применении у детей препарат практически безопасен благодаря преимущественному метаболизму путем глюкуронирования, не приводящему к образованию токсических метаболитов.
Терапия НПВС в сложныхклинических ситуациях
Сильные и слабые стороны, а также «рабочие» дозировки наиболее широко применяемых в нашей стране НПВС приведены в таблице 1. При составлении комментариев учитывались важные для практикующих врачей аспекты. Ниже мы рассмотрим проблему рационального выбора НПВС, возникающую в сложных, но типичных для современной клинической практики ситуациях.
Необходимость применения НПВС у пациентов, получающих низкие дозы аспирина с целью кардиопротекции Сложность комбинированной терапии в данном случае определяется, с одной стороны, ростом риска кровотечений и эрозивноязвенных поражений органов ЖКТ, а с другой – снижением эффективности кардиопротективного эффекта аспирина [16]. Следует учитывать, что НПВС в высоких дозах в комбинации с аспирином могут повышать риск осложнений на ЖКТ до 13,3 раз [17]. В практическом ключе возможно предпринять следующие шаги.
- Обсудить с кардиологом целесообразность применения аспирина или возможность прекращения приема аспирина на время назначения НПВП. Здесь важно подчеркнуть: аспирин может быть назначен как по жизненным показаниям (острый коронарный синдром, инсульт или инфаркт миокарда в анамнезе), так и в рамках первичной профилактики (например, у больных с артериальной гипертензией без стенокардии). В последнем случае доказательная база в отношении эффективности профилактического применения аспирина достаточно слабая [18].
- Проводить терапию «под прикрытием» ингибитора протонной помпы (ИПП) или блокатора Н2-гистаминовых рецепторов. Эта стратегия применяется достаточно часто, однако следует помнить о том, что ИПП также не лишены побочных эффектов. Их применение может вызывать зависимость, а также приводить к росту риска перелома шейки бедренной кости [19].
- Рассмотреть вопрос использования НПВС совместно с мизопростолом. Здесь нужно отметить, что, во-первых, эффективность мизопростола может быть недостаточной для профилактики поражения ЖКТ и, вовторых, мизопростол сам может служить причиной появления боли в животе, тошноты, рвоты и гинекологических побочных эффектов.
Наконец, следует выбрать НПВС с наименьшим потенциалом влияния на ЖКТ. Наиболее подходящим в этом ключе представляется мелоксикам (Мовалис) [20]. Можно также использовать напроксен, диклофенак или парацетамол.
Необоснованные назначения
- «Переключение» с аспирина на клопидогрел сильно удорожает стоимость лечения, но навряд ли связано со снижением риска тяжелых побочных эффектов на ЖКТ [21].
- Снижение дозы аспирина до 50 мг (при использовании в дозировках менее 81 мг нет доказательств кардиопротективного эффекта).
- Применение кишечнорастворимых форм аспирина и кардиомагнила должно рассматриваться с точки зрения психологического комфорта, но не профилактики НПВС-ассоциированной гастропатии.
- Препараты из группы коксибов (Целебрекс, Аркоксиа) применять в данном случае не представляется возможным ввиду повышения риска инсульта, инфаркта миокарда и нивелирования кардиопротективных свойств аспирина [6].
Лечение пациентов с высоким риском эрозивно-язвенного поражения ЖКТ
Среди факторов, повышающих риск развития НПВС-гастропатии, можно выделить следующие [1, 6]:
- возраст > 65 лет (риск в 4 раза выше);
- наличие анамнеза, отягощенного по язвенной болезни (риск повышается в 14–17 раз);
- продолжительность приема НПВП;
- высокая доза и частый режим приема НПВС;
- одновременное лечение несколькими НПВП;
- прием оральных глюкокортикостероидов, антикоагулянтов;
- инфекция Helicobacter pylori (данные противоречивы).
В случае очень низкого риска сердечно-сосудистых осложнений и короткого курса приема возможно использовать высокоселективный ингибитор ЦОГ-2 целекоксиб. При планировании более длительного курса терапии, при необходимости парентерального введения препарата, а также с учетом высокой распространенности болезней сердца в нашей стране, следует применять мелоксикам (Мовалис). Риск развития НПВС-ассоциированной гастропатии возр
