Лабораторные проявления синдрома некроза миокарда острая фаза
Определение концентрации маркеров повреждения миокарда, используемое для диагностики острого коронарного синдрома (ОКС) и инфаркта миокарда (ИМ).
Синонимы русские
Анализы крови при ОКС, маркеры ОКС.
Синонимы английские
Biomarkers of Acute Coronary Syndrome, ACS; Creatine kinase MB (CK-MB), Troponin I, Myoglobin, AST, ALT.
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Детям в возрасте от 1 до 5 лет не принимать пищу в течение 2-3 часов до исследования.
- Не принимать пищу в течение 12 часов до исследования, можно пить чистую негазированную воду.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Острый коронарный синдром (ОКС) – это совокупность клинических признаков и симптомов, позволяющих подозревать у пациента нестабильную стенокардию или острый инфаркт миокарда (ИМ). Для дифференциальной диагностики ОКС и других заболеваний, которые могут протекать со схожей клинической картиной (например, тромбоэмболия легочной артерии), и для дифференциальной диагностики клинических форм ОКС (нестабильная стенокардия, ИМ с подъемом сегмента ST или без подъема сегмента ST) проводят ряд дополнительных исследований. Лабораторные тесты – неотъемлемая часть диагностического обследования пациента с ОКС и подозрением на ИМ.
Диагностическое обследование при ОКС включает измерение в крови концентрации креатинкиназы MB, тропонина I и миоглобина, а также аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ).
Тропонин I
Тропонины (C, T и I) – группа белков сократительного комплекса миокарда и поперечно-полосатых мышц. Благодаря тому, что существуют характерные исключительно для миокарда изоформы тропонинов T и I (сердечные тропонины Tи I), их используют в качестве маркеров повреждения миокарда.
Тропонины – это самые точные и предпочтительные в настоящий момент маркеры повреждения миокарда. Тропонин I и тропонин T имеют примерно одинаковую чувствительность и специфичность в отношении повреждения миокарда. Эти маркеры часто используются вместе, но могут применяться и по отдельности.
Концентрация сердечных тропонинов при наличии ИМ повышается через 4-10 часов после возникновения симптомов болезни и остается повышенной в течение двух недель после появления симптомов, поэтому эти маркеры могут быть использованы для диагностики недавно перенесенного ИМ.
Чувствительность сердечных тропонинов в отношении ИМ при исследовании в первые 4 часа от возникновения симптомов составляет около 35 %, через 10 часов — 95 %. Поэтому тропонин I измеряют несколько раз – при поступлении, через 6 и 12 часов. Специфичность сердечных тропонинов в отношении ИМ достигает 96 %.
Важно отметить, что специфичность лабораторных маркеров в отношении повреждения миокарда и инфаркта миокарда – это не одно и то же. Так, сердечные тропонины имеют 100 % специфичность в отношении повреждения миокарда, но не инфаркта миокарда. Повышение уровня тропонинов может наблюдаться и при других заболеваниях сердца, например при травме сердца, хронической сердечной недостаточности, миокардите, перикардите, гипертрофии левого желудочка, или при других заболеваниях и состояниях, сопровождающихся повреждением миокарда, например при сепсисе, дыхательной недостаточности, тромбоэмболии легочной артерии, химиотерапии при злокачественном новообразовании или хронической почечной недостаточности.
Следует особо подчеркнуть, что концентрация сердечных тропонинов может оставаться нормальной в течение первых 4-6 часов даже при случившемся инфаркте.
Сердечные тропонины – это не только диагностические, но и прогностические маркеры. Повышение их концентрации связано с повышенным риском смерти от ИМ и его осложнений. Показано, что степень риска находится в прямой зависимости от степени повышения концентрации тропонинов.
Креатинкиназа МВ
Креатинкиназа МВ (CK-MB) представляет собой одну из изоформ фермента креатинкиназы, участвующего в энергетическом обмене клеток. Фермент креатинкиназа состоит из двух субъединиц M (от англ. muscle) и B (от англ. brain). Комбинации этих субъединиц образуют изоформы креатинкиназы CK-BB, CK-MM и CK-MB. Изоформы CK-MM и CK-BB преобладают в мышечной и нервной ткани, а креатинкиназа MB находится практически исключительно в сердечной мышце. Поэтому увеличение концентрации креатинкиназы MB служит в качестве специфичного индикатора повреждения миокарда.
В крови человека, переживающего острый инфаркт миокарда, увеличение концентрации креатинкиназы MB может быть выявлено в течение первых 4-8 часов после возникновения симптомов заболевания. Пик повышения концентрации приходится на 24-48 ч, а нормализация показателя обычно заканчивается к 3 суткам. Быстрая нормализация этого показателя позволяет использовать креатинкиназу MB не только для диагностики первичного ИМ, но и для диагностики рецидивирующего инфаркта. Считается, что пиковая концентрация креатинкиназы MB не отражает объема повреждения миокарда.
Чувствительность креатинкиназы MB в отношении ИМ при однократном исследовании составляет около 35 %, а при повторных исследованиях достигает 95 %. По этой причине исследования концентрации креатинкиназы MB, как правило, повторяют через 6 и 12 часов после поступления в приемный покой. Специфичность теста достигает 80 %. Следует особо подчеркнуть, что концентрация креатинкиназы MB может оставаться нормальной в течение первых 4-8 часов даже при наличии случившегося инфаркта.
Если у пациента обнаруживается повышение уровня тропонина I при нормальном значении креатинкиназы MB, говорят о микроинфаркте или продолжительном незначительном повреждении миокарда. Повышение как креатинкиназы MB, так и тропонина I свидетельствует о наличии острого ИМ.
Как и в случае с сердечными тропонинами, повышение креатинкиназы MB может наблюдаться не только при ИМ, но и при других заболеваниях сердца и некоторых других органов.
Миоглобин
Миоглобин – это низкомолекулярный белок, присутствующий в миокарде и поперечно-полосатой мускулатуре. Повышение концентрации миоглобина может быть обнаружено в первые 2 часа после возникновении некроза миокарда. Таким образом, миоглобин – это самый ранний клинико-лабораторный маркер ИМ. Этот маркер не специфичен для повреждения миокарда, но очень чувствителен. Высокая чувствительность этого маркера означает, что диагноз «ИМ» может быть практически исключен, если концентрация миоглобина, измеренная в первые 4-8 часов от начала симптомов заболевания, находится в пределах нормальных значений. Следует отметить, что концентрация миоглобина быстро снижается.
АСТ и АЛТ
АСТ и АЛТ – это ферменты, катализирующие перенос аминогрупп между аминокислотами (трансаминазы). Они находятся во многих тканях и органах и поэтому не являются специфичными для сердечной мышцы маркерами. Повреждение миокарда сопровождается повышением концентрации АСТ и АЛТ в крови, которое может быть выявлено через 6-12 часов после возникновения некроза миокарда, достигает пика через 24-48 часов и нормализуется к 7 дню болезни.
Изменения концентрации АСТ и АЛТ могут наблюдаться при многих других заболеваниях, в том числе при заболеваниях печени, гемолизе, ишемии почек, селезенки и кишки, а также при применении салицилатов, опиоидных препаратов и варфарина.
В настоящее время АСТ и АЛТ рассматриваются в качестве дополнительных маркеров повреждения миокарда. По своей информативности они значительно уступают сердечным тропонинам и креатинкиназе MB.
При подтверждении диагноза «ИМ» или другой клинической формы ишемической болезни сердца (ИБС) целесообразно провести дополнительное лабораторное обследования для выявления и коррекции факторов риска ИБС, в первую очередь гиперхолестеринемии (липидограмма) и сахарного диабета (глюкоза натощак или гликированный гемоглобин).
Для чего используется исследование?
- Для диагностики острого коронарного синдрома (ОКС) и инфаркта миокарда (ИМ).
Когда назначается исследование?
- При наличии типичных симптомов ОКС: внезапной интенсивной боли в области сердца, связанной с физической нагрузкой или возникшей в покое, иррадиирующей в левую руку, шею, нижнюю челюсть, длящейся более 15 минут и сопровождающейся головокружением, слабостью, одышкой, чувством сердцебиения и беспокойством;
- при выявлении ЭКГ-признаков инфаркта миокарда.
Что означают результаты?
Референсные значения
Для каждого показателя, входящего в состав комплекса:
- [06-003] Аланинаминотрансфераза (АЛТ)
- [06-010] Аспартатаминотрансфераза (АСТ)
- [06-023] Креатинкиназа MB
- [06-076] Тропонин I
- [06-079] Миоглобин
Что может влиять на результат?
- Время, прошедшее с момента возникновения первых симптомов заболевания;
- объем поражения миокарда;
- наличие сопутствующих заболеваний сердца;
- наличие заболеваний скелетной мускулатуры, почек, печени и некоторых других органов;
- прием кардиотоксичных препаратов (доксорубицин, митоксантрон).
Важные замечания
- Повторные исследования рекомендуется выполнять с помощью одних и тех же тест-систем, то есть в одной лаборатории;
- результат комплексного анализа необходимо оценивать с учетом клинических, дополнительных лабораторных и инструментальных данных.
Также рекомендуется
[40-039] Липидограмма
[06-015] Глюкоза в плазме
[06-014] Гликированный гемоглобин (HbA 1c)
Кто назначает исследование?
Кардиолог, терапевт, врач общей практики.
Литература
- Mosleh W, Abdel-Qadir H, Farkouh M. Biomarkers in the emergency workup of chest pain: uses, limitations, and future. Cleve Clin J Med. 2013 Sep;80(9):589-98. Review.
- Achar SA, Kundu S, Norcross WA. Diagnosis of acute coronary syndrome. Am Fam Physician. 2005 Jul 1;72(1):119-26.
- McPhee S.J., Papadakis M. CURRENT Medical Diagnosis and Treatment / S. J. McPhee, M. Papadakis; 49 ed. — McGraw-Hill Medical, 2009.
Источник
Август 22, 2018
Нет комментариев
Некротические повреждения сердечной мышцы, т. е. гибель участков миокарда, бывают связаны или не связаны с нарушением коронарного кровообращения. В зависимости от этого они подразделяются на коронарогеннш и некоронарогенные некрозы.

Коронарогенные (ишемические) некрозы миокарда
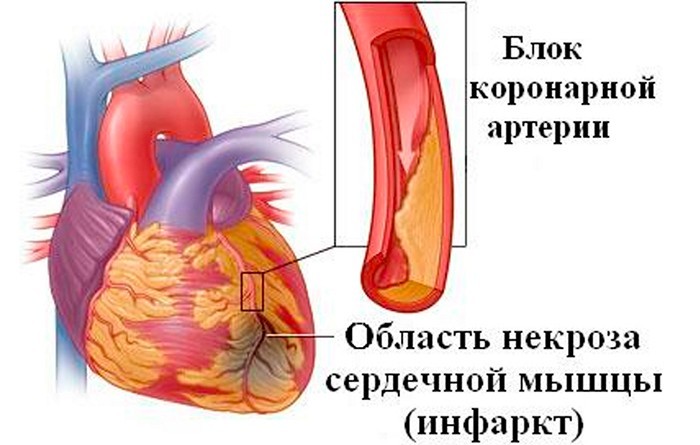
Некроз миокарда, возникающий вследствие ухудшения коронарного кровотока (ишемии), называется инфарктом миокарда.
Некроз инфаркт миокарда
представляет собой одну из острых форм ИБС, при которой доставка к сердцу кислорода и питательных веществ не удовлетворяет потребности сердца в этих веществах.
Этиология
В этиологии инфаркта миокарда играют важную роль атеросклероз коронарных артерий, их тромбоз, спазм и (достаточно редко) эмболия коронарных артерий. К факторам риска инфаркта миокарда можно отнести все те, которые указаны как факторы риска ИБС (см. начало данного раздела). Сочетание двух или трех факторов риска увеличивает вероятность возникновения инфаркта миокарда.
Патогенез
Выделяют следующие последовательно развивающиеся стадии в патогенезе инфаркта миокарда.
1. Выключение дыхательной цепи митохондрий и активация гликолиза как следствие начавшейся ишемии. Накопление недоокисленных продуктов метаболизма (прежде всего молочной кислоты) обусловливает появление боли.
2. Ингибирование основных метаболических путей, подавление гликолиза (из-за слишком большого снижения pH в ткани миокарда) и цикла Кребса, вследствие чего развивается дефицит аденозинтрифосфата. Наблюдается накопление жирных кислот вследствие угнетения их р. окисления, а также нарушение ионного равновесия в кардиомиоцитах
3. Разрушение мембран кардиомиоцитов в результате включения в патогенез инфаркта так называемой липидной триады. В нее входят активация липаз и фосфолипаз, активация свободнорадикального перекисного окисления липидов и детергентное действие на миокард избытка жирных кислот. Все указанные изменения происходят в мембранах сарколеммы, лизосом, саркоплазматического ретикулума и митохондрий и приводят к их повреждению и повышению проницаемости. Следствием этого является выход аутолитических ферментов лизосом в клетки миокарда, а также накопление в них избытка свободного Са++. Избыток Са++ вызывает контрактуру миофибрилл и приводит к дальнейшей активации липаз и фосфолипаз.
4. Заключительная стадия необратимых повреждений кардиомио-цитов и некроз ишемического участка миокарда.
Клинические проявления
Основными клиническими симптомами инфаркта миокарда являются:
1. Локализующаяся за грудиной сильнейшая боль, иррадиирующая в левое плечо, левую руку и межлопаточную область. Эта боль может возникать в покое днем или в ночное время.
В отличие от приступа стенокардии болевой синдром при инфаркте миокарда длится дольше и не купируется повторным приемом нитроглицерина. Следует отметить, что в тех случаях, когда болевой приступ длится более 15 мин, а принимаемые меры неэффективны, необходимо немедленно вызвать бригаду скорой медицинской помощи.
Встречаются и атипичные формы инфаркта миокарда, при которых характерные симптомы, в частности болевой синдром, могут отсутствовать (безболевая форма инфаркта миокарда).
2. Ослабление сократительной способности миокарда вследствие выпадения из акта сокращения поврежденного участка миокарда ведет к уменьшению сердечного выброса. При этом в зоне некроза с помощью эхокардиографии могут выявляться различные нарушения движения стенки поврежденного желудочка: акинезия, гипокинезия, дискинезия (выбухание участка инфаркта в момент систолы). Последнее может свидетельствовать о формировании острой аневризмы сердца-
3. Аритмии. В связи с изменением в зоне инфаркта биоэлектрических свойств кардиомиоцитов возникают нарушения сердечного ритма (вплоть до развития фибрилляции сердца), что приводит к значительным расстройствам системной гемодинамики и усугубляет нарушение контрактильной функции сердца. Источником эктопической активности на ранних стадиях развития инфаркта служит, как правило, окржающая зону некроза так называемая паранекротическая зона.
4. Появление типичных изменений ЭКГ. К ним относятся смещение сегмента ST выше или ниже относительно изоэлектрической линии, появление патологического комплекса QS (свидетельствует о наличии в миокарде очага глубокой ишемии или некроза), а также появление гигантского зубца Т. Он может быть положительным или отрицательным. Если подобный зубец Т появляется в раннем периоде инфаркта миокарда, его трактуют (как и смещение сегмента ST) как проявление острой ишемии миокарда. Если же он появляется на поздних стадиях, его связывают с формированием в миокарде рубцовых изменений.
В зависимости от особенностей изменений ЭКГ различают следующие формы инфаркта миокарда:
• Q-образующий инфаркт, или Q-инфаркт (с формированием патологического глубокого зубца Q, что может свидетельствовать о крупноочаговом трансмуральном инфаркте);
• Q-необразующий инфаркт, или He-Q-инфаркт (сопровождается не появлением зубца Q, а появлением отрицательного зубца Т, что свидетельствует о мелкоочаговом инфаркте миокарда).
5. В крови повышается содержание так называемых маркеров инфаркта миокарда: миокардиальной фракции креатинфосфокиназы, миоглобина, а также тропонина-Т, который имеет на сегодняшний день наиболее важное значение в диагностике инфаркта миокарда.
6. Одно из важных проявлений инфаркта миокарда – ухудшение реологических свойств крови, что способствует тромбообразованию. При инфаркте миокарда венозный тромбоз диагностируется у 10-15 % больных.
7. Кроме описанных выше изменений могут наблюдаться расстройства мозгового кровообращения, нарушения функции желудочно-кишечного тракта. Через несколько часов от начала инфаркта миокарда развивается лейкоцитоз. Весьма характерно для инфаркта появление так называемого симптома перекреста между числом лейкоцитов в крови и СОЭ, когда в конце 1-й недели выраженность лейкоцитоза снижается, а СОЭ увеличивается.
Осложнения
К ранним осложнениям относят острую сердечную недостаточность, кардиогенный шок, отек легких, механические осложнения (разрыв папиллярных мышц, перегородки и стенок миокарда), тампонаду сердца, перикардит, тромбоэмболию легочной артерии, являющуюся одной из наиболее частых причин внезапной смерти.
К поздним осложнениям (возникают через 2-3 нед. и более от начала инфаркта) относят постинфарктный синдром Дресслера, хроническую недостаточность кровообращения, развитие аневризм сердца, тромбоэмболию легочной артерии и повторные инфаркты миокарда. Что касается синдрома Дресслера, то он возникает через 2-6 нед. от начала инфаркта и проявляется перикардитом, плевритом и пневмонией. В его патогенезе играет роль образование аутоантител к деструктивно измененным при инфаркте белкам миокарда — миокардиальным аутоантигенам.
Принципы патогенетической терапии
1. Ликвидация болевого приступа с помощью сильнодействующих анальгетиков и наркотических средств.
2. Использование антиагрегантов и тромболитических препаратов. В качестве доврачебной помощи рекомендуется использовать аспирин.
3. Уменьшение потребности сердца в кислороде, улучшение его доставки и снижение риска возникновения аритмий ф-адреноблокаторы).
Рекомендуется также использовать:
• ингибиторы ангиотензинпревращающего фермента;
• седативные и снотворные препараты;
• противоаритмические средства.
4. Важное значение имеют и хирургические методы лечения, в частности аортокоронарное шунтирование и баллонная ангиопластика со стентированием коронарных артерий.
Некоронарогенные (неишемические) некрозы миокарда
Поражения сердца этого типа возникают как результат нарушения метаболизма в сердечной мышце в связи с действием на сердце избытка электролитов, гормонов, токсических продуктов обмена, кардиальных аутоантител. Различают следующие виды некоронарогенных некрозов миокарда.
Электролитно-стероидные некрозы
Образование данного вида некрозов связано с патогенным действием на миокард избытка вводимых в организм гормонов коры надпочечников (прежде всего минералокортикоидов) в сочетании с солями натрия. Такое воздействие приводит к увеличению проницаемости мембран кардиомиоцитов для натрия и накоплению его в сердце. Развивающийся впоследствии отек и «осмотический взрыв» клеток миокарда сопровождается возникновением очагов некроза.
Катехоламиновые некрозы миокарда
Повреждающее действие избыточных концентраций катехоламинов на сердце объясняется следующими механизмами.
Во-первых, сами катехоламины, и прежде всего адреналин, обладают прямым повреждающим действием на миокард.
Во-вторых, несмотря на то что катехоламины расширяют коронарные сосуды, они в значительно большей степени увеличивают потребность сердца в кислороде, т. к. повышают частоту сердечных сокращений и артериальное давление. Поэтому при прохождении крови по венечным сосудам кислород утилизируется раньше, чем кровь достигнет прекапиллярного отдела микрососудистого русла. Это приводит к тому, что в миокарде появляются участки, получающие кровь, обедненную кислородом.
В-третьих, под влиянием избытка катехоламинов в миокарде происходит активация перекисного окисления липидов, продукты которого повреждают мембраны кардиомиоцитов.
Токсические и воспалительные некрозы миокарда
Данные виды некрозов возникают при интоксикации или поражении миокарда воспалительным процессом. Токсический миокардит может возникать вследствие воздействия некоторых химических соединений и фармакологических препаратов, например кокаина, лекарственных средств, применяемых при лечении злокачественных опухолей. Эти токсические вещества оказывают прямое повреждающее действие на миокард, приводя к развитию необратимой дистрофии и появлению мелкоочаговых некрозов.
Примером воспалительных некрозов миокарда служат различные миокардиты: ревматические и дифтерийные. При любом воспалительном процессе, как и в данном случае, наблюдается альтерация (повреждение) миофибрилл. Развивающийся воспалительный отек также способствует альтерации. Все это ведет к развитию микронекрозов миокарда.
Аутоиммунные некрозы
Одним из примеров аутоиммунных некрозов миокарда служит синдром Дресслера, о котором было сказано выше.
Поврежденные белки при инфаркте миокарда могут стать аутоантигенами, к которым в организме вырабатываются антитела. Повторное развитие некротического процесса обусловливает запуск реакции «антиген-антитело» во многих участках сердечной мышцы, что вызывает множественные микронекрозы.
Загрузка…
Источник
