Код по мкб с91
MKБ 10 или международная классификация всех заболеваний 10 созыва имеет в себе практически все короткие обозначения известных патологий, в том числе и онкологических. Лейкоз коротко по МКБ 10 имеет две точные кодировки:
- С91 — Лимфоидная форма.
- С92 — Миелоидная форма или миелолейкоз.
Но также нужно учитывать и характер заболевания. Для обозначения используют подгруппу, которая пишется после точки.
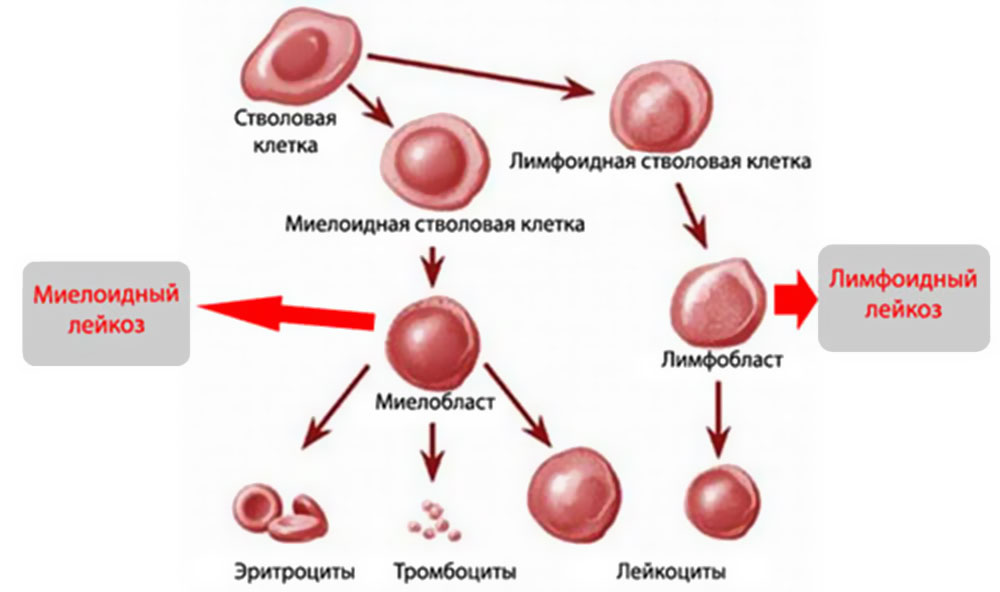
Лимфолейкоз
| Кодировка | Лимфоидный лейкоз |
| C 91.0 | Острый лимфобластный лейкоз при Т или В клеток предшественников. |
| C 91.1 | Лимфоплазматическая форма, Синдром Рихтера. |
| C 91.2 | Подострый лимфоцитарный (в данной время код не используется) |
| C 91.3 | Пролимфоцитарный В-клеточный |
| C 91.4 | Волосатоклеточный и лейкемический ретикулоэндотелиоз |
| C 91.5 | Т-клеточная лимфома или лейкемия взрослых с параметром HTLV-1-ассоциированная. Варианты: Тлеющий, острый, лимфоматоидный, тлеющий. |
| C 91.6 | Пролимфоцитарный T-клеточный |
| C 91.7 | Хронический из больших зернистых лимфоцитов. |
| C 91.8 | Зрелый B-клеточный (Беркитта) |
| C 91.9 | Неутонченная форма. |
Миелолейкоз
Включает в себя гранулоцитарный и миелогенный.
| Коды | Миелоидный лейкоз |
| C 92.0 | Острый миелобластный лейкоз (ОМЛ) с низким показателем дифференцировки, а также форма с созреванием. (AML1/ETO, AML M0, AML M1, AML M2, AML с t (8 ; 21), AML ( без FAB классификации ) БДУ) |
| С 92.1 | Хроническая форма (ХМЛ) [CML], BCR/ABL-положительный. Филадельфийская хромосома (Ph1) положительная. t (9 : 22) (q34 ;q11). С бластным кризом. Исключения: неклассифицированное миелопролиферативное заболевание; атипичный, BCR / ABL-отрицательный; Хронический миеломоноцитарный лейкоз. |
| C 92.2 | Атипичный хронический, BCR/ABL-отрицательный. |
| С 92.3 | Миелоидная саркома в которой новообразование состоит из незрелыз атипичных мелеоилных клеточек. Также в нее входит гранулоцитарная саркома и хлорома. |
| C 92.4 | Острый промиелоцитарный лейкоз [PML] с параметрами: AML M3 и AML M3 с t (15 ; 17). |
| С 92.5 | Острый миеломоноцитарный с параметрами AML M4 и AML M4 Eo с inv (16) or t(16;16) |
| C 92.6 | С 11q23-аномалией и с вариацией MLL хромосомы. |
| С 92.7 | Другие формы. Исключение — гиперэозинофильный синдром или хронический эозинофильный. |
| C 92.8 | С многолинейной дисплазией. |
| С 92.9 | Неутонченные формы. |
Причины
Напомним, что точной причины из-за чего происходит развитие рака крови не известно. Именно поэтому врачам, так сложно бороться с этим недугом и предотвращать его. Но есть ряд факторов, которые могут увеличивать шанс возникновения онкологии красной жидкости.
- Повышенная радиация
- Экология.
- Плохое питание.
- Ожирение.
- Чрезмерное употребление лекарственных средств.
- Лишний вес.
- Курение, алкоголь.
- Вредная работа, связанная с пестицидами и химическими реагентами, которые могут влиять на кроветворную функцию.
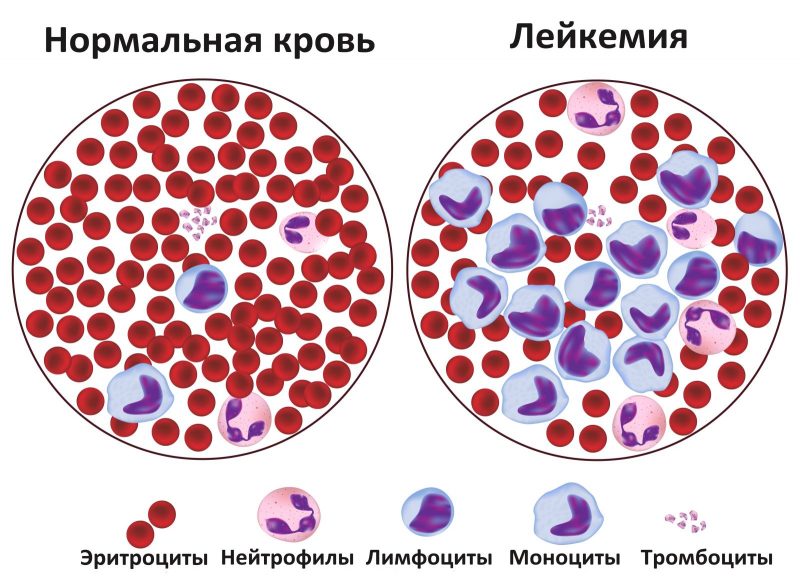
Симптомы и аномалии
- Анемия возникает в результате угнетения эритроцитов из-за чего кислород до здоровых клеток доходит не в полном объеме.
- Сильные и частые головные боли. Начинается с 3 стадии, когда возникает интоксикация из-за злокачественной опухоли. Также может быть результатом запущенной анемии.
- Постоянная простуда и инфекционные и вирусные заболевания с продолжительным периодом. Бывает, когда здоровые лейкоциты заменяются на атипичные. Они не выполняют свою функцию и организм становится менее защищенным.
- Боль в суставах и ломка.
- Слабость, утомляемость, сонливость.
- Систематическая субфебрильная температура без причины.
- Изменение запаха, вкусов.
- Потеря веса и аппетита.
- Долгие кровотечения при снижении количество тромбоцитов в крови.
- Болезненность воспаление лимфатических узлов по всему телу.
Диагностика
Точный диагноз можно поставить, только после проведения тщательного обследования и сдачи определенного перечня анализов. Чаще всего людей ловят на аномальных показателях при биохимическом и общем анализе крови.
Для более точного диагноза делают пункцию костного мозга из тазовой кости. Позже клетки отправляют на биопсию. Также врач-онколог проводит полный осмотри тела: МРТ, УЗИ, КТ, рентген, для выявления метастазов.
Лечение, терапия и прогноз
Основным типом лечения используется химиотерапия, когда в кровь вводят химические яды, которые направлены на уничтожение аномальных клеток крови. Опасность и малоэффективность данного типа лечения в том, что также уничтожаются и здоровые клетки крови, коих и так мало.
При выявлении первичного очага, врач может назначить химию для полного уничтожения костного мозга в данной зоне. После проведения процедуры также могут проводить и облучение для уничтожения остатков раковых клеток. В процессе происходит пересадка стволовых клеток от донора.
(1 оценок, среднее: 5,00 из 5)
Загрузка…
Источник
Рубрика МКБ-10: C91.0
МКБ-10 / C00-D48 КЛАСС II Новообразования / C00-C97 Злокачественные новообразования / C81-C96 Злокачественные новообразования лимфоидной, кроветворной и родственных им тканей / C91 Лимфоидный лейкоз лимфолейкоз
Определение и общие сведения[править]
Острые лейкозы (ОЛ) — группа опухолевых заболеваний системы крови (гемобластозов), для которых характерно первичное поражение костного мозга опухолевыми (бластными) кроветворными клетками с вытеснением ими нормальных элементов гемопоэза.
Эпидемиология
Среди гемобластозов ОЛ занимают одно из первых мест по частоте встречаемости. Заболеваемость ОЛ составляет 5-6 случаев на 100 000 населения в год, 6-7% от всех злокачественных новообразований.
У взрослых соотношение миелоидных и лимфоидных лейкозов составляет приблизительно 6:1, в детском возрасте 80-90% всех острых лейкозов приходится на лимфобластные формы, а после 40 лет наблюдают обратное соотношение — у 80% больных острым лейкозом диагностируют миелоидный вариант заболевания.
Лейкозы подразделяют на острые и хронические.
Классификация
В настоящее время наиболее распространена морфологическая классификация острых лейкозов, предложенная франко-американо-британской группой в 1976 г., пересмотренная и дополненная в 1991 г. (классификация FAB). В 2001 г. FAB-классификация стала составной частью классификации ВОЗ, предложенной международной группой экспертов. По классификации ВОЗ острые лейкозы характеризуются в соответствии c морфоцитохимическими реакциями бластных клеток, с учетом их генотипа, иммунофенотипа, возникновения после предшествующей химиорадиотерапии. ОМЛ в этой классификации подразделяется на 4 категории:
1. ОМЛ, ассоциированный со стабильно выявляемыми транслокациями;
2. ОМЛ с мультилинейной дисплазией;
3. ОМЛ после предшествующей химиотерапии;
4. Другие формы ОМЛ.
Острые лимфобластные лейкозы (ОЛЛ) в новой классификации ВОЗ рассматривают в разделе опухолей из предшественников Т- и В-лимфоцитов. По классификации ВОЗ в разделе лимфатических опухолей из ранних предшественников представлены:
• лимфобластный лейкоз/лимфома из В-предшественников (синоним «острый лимфобластный лейкоз из предшественников В-клеток»);
• лимфобластный лейкоз/лимфома из Т-предшественников (синоним «острый лимфобластный лейкоз из предшественников Т-клеток»).
Третья форма ОЛЛ по FAB-классификации в современной классификации отнесена в большой раздел опухолей из фенотипически зрелых В-клеток как беркиттоподобный лейкоз/лимфома.
Основные варианты острых лейкозов:
• острый миелобластный недифференцированный лейкоз (М0 по FAB);
• острый миелобластный лейкоз без созревания (М1 по FAB);
• острый миелобластный лейкоз с созреванием (М2 по FAB);
• острый промиелоцитарный лейкоз (М3 по FAB);
• острый миеломонобластный лейкоз (М4 по FAB);
• острый монобластный лейкоз (М5 по FAB);
• острый эритробластный лейкоз (М6 по FAB).
Вследствие мутации в генетическом материале клоногенной кроветворной клетки при отсутствии дифференцировки возникает бесконтрольная пролиферация и накопление патологических клеток. Обнаружение различных хромосомных аберраций при ряде врожденных заболеваний [синдром Эллиса-Ван-Кревельда, анемия Фанкони, синдром Вискотта-Олдрича, синдром Клайн-фелтера, нейрофиброматоз (болезнь Реклингхаузена) и т.д.] подтверждает, что патогенез острых лейкозов связан с генетическими поломками.
Прямое доказательство вирусного происхождения острых лейкозов у взрослых получено лишь для Т-клеточного лейкоза/лимфомы взрослых, вызванного вирусом HTLV-1. Доказана взаимосвязь между дозой ионизирующей радиациии и использованием химио/радиотерапии по поводу других опухолей и возникновением острых лейкозов.
Этиология и патогенез[править]
Клинические проявления[править]
В течении острых лейкозов выделяют:
• первый острый период (дебют или манифестация);
• ремиссии;
• рецидивы.
Клиническая картина при различных формах острых лейкозов схожа, в основном ее проявления связаны с замещением нормальной гемопоэтической ткани опухолевыми клетками, инфильтрацией ими различных органов. Дебют острого лейкоза может быть острым с высокой лихорадкой, резкой слабостью, интоксикацией, кровоточивостью, присоединением тяжелых инфекций. Часто диагноз устанавливают случайно, пожилых пациентов нередко госпитализируют в связи с возникновением или усугублением стенокардии, нарушений ритма сердца на фоне дебюта острого лейкоза. В клинической картине обнаруживается лимфаденопатия, гепатоспленомегалия, гиперплазия десен, геморрагический синдром различной степени тяжести, оссалгии и артралгии, возможны неврологическая и менингеальная симптоматика, лейкозная инфильтрация периферических нервов с разнообразными двигательными и чувствительными нарушениями. При глубокой гранулоцитопении возникают язвенно-некротические поражения слизистой оболочки полости рта, пищевода, кишечника, признаки общей интоксикации. К экстрамедуллярным поражениям при острых лейкозах относят поражения сетчатки, яичек, яичников, кожи (лейкемиды), мягких тканей (миелоидная или гранулоцитарная саркома), легких, сердечной мышцы.
В анализах крови изменения варьируют от трехростковой цитопении до форм с гиперлейкоцитозом и тотальной бластемией.
Острый лимфобластный лейкоз
Самая распространенная опухоль кроветворной ткани у детей. При формах с гиперлейкоцитозом, которые не сопровождаются, в отличие от ОМЛ, церебральной и легочной недостаточностью, выявляется значительная лимфаденопатия и гепатоспленомегалия. Характерны высокий уровень ЛДГ, гиперурикемия, гиперфосфатемия, гиперкальциемия, часта нейролейкемия.
Острый лимфобластный лейкоз: Диагностика[править]
Диагностика острых лейкозов базируется на оценке морфологических особенностей клеток костного мозга и периферической крови (обнаружение бластных клеток). Для установления варианта острого лейкоза и определения прогностических групп выполняются цитохимическое исследование, ИФТ, цитогенетическое и молекулярно-биологическое исследования.
ИФТ острых лейкозов позволяет определять линейную принадлежность бластных клеток и этап дифференцировки. Обнаружение на клетке одномоментной экспрессии антигенов, в норме вместе не встречающихся, указывает на ее аберрантный (лейкемический) иммунофенотип. Выделение при ИФТ по меньшей мере 6 подтипов ОЛЛ привело к разработке дифференцированных программ лечения ОЛЛ и позволило добиться значительных успехов в лечении. К антигенам, определяемым на клетках лимфоидной принадлежности, относят CD1-5, CD7-10, CD19-20, CD22, CD23, CD56, CD57, CD79а; миелоидной — CD11, CD13, CD14, CD15, CD33, CD36, CD41, CD42, CD65, HLA-DR; антигеном ранних клеток-предшественниц считают CD34.
Цитогенетическая характеристика острых лейкозов
Практически у 90% больных острыми лейкозами находят цитогенетические аномалии (транслокации, делеции, инверсии, гиперплоидию, исчезновение одной из пары хромосом и т.д.), что позволило классифицировать острые лейкозы и выделить их отдельные формы. Определение цитогенетических маркёров заболевания принципиально важно как для терапии, так и для прогноза течения острого лейкоза.
Целый ряд транслокаций при ОМЛ [t(8;21), t(15;17), inv16] составляют группы благоприятного прогноза, для которых созданы программы дифференцированного лечения, позволяющие достигать длительной безрецидивной выживаемости. При ОЛЛ к неблагоприятным в прогностическом отношении аномалиям ка-риотипа относятся t(9;22), t(4;11).
Дифференциальный диагноз[править]
Проведение дифференциальной диагностики необходимо при метастазировании в костный мозг лимфосарком, некоторых солидных опухолей. В любом случае диагноз устанавливают только на основании комплексного анализа (морфология, цитохимия, ИФТ, цитогенетика) бластных клеток.
Острый лимфобластный лейкоз: Лечение[править]
Основная цель лечения острых лейкозов — эрадикация лейкемического клона и восстановление нормального кроветворения. Основополагающие принципы химиотерапии (ХТ) острых лейкозов:
• принцип дозоинтенсивности, т.е. использование адекватных доз цитостатических препаратов в сочетании с четким соблюдением временных межкурсовых интервалов;
• использование сочетания цитостатических средств с целью получения наилучшего эффекта;
• принцип этапности терапии. Основные этапы терапии острых лейкозов:
• индукция ремиссии;
• консолидация;
• поддерживающая терапия;
• профилактика нейролейкемии (для некоторых вариантов ОЛ).
Цель индукции ремиссии (период начального лечения) — максимально быстрое и существенное сокращение опухолевой массы и достижение полной ремиссии. В настоящее время консолидация — наиболее агрессивный этап лечения острых лейкозов, задачей которого является полная эрадикация лейкемического клона. Длительность и интенсивность поддерживающей терапии при разных вариантах ОЛ варьирует, но принцип ее одинаков для всех видов ОЛ — продолжение цитостатического воздействия на возможно остающийся опухолевый клон. Профилактика нейролейкемии — принципиальный этап в лечении лимфобластных, миеломоно- и монобластных вариантов ОЛ, промиелоцитарного ОЛ, для форм ОЛ, протекающих c гиперлейкоцитозом и большой средостенной опухолью в дебюте заболевания. Профилактику нейролейкемии распределяют на все периоды программного лечения: индукцию ремиссии, консолидацию и поддерживающее лечение.
Методы нейропрофилактики и терапии нейролейкемии:
• интратекальное введение химиопрепаратов;
• лучевая терапия;
• системное использование высоких доз метотрексата и цита-рабина.
Основной метод нейропрофилактики — интратекальное введение трех препаратов (метотрексата, цитарабина, дексаметазона). Лечение нейролейкемии осуществляют по общим законам как для ОЛЛ, так и для ОНЛЛ. На 1-м этапе — спинномозговые пункции 1 раз в 2-3 дня до нормализации показателей цереброспинальной жидкости и получения как минимум трех нормальных люмбальных пунктатов. Затем пункции в течение 3 мес проводятся с частотой 1 раз в 2 нед. При специфическом поражении оболочек и/или вещества головного мозга интратекальное введение препаратов дополняют в ряде случаев краниоспинальным облучением в дозе 18-24 Гр. Альтернативная схема профилактики нейролейкемии — системное введение цитарабина в высоких дозах (1-3 г/м2).
Общепризнанной программой полихимиотерапии при острых нелимфобластных лейкозах является сочетание цитарабина и даунорубицина по схеме «7 + 3» (ежедневное в течение 7 дней введение цитарабина по 100 мг/м2 2 раза в сутки и даунорубицина по 45 мг/м2 в течение первых трех дней). Большинство авторов для консолидации и поддерживающей терапии используют те же курсы, что и для индукционной терапии. Однако применение курса «НАМ» (высокие дозы цитарабина и митоксантрон) в качестве консолидации позволяет значительно улучшить результаты лечения. При этом «НАМ» (цитарабин 3000 мг/м2 каждые 12 ч в первые 1-3 дня курса, митоксантрон 10 мг/м2 в 3-5-й дни курса) используют как 2-ю индукцию, если ремиссия не была достигнута после 1-го курса индукции по программе «7 + 3». После курса «НАМ» выполняют консолидацию высокодозным цитарабином (цитарабин 3000 мг/м2 каждые 12 ч в 1-й, 3-й, 5-й дни курса). Терапия ОЛ, протекающих с гиперлейкоцитозом, проводится по программам, предусмотренным для конкретного варианта лейкоза, в соответствии с возрастом больного и иммунофенотипом/генотипом опухолевых клеток. Обязательно применение аллопуринола, гидратации. Циторедуктивную предфазу проводят в зависимости от конкретного варианта ОЛ. При лейкоцитозе выше (70-100)х109/л до подтверждения варианта ОЛ рекомендован гидроксикарбамид в дозе 100 мг/кг в сутки. При появлении на фоне гиперлейкоцитоза синдрома лейкостазов (нарушение сознания, одышка, поражение легких, ОПН) наряду с приемом гидроксикарбамида и гидратацией используют лейкаферез. ХТ начинают не откладывая, если после лейкафереза лейкоцитоз уменьшился и улучшилась клиническая симптоматика. Параллельно с проведением полихимиотерапии рекомендованы плазмаферезы, особенно при развитии синдрома лизиса опухоли.
Основополагающее правило при лечении ОПЛ состоит в сочетанном применении полного изомера трансретиноевой кислоты (ATRA) — весаноида — и антрациклиновых антибиотиков с цитарабином или без него. ATRA назначают всегда при малейшем клиническом подозрении на ОПЛ (морфология бластных клеток, геморрагический синдром, низкие показатели протромбина и фибриногена). Индукция ремиссии требует массивной заместительной гемотрансфузионной терапии (тромбоцитные концентраты, свежезамороженная плазма). Всем больным ОПЛ может быть рекомендована программа AIDA. Включение цитарабина в схему лечения ОПЛ может быть показано для больных с исходным лейкоцитозом >10 x 109/л. Всем больным независимо от исходного лейкоцитоза курс ХТ должен быть начат не позднее 3-го дня от начала приема ATRA. Больным с числом лейкоцитов >10 χ 109/л курс химиотерапии с цитостатическими препаратами начинают одномоментно с назначением ATRA. При исходном гиперлейкоцитозе (особенно если число лейкоцитов >50 χ 109/л) на фоне проведения полихимиотерапии целесообразно выполнение плазмообмена, позволяющего профилактировать синдром лизиса опухоли и корригировать коагуляционные расстройства. При малейшем подозрении на развитие ретиноидного синдрома (одышка, фебрильная лихорадка, отечный синдром, почечно-печеночная недостаточность) назначают дексаметазон 10 мг/м22 2 раза в сутки в течение 3 дней, при этом отмены ATRA обычно не требуется. Однозначных рекомендаций по выполнению аутологичной трансплантации гемопоэтических стволовых кроветворных клеток (ГСКК) больным ОНЛЛ нет. Ее можно рассматривать в качестве высокодозной альтернативы для больных в 1-й ремиссии. На основании анализа результатов применения аллогенной трансплантации ГСКК даны четкие рекомендации по целесообразности ее выполнения больным в 1-й ремиссии.
Единого мнения о терапии рецидивов и резистентных форм ОНЛЛ не выработано. Большинство программ ХТ основаны на использовании цитарабина в дозах, превышающих стандартные (500-3000 мг/м2), в сочетании с антрациклинами (митоксантрон 10-12 мг/м2 в сутки 3 дня; идарубицин 12 мг/м2 в сутки 3 дня). Всех больных с достигнутой 2-й полной ремиссией следует рассматривать как потенциальных кандидатов на выполнение трансплантации аллогенных ГСКК. Для лечения рецидива ОНЛЛ, развившегося после аллогенной трансплантации ГСКК, применяют переливание лимфоцитов донора с целью индукции эффекта «трансплантат против лейкоза».
Лечение острого лимфобластного лейкоза
Общие принципы терапии ОЛЛ:
• использование сочетания 5 или более цитостатических средств;
• профилактика нейролейкемии;
• высокодозная консолидация;
• длительная поддерживающая терапия.
Факторы, определяющие принадлежность больного к группе высокого риска:
• лейкоцитоз в дебюте заболевания для В-клеточного ОЛЛ >30х109/л;
• лейкоцитоз в дебюте заболевания для Т-клеточного ОЛЛ >100х109/л;
• достижение ремиссии более чем за 4 нед;
• иммунофенотип — ранний пре-В- и ранний Т-вариант;
• цитогенетические/молекулярные маркёры — t(9;22), или транскрипт bcr/abl; t(4;11), или транскрипт MLL-AF4; множественные хромосомные аберрации.
В большинстве клиник при лечении ОЛЛ за основу принимается немецкий протокол. После 7-дневной предфазы преднизолоном в дозе 60мг/м2 следует 8-недельная двухфазная индукция, включающая несколько цитостатических препаратов (винкристин, даунорубицин, аспарагиназу, глюкокортикоидные гормоны, циклофосфамид, меркаптопурин, цитарабин). Курсы консолидации проводят в соответствии с факторами риска, для ряда больных предусмотрена высокодозная консолидация по программе RACOP. Реиндукционная терапия продолжительностью 6 нед включает ХТ-препараты, использующиеся в курсе индукции. Поддерживающая терапия проводится в течение 2 лет, включает ротирующие курсы RACOP, COMP, COAP.
Долгосрочные результаты лечения Ph-позитивных ОЛЛ остаются крайне неудовлетворительными. Добавление иматиниба значительно улучшило результаты лечения, и в настоящее время комбинированную (полихимиотерапия + иматиниб) терапию следует рассматривать как этап подготовки к аллогенной (родственной и неродственной) трансплантации ГСК.
Профилактика[править]
Прочее[править]
Источники (ссылки)[править]
Онкология [Электронный ресурс] : Национальное руководство. Краткое издание / под ред. В.И. Чиссова, М.И. Давыдова — М. : ГЭОТАР-Медиа, 2014. — https://www.rosmedlib.ru/book/ISBN9785970431535.html
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
- Аспарагиназа
- Блинатумомаб
- Винкристин
- Дазатиниб
- Даунорубицин
- Доксорубицин
- Идарубицин
- Иматиниб
- Инотузумаб озогамицин
- Клофарабин
- Меркаптопурин
- Метотрексат
- Неларабин
- Пэгаспаргаза
- Циклофосфамид
- Цитарабин
Источник
