Интенсивность болевого синдрома при травмах
Болевой синдром, или альгосиндром – это сложный комплекс болезненных ощущений различной степени тяжести. Обычно располагается в области основной патологии – травмы, места сосудистого спазма, больного органа, сустава; реже имеет неясный или блуждающий характер.
Внимание! Боль – это защитная реакция на патологическое воздействие, которая сигнализирует об угрозе здоровью. Даже незначительное проявление дискомфорта игнорировать нельзя, так как болевой синдром – основной маркер проблем с организмом.
При травматических болях следует обращаться к травматологу или хирургу, при внутренних (органных) – к терапевту или узкому специалисту. Диагностикой и лечением альгосиндромов неясной этиологии или с поражением нервной системы занимается врач-невролог.
Классификация
По субъективным проявлениям боль может быть колющей, режущей, тянущей, пульсирующей, давящей, ноющей и т.п. Вне зависимости от причины, проявление может быть острым и хроническим.
Острый болевой синдром сопровождает острые патологические процессы и длится не более 2-3 месяцев. По истечение этого срока он либо проходит вместе с причиной его вызывающей, либо переходит в хроническую стадию. Это совсем не обязательно сильная и резкая (острая) боль, и ее легко можно устранить анальгетиками и анестетиками.
Хронический болевой синдром может длиться годами. Часто является единственным признаком патологии и плохо поддается медикаментозному купированию. Со временем провоцирует депрессию, беспокойство, апатию – вплоть до полной деградации личности.
На заметку! И острая, и хроническая форма могут иметь различную степень интенсивности – от легкой до нестерпимой. Многое зависит от причины, расположения и субъективных особенностей пациента.
В зависимости от локализации можно выделить широкий спектр альгосиндромов. Основные из них:
- миофасциальный – связан с перенапряжением мышц и фасций, не имеет четкой привязки к органу, связан с травмами и физическими перегрузками;
- абдоминальный – объединяет патологии брюшной полости, в первую очередь в области ЖКТ;
- вертеброгенный – в медицине известен как корешковый болевой синдром; проявляется при сжатии или травмировании спинномозговых отростков;
- анокопчиковый – формируется в нижнем отделе позвоночного ствола и задней стенки малого таза с вовлечением прилежащих органов – толстой кишки, половой системы;
- пателлофеморальный – является следствием артрозных изменений в коленном суставе;
- нейрогенный – связан с поражением нервных структур, в первую очередь – головного и спинного мозга.
Болевой синдром: причины возникновения
Основные причины боли – травмы, спазмы, нарушения кровообращения, инфекции, отравления, ожоги и переохлаждения, деформации и деструкции различных участков опорно-двигательной системы (позвоночника, суставов).
С учетом особенностей происхождения различают 2 большие группы альгосиндромов – ноцицептивный и нейропатический.
Ноцицептивная боль
Возникает при воздействии раздражителей непосредственно на болевые рецепторы, расположенные в тканях по всему организму. Может быть легкой или нестерпимой, но в любом случае легко купируется анальгетиками и быстро проходит при устранении причины. В зависимости от типа и расположения этих рецепторов, ее подразделяют на 2 подвида:
- соматическая боль – имеет поверхностное проявление с четкой локализацией; характерна для воспалительного процесса, отеков, травматических повреждений (ушибы, переломы, разрывы, растяжения и т.п.), а также некоторых нарушений метаболизма и кровообращения;
- висцеральная боль – появляется при повреждении внутренних органов; имеет более глубокое залегание и плохо просматриваемую локализацию; в качестве примера можно привести кардиомиалгию, почечную колику, язвенную болезнь.
Механизм ноцицептивного синдрома связан с выработкой специальных медиаторов боли – ацетилхолина, гистамина, брадикининов, простагландинов. Накапливаясь в области повреждения, они раздражают ткани, вызывая неприятные ощущения. Дополнительный эффект исходит от факторов воспаления, вырабатываемых лейкоцитами.
Нейропатическая боль
Возникает при воздействии непосредственно на функциональные структуры периферической и центральной нервной системы – нервные отростки, а также отделы головного и спинного мозга. Иногда сопровождается патологическим возбуждением нейроструктур с формированием аномальной реакции на неболевые раздражители (простое прикосновение). Часто проявляется как хроническая боль, поэтому может плохо поддаваться купированию.
Имеет 2 разновидности:
- периферическая – при поражении нервных отростков в виде невралгий, невропатий, невритов, туннельных синдромов;
- центральная – развивается как следствие острого нарушения мозгового кровообращения, спинномозговых травм, миелопатий, рассеянного склероза;
- дисфункциональная – проявляется как несоответствие между силой воздействия раздражителя и ответной реакцией организма; является следствием дисфункции ЦНС.
На заметку! В качестве отдельной группы выделяют психогенный альгосиндром. В этом случае повреждения организма отсутствуют, а характерные для него хронические боли являются следствием фантазий и страхов самого пациента. Он может развиваться как вариант нейропатической боли или при вынужденном длительном существовании с сильными ноцицептивным болевым синдромом.
Симптоматика
Основной признак болевого синдрома – постоянная или периодическая боль определенной, мигрирующей или неясной локализации. При этом ощущения могут быть резкими или тянущими, колющими, ноющими, пульсирующими. Все остальные признаки зависят от причины и характера недуга. Среди них:
- дискомфорт при движении, стихающий в состоянии покоя;
- болезненные ощущения в неподвижном положении;
- иррадиация в другие части тела;
- повышение температуры в области болезненных ощущений;
- проявление альгосиндрома при незначительном прикосновении (характерно для нейропатий);
- нарушение чувствительности в прилегающей зоне.
Болевой синдром может сопровождаться отечностью и покраснением поврежденных тканей, а также слабостью, повышенной утомляемостью, общей подавленностью.
Диагностика

Последовательность действий при диагностике причин болевого синдрома зависит от его расположения, характера и сопутствующих симптомов. При болях невыясненной локализации первоочередное внимание уделяют инструментальным методам – УЗИ, рентгенографии, МРТ, КТ, ЭКГ, гастродуоденоскопии и т.п. Список тестов и анализов назначает травматолог, терапевт, хирург или другой узкий специалист.
Для оценки интенсивности болевого синдрома используют 2 системы градации – упрощенную и расширенную.
Упрощенная «шкала переносимости» включает 3 стадии:
- легкая боль – не мешает движению и выполнению повседневных дел;
- сильная боль – нарушает нормальный ритм жизни, не позволяет выполнять обычные действия;
- нестерпимая боль – спутывает сознание, способна спровоцировать обморок и шоковое состояние.
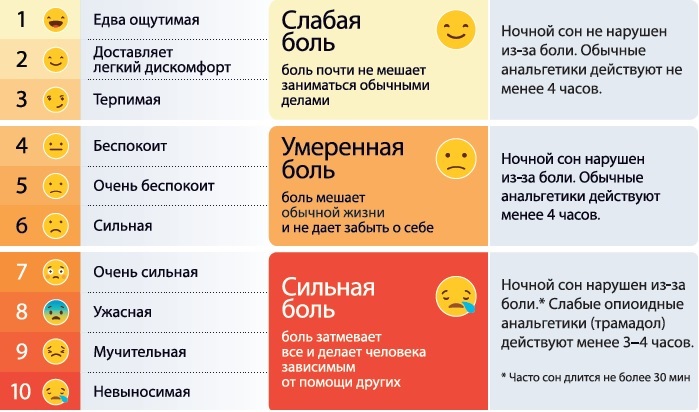
Расширенная градация подразумевает использование визуальной шкалы субъективной оценки – от 0 до 10, где «десятка» означает сильный болевой шок. В процессе обследования пациенту предлагают самому оценить интенсивность боли, потому результат может не соответствовать реальности.
Внимание! Интенсивность боли не всегда свидетельствует о тяжести патологического процесса, поэтому «прощаться с жизнью» при сильных болях, так же как и недооценивать легкую болезненность, не стоит.
Только установив причину боли, ее интенсивность и характер, врач назначит подходящие обезболивающие препараты. Это связано с отличиями в механизме действия у разных групп анальгетиков – что подходит при ноцицептивном синдроме совершенно не эффективно при нейропатическом.
Особенности терапии болевого синдрома
Лечение напрямую зависит от причины боли и ее характера (ноцицептивный, нейропатический). В арсенале средств присутствуют как консервативные методики с использованием медикаментозных средств и физиотерапии, так и радикальные хирургические методы.
Лекарственная терапия:
- обезболивающие – анальгетики, анестетики;
- противовоспалительные – преимущественно НПВС, реже – инъекции кортикостероидов;
- миорелаксанты;
- спазмолитики;
- седативные препараты.
Внимание! Самостоятельный прием обезболивающих средств без воздействия на причину недуга может затруднить диагностику, усугубить ситуацию и сделать дальнейшее лечение неэффективным.
Методы физиотерапии улучшают усвоение медикаментозных средств, снимают воспаление, отечность, спазмы, повышают регенерацию, расслабляют мышцы, успокаивают нервную систему.

На практике применяют:
- УВЧ;
- токовую терапию;
- грязевые компрессы;
- электрофорез;
- массаж;
- иглоукалывание;
- гирудотерапию.
При нарушениях опорно-двигательной системы широко применяют метод иммобилизации поврежденных участков – шины, гипсовые повязки, корсеты, воротники, бандажи.
Хирургическое лечение является крайней мерой и применяется только в том случае, если консервативные методы неэффективны.
На заметку! Боль – универсальный симптом для патологических процессов, поэтому его лечением занимаются врачи самых различных специальностей – терапевты, невропатологи, гастроэнтерологи и др. В экстренных случаях, при остром болевом синдроме может потребоваться срочная помощь реаниматологов, травматологов, хирургов.
Профилактические меры
В целях предотвращения ангиосиндрома, придерживайтесь некоторых общих рекомендаций:
- избегайте травм, в особенности с поражением позвоночника, черепа, суставов;
- следите за своей осанкой – тренируйте, но не перегружайте мышцы спины;
- практикуйте умеренные физические нагрузки – гиподинамия, также как и перенапряжение, плохо влияет на состояние опорно-двигательной системы, вызывая со временем артралгию и/или невралгию;
- при наличии заболеваний (острых, хронических) обеспечьте их своевременное лечение;
- поддерживайте нормальный вес тела, не допускайте ожирения или дистрофии тканей;
- откажитесь от неудобной одежды и обуви – они вызывают боли, связанные с нарушением кровообращения и деформацией скелета;
- избегайте длительных нервных стрессов и психологических перегрузок;
- регулярно проходите профилактические осмотры в клинике по месту жительства.
Очень важно обращаться к врачу при первых же признаках болевого синдрома. Решение перетерпеть или заняться самолечением может дорого обойтись вашему здоровью!
Источник
ПРО ПАЛЛИАТИВ использует cookie для статистики и аналитики, чтобы сделать сайт максимально удобным. Оставаясь на сайте, вы подтверждаете свое согласие на использование файлов cookie.
Представляем фрагмент брошюры для врачей «Обезболивание в паллиативной помощи. Практическое руководство для врача», подготовленной благотворительным фондом «Вера». Полная версия брошюры доступна для скачивания по ссылке.
Только сам пациент может оценить уровень боли, которую испытывает. При каждом осмотре пациента спрашивайте его о наличии боли и прислушивайтесь к его жалобам.
Оцените интенсивность болевого синдрома до назначения анальгетиков: для вербальных пациентов используйте комплексную шкалу оценки боли:
Шкалы боли для детейОбзор различных инструментов для определения интенсивности боли у детей

Комплексная шкала оценки боли
Для оценки болевого синдрома у невербальных пациентов и пациентов с когнитивными нарушениями используйте шкалу PAINAD (Pain Assessment in Advanced Dementia — Шкала оценки боли при тяжелой деменции):
«Не мешайте человеку жить прошлым»12 правил, которые помогут в уходе за людьми с деменцией
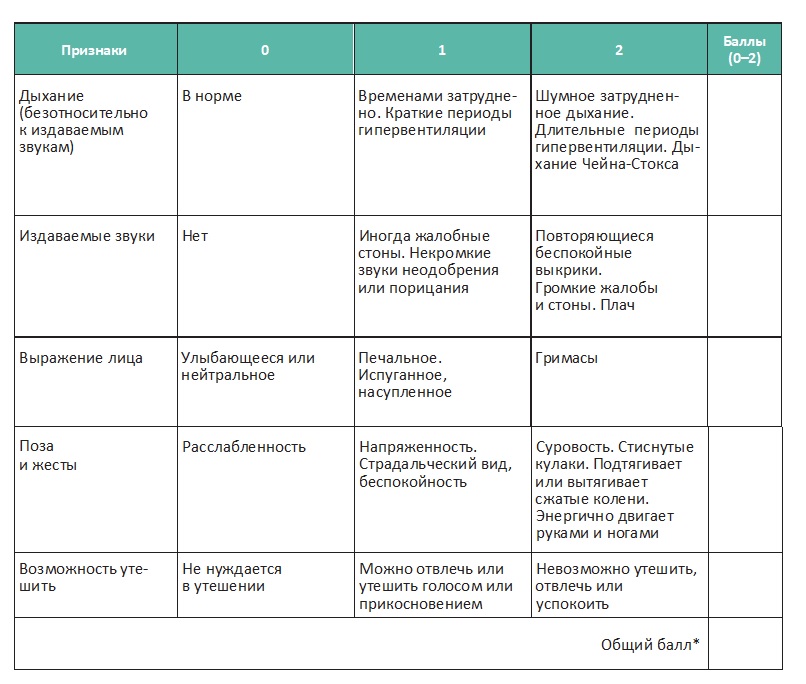
* Общее количество баллов составляет от 0 до 10 (шкалы от 0 до 2 для пяти пунктов); наивысший балл указывает на более сильную боль (0 — боли нет, 10 — сильная боль).
Полученные баллы не определяют абсолютную интенсивность боли. Правильнее сравнивать полученный общий балл с предыдущим значением. Увеличение балла говорит об увеличении боли, в то время как более низкое его значение позволяет предположить, что боль уменьшилась.
Спросите пациента
Навыки общения с пациентами10 советов для врачей при проведении консультаций
- Когда начались боли и сколько они продолжаются (недели, месяцы)?
- Где болит?
- Появляется боль днем или ночью; она постоянная, периодическая или «прорывная»?
- Какая это боль: острая, тупая, жгучая, пронзающая, давящая, распирающая, пульсирующая и др.?
- Есть ли симптомы нейропатической боли: прострелы, чувство жжения, зоны онемения кожи, гиперестезия, аллодиния, дизестезия и др.?
- Как он спит? Если сон нарушен, то как часто пациент просыпается и почему: дискомфорт, боль, привычка мало спать, одышка, неудобное положение? Если есть сложности с засыпанием, в чем причина: дискомфорт, боль, одышка?
- Если сон не нарушен, испытывает ли пациент дискомфорт, боли и т.д., когда просыпается утром?
- Что усиливает боль (например, прием пищи, дефекация и т.п.) и что ее облегчает (например, особое положение в постели)?
- Сопровождается ли боль другими симптомами: тошнота, рвота, диарея, запоры, одышка, потеря аппетита, кашель, слабость и др.?
- Принимает ли пациент анальгетики? Если да, то какие и на протяжении какого времени; как долго действует одна доза анальгетика?
- Есть ли побочные эффекты от анальгетика и как они выражены?
- Какие есть сопутствующие заболевания и какие препараты пациент принимает для их лечения?
Читайте дальше: «Лечение болевого синдрома. Общие принципы».
Горячая линия помощи неизлечимо больным людям
Если вам или вашим близким срочно необходимо обезболивание, помощь хосписа, консультация по уходу или поддержка психолога.
8-800-700-84-36
Круглосуточно, бесплатно
Источник
Боль определяют как специфическое психофизиологическое состояние, возникающее в результате воздействия сверхсильных или разрушительных раздражителей, вызывающих органические либо функциональные нарушения в организме.
Это комплексное патофизиологическое явление (интегративная функция), включающее три основных компонента:
1) индивидуальное ощущение вредоносного агента (ранение, травма, ожог и пр.);
2) типовые вегетативные, двигательные и другие реакции защиты от патогенного воздействия;
3) оценку болевых влияний на основе опыта множества событий, сопровождающихся сенсорными и эмоциональными состояниями.
Таким образом, речь идет не просто о болевых ощущениях в узком смысловом значении, но и о физиологическом акте с участием нескольких систем, а именно сознания, ощущения, памяти, мотивации, а также вегетативных: соматических и поведенческих реакциях. Поэтому правильнее говорить не о боли или болевых ощущениях, а о ноцицептивных [(лат.) — вредить] воздействиях, иди патологической афферентной импульсации, или ноцицептивной афферентации, которые следует рассматривать как синонимы.
В начале своего воздействия ноцицептивная афферентация имеет положительный биологический смысл, поскольку вызывает комплекс приспособительно-компенсаторных реакций, направленных на срочное устранение источника вредоносных раздражений или воздействий. Например, мобилизуется симпатико-адреналовая система, обеспечивающая готовность к преодолению неблагоприятного воздействия; активизируются адренергические механизмы заднего отдела подбугорной области и сетевидного образования; стимулируется обмен медиаторов в ЦНС и периферических отделах симпатико-адреналовой системы; усиливается секреция «адаптивных» гормонов гипофиза.
Начальные проявления ноцицептивного воздействия не отличаются от типичных признаков первой фазы стресс-реакции. Непосредственно в тканях зоны повреждения выделяются биологически активные полипептиды типа брадикинина, вызывающие раздражение болевых рецепторов.
В результате стимулирующего влияния ноцицепции вначале усиливается функция внешнего дыхания и кровообращения, усиливается тканевый газообмен. Когда ноцицептивное раздражение по интенсивности и длительности воздействия превышает критический порог восприятия боли, развивается качественно новое состояние — «боль—страдание». Оно характеризуется возникновением болевой доминанты, охватывающей все отделы ЦНС и нарушающей функциональную деятельность внутренних органов.
Иначе говоря, «физиологическая» боль сменяется патологическим болевым синдромом, когда внешние, раздражители, вступая в условную связь, превращаются в дополнительные источники усиления мучительной боли. На стадии «боль—страдание» угнетается ЦНС, нарушается регуляция внешнего дыхания. Интенсивное раздражение афферентных волокон соматических и висцеральных нервов вызывает усиление симпатической импульсации с подъемом системного артериального давления.
Вряд ли можно сомневаться в том, что ноцицептивные раздражения, сопутствующие тяжелым (шокогенным) травмам, длительным и травматичным хирургическим вмешательствам, всякий раз значительно превышают пороговую величину и логически утверждают действие феномена «боль—страдание».
В основе патогенетического механизма «боль—страдание» лежит возникновение генераторов патологически усиленного возбуждения, обусловленных способностью каждого из образований ноцицептивной системы усиливать болевую стимуляцию; любой из таких генераторов — это патологическая детерминанта, определяющая деятельность активируемой ею системы с прямым патогенным значением [Крыжановский Г. Н., 1983; цит. по В. Ю. Шанину, 1990].
Целостная ответная реакция на болевое воздействие определяется двумя физиологическими системами:
1) ноцицепция сегментарного уровня, за счет которой обеспечивается резкая активация действия (реакции избегания, защиты);
2) антиноцицептивная надсегментарная система, осуществляющая контроль афферентного входа и модуляцию сегментарной интеграции высокопороговой и низкопороговой афферентации.
Влияния антиноцицептивной системы — это один из биологических способов самозащиты организма от чрезвычайных воздействий, тот адаптивный механизм, который корригирует болевой стресс за счет модуляции перцептивного компонента боли и нисходящего контроля афферентных входов, подавления эмоционально-поведенческого реагирования.
Реализация антиноцицептивного эффекта связана с повышением активности серотонинергических систем мозга, эндогенно образующихся морфиноподобных пептидов — энкефалинов, эндорфинов. Антиноцицепция является как бы дополнительным контуром гомеостатического регулирования, адаптации при длительном ноцицептивном раздражении, которого не удается избежать организму.
Первичный морфологический субстрат ноцицептивной системы — нейроны заднего рога спинного мозга. Упрощенно можно принять, что дискриминационная система связана с толстыми (низкопороговыми) афферентными проводниками группы А, а ноцицептивная — с более тонкими высокопороговыми волокнами (А — гамма, дельта, С). Однако на основании современных представлений об организации афферентных систем нельзя выделить специфические нейронные группировки, связанные исключительно с ноцицептивной чувствительностью.
Уже на сегментарном уровне происходит внутрицентральное взаимодействие разномодальных афферентных входов. Биологическое значение сигналов, поступающих по различным афферентным каналам, во многом обусловлено соотношением импульсации высокопороговых и низкопороговых афферентных волокон. Существенная роль в модулирующем процессе принадлежит желатинозному образованию в дорсальных отделах заднего рога на пути прохождения афферентных волокон заднего корешка.
Нейрогенный компонент тяжелого повреждения извращает гомеостатические рефлексы в системах дыхания, кровообращения, терморегуляции и др. Установлено, что механизм этих нарушений связан с центральным, главным образом супрасегментарным патогенным влиянием ноцицептивной импульсации, исходящей из поврежденных ишемизированных тканей.
Возникновение этого дезадаптивного афферентного потока зарегистрировано в полимодальных ноцицепторах, продолжающих функционировать и в ишемизированных тканях. Угнетение гомеостатических рефлексов, напримёр в системе дыхания, связано именно с ноцицептивной афферентацией (не с плазмо- и кровопотерей); проводниковое обезболивание устраняет этот нейрогенный компонент травмы.
Не без основания допускают, что нейрогенным механизмам принадлежит ведущая роль в эндокринной метаболической реакции на травму и операцию, поскольку большую часть ее патологического компонента удается устранить с помощью проводниковой, эпидуральной блокады.
Представленные кратко основы патофизиологии боли позволяют сформулировать рекомендации, имеющие принципиальное значение для практики анальгезии-анестезии при тяжелых механических повреждениях [Шанин В. Ю., 1990]. Во-первых, все усилия анестезиолога должны направляться на афферентное звено рефлекторной дуги, всячески избегая включения механизмов, ответственных за эфферентную импульсацию. Во-вторых, необходимо принять за аксиому, что предотвращение субъективных ощущений боли не означает блокаду ноцицептивной импульсации с ее патогенными влияниями.
Оптимальным защитным эффектом будет обладать та анестезия, которая одновременно с болью блокирует вегетативный нейрональный и двигательный компоненты ноцицептивной афферентации. Оптимальным является сочетание деафферентации с активацией антиноцицептивной системы (анальгетики и анестетики).
Третье, пожалуй, наиболее важное положение касается той задачи анестезиолога, которую можно сформулировать как предотвращение возбуждения в ноцицептивной системе. Очень часто анестезия и деафферентация по ходу операции сама по себе обладает положительным эффектом, но в определенных условиях формируются вторичные генераторы патологически усиленного возбуждения в отделах ноцицептивной системы, удаленных от ее рецепторных и первых афферентных образований.
Вследствие этого, а также по причине многообразия афферентных входов в ноцицептивную систему диафферентация местноанестезирующими средствами не всегда дает положительный эффект и тогда ее необходимо дополнять активацией антиноцицептивной системы при помощи анальгетиков.
В-четвертых, по ходу анестезии следует постоянно стремиться к сохранению устойчивого возбуждения в антиноцицептивной системе, используя не вызывающие излишнего угнетения организма дозы анальгетиков, анестетиков. Фармакологические воздействия по линии подавления патологических очагов в ноцицептивной системе тогда достигают успеха, когда не угнетаются физиологические механизмы антиноцицепции.
С данной точки зрения углубление наркоза — не лучший способ усиления аналгезии, так как при этом угнетаются функции всего организма, в том числе антиноцицептивной системы. В период операционного стресса основные усилия должны направляться на улучшение газообмена, гемодинамики, способствующих восстановлению нормального функционирования всех систем организма; это обусловливает возможность активации антиноцицептивной системы.
Пятое положение касается оптимальных сроков проведения деафферентации и активации антиноцицептивной системы. Следует подчеркнуть, что из-за способности ноцицептивной системы к самоактивации эти важнейшие действия анестезиолога должны начинаться до начала операции или травматической процедуры.
История общей анестезии при травмах и ранениях начинается, пожалуй, с тех времен, когда стали оказывать медицинскую помощь при повреждениях, полученных в ходе военных действий. Уже в «Иллиаде» Гомера можно найти подобные упоминания, причем в древности для обезболивания лечебных действий прибегали к примитивным приемам как общей, так и местной анестезии.
Среди этих методов были и довольно распространенные. Например, в древней Ассирии для получения общей анестезии, необходимой для выполнения операций и других лечебных мероприятий при травмах, сознание пострадавших выключали временным пережатием сонных артерий.
Кстати говоря, именно по этой причине сонные артерии и получили свое название; так, слово karos (греч.) в переводе на русский язык означает глубокий сон. На протяжении веков, начиная со времен Гиппократа (он упоминает об этом в своих знаменитых «Афоризмах»), для местной анестезии при травмах широко использовали холод [цит. по Armstrong Davison М. Н., 1958].
Крупнейший военно-полевой хирург и главный хирург наполеоновской армии Jean Larrey за свою жизнь выполнил множество ампутаций в непосредственной близости от поля сражения, используя для анестезии лед и снег. Сам термин «замораживание» (англ.— freezing) как синоним местной анестезии был введен в медицинскую литературу в 1866 г. английским врачом В. W. Richardson, предложившим для, этой цели быстро испаряющийся углеводород риголен, который наносился на кожу в области предстоящей операции или болезненной манипуляции. Забегая вперед, отметим, что гипотермия имеет значение не только как средство для достижения местной анестезии, но и как метод воздействия на общую болевую чувствительность, которым можно пользоваться при проведении общей анестезии.
Одно из первых описаний лечения раненых на войне, включая анестезию, приведено в работе доктора Петера Юлиана (1260), будущего Папы Римского Иоанна XXI и автора одного из первых руководств по офтальмологии [Oner W. В., Onnway A. J., 1965]. Многие неверно полагают, что эра общей фармакологической анестезии при операциях и манипуляциях при травмах началась после открытия ингаляционного эфирного наркоза W. Т. Morton в 1846 г.
В действительности операции по поводу травм под энтеральным медикаментозным наркозом тсусенсаном выполнял еще японский врач С. Ханаока (1760—1855) в течение трех десятилетий, начиная с 1805 г. Тсусенсан представляет собой смесь хиосциамина, атропина, аконатина, салонина и некоторых других нейротропных средств [Steven J. Е., 1986].
После предварительных экспериментов на животных и апробации на людях С. Ханаока выполнял под энтеральным наркозом довольно обширные и травматичные вмешательства, включая ампутацию конечностей, трепанацию черепа, ушивание ран, ортопедические операции и др. Автор данной методики широко обучал ей японских врачей в специально созданной для этой цели школе.
Наиболее систематизированные материалы по использованию эфирного наркоза для обезболивания операций у раненых на войне были представлены Н. И. Пироговым в специальной главе «Отчет о путешествии по Кавказу» (1849). В нем же было описано применение эфирного наркоза в ходе крымской военной кампании у 100 раненых.
Весной 1847 г. эфирный наркоз на поле боя был применен американским хирургом Е. Barton в период Мексикано-американской войны [цит. по Aldrette J. A. et al., 1984]. В ходе гражданской войны 1861—1865 гг. в США у раненых было проведено около 60 000 анестезий, в том числе у 76% из них с использованием эфира, у 15% — хлороформа и у 9% была применена анестезия смешанного типа [Brown D. L., 1987].
В годы первой мировой войны наряду с методами общей ингаляционной анестезии у раненых широко применяли спинномозговую (субдуральную) анестезию, а во время второй мировой войны — внутривенный барбитуровый наркоз и местную инфильтрационную анестезию, которая особенно широко использовалась отечественными военными врачами.
Таким образом, анестезиологическое пособие при травмах прошло исторический путь, неразрывно связанный с развитием и становлением военно-полевой хирургии. Этот путь отражал главным образом общее состояние науки и практики в соответствующем периоде.
В.Н. Цибуляк, Г.Н. Цибуляк
Опубликовал Константин Моканов
Источник

