Индуцированный апоптоз и антифосфолипидный синдром

Особенно большой интерес представляет связь между синтезом аФЛ и апоптозом (программированной гибелью) ЭК. Напомним, что основная черта клеточного апоптоза — асимметрия фосфолипидной мембраны с экспонированием отрицательно заряженного фосфолипида фосфатидилсерина (ФС), который, как и кардиолипин, является мишенью для аФЛ.
Экспонирование ФС на внешней мембране клеток является самым ранним проявлением клеточного апоптоза, предшествующим фрагментации ДНК и нарушению целостности мембраны. Известно, что при активации тромбоцитов экспонирование ФС ассоциируется с активацией свертывания. Отрицательно заряженные фосфолипиды принимают участие в фактор VIII- и фактор IXa-зависимой активации фактора X на ЭК, а анексин V полностью ингибирует эту реакцию. Подвергнутые апоптозу ЭК обладают способностью увеличивать скорость активации фактора X, что ассоциируется с повышенным экспонированием ФС. Сходным образом увеличение экспозиции анионных фосфолипидов на мембране моноцитов сопровождается повышением активности протромбиназного комплекса.
Имеются данные о том, что эндотоксинстимулированные ЭК и тканевые факторы, экспрессируемые моноцитами в процессе развития апоптоза, проявляют прокоагулянтную активность, а стимулы, подавляющие активность тромбомодулина и гепарансульфата (провоспалительные цитокины, эндотоксины, гипоксия, гомоцистеинемия), обладают способностью индуцировать апоптоз ЭК. В недавних исследованиях было показано, что аФЛ обладают способностью связываться с поверхностью ЭК, подвергнутых апоптозу, и сами индуцируют процесс апоптоза ЭК, причем связывание аФЛ с находящимися в апоптозе клетками зависит от присутствия β-ГШ. Все эти данные свидетельствуют о том, что аФЛ-индуцированное нарушение нормальных механизмов апоптоза ЭК может иметь важное значение в развитии нарушений свертывания крови при АФС.
Наряду с β2-ГШ мишенью для аФЛ могут являться отдельные белки, регулирующие коагуляционный каскад, такие как белок С, белок S или тромбомодулин, экспрессирующиеся на мембране ЭК. Имеются данные о том, что моноклональные аКЛ связываются с белком S только в присутствии β-ГШ и кардиолипина. Эти данные позволили высказать предположение о том, что индуцированный β2-ГП1-зависимыми аФЛ дефицит свободного белка S является одним из важных патогенетических механизмов развития тромбозов при АФС.
Акушерская патология
Акушерская патология при АФС также связана с синтезом β2-ГШ-зависимых аФЛ. Полагают, что в основе внутриутробной гибели плода лежит гипоксия, обусловленная недостаточным утероплацентарным кровотоком вследствие тромбоза сосудов плаценты и нарушением имплантации эмбриона. Инфаркты плаценты связывают также с аФЛ-зависимым снижением экспрессии анексина V на поверхности плацентарных ворсинок, способностью аФЛ перекрестно реагировать с клетками трофобласта.
IgG-фракция, выделенная из сыворотки, содержащей ВА, увеличивает синтез плацентарного тромбоксана без компенсаторного увеличения продукции простациклина. Это может иметь значение при развитии акушерской патологии во втором триместре беременности. Кроме того, другие исследования показали, что поликлональные аКЛ ингибируют синтез плацентарного β-хориогонадотропина.
Сосудистые катастрофы (инфаркт миокарда и инсульт) относятся к числу частых причин преждевременной смерти больных СКВ. Среди причин сосудистой патологии при СКВ и других системных ревматических заболеваниях обсуждается вопрос об атеросклеротическом поражении сосудов. Тромбоз мозговых и коронарных артерий — характерные локализации тромбоза у больных с АФС. Наши результаты свидетельствуют о том, что эхокардиографические изменения, отражающие ишемическое поражение миокарда (очаговая акинезия или диффузная гипокинезия), чаще выявляются у тех больных СКВ, в сыворотках которых присутствуют аФЛ, а тромбоз коронарных артерий у мужчин с СКВ — наиболее частая форма артериального тромбоза.
Хорошо известно, что увеличение уровня липопротеида(а)[ЛП(а)] рассматривается как важный фактор риска атеросклеротического поражения сосудов. Поскольку ЛП(а) принимает участие в отложении липидов в сосудистую стенку и имеет структурную гомологию с плазминогеном, он может играть определенную роль в развитии атеротромбоза.
По нашим данным, при СКВ увеличение уровня ЛП(а) более 30 мг% отмечено у 6 (25 %) из 24 больных. При этом тромботические (в первую очередь артериальные) осложнения достоверно чаще наблюдались в группе больных с повышенным, чем с нормальным уровнем ЛП(а) (р=0,02), а титры аКЛ коррелировали с концентрацией ЛП(а). Поражение коронарных артерий (ишемическая болезнь сердца у 2 больных и инфаркт миокарда — у одного больного) наблюдалось только у больных с повышенным уровнем ЛП(а) (р=0,009). Другой механизм атеротромбоза может быть связан с перекисным окислением липопротеидов низкой плотности (ЛНП).
Установлено, что взаимодействие малонового альдегида (конечный продукт перекисного окисления липидов) с лизиновыми остатками аполипопротеина В приводит к формированию аутоантигенного эпитопа, стимулирующего синтез антител к окисленному ЛНП (оЛНП). Увеличение уровня антител к оЛНП ассоциируется с атеросклеротическим поражением коронарных сосудов, прогрессированием атеросклероза каротидных артерий и развитием инфаркта миокарда. Интересно, что поверхностная конфигурация оЛНП, включающая аполипопротеин В и монослой, состоящий из фосфолипидов и холестерина, в определенной степени напоминает антигенный эпитоп, с которым взаимодействуют аФЛ. Последний, как уже отмечалось, образуется в процессе взаимодействия анионных фосфолипидов и β-ГШ.
Имеются данные о том, что антитела к оЛНП часто присутствуют в сыворотках больных СКВ с АФС, причем аФЛ обладают способностью перекрестно реагировать с оЛНП. Совсем недавно было обнаружено, что аФЛ и моноклональные антитела к оЛНП перекрестно реагируют с модифицированным окисленным кардиолипином. Хотя наши результаты и данные других авторов свидетельствуют об отсутствии связи между увеличением уровня антител к оЛНП и развитием тромбозов у больных АФС, установлено, что увеличение концентрации аФЛ и повышенный уровень антител к оЛНП являются независимыми факторами риска коронарного тромбоза, и их одномоментное выявление у одних и тех же больных резко увеличивает риск развития этого осложнения.
Исследования
О важной роли иммунного ответа против оЛНП свидетельствуют данные экспериментальных исследований мышей линии (NZWVBXSB)F1, у которых спонтанно развивается окклюзионное поражение коронарных артерий, а в сыворотках обнаруживаются как аФЛ, так и антитела к оЛНП. При этом моноклональные антитела, полученные при гибридизации селезеночных клеток мышей линии (NZWVBXSB)F1, реагирующие с аФЛ в присутствии β-ГШ, обладают способностью перекрестно реагировать с оЛНП.

Факторы, предрасполагающие к раннему развитию атеротромбоза при системных ревматических заболеваниях
Интересно, что хотя сам 2-ГП1 частично ингибирует захват и протеолитическое расщепление оЛНП макрофагами и, таким образом, обладает определенной антиатерогенной активностью, особенно на фоне окислительного стресса, в присутствии антител к β2-ГШ захват оЛНП макрофагами существенно усиливается. Все эти данные свидетельствуют о тесной патогенетической взаимосвязи между гиперпродукцией аФЛ, окислительным стрессом и развитием сосудистой патологии при ревматических заболеваниях.

Синовиальная оболочка. Гистологические признаки апоптоза. Окраска гематоксилином и эозином Х400
Курация больных АФС представляет сложную проблему. Это обусловлено неоднородностью патогенетических механизмов, лежащих в основе АФС, полиморфизмом клинических проявлений, отсутствием достоверных клинических и лабораторных показателей, позволяющих прогнозировать рецидивирование тромботических нарушений. Полагают, что риск повторных тромбозов особенно высок у лиц молодого возраста, с высоким уровнем аКЛ (β2-ГШ-зависимая популяция антител), ВА или антител к β2-ГШ, наличием рецидивирующих тромбозов и/или акушерской патологии в анамнезе.
Лечение больных АФС основывается на назначении непрямых антикоагулянтов и антиагрегантов (низкие дозы аспирина). Терапия АФС имеет свои особенности, что в первую очередь связано с более высоким риском рецидивирования тромбозов, чем у больных тромбофилией, и необходимостью лечения ведущего заболевания (при вторичном АФС)
Общие принципы лечения АФС
Основные препараты | Вспомогательные препараты | Другие препараты |
Непрямые антикоагулянты Аспирин (низкие дозы) | Антималярийные средства (только при СКВ) Даназол (тромбоцитопения) Внутривенный иммуноглобулин (акушерская патология) Плазмаферез + цнклофосфамид («катастрофический» АФС) | Полиненасыщенные жирные кислоты, ингизы 2, антиоксиданты витамины (Bj2, Bs, фолиевая кислота), тиклопидин, пентоксифиллин гируидин, антикоаглянтные пептиды моноклокальные антитела к тромбоцитам RGD-пептиды, ингибиторы апоптоза, цитокины (ИЛ-3) |
Полагают, что у больных с высоким уровнем аФЛ в сыворотке, но без клинических признаков АФС (в том числе у беременных женщин без акушерской патологии в анамнезе) следует ограничиться назначением небольших доз аспирина (75—100 мг/сут). Однако эти больные требуют тщательного динамического наблюдения, так как риск тромботических осложнений у них весьма высок. По нашему мнению, в схему лечения таких больных целесообразно включение антималярийного препарата плаквенила (200 мг/сут), который широко используется в лечении воспалительных ревматических заболеваний и отличается очень низкой токсичностью.
Установлено, что плаквенил наряду с противовоспалительным действием, обладает антитромботическим (подавляет агрегацию и адгезию тромбоцитов, уменьшает размер тромба) и гиполипидемическим эффектами. Все это дает основание полагать, что лечение плаквенилом (в сочетании с низкими дозами аспирина, а при необходимости и с другими препаратами) показано почти всем больным с АФС. Наличие АФС, и тем более только аФЛ, не является показанием к назначению или увеличению доз глюкокортикостероидов
Применение антикоагулянтов чревато осложнениями, поэтому их назначение требует тщательного лабораторного контроля и динамического наблюдения за больными. Различают 2 группы непрямых антикоагулянтов производные кумарина и индандиона. В настоящее время предпочтение отдается производным кумарина, которые реже вызывают аллергические реакции и дают стабильный антикоагулянтный эффект. В США и многих других странах препаратом выбора является варфарин. Основными непрямыми антикоагулянтами, используемыми в России, из производных кумарина являются инкумар, неодикумарин и др., а также фенилин — производное индандиона.
Контроль за лечением, как известно, осуществляется по протромбиновому времени, что не может считаться теперь достаточно надежным. Для определения протромбинового времени используется тромбопластин, биологическая активность которого зависит от вида ткани и технологии получения. Для стандартизации результатов определения протромбинового времени с применением различных тромбопластинов ВОЗ (1983) рекомендовала использовать международный нормализационный индекс (МНИ).
Некоторым больным, резистентным к антикоагулянтной терапии, требуется достаточно высокая доза варфарина (до 20 мг/сут) для поддержания МНИ в терапевтических пределах — от 2 до 3, хотя наиболее оптимальными при АФС являются значения МНИ, составляющие 3 и 4.
На сегодняшний день стандартом профилактики рецидивирующих потерь плода являются малые дозы аспирина (50—100 мг/сут), которые рекомендуется принимать до, в течение беременности и после рождения ребенка. Во время беременности малые дозы аспирина можно комбинировать с подкожным введением гепарина. Необходимо подчеркнуть, что риск развития гепаринового остеопороза у матери может быть сведен к минимуму при назначении низкомолекулярных гепаринов (фраксипарин, клексан и др.).
Прием непрямых антикоагулянтов должен быть прерван при наступлении беременности из-за их возможных тератогенных влияний на плод. В течение всей беременности необходим мониторинг с помощью ультразвуковых исследований для раннего выявления сосудистой плацентарной недостаточности и дистресс-синдрома у плода.
В отдельных, клинических наблюдениях или небольших открытых. испытаниях сообщается об эффективности плазмафереза, внутривенного введения иммуноглобулина, простациклина, фибринолитических препаратов, препаратов рыбьего жира у женщин с акушерской патологией. Лечение плазмаферезом, высокими дозами ГКС (в том числе пульс-терапия) и цитотоксическими иммунодепрессантами продолжает оставаться основным методом лечения «катастрофического» АФС.
Определенные надежды возлагают на использование тиклопидина и пентоксифиллина, а особенно на внедрение новых методов антикоагулянтной терапии, основанных на использовании аргиналов, гируидинов, антикоагулянтных пептидов, антитромбоцитарных агентов (моноклональные антитела к тромбоцитам, RGD-пептиды). Большой интерес представляет оценка эффективности ингибиторов апоптоза (в том числе антиоксидантов), поскольку развитие апоптоза эндотелиальных клеток является одним из ключевых факторов, обеспечивающих их прокоагулянтные свойства.
Таким образом, в настоящее время АФС следует рассматривать как уникальную модель аутоиммунной тромботической васкулопатии, изучение которой имеет существенное значение для расшифровки взаимоотношений между патологическими процессами, составляющими основу сосудистых изменений при заболеваниях человека, таких как атеросклероз, васкулиты, нарушения свертывания крови и системы иммунитета.
Несмотря на достигнутый прогресс, изучение механизмов развития, клинических особенностей и подходов к лечению сосудистых нарушений продолжает оставаться одной из наиболее актуальных мультидисциплинарных проблем современной медицины, для решения которой необходимо объединение усилий специалистов различных областей медицины — ревматологов, кардиологов, невропатологов, акушеров-гинекологов, гематологов, иммунологов.
В.А.Насонова, Н.В.Бунчук
Опубликовал Константин Моканов
Источник
Антифосфолипидный синдром — аутоиммунная патология, в основе которой лежит образование антител к фосфолипидам, являющимся главными липидными компонентами клеточных мембран. Антифосфолипидный синдром может проявляться венозными и артериальными тромбозами, артериальной гипертензией, клапанными пороками сердца, акушерской патологией (привычным невынашиванием беременности, внутриутробной гибелью плода, гестозом), поражением кожи, тромбоцитопенией, гемолитической анемией. Основными диагностическими маркерами антифосфолипидного синдрома являются Ат к кардиолипину и волчаночный антикоагулянт. Лечение антифосфолипидного синдрома сводится к профилактике тромбообразования, назначению антикоагулянтов и антиагрегантов.
Общие сведения
Антифосфолипидный синдром (АФС) – комплекс нарушений, вызванных аутоиммунной реакцией к фосфолипидным структурам, присутствующим на клеточных мембранах. Заболевание было детально описано английским ревматологом Hughes в 1986 году. Данные об истинной распространенности антифосфолипидного синдрома отсутствуют; известно, что незначительные уровни АТ к фосфолипидам в сыворотке крови обнаруживаются у 2-4% практически здоровых лиц, а высокие титры – у 0,2%. Антифосфолипидный синдром в 5 раз чаще диагностируется среди женщин молодого возраста (20-40 лет), хотя заболеванием могут страдать мужчины и дети (в т. ч. новорожденные). Как мультидисциплинарная проблема, антифосфолипидный синдром (АФС) привлекает внимание специалистов в области ревматологии, акушерства и гинекологии, кардиологии.
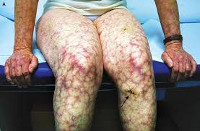
Антифосфолипидный синдром
Причины
Основополагающие причины развития антифосфолипидного синдрома неизвестны. Между тем, изучены и определены факторы, предрасполагающие к повышению уровня антител к фосфолипидам. Так, транзиторное нарастание антифосфолипидных антител наблюдается на фоне вирусных и бактериальных инфекций (гепатита С, ВИЧ, инфекционного мононуклеоза, малярии, инфекционного эндокардита и др.). Высокие титры антител к фосфолипидам обнаруживаются у пациентов с системной красной волчанкой, ревматоидным артритом, болезнью Шегрена, узелковым периартериитом, аутоиммунной тромбоцитопенической пурпурой.
Гиперпродукция антифосфолипидных антител может отмечаться при злокачественных новообразованиях, приеме лекарственных средств (психотропных препаратов, гормональных контрацептивов и др.), отмене антикоагулянтов. Имеются сведения о генетической предрасположенности к повышенному синтезу антител к фосфолипидам у лиц-носителей антигенов HLA DR4, DR7, DRw53 и у родственников больных антифосфолипидным синдромом. В целом иммунобиологические механизмы развития антифосфолипидного синдрома требуют дальнейшего изучения и уточнения.
В зависимости от структуры и иммуногенности различают «нейтральные» (фосфатидилхолин, фосфатидилэтаноламин) и «отрицательно заряженные» (кардиолипин, фосфатидилсерин, фосфатидилинозитол) фосфолипиды. К классу антифосфолипидных антител, вступающих в реакцию с фосфолипидами, относятся волчаночный антикоагулянт, Ат к кардиолипину, бета2-гликопротеин-1-кофакторзависимые антифосфолипиды и др. Взаимодействуя с фосфолипидами мембран клеток эндотелия сосудов, тромбоцитов, нейтрофилов, антитела вызывают нарушение гемостаза, выражающиеся в склонности к гиперкоагуляции.
Классификация
С учетом этиопатогенеза и течения различают следующие клинико-лабораторные варианты антифосфолипидного синдрома:
- первичный – связь с каким-либо фоновым заболеванием, способным индуцировать образование антифосфолипидных антител, отсутствует;
- вторичный — антифосфолипидный синдром развивается на фоне другой аутоиммунной патологии;
- катастрофический – острая коагулопатия, протекающая с множественными тромбозами внутренних органов;
- АФЛ-негативный вариант антифосфолипидного синдрома, при котором серологические маркеры заболевания (Ат к кардиолипину и волчаночный антикоагулянт) не определяются.
Симптомы антифосфолипидного синдрома
Согласно современным взглядам, антифосфолипидный синдром представляет собой аутоиммунную тромботическую васкулопатию. При АФС поражение может затрагивать сосуды различного калибра и локализации (капилляры, крупные венозные и артериальные стволы), что обусловливает чрезвычайно разнообразный спектр клинических проявлений, включающий венозные и артериальные тромбозы, акушерскую патологию, неврологические, сердечно-сосудистые, кожные нарушения, тромбоцитопению.
Наиболее частым и типичным признаком антифосфолипидного синдрома являются рецидивирующие венозные тромбозы: тромбоз поверхностных и глубоких вен нижних конечностей, печеночных вен, воротной вены печени, вен сетчатки. У больных с антифосфолипидным синдромом могут возникать повторные эпизоды ТЭЛА, легочная гипертензия, синдром верхней полой вены, синдром Бадда-Киари, надпочечниковая недостаточность. Венозные тромбозы при антифосфолипидном синдроме развиваются в 2 раза чаще артериальных. Среди последних преобладают тромбозы церебральных артерий, приводящие к транзиторным ишемическим атакам и ишемическому инсульту. Прочие неврологические нарушения могут включать мигрень, гиперкинезы, судорожный синдром, нейросенсорную тугоухость, ишемическую нейропатию зрительного нерва, поперечный миелит, деменцию, психические нарушения.
Поражение сердечно-сосудистой системы при антифосфолипидном синдроме сопровождается развитием инфаркта миокарда, внутрисердечного тромбоза, ишемической кардиомиопатии, артериальной гипертензии. Довольно часто отмечается поражение клапанов сердца – от незначительной регургитации, выявляемой с помощью ЭхоКГ, до митрального, аортального, трикуспидального стеноза или недостаточности. В рамках диагностики антифосфолипидного синдрома с сердечными проявлениями требуется проведение дифференциальной диагностики с инфекционным эндокардитом, миксомой сердца.
Почечные проявления могут включать как незначительную протеинурию, так и острую почечную недостаточность. Со стороны органов ЖКТ при антифосфолипидном синдроме встречаются гепатомегалия, желудочно-кишечные кровотечения, окклюзия мезентериальных сосудов, портальная гипертензия, инфаркт селезенки. Типичные поражения кожи и мягких тканей представлены сетчатым ливедо, ладонной и подошвенной эритемой, трофическими язвами, гангреной пальцев; опорно-двигательного аппарата — асептическими некрозами костей (головки бедренной кости). Гематологическими признаками антифосфолипидного синдрома служат тромбоцитопения, гемолитическая анемия, геморрагические осложнения.
У женщин АФС часто выявляется в связи с акушерской патологией: повторным самопроизвольным прерыванием беременности в различные сроки, задержкой внутриутробного развития плода, фетоплацентарной недостаточностью, гестозом, хронической гипоксией плода, преждевременными родами. При ведении беременности у женщин с антифосфолипидным синдромом акушер-гинеколог должен учитывать все возможные риски.
Диагностика
Антифосфолипидный синдром диагностируется на основании клинических (сосудистый тромбоз, отягощенный акушерский анамнез) и лабораторных данных. Основные иммунологические критерии включают выявление в плазме крови средних или высоких титров Ат к кардиолипину класса IgG/IgM и волчаночного антикоагулянта дважды в течение шести недель. Диагноз считается достоверным при сочетании, по меньшей мере, одного основного клинического и лабораторного критерия. Дополнительными лабораторными признаками антифосфолипидного синдрома являются ложноположительная RW, положительная реакция Кумбса, повышение титра антинуклеарного фактора, ревматоидного фактора, криоглобулинов, антител к ДНК. Также показано исследование ОАК, тромбоцитов, биохимического анализа крови, коагулограммы.
Беременные с антифосфолипидным синдромом нуждаются в мониторинге показателей свертывающей системы крови, проведении динамического УЗИ плода и допплерографии маточно-плацентарного кровотока, кардиотографии. Для подтверждения тромбозов внутренних органов выполняется УЗДГ сосудов головы и шеи, сосудов почек, артерий и вен конечностей, глазных сосудов и др. Изменения створок сердечных клапанов выявляются в процессе ЭхоКГ.
Дифференциально-диагностические мероприятия должны быть направлены на исключение ДВС-синдрома, гемолитико-уремического синдрома, тромбоцитопенической пурпуры и др. Учитывая полиорганность поражения, диагностика и лечение антифосфолипидного синдрома требуют объединения усилий врачей различных специальностей: ревматологов, кардиологов, неврологов, акушеров-гинекологов и др.
Лечение антифосфолипидного синдрома
Основной целью терапии антифосфолипидного синдрома служит предотвращение тромбоэмболических осложнений. Режимные моменты предусматривают умеренную физическую активность, отказ от долгого нахождения в неподвижном состоянии, занятий травматичными видами спорта и длительных авиаперелетов. Женщинам с антифосфолипидным синдромом не следует назначать пероральные контрацептивы, а перед планированием беременности необходимо обязательно обратиться к акушеру-гинекологу. Беременным пациенткам в течение всего периода гестации показан прием малых доз глюкокортикоидов и антиагрегантов, введение иммуноглобулина, инъекции гепарина под контролем показателей гемостазиограммы.
Медикаментозная терапия при антифосфолипидном синдроме может включать назначение непрямых антикоагулянтов (варфарина), прямых антикоагулянтов (гепарина, надропарина кальция, эноксапарина натрия), антиагрегантов (ацетилсалициловой кислоты, дипиридамола, пентоксифиллина). Профилактическая антикоагулянтная или антиагрегантная терапия большинству больных с антифосфолипидным синдромом проводится длительно, а иногда пожизненно. При катастрофической форме антифосфолипидного синдрома показано назначение высоких доз глюкокортикоидов и антикоагулянтов, проведение сеансов плазмафереза, переливание свежезамороженной плазмы и т. д.
Прогноз
Своевременная диагностика и профилактическая терапия позволяют избежать развития и рецидивирования тромбозов, а также надеяться на благоприятный исход беременности и родов. При вторичном антифосфолипидном синдроме важным представляется контроль за течением основной патологии, профилактика инфекций. Прогностически неблагоприятными факторами служат сочетание антифосфолипидного синдрома с СКВ, тромбоцитопения, быстрое нарастание титра Ат к кардиолипину, стойкая артериальная гипертензия. Все пациенты с диагнозом «антифосфолипидный синдром» должны находиться под наблюдением ревматолога с периодическим контролем серологических маркеров заболевания и показателей гемостазиограммы.
Источник
