Хронического эндометрита или синдрома ашермана
Статья посвящена современным возможностям в лечении внутриматочных синехий (синдрома Ашермана)
Внутриматочные синехии, или синдром Ашермана (СА), — патологическое состояние, характеризующееся образованием спаек и выростов эндометрия с его склерозом и фиброзом. Заболевание названо в честь Д. Ашермана – гинеколога, подробно описавшего и исследовавшего данную патологию. Внутриматочные спайки (синехии) представляют собой соединительнотканные сращения, спаивающие стенки матки и вызывающие ее деформацию. При наличии синехий нормальный эндометрий подвергается атрофической трансформации [1].
Истинное понятие СА включает в себя нарушение менструальной (гипоменорея, аменорея) и детородной функций, обусловленное наличием внутриматочных синехий [2]. Основными клиническими проявлениями этой патологии являются: альгодисменорея, гипоменорея, в тяжелых случаях – аменорея; гематометра, или гематосальпингс; привычное невынашивание беременности, повторные выкидыши, вторичное бесплодие. СА может сопутствовать эндометриоз различной степени тяжести [3]. В 61,5% случаев внутриматочные синехии являются причинами бесплодия [4]. Бесплодие и гипоменорея – наиболее частые клинические проявления СА (55,1% и 32,1% случаев соответственно) [4].
Наиболее частой причиной СА служат предшествующие механические травмы базального эндометрия. Травмирование эндометрия может происходить вследствие хирургического прерывания беременности, использования внутриматочных контрацептивов, диагностических выскабливаний полости матки при маточных кровотечениях или полипах эндометрия, операций на полости матки (миомэктомия, метропластика, конизация шейки матки). Повреждение эндометрия может усугубляться присоединением инфекции во время раневой фазы с развитием эндометрита [5]. Чем больше период задержки плодных оболочек после родов или выкидыша, тем выше вероятность возникновения заболевания. Также имеет значение число процедур: после однократного выскабливания полости матки риск составляет около 16%, а 3 и более процедуры увеличивают вероятность возникновения СА до 32% [3].
В диагностике внутриматочных синехий данные гинекологического исследования неспецифичны. УЗИ малого таза при СА малоинформативно: эхоскопическая картина может быть представлена нечеткими контурами эндометрия, в случае гематометры – анэхогенным образованием в полости матки. Проведение гидросонографии позволяет более четко определять наличие внутриматочных сращений. Гистеросальпингография выявляет одиночные либо множественные дефекты наполнения, имеющие лакунообразную форму и различные размеры. При плотных множественных внутриматочных синехиях полость матки на рентгенограмме выглядит многокамерной, с мелкими, соединяющими отдельные камеры протоками. Однако нередко гистеросальпингография сопровождается ложноположительными результатами из-за наличия в матке слизи, искривлений, обрывков эндометрия.
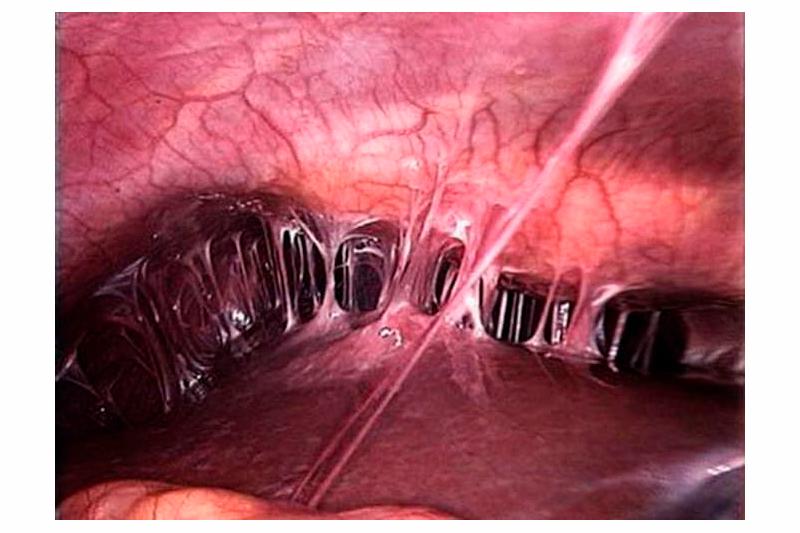
«Золотым стандартом» диагностики внутриматочных синехий является гистероскопия. При гистероскопии внутриматочные синехии определяются как белесоватые бессосудистые тяжи разной плотности и длины, соединяющие стенки матки, обнаруживается облитерация или деформация полости матки.
Целью лечебных мероприятий при СА служит малотравматичное устранение внутриматочных сращений с последующим восстановлением менструальной функции и фертильности. На первом этапе показано проведение гистероскопии с целью рассечения спаек под визуальным контролем. Во избежание перфорации матки рекомендуется использовать тонкие офисные гистероскопы, т. к. у таких пациенток имеется полная или частичная атрезия цервикального канала, которая делает невозможными любые хирургические манипуляции без предварительного рассечения синехий цервикального канала при помощи эндоскопических ножниц.
Разделение синехий в зависимости от их плотности производится тубусом гистероскопа, эндоскопическими ножницами, щипцами, гистерорезектоскопом, лазером. Нельзя разрушать синехии вслепую при помощи выскабливания стенок полости матки и цервикального канала кюреткой, т. к. это наносит дополнительную травму уже скомпрометированного эндометрия! Для исключения перфорации матки используется контроль с помощью УЗИ или лапароскопии.
После операционного этапа пациентке с СА назначается циклическая гормонотерапия эстрогенами и гестагенами, направленная на стимуляцию восстановления эндометрия и его циклической трансформации. Назначение комбинированных оральных контрацептивов при этой патологии нецелесообразно, поскольку данная группа препаратов способствует атрофическим изменениям эндометрия.
При инфекционной этиологии СА производится бактериологическое и вирусологическое исследование содержимого полости матки (биоптат, материал вакуумной биопсии) с последующей антибактериальной терапией.
Даже после самого грамотного (бережного и тщательного разрушения) внутриматочных синехий риск рецидивов остается высоким. Средняя частота возникновения рецидива после оперативного лечения внутриматочных синехий – 28% [1].
Для профилактики рецидива в полость матки после операции вводят гелеобразные наполнители, препятствующие контакту стенок и образованию спаек. Примером такого противоспаечного барьера может служить изделие медицинского назначения Антиадгезин (АО «Нижфарм»), представляющий собой гель из высокоочищенной натриевой соли гиалуроновой кислоты, полученной без использования генномодифицированных микроорганизмов [6]. Терапевтический эффект геля Антиадгезин связан с созданием искусственного временного барьера между поврежденными тканями, что обеспечивает эффективное разделение поверхностей на время их заживления. После аппликации геля Антиадгезин в области операционного поля он прилипает к анатомическим поверхностям, не растекаясь, и образует вязкое смазывающее покрытие, которое обеспечивает скольжение соседних поврежденных поверхностей и предупреждает их слипание. Антиадгезин является биодеградируемым покрытием, которое разделяет соприкасающиеся поверхности только на период критической фазы раневого заживления и послеоперационного спайкообразования, продолжающийся в течение 7 дней, не влияя при этом на нормально протекающие процессы регенерации. После применения гель полностью рассасывается [6].
Средние показатели эффективности лечения коррелируют с частотой наступления беременности. При легкой степени заболевания беременность наблюдается у 93% пациенток, при средней — у 78%. Лечение тяжелой степени СА дает возможность забеременеть 57% женщин. Однако рождение здорового ребенка наблюдается в 81, 66 и 32% случаев соответственно тяжести заболевания [1].
Таким образом, внутриматочные синехии и СА как крайне тяжелый их вариант являются многокомпонентной проблемой, требующей комплексного подхода. Тактика ведения таких женщин должна включать диагностический модуль (с использованием преимущественно тонких офисных гистероскопов), щадящую внутриматочную хирургию с введением в полость матки противоспаечных барьеров и послеоперационную реабилитацию с использованием гормональных препаратов, направленных на стимуляцию пролиферации эндометрия, а также на профилактику рецидивов спаечного процесса.
Клинический пример № 1
Пациентка П., 30 лет, поступила в клинику г. Красноярска с жалобами на гипоменорею, постепенно перешедшую в аменорею, вторичное бесплодие. В анамнезе – выскабливание полости матки по поводу неразвивающейся беременности. По результатам УЗИ органов малого таза: эндометрий неравномерной толщины, М-ЭХО до 13 мм с гиперэхогенными фрагментами. Пациентка поступила для планового проведения гистероскопии. Нами был использован офисный гистероскоп B.I.O.H (Storz). При проведении цервикоскопии выявлена полная атрезия цервикального канала за счет грубых синехий. С использованием эндоскопических ножниц с большими техническими сложностями проведено рассечение синехий цервикального канала, гистероскоп был продвинут к полости матки. При осмотре: полость матки резко уменьшена, в виде туннеля визуализируется левое маточное устье. Для исключения аномалии развития половых органов было решено провести лапароскопию, при этом визуализировано тело матки нормальных размеров и формы, обе маточные трубы – без видимой патологии, на обоих яичниках и брюшине малого таза – множественные очаги эндометриоза. Последние коагулированы биполярным электродом. При проведении последующей гистероскопии было выполнено рассечение поперечной синехии полости матки с помощью эндоскопических ножниц (крайне редкий вариант формирования спайки в полости матки). Анатомия полости матки была восстановлена: оба маточных устья стали визуализироваться, полость матки – чуть больше нормы. Эндометрий очень тонкий, с участками фиброзирования и резко усиленным сосудистым рисунком. После адгезиолизиса в полость матки было введено 5 г геля Антиадгезин. Для профилактики формирования СА в послеоперационном периоде была назначена циклическая гормональная терапия на 3 менструальных цикла с использованием препаратов для менопаузальной гормональной терапии, а также курс введения противоспаечного геля Антиадгезин № 5 с интервалом от 3 до 7 дней. В последующем у пациентки отмечено восстановление менструальной функции. Через 3 мес. при проведении контрольной офисной гистероскопии полость матки имела нормальную анатомию, синехии отсутствовали, эндометрий соответствовал фазе менструального цикла. В настоящее время пациентка планирует спонтанную беременность.
Клинический пример № 2
Пациентка К., 32 года, обратилась в профессорскую клинику г. Красноярска в мае 2016 г. с жалобами на вторичное бесплодие. В анамнезе 3 беременности: в 2012 г. при сроке беременности 30–31 нед. проведено экстренное кесарево сечение по поводу преждевременной отслойки нормально расположенной плаценты. Ребенок умер. Далее дважды имели место неразвивавшиеся беременности: в 2013 г. в сроке 8–9 нед. и в 2014 г. в сроке 10 нед., по поводу чего пациентке были проведены выскабливания полости матки. Все беременности возникали спонтанно.
По результатам УЗИ органов малого таза (на 7-й день менструального цикла): эхографически определяются 2 М-эха: справа – высотой 5 мм, слева – 4 мм. Справа эндометрий неравномерной толщины, с гиперэхогенными фрагментами. Ультразвуковое заключение: двурогая матка. Синехии в полости матки? Хронический эндометрит?
Пациентка поступила для проведения лапароскопии и гистероскопии. При проведении лапароскопии: в полости малого таза визуализирована одна матка, широкая, чуть больше нормальных размеров. Область рубца на матке и придатки – без видимой патологии. Спаек в полости малого таза не выявлено. При проведении хромосальпингоскопии – обе маточные трубы свободно проходимы для контраста. Далее была проведена гистероскопия. Первоначально с целью диагностики нами был использован офисный гистероскоп B.I.O.H (Storz). При проведении цервикоскопии – цервикальный канал без особенностей. Полость матки разделена на 2 гемиполости за счет очень широкой внутриматочной перегородки, практически доходящей до внутреннего зева. В правой гемиполости имеются множественные линейные синехии, частично облитерирующие ее, но устье правой маточной трубы свободно. Левая гемиполость несколько меньше правой, устье левой трубы свободно. Область рубца на матке – без особенностей (ниш и деформаций нет).
С использованием эндоскопических ножниц выполнено рассечение синехий в правой гемиполости матки. Далее проведено расширение цервикального канала до № 10 расширителями Гегара. В полость матки введен монополярный гистерорезектоскоп (Storz). При помощи электрода (прямой петли) внутриматочная перегородка полностью рассечена. При контрольном осмотре: полость матки нормальных размеров, устья обеих маточных труб свободные. Эндометрий высотой 2–3 мм (соответствует дню менструального цикла), но с резко усиленным сосудистым рисунком (по типу «земляничного поля»).
По завершении операции в полость матки было введено 3 г геля Антиадгезин. Для профилактики формирования СА в послеоперационном периоде были назначены циклическая гормональная терапия на 2 менструальных цикла с использованием препаратов для менопаузальной гормональной терапии, а также курс введения противоспаечного геля Антиадгезин № 3 с интервалом 5–7 дней. Через 2 мес. при проведении контрольной офисной гистероскопии полость матки имела нормальную анатомию, синехии отсутствовали, эндометрий соответствовал фазе менструального цикла. В настоящее время пациентке разрешено планирование беременности.
Таким образом, внутриматочные синехии (и как крайне тяжелый их вариант – СА) являются многокомпонентной проблемой, требующей комплексного подхода. Тактика ведения таких женщин должна включать диагностический модуль (с использованием преимущественно тонких офисных гистероскопов), щадящую внутриматочную хирургию и послеоперационную реабилитацию с использованием гормональных препаратов, направленных на стимуляцию пролиферации эндометрия, а также профилактику рецидивов спаечного процесса в полости матки при помощи внутриматочного использования современных противоспаечных барьеров (примером которых является Антиадгезин). И только комплексный подход, направленный на все звенья патогенеза, позволит излечить таких пациенток, избежать рецидива и вернуть менструальную и фертильную функции.
Источник
Синдром Ашермана, или внутриматочные синехии — это патологическое состояние, характеризующееся образованием спаек и выростов эндометрия с его склерозом и фиброзом. Заболевание известно также как синдром Фритча, травматическая атрофия эндометрия или склероз эндометрия. Заболевание названо в честь гинеколога, подробно описавшего и исследовавшего данную патологию, Джозефа Ашермана. Впервые синдром был описан в 1894 году немецким врачом-гинекологом — Генрихом Фритчем.
Содержание статьи:
- Классификация синдрома Ашермана
- Заболеваемость
- Внутриматочные синехии и беременность
- Причины образования внутриматочных синехий
- Симптомы синдрома Ашермана
- Диагностика синдрома Ашермана
- Лечение синдрома Ашермана (внутриматочных синехий)
- Прогноз при лечении синдрома Ашермана
- Профилактика синдрома Ашермана

Классификация синдрома Ашермана
В зависимости от степени повреждения базального слоя эндометрия спайки могут быть разного характера и протяжённости. В основном выделяют 3 степени тяжести заболевания:
- лёгкая степень: сращения состоят из тонкой ткани базального слоя, легко разрушаются при контакте с рабочей частью эндоскопа, занимают менее 25% полости матки;
- средняя степень: сращения фиброзно-мышечные, прочно спаяны со слизистой оболочкой матки, занимают большую часть полости матки;
- тяжёлая степень: сращения плотные, состоят из склерозированной соединительной ткани, заполняют более 75% полости матки, блокируют устья маточных труб, дно матки.
Заболеваемость
Синдром Ашермана возникает у женщин всех рас с одинаковой частотой. После выскабливания полости матки у родивших женщин риск возникновения заболевания составляет 25%. Неразвивающаяся, или замершая беременность, чаще приводит к возникновению данной патологии и составляет до 30% случаев. При обычном выкидыше с задержкой частей плодных оболочек и последующего выскабливания риск заболевания не превышает 7%.
Чем больше период задержки плодных оболочек после родов или выкидыша, тем выше вероятность возникновения заболевания. Также имеет значение число процедур: после однократного выскабливания риск составляет 16%, а 3 и более процедуры увеличивают вероятность возникновения синдрома Ашермана до 32%.
Внутриматочные синехии и беременность
При синдроме Ашермана серьёзно страдает репродуктивная функция. Из-за синехий облитерируется полость матки и нарушается проходимость маточных труб. В тяжёлых случаях вся полость матки перекрыта сращениями, стенки слипаются, что приводит к невозможности зачатия и имплантации эмбриона. Более того, эндометрий теряет способность отвечать на циклические колебания уровня эстрогенов, в результате чего возникает вторичное бесплодие и возможна аменорея, то есть отсутствие менструаций.
Синехии в области шейки матки приводят к скоплению и задержке менструальных выделений в полости матки. Об этом свидетельствуют боли и скудные выделения во время менструации (олигоменорея). Возможные нарушения менструального цикла обычно свидетельствуют о тяжёлой форме заболевания.
В зависимости от тяжести заболевания эффект на репродуктивную функцию может варьировать от осложнённого течения беременности до повторяющихся спонтанных абортов, выкидышей и вторичного бесплодия. Возможны преждевременные роды, разрыв матки на поздних сроках, истинное приращение плаценты и другие патологии беременности.
Причины образования внутриматочных синехий
Матка — полый мышечный орган, состоящий из 3 слоёв. Снаружи она покрыта брюшиной. Стенка матки образована гладкомышечной тканью. Полость матки выстилает эндометрий, который состоит из поверхностного функционального и глубокого базального слоёв. Эндометрий под действием женских половых гормонов претерпевает циклические изменения, зависящие от фазы менструального цикла. Ближе к фазе овуляции, когда вероятность зачатия наиболее высока, слизистая оболочка матки утолщается. В клетках эндометрия идёт активный синтез питательных и биологически активных веществ. При попадании оплодотворённой яйцеклетки происходит имплантация — погружение эмбриона в толщу слизистой оболочки матки. Контакт оболочек эмбриона с нормальным эндометрием — вот важное условие для успешного начала беременности. Если беременность не наступила, функциональный слой полностью отторгается во время менструации. С началом нового цикла он начинает нарастать заново, регенерируя с помощью стволовых клеток базального слоя.
Внутриматочные синехии — это выросты, или спайки, склерозированного эндометрия, нарушающие нормальную анатомию и физиологию слизистой оболочки матки.
Основной причиной синдрома Ашермана является повреждение и травма базального слоя в ходе выполнения гинекологических процедур (дилатация полости матки, лечебно-диагностическое выскабливание полости матки, кесарево сечение, операции на матке). Реже внутриматочные синехии образуются после эндометрита — воспаления слизистой оболочки матки.
Симптомы синдрома Ашермана
Клиника синдрома Ашермана обычно не влияет на общее состояние и самочувствие больных. Основные симптомы связаны со спаечным процессом и его влиянием на функцию репродуктивной системы. Среди них можно выделить:
- Альгодисменорея, то есть расстройства менструальной функции: болезненные длительные обильные или скудные месячные.
- Олигоменорея, гипоменорея, в тяжёлых случаях аменорея: уменьшение количества и длительности менструаций.
- Гематометра, или гематосальпингс — скопление менструальных выделений в полости матки или маточных труб из-за сращений в области шейки матки, блокирующих цервикальный канал. В результате возможен выраженный болевой синдром, возникающий во время менструации. Попадание крови через маточные трубы в брюшную полость вызывает сильные боли, напоминающие картину острого живота.
- Привычное невынашивание беременности, повторные выкидыши без причин, вторичное бесплодие.
Синдрому Ашермана может сопутствовать эндометриоз (аденомиоз) различной степени тяжести. Эндометриоз — эктопический рост функционального слоя эндометрия вне полости матки. Такая комбинация ухудшает прогноз и перспективы лечения и сильнее влияет на репродуктивную функцию.
Диагностика синдрома Ашермана
В основном для диагностики используются инструментальные методы исследования, позволяющие визуализировать полость матки изнутри. Для поиска в нужном направлении необходимо учитывать данные акушерского анамнеза — число беременностей, родов, абортов и других медицинских процедур.
УЗИ традиционно считается самым доступным и неинвазивным методом исследования органов малого таза. Более информативным вариантом сонографии является трансвагинальное ультразвуковое исследование. Для точной диагностики необходимо проводить исследование в разных фазах менструального цикла.
Золотым стандартом диагностики внутриматочных синехий является эндоскопическое исследование полости матки или гистероскопия. В полость матки через цервикальный канал вводится эндоскоп, что позволяет видеть состояние эндометрия в режиме реального времени на мониторе. Кроме того, диагностическая гистероскопия может предшествовать непосредственному эндоскопическому вмешательству с целью удаления сращений. Это лучший способ оценить степень распространённости процесса и определить характер спаек и возможность их удаления.
В некоторых случаях проводится гистеросальпингография. Этот метод в основном применяется для оценки проходимости маточных труб.
Результаты исследования необходимо сочетать с клиникой, предыдущими попытками лечения и акушерским анамнезом, что позволяет прогнозировать результаты и эффективность лечения.
Лечение синдрома Ашермана (внутриматочных синехий)
Легкая и средняя степень тяжести заболевания обычно хорошо поддаётся лечению. В тяжёлых случаях синдром Ашермана и возникающее бесплодие можно преодолеть только с помощью суррогатного материнства. В некоторых случаях (при расположении синехий на ограниченном участке матки) эффективно экстракорпоральное оплодотворение.
Удаление (диссекция) синехий проводится методом оперативной гистероскопии. Метод не требует общего наркоза и не имеет осложнений, характерных для обычных операций. Через каналы в эндоскопической установке можно провести микроинструменты. Удаление и рассечение синехий микроножницами проводится с осторожностью из-за вероятности нанесения дополнительных травм. Особую опасность представляет перфорация стенки матки во время проведения операции. Технически это нелёгкая операция. В тяжёлых случаях синехии заполняют всю полость матки и плотно сращены со стенками, а при рассечении кровоточат.
Высок процент рецидивов. У части больных после оперативного лечения вновь возникают внутриматочные сращения. Для профилактики рецидива в полость матки после операции вводят гелеобразные наполнители, препятствующие контакту стенок и образованию спаек. Средняя частота возникновения рецидива после оперативного лечения — 28%.
В послеоперационный период назначают антибиотики для профилактики инфекционных осложнений. Медикаментозное лечение в послеоперационный период обязательно дополняют гормональной терапией. Циклическое назначение эстрогенов и прогестинов проводят для стимуляции роста эндометрия.
Через некоторое время после операции проводят повторную гистероскопию для оценки результатов лечения и своевременной диагностики рецидива.
Прогноз при лечении синдрома Ашермана
Средние показатели эффективности лечения коррелируют с частотой наступления беременности. При лёгкой степени заболевания беременность наблюдается у 93% пациенток, при средней — у 78%. Лечение тяжёлой степени синдрома Ашермана даёт возможность забеременеть 57% женщин. Однако рождение здорового ребёнка наблюдается в 81, 66 и 32%% случаев соответственно тяжести заболевания.
Возраст пациенток также имеет прогностическое значение. 66% женщин моложе 35 лет, имеющие тяжёлую степень синдрома Ашермана, способны зачать ребёнка после лечения. Однако у женщин старше 35 этот показатель не превышает 24%.
Профилактика синдрома Ашермана
Выскабливание полости матки острой гинекологической кюреткой или вакуумная аспирация — это процедуры, проводящиеся практически вслепую, врач во время манипуляций полагается только на свои ощущения. Ткани эндометрия под действием эстрогенов при беременности мягкие и легко травмируются. В результате лечебное или диагностическое выскабливание практически всегда сопровождается повреждением базального слоя эндометрия в той или иной степени.
Альтернативой выскабливанию при абортах или выкидышах является применение лекарственных препаратов для стимуляции родовой деятельности (терапевтический аборт). Однако эффективность данного метода 80-85%. В 10-15% случаях после терапевтического аборта происходит задержка частей плодных оболочек, что вновь требует проведение выскабливания.
Возможно, безопасность и эффективность лечебно-диагностического выскабливания полости матки можно увеличить, если проводить процедуру под контролем УЗИ.
Источник
