Гангренозная пиодермия как паранеопластический синдром
Гангренозная пиодермия (ГП) является редким хроническим заболеванием, относимым к группе нейтрофильных дерматозов. ГП регистрируют с частотой 3—10 случаев на 1 млн населения в год. Женщины страдают чаще мужчин. Наиболее часто заболевание регистрируют в возрасте от 20 до 50 лет.
Впервые ГП была описана французским дерматологом L. Brocq под названием «phagedenismegeometrique», а современный термин ввели американские дерматологи A. Brunsting, W. Goeckerman и P. O’Leary в 1930 г. [1].
Этиопатогенез ГП до сих пор окончательно не установлен. В большинстве случаев (25—50%) заболевание оказывается идиопатическим, в остальных сочетается с различными по природе нозологиями: болезнью Крона, лейкозами, ревматоидным артритом и другими [2]. ГП также может стать следствием лекарственной терапии, в частности ароматическими ретиноидами. Что касается злокачественных новообразований, то лишь у нескольких больных ГП была расценена в качестве паранеопластического процесса при раке простаты, толстого кишечника, бронхов, молочной железы.
В патогенезе заболевания отводят роль аберрантной иммунной реакции. В свете последних данных также необходимо отметить участие в патогенезе генетической предрасположенности, о чем свидетельствуют недавно описанные синдромы PAPA, PASH и PASS. Определенное значение в патогенезе заболевания имеет патергия.
В настоящее время выделяют несколько форм ГП: классическую (язвенная), пустулезную, вегетирующий пиодерматит (пиостоматит), поверхностную гранулематозную (злокачественная) и буллезную (буллезно-геморрагическая).
Буллезно-геморрагическая гангренозная пиодермия (БГП) — это редкая атипично протекающая форма Г.П. Описана H. Perry и R. Winkelmann [3] в 1972 г. у больных лейкозами. В последующем подобные наблюдения ассоциировали в основном с миелодиспластическими синдромами [4—6]. В единичных сообщениях отмечено сочетание БГП с воспалительными заболеваниями кишечника, бронхиальной астмой или раком легкого [7—9].
Кожный процесс начинается с появления неизъязвленных узлов или бляшек красно-коричневого цвета или пузырей с серозным либо геморрагическим содержимым. Элементы почти всегда крупные (до 15—18 см в поперечнике). Эффлоресценции быстро изъязвляются с образованием поверхностных дефектов с фиолетово-красным валиком или более мелких пузырей по периферии. В дальнейшем возможно постепенное расширение площади язв или их спонтанная эпителизация с образованием атрофических рубцов и одновременное появление новых элементов, подвергающихся аналогичной эволюции.
Из-за разнообразных проявлений и локализации постановка диагноза нередко оказывается затруднительной. ГП может симулировать синдром Свита, некротизирующий фасциит, неоплазии, глубокие микозы, патомимию, трофические язвы и другие патологические процессы. В диагностике ГП предложено выделять главные и малые критерии. К главным критериям относят: быстро прогрессирующие эксцентрически растущие болезненные язвы неправильной формы с элевирующими, фиолетового цвета краями; отсутствие специфических причин изъязвления кожи (например, бактериальной инфекции, сифилиса, туберкулеза, глубоких микозов).
К малым критериямпредлагают относить: наличие феномена патергии в анамнезе или клинически крибриформных рубцов (неправильная форма с неровным рельефом и неравномерной пигментацией); ассоциацию язвенных дефектов с гематологическими заболеваниями, воспалительными процессами в желудочно-кишечном тракте, неоплазиями и другими; гистологические признаки (воспаление, стерильный нейтрофильный инфильтрат, лимфоцитарный васкулит); быструю положительную динамику при назначении кортикостероидов.
Приводим клинический случай.
Больной Т., 63 лет, пенсионер, поступил в клинику кожных болезней с жалобами на болезненные высыпания геморрагического характера на коже туловища и верхних конечностей, повышение температуры тела до 38 °C. Считает себя больным с января 2012 г., когда впервые отметил вечерние подъемы температуры, появление немногочисленных высыпаний на коже туловища и снижение массы тела на 12 кг в период с января по март 2012 г.
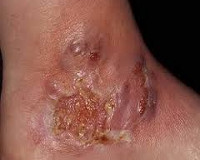
При поступлении кожный патологический процесс носил распространенный характер. Высыпания ложно полиморфные, состоят из везикуло-пустулезных, пузырных и корковых элементов геморрагического характера с преимущественной локализацией на туловище и верхних конечностях. Начальными элементами сыпи были отечные бляшки с синеватой окраской в центре и зоной эритемы в окружности. В дальнейшем вследствие нарастания экссудации они превращались в крупные пузыри с плоской покрышкой и геморрагическим содержимым (рис. 1). Из-за плотности покрышки пузыри обычно не вскрывались, а ссыхались в корку коричневато-красного цвета, под которой происходило поверхностное изъязвление кожи. Эволюция элементов заканчивалась формированием атрофических рубцов с неровным рельефом поверхности (рис. 2).
 Рис. 1. Буллезная геморрагическая гангренозная пиодермия, типичный элемент на высоте развития.
Рис. 1. Буллезная геморрагическая гангренозная пиодермия, типичный элемент на высоте развития.
 Рис. 2. Буллезная геморрагическая гангренозная пиодермия, элементы сыпи на разных стадиях эволюции.
Рис. 2. Буллезная геморрагическая гангренозная пиодермия, элементы сыпи на разных стадиях эволюции.
Общий анализ крови: умеренная анемия — 3,65·1012/л, СОЭ — 33 мм/ч.
УЗИ щитовидной железы: признаки узловатых изменений щитовидной железы, фиброзное округлое образование в правой доле 3,4×4,1 мм.
Уровень тиреотропного гормона соответствует норме.
Миелограмма костного мозга: резкая задержка созревания гранулоцитов, раздражение мегакариоцитарного ростка, лимфоидная реакция костного мозга (Li — 15,6%).
Иммунофенотипирование костного мозга: патологических клеток не выявлено.
УЗИ органов брюшной полости: спленомегалия, диффузные изменения паренхимы печени и поджелудочной железы. Хронический калькулезный холецистит.
Пункция селезенки и цитограмма пунктата. Метастазы фолликулярного рака щитовидной железы. Патогистологическое исследование: в сосочковом и сетчатом слоях отмечается наличие микроабсцессов, в дерме обнаружены нейтрофильный и лимфоцитарный инфильтраты с примесью плазмоцитов. Эндотелий сосудов отечен, отмечается воспалительная инфильтрация и экстравазаты эритроцитов. Заключение: отмеченные изменения укладываются в картину гангренозной пиодермии.
Диагноз: буллезно-геморрагический вариант гангренозной пиодермии. Фолликулярный рак щитовидной железы с метастазами в селезенку.
Лечение. После консультации с онкологом больному была назначена системная терапия кортикостероидами из расчета 1 мг на 1 кг массы тела в сутки. Проводимая терапия дала хорошие результаты. Заметный регресс большинства элементов был отмечен на 5—7-й дни лечения. Новые элементы отсутствовали. Больной для дальнейшего обследования и лечения был переведен в краевой онкодиспансер.
Интерес данной публикации определяется редкостью описываемой патологии — буллезно-геморрагического варианта ГП и трудностями его диагностики [10]. К особенностям нашего наблюдения следует также отнести обнаруженную ассоциацию БГП с фолликулярным раком щитовидной железы. В доступной нам литературе подобных сообщений найдено не было. Поскольку в большинстве случаев ГП является вторичной по отношению к основному заболеванию, то следует считать целесообразным всесторонне обследовать больных для исключения висцеральной патологии. В первую очередь это касается болезней крови и онкологических заболеваний [11].
Источник
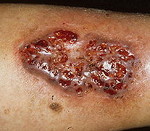
Гангренозная пиодермия – вторичный дерматоз с деструкцией кожи и омертвением подлежащих тканей, сопровождающий системные патологии. Клинически проявляется высыпанием булл с серозным, гнойным или геморрагическим содержимым, которые вскрываются, образуя расширяющиеся по периферии розовые язвы размером с ладонь с рваными краями и пиогенным отделяемым. Появление язв сопровождается продромой. Диагностируют гангренозную пиодермию на основании системной патологии в анамнезе и типичной кожной симптоматики – пиогенных язв. Для исключения других дерматозов выполняют комплекс лабораторных исследований. Осуществляют лечение первичной патологии, параллельно назначают кортикостероиды и антибиотики внутрь, наружно применяют турбулентные ванны, влажные антисептические повязки.
Общие сведения
Гангренозная пиодермия – тяжёлый прогрессирующий некроз кожи, возникающий на фоне системной патологии и характеризующийся образованием глубоких язв с гнойно-некротическим отделяемым. Гангренозная пиодермия является редким заболеванием, ежегодно диагностируется у 1-3 из 100 000 человек. Чаще всего кожная патология сопровождает воспалительные заболевания пищеварительной системы (30%), патергию (30%), артриты, опухоли, лейкозы. От 25% до 50% случаев гангренозной пиодермии имеют идиопатический характер. Первые описания гангренозной фагеденической язвы принадлежат французскому дерматологу Луи Броку, исследовавшему данную патологию в начале ХХ столетия. Современное представление о нозологии ввели в дерматологию американские специалисты А. Бранстинг, В. Хокерман и П. O’Лейри в 1930 году.
Гангренозная пиодермия имеет и другие названия: геометрический фагеденизм, язвенный дерматит, серпингинирующая и гангренозно-язвенная вегетирующая пиодермия. Суть названий патологии связана с основным клиническим симптомом заболевания – прогрессирующей гнойно-некротической язвой. Фагеденическая форма заболевания встречается исключительно в тропических и субтропических странах обоих полушарий, там, где климат сырой и жаркий. Другие формы неэндемичны. Патологический процесс возникает в любом возрасте, пик заболеваемости приходится на 20-40 лет, дети болеют редко. Отмечается незначительное преобладание пациентов женского пола. Актуальность проблемы связана с серьёзными трофическими нарушениями, которые существенно снижают качество жизни пациентов.

Гангренозная пиодермия
Причины гангренозной пиодермии
Этиология и патогенез патологического процесса точно не установлены. В ряде случаев имеет значение наследственная предрасположенность. Гангренозная пиодермия в качестве симптомокомплекса входит в состав редких генетически детерминированных синдромов PAPA (гнойный артрит, гангренозная пиодермия, гангренозные акне), PASH (гангренозная пиодермия, акне, гнойный гидраденит) и PASS (гнойный артрит, гангренозная пиодермия, акне, гнойный гидраденит). Причиной перечисленных синдромов являются мутации гена PSTPI1/CD2BP1, расположенного в хромосоме 15q. Патологии наследуются по аутосомно-доминантному механизму.
Существует также иммунная теория развития гангренозной пиодермии. Согласно данной теории патологический процесс возникает на фоне изменённой чувствительности дермы к эндогенным и экзогенным агентам. Длительно существующие хронические соматические заболевания вызывают изменения клеточного и гуморального иммунитета за счёт нарушения нейроэндокринной регуляции, обменных процессов, трофики тканей. Начинается аберрантная иммунная реакция, в которой задействованы Т-лимфоциты и цитокины. Клетки иммунной системы Т-хелперы вырабатывают антитела – реагины, создающие основу сенсибилизации кожи. Одновременно Т-супрессоры пытаются подавить эти реакции, в результате развивается нестандартный иммунный ответ в виде некротической деструкции соединительной ткани.
Процесс формирования язвы при гангренозной пиодермии проходит три стадии. На стадии иммунных реакций происходит накопление специфических для определённого вида антигена антител. При этом иммунные лимфоциты и антитела класса Е из крови переходят в ткани кожи, сенсибилизируя её. На второй (патохимической) стадии заболевания повторное попадание чужеродного антигена вызывает активацию протеолитических ферментов клеток и тканей с нарушением их функций. Эпидермальные клетки начинают вырабатывать биологически активные вещества, провоцирующие воспаление. На третьей (патофизиологической) стадии возникает специфический ответ кожи на внедрение патологического антигена в виде дегрануляции клеток, разрушения сосудов, нарушения трофики и локальной деструкции ткани. Глубина деструкции зависит от количества патогенного антигена и степени устойчивости иммунной системы.
Классификация
В современной дерматологии принято различать несколько разновидностей патологического процесса. Выделяют:
- Классическую (язвенную) гангренозную пиодермию, которая характеризуется глубокими язвами фиолетового оттенка с краями, нависающими над поверхностью дефекта кожи. Патология сочетается с системными процессами в кишечнике, суставах, лёгочной ткани. В эту группу входят пиостоматит, пиогенное гангренозное поражение половых органов, периорбитальных тканей, слизистых верхних дыхательных путей.
- Атипичную гангренозную пиодермию, состоящую из буллёзной и пустулёзной разновидности. Данная форма заболевания сопутствует бластным лейкозам или миелопролиферативным заболеваниям, характеризуется пузырными или гнойчиковыми высыпаниями на отёчной кайме по периферии язвы с локализацией на лице и конечностях.
- Посттравматическую гангренозную пиодермию, возникающую на фоне патергии.
- Фагеденическую гангренозную пиодермию, эндемичную для тропиков и субтропиков, отличительной чертой которой является множественность и прочное спаивание с подлежащими тканями.
- Злокачественную поверхностную гранулематозную гангренозную пиодермию, сопровождающую системные патологии и злокачественные опухоли.
Симптомы гангренозной пиодермии
Изменения на поверхности дермы дебютируют фурункулоподобными элементами с прозрачным или геморрагическим содержимым на фоне гиперемии. Поверхность кожи в местах высыпаний при гангренозной пиодермии инфильтрируется, затем некротизируется с формированием увеличивающейся вглубь и вширь язвы полициклической формы, достигающей размеров ладони взрослого человека. На пике своего развития очаг поражения представляет собой сплошную язвенную поверхность с валикообразными краями и оборками из остатков эпидермиса. Язва ливидного цвета с приподнятыми краями и широкой полосой гиперемии по периметру наполнена гноем, сгустками крови, остатками эпидермиса и бактериями, источает зловоние. Дно дефекта кожи бугристое, покрыто яркими грануляциями. Исход гангренозной пиодермии – реэпителизация с краёв дефекта в рубец.
Субъективное состояние нарушается мало, образование язвы сопровождается болезненностью, в период обострений появляются продромальные явления, присоединяются артралгии, миалгии. Гангренозная пиодермия начинается остро, но довольно быстро хронизируется, обладает волнообразным течением с частыми рецидивами. В 50% локализацией патологического процесса является голень, как правило, очаг единичный. Фагеденические язвы чаще множественные, возникают преимущественно на половых органах. Отличительной особенностью этой формы гангренозной пиодермии является быстрое формирование язвы, покрытой дифтероидным налётом серого цвета и плотно спаянной с подлежащими тканями. Валик вокруг дефекта кожи имеет заостренные края и чрезвычайно плотную консистенцию. Образование дефекта тканей сопровождается полиневритами и лимфангоитами.
Диагностика
Клинический диагноз ставится дерматологом на основании анамнеза, специфической симптоматики и консультаций узких специалистов, поскольку гангренозная пиодермия является междисциплинарным заболеванием. Гистология очага поражения не показательна, но в сложных случаях полезна. Выявляется тромбоз сосудов, гранулематозные инфильтраты, островки деструкции в эпидермисе и дерме. Дополнительно проводят электрофорез сывороточного белка, исключают микотическую природу язвы, берут кровь на RW. Дифференцируют гангренозную пиодермию с язвенным туберкулёзом кожи, третичным сифилисом, глубокими дерматомикозами, вегетирующей язвенной пиодермией, карбункулом, гранулематозом Вегенера, панникулитом, амёбиазом, бромодермой, гангреной, вегетирующей пузырчаткой, микобактериальной и клостридиальной инфекцией, трофическими нарушениями, пустулёзным псориазом.
Лечение гангренозной пиодермии
Терапию гангренозной пиодермии начинают с коррекции соматической патологии у профильных специалистов, поскольку кожный патологический процесс без этого плохо поддаётся терапии. Целью дерматологического лечения является снятие воспалительных проявлений, болезненных ощущений, восстановление кожных покровов. Для этого проводят курсы гормонотерапии и антибиотикотерапии. В тяжёлых случаях подключают цитостатики, иммуносупрессоры, калия иодид, внутривенно вводят иммуноглобулин. Показан плазмаферез. Наружно при гангренозной пиодермии очищают поверхность дефекта кожи с помощью вибрационно-турбулентных ванн, антисептических растворов. Применяют влажно-высыхающие повязки с растворами серебра, гормональные препараты. С учётом патергии стараются избегать хирургических манипуляций. Прогноз гангренозной пиодермии определяется первичной патологией, вызвавшей язву.
Источник
Паранеопластический синдром (ПНС) — клинико-лабораторное проявление злокачественной опухоли, обусловленное не её локальным или метастатическим ростом, а неспецифическими реакциями со стороны различных органов и систем или эктопической продукцией опухолью биологически активных веществ.[1] Паранеопластические синдромы распространены у пациентов среднего и пожилого возраста, и наиболее часто развиваются при раке лёгких, молочной железы, яичников, а также при лимфоме.[2] Иногда симптомы паранеопластического синдрома манифестируют ещё до диагностики злокачественной опухоли.
Классификация[править | править код]
Паранеопластические синдромы разделяются на 4 основные категории — эндокринные, неврологические, кожно-слизистые и гематологические ПНС, а также другие, не включённые в основные категории:
Неврологические ПНС[править | править код]
Наиболее тяжёлая в клиническом отношении группа паранеопластических синдромов — паранеопластические неврологические расстройства.[8] Эти синдромы могут вовлекать как центральную, так и периферическую нервную систему; некоторые из них сопровождаются нейродегенерацией [9], хотя некоторые (например, миастенический синдром Ламберта — Итона) могут клинически улучшаться на фоне лечения. В числе симптомов паранеопластических неврологических расстройств — атаксия, головокружение, нистагм, затруднение глотания, потеря мышечного тонуса, нарушение координации движений, дизартрия, проблемы со зрением, расстройства сна, деменция, потеря кожной чувствительности.
Более распространены паранеопластические неврологические расстройства при раке молочной железы, лёгких, опухолях яичников, однако встречаются и при многих других злокачественных заболеваниях.
Лечение включает в себя:
- Методы, направленные на лечение опухоли (химиотерапия, радиотерапия, хирургия);
- Методы, направленные на уменьшение или замедление нейродегенерации. Быстрая диагностика и лечение очень важны для возможности неврологического восстановления пациента. В связи с редкостью этой патологии лишь немногие специалисты встречались с ними в клинической практике, поэтому консультация таких специалистов необходима при лечении паранеопластических неврологических расстройств.
Примечания[править | править код]
- ↑ Л. И. Дворецкий — Паранеопластические синдромы
- ↑ NINDS Paraneoplastic Syndromes Information Page Архивировано 4 января 2015 года. National Institute of Neurological Disorders and Stroke (англ.)
- ↑ MeSH Paraneoplastic+endocrine+syndromes
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 Table 6-5 in: Mitchell, Richard Sheppard; Kumar, Vinay; Abbas, Abul K.; Fausto, Nelson. Robbins Basic Pathology (неопр.). — Philadelphia: Saunders, 2007. — ISBN 1-4160-2973-7. 8th edition.
- ↑ MeSH Nervous+system+paraneoplastic+syndromes
- ↑ Cohen P.R., Kurzrock R. Mucocutaneous paraneoplastic syndromes (неопр.) // Semin. Oncol.. — 1997. — Т. 24, № 3. — С. 334—359. — PMID 9208889.
- ↑ Staszewski H. Hematological paraneoplastic syndromes (неопр.) // Semin. Oncol.. — 1997. — Т. 24, № 3. — С. 329—333. — PMID 9208888.
- ↑ Rees J.H. Paraneoplastic syndromes: when to suspect, how to confirm, and how to manage (англ.) // J. Neurol. Neurosurg. Psychiatr. (англ.)русск. : journal. — 2004. — Vol. 75 Suppl 2. — P. ii43—50. — doi:10.1136/jnnp.2004.040378. — PMID 15146039.
- ↑ Darnell R.B., Posner J.B. Paraneoplastic syndromes affecting the nervous system (англ.) // Semin Oncol : journal. — 2006. — Vol. 33, no. 3. — P. 270—298. — doi:10.1053/j.seminoncol.2006.03.008. — PMID 16769417.
Ссылки[править | править код]
- Neuroimmunology, The Medical School, Birmingham University (англ.) — Paraneoplastic neurological autoantibodies, Birmingham UK
- https://www.antibodypatterns.com/hu.php (англ.)
- IPA website (англ.)
- Rockefeller University clinical research laboratory (англ.) devoted to the paraneoplastic neurologic disorders
- Паранеопластические синдромы, видеолекция
Источник
