Другие кардиомиопатии код мкб
Содержание
- Синонимы диагноза
- Описание
- Причины
- Патогенез
- Симптомы
- Диагностика
- Лечение
- Прогноз
- Основные медицинские услуги
- Клиники для лечения
Названия
Название: I42,8 Другие кардиомиопатии.

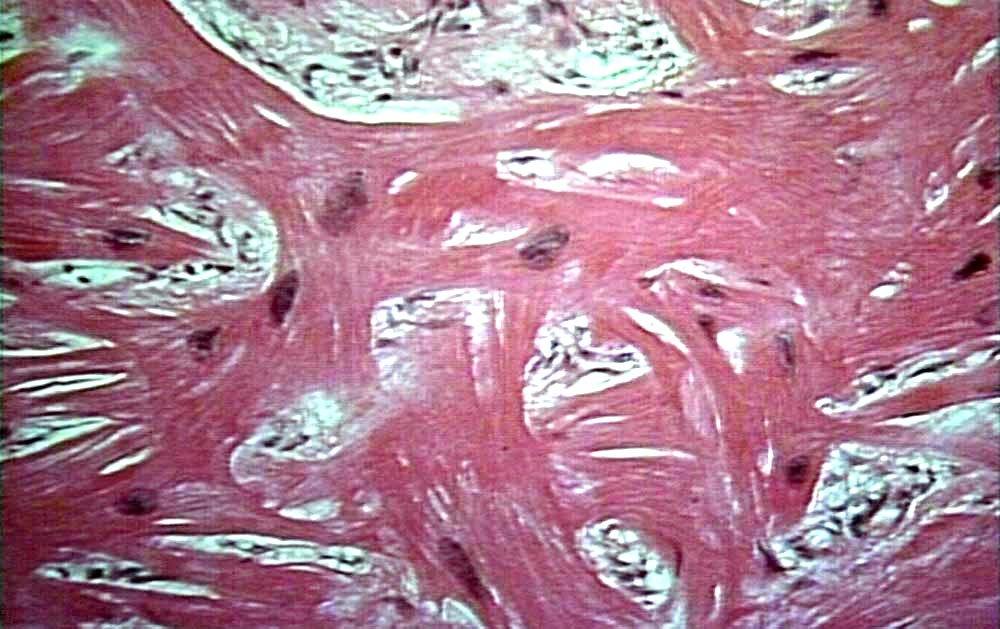
Аритмогенная кардиомиопатия правого желудочка (гистологически)
Синонимы диагноза
Другие кардиомиопатии, детская кардиомиопатия, болезнь кэшань.
Описание
Рестриктивная кардиомиопатия представляет собой редкое заболевание миокарда с частым вовлечением в процесс эндокарда, которое характеризуется нарушением наполнения одного или обоих желудочков с уменьшением их объема при неизмененной толщине стенок. Она может быть идиопатической или обусловленной инфильтративными или системными заболеваниями. К идиопатической рестриктивной кардиомиопатии как болезни миокарда неизвестной этиологии относят фибропластический париетальный эндокардит (или эндомиокардиальную болезнь) Леффлера и эндомиокардиальный фиброз Дэвиса. Фибропластический эндокардит Леффлера сочетается со стойким повышением содержания эозинофилов в периферической крови, не связанным с какой-либо известной причиной или системным заболеванием. Эндомиокардиальный фиброз протекает без эозинофилии. Ввиду сходства морфологических изменений в миокарде, патофизиологических механизмов нарушения кардиогемодинамики и клиники оба заболевания в настоящее время большинство авторов рассматривают как варианты одной и той же патологии миокарда и эндокарда, в обоих случаях, очевидно, вызываемой токсическим воздействием эозинофилов. Широкое распространение для их обозначения получили также термины эндомиокардиальная болезнь с эозинофилией и эндомиокардальная болезнь без эозинофилии.
Эпидемиология. Фибропластический эндокардит Леффлера встречается в основном в странах с умеренным климатом и является очень редким заболеванием. Эндомиокардиальный фиброз поражает почти исключительно жителей тропиков, реже субтропиков, и наиболее распространен в Уганде, Нигерии, южной Индии, Шри-Ланка, где на его долю приходится около 10—15 % случаев смерти от застойной сердечной недостаточности. Хотя в литературе имеется достаточно много сообщений о случаях этого заболевания у жителей Западной Европы и США, большинство таких больных длительное время проживало в тропических странах.
Причины
Причина эндомиокардиальной болезни окончательно не установлена. Предположение об этиологической роли паразитарных и других инфекций не подтвердилось. Имеются данные о связи распространенности эндомиокардиального фиброза с содержанием в почве монацитов и накоплении в миокарде и эндокарде больных отдельных представителей этого семейства химических элементов, в частности тория и церия, способных стимулировать синтез коллагена фибробластами сердца. Главную роль в патогенезе отводят активированным эозинофилам, которые легко подвергаются дегрануляции под воздействием частиц, покрытых иммуноглобулинами G и компонентом СЗ системы комплемента. Освобождающиеся при этом катионные белки вызывают повреждение мио- и эндокарда и стимулируют пролиферацию соединительной ткани. Возможно, эндомиокардиальная болезнь, подобно идиопатической дилатационной кардиомиопатии, представляет собой общую конечную стадию поражения миокарда, вызываемого несколькими различными этиологическими факторами.
Патологическая анатомия. Макроскопически размеры сердца увеличены незначительно, гипертрофия практически отсутствует. В патологический процесс чаще вовлекается левый желудочек, но может быть и изолированное поражение правого или обоих желудочков. Весьма характерно резкое утолщение эндокарда, преимущественно в области путей притока крови и верхушки, с тромботическими наложениями, что может приводить к уменьшению полости желудочка, подчас значительному (отсюда устаревший термин — облитеративная кардиомиопатия). Фиброз предсердно-желудочковых клапанов, сосочковых мышц и покрывающего их эндокарда приводит к развитию митральной недостаточности и недостаточности трехстворчатого клапана.
При гистологическом исследовании сердца больного фибропластическим эндокардитом выделяют три стадии поражения. Для первой, некротической, характерна выраженная эозинофильная инфильтрация миокарда с развитием миокардита и коронарита. В течение примерно 10 мес эозинофилы постепенно исчезают из очагов воспаления и наступает тромботическая стадия. Она проявляется утолщением эндокарда вследствие фибриноидных изменений и тромботических наложений и тромбозом мелких венечных артерий. В среднем через 24 мес развивается стадия фиброза с характерным значительным утолщением соединительнотканных элементов эндокарда и распространенным интерстициальным фиброзом миокарда, который, несмотря на сопутствующий неспецифический облитерирующий эндартериит интрамуральных венечных артерий, имеет преимущественно некоронарогенное происхождение.
Патогенез
Нарушения кардиогемодинамики характеризуются развитием так называемого синдрома рестрикции, В его основе лежит резкое повышение эластической жесткости желудочка, вследствие чего после короткого периода быстрого наполнения, обеспечиваемого значительным повышением давления, дальнейшее поступление крови в желудочек практически прекращается, так что его объем в течение второй половины диастолы существенно не возрастает. Это сопровождается характерным изменением кривой диастолического давления в желудочках, которая приобретает форму квадратного корня ( 11) со значительным снижением давления в начале диастолы и последующим резким подъемом с переходом в плато. При этом определяется выраженное повышение уровня внутрижелудочкового КДД, давления в системных и легочных венах и систолического давления в легочной артерии. Сократимость миокарда и систолическая функция желудочков обычно сохранены, о чем свидетельствуют неизмененные величины КДО (менее ПО см3/м2) и ФВ (более 50%).
Симптомы
Основные клинические проявления обусловлены синдромом рестрикции, характеризующимся венозным застоем крови на путях притока к левому и правому желудочкам, обычно с преобладанием застоя крови в большом круге кровообращения. Как правило, больных беспокоят выраженная одышка и слабость при малейшей физической нагрузке, связанные с усугублением нарушения диастолического наполнения при тахикардии. Быстро нарастают периферические отеки, гепатомегалия и асцит, часто устойчивые к проводимой терапии. При объективном исследовании отмечаются набухание шейных вен, увеличение ЦВД, которое часто увеличивается на вдохе (признак Куссмауля). Может определяться парадоксальный пульс. Обращает на себя внимание несоответствие между тяжестью проявлений сердечной недостаточности и отсутствием кардиомегалии, что еще до выполнения инструментального обследования позволяет предположить наличие диастолической дисфункции желудочков. При аускультации сердца отмечаются протодиастолический, пресистолический или суммационный ритм галопа и в значительной части случаев — также систолический шум митральной недостаточности или недостаточности трехстворчатого клапана. Заболевание часто осложняется мерцанием предсердий и эктопическими желудочковыми аритмиями, а также тромбоэмболиями в артериях малого и большого круга кровообращения, источниками которых обычно являются тромбы в желудочках.
Фибропластический эндокардит Леффлера часто начинается подостро с системных проявлений — лихорадки, похудения, кожной сыпи, пульмонита, сенсорной полинейропатии, сопровождающихся эозинофилией. Эти проявления отсутствуют при эндомиокардиальном фиброзе, для которого характерны постепенное развитие и прогрессирование застойной сердечной недостаточности.
Диагностика
При рентгенографии грудной клетки размеры сердца не изменены или немного увеличены. Кардиомегалия может наблюдаться только при развитии гидроперикарда. Отмечаются также увеличение одного или обоих предсердий и венозный застой в легких.
Изменения на ЭКГ встречаются часто, но лишены специфичности. Могут регистрироваться признаки гипертрофии предсердий и желудочков, блокада левой или правой (реже) ножки пучка Гиса, неспецифические нарушения реполяризации, различные нарушения сердечного ритма.
При допплерэхокардиографии дилатация и гипертрофия желудочков отсутствуют, сократительная способность их не изменена, У ряда больных полость желудочков уменьшена за счет облитерации верхушечного сегмента, где часто определяются тромбы. Часто выявляется жидкость в полости перикарда, а при допплеровском исследовании — умеренная регургитация крови из предсердий в желудочки, сопровождающаяся дилатацией предсердий, иногда — умеренным фиброзом клапанов. У ряда больных фибропластическим эндокардитом Леффлера обнаруживают признаки вальвулита и вегетации на предсердно-желудочковых клапанах ( F. Cetta и соавт. , 1995, и )- Весьма характерны, но неспецифичны свойственные рестриктивному типу диастолической дисфункции увеличение максимальной скорости раннего диастолического наполнения (Е), которая значительно преобладает над таковой в период систолы предсердий (Е/А > 1,5), и укорочение периода замедления скорости раннего наполнения.
Другие неинвазивные методы визуализации сердца — такие как компьютерная и магниторезонансная томография — используют в основном для исключения констриктивного перикардита, при котором отмечается утолщение перикарда, не характерное для рестриктивной кардиомиопатии.
При катетеризации сердца отмечаются характерные для гемодинамического синдрома рестрикции повышение К ДА, в желудочках и изменение формы кривой диастолического давления в них. При этом вследствие негомогенности поражения миокарда и эндокарда левого и правого желудочков величины их КДД обычно неодинаковы и различаются более чем на 5 мм Нарушение диастолического наполнения желудочков при неизмененных показателях систолической функции определяется также при рентгеноконтрастной вентрикулографии. При этом у большинства больных отмечается та или иная степень регургитации крови из предсердий в желудочки.
При эндомиокардиальной биопсии в ранней воспалительной стадии фибропластического эндокардита Леффлера можно обнаружить характерные эозинофильные инфильтраты, а в поздней стадии заболевания и при эндомиокардиальном фиброзе — неспецифические изменения в виде более или менее распространенного интерстадиального фиброза и дистрофии кардиомиоцитов. При этом основная роль биопсии состоит в исключении констриктивного перикардита и рестриктивной кардиомиопатии вследствие системных и инфильтративных поражений миокарда.
Отличительным лабораторным признаком фибропластического эндокардита Леффлера служит повышение содержания эозинофилов в периферической крови (более 1,5-109/л), что часто сопровождается анемией и неспецифическими воспалительными сдвигами.
Лечение
При наличии активного воспалительного процесса в миокарде и мелких сосудах, о чем косвенно свидетельствуют эозинофилия и системные проявления заболевания, в качестве средств патогенетической терапии используют глюкокортикостероиды в сочетании с цитостатическими иммуносупрессантами, главным образом гидроксимочевиной. После получения клинического эффекта переходят на длительный прием поддерживающих доз. Достаточно рано начатая такая терапия способна несколько улучшать выживаемость. Широко используют симптоматическое лечение диастолической сердечной недостаточности, которое в целом мало эффективно. Оно включает ограничение жидкости и соли и очень осторожное, во избежание ухудшения диастолического наполнения желудочков и снижения МОС, применение мочегонных средств и периферических вазодилататоров — нитратов и ингибиторов АПФ. Сердечные гликозиды эффективны только при мерцательной аритмии. Для профилактики и лечения тромбоэмболии используют антикоагулянты непрямого действия.
При выраженном утолщении эндокарда и наличии признаков облитерации полости желудочка у части больных удается выполнить эндокардэктомию, которая иногда приносит существенное облегчение. При выраженной митральной недостаточности и недостаточности трехстворчатого клапана прибегают к протезированию или пластике этих клапанов, что, однако, сопряжено с высокой летальностью.
Прогноз
Прогноз неблагоприятный. Половина больных умирают в течение 2 лет после появления первых симптомов поражения сердца. Профилактика заболевания не разработана.
Основные медуслуги по стандартам лечения | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Клиники для лечения с лучшими ценами
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Источник
Рубрика МКБ-10: I42.8
МКБ-10 / I00-I99 КЛАСС IX Болезни системы кровообращения / I30-I52 Другие болезни сердца / I42 Кардиомиопатия
Определение и общие сведения[править]
Аритмогенная дисплазия правого желудочка
Синонимы: аритмогенная кардиомиопатия правого желудочка
Аритмогенная дисплазия правого желудочка (АДПЖ) — заболевание, при котором нормальный миокард правого желудочка замещается жировой или фиброзно-жировой тканью. Обычно возникает изолированное поражение правого желудочка, однако, в процесс может вовлекаться межжелудочковая перегородка и миокард левого желудочка.
Эпидемиология
Распространённость заболевания в популяции зависит от региона и находится в пределах от 6 до 44 случаев на 10 000 населения. Наибольшую распространенность отмечают в средиземноморских регионах. В 80% случаев ее выявляют в возрасте до 40 лет, чаще у мужчин. Аритмогенная дисплазия правого желудочка выступает причиной 5-20% случаев внезапной смерти в молодом возрасте, занимая второе место после ГКМП.
У более чем половины пациентов аритмогенная кардиомиопатия правого желудочка является семейной, передается главным образом аутосомно-доминантно с переменной пенетрантностью и полиморфной экспрессией. Болезнь Наксоса и синдром Карвахаля показывают аутосомно-рецессивный способ наследования.
Этиология и патогенез[править]
Аритмогенная кардиомиопатия правого желудочка является результатом фиброзно-жировой дисплазии миокарда. Считается, что она является нарушением десмосом с дефектом контакта между клетками и сигналами. Мутации наблюдаются в генах, кодирующих белки сердечных десмосом (JUP, DSP, PKP2, DSG2 и DSC2). Однако у меньшего количества пациентов были обнаружены также мутации в не-десмосомных генах (TGFβ3, TMEM43 / LUMA, DES, CTNNA3, PLN, LMNA, TTN). Обнаружена переменная пенетрантность, предполагающая роль дополнительных генетических или экологических модификаторов. Компаундные / дигенические гетерозиготы идентифицируется у до 25% носителей мутаций и, по-видимому, является дополнительным фактором риска. Недавние исследования указывают на роль канонического сигнального пути Wnt в патогенезе аритмогенной дисплазии правого желудочка.
Макроскопически у больных с АДПЖ выявляют локальную или генерализованную дилатацию ПЖ с истончением миокарда. Типичная локализация изменений: верхушка, инфундибулярная и субтрикуспидальная область («треугольник дисплазии»). Микроскопический критерий диагноза — наличие очагов фиброзно-жировой ткани, перемежающихся с неизменённым миокардом.
Клинические проявления[править]
Клиника аритмогенной кардиомиопатии правого желудочка варьирует от бессимптомных форм до случаев внезапной смерти или тяжелой бивентрикулярной сердечной недостаточности.
Аритмогенная дисплазия правого желудочка обычно дебютирует желудочковыми нарушениями ритма сердца: экстрасистолией различных градаций, короткими «пробежками» желудочковой тахикардии, а в ряде случаев — пароксизмами устойчивой желудочковой тахикардии. Поскольку аритмогенный очаг находится в ПЖ, эктопические желудочковые комплексы имеют вид блокады левой ножки пучка Гиса.
Могут возникать нетипичные боли в груди, слабость, повышенная утомляемость, эпизоды учащённого сердцебиения при физической нагрузке. Аритмогенные коллапсы могут возникать во время нагрузки или спонтанно.
Аритмогенная дисплазия правого желудочка может сопровождаться ладонно-подошвенной кератодемией и шерстистыми волосами, являясь частью фенотипа сердечно-кожных синдромов — болезни Наксоса и синдрома Карвахаля.
Другие кардиомиопатии: Диагностика[править]
Анамнез
Анамнестические сведения, как правило, малоинформативны для постановки диагноза. Следует учитывать возможность семейного характера заболевания, более высокую частоту АДПЖ у жителей средиземноморского региона.
Физикальное исследование
При физикальном исследовании в половине случаев не выявляют никаких отклонений.
Лабораторные исследования
Для диагностики АДПЖ лабораторные исследования диагностической ценности не имеют. Тем не менее, стандартные клинические и биохимические исследования должны входить в программу обследования больных с установленным или предполагаемым диагнозом АДПЖ.
Инструментальные исследования
1. Электрофизиологическое исследование сердца. Его выполняют для уточнения характера нарушений ритма и оценки риска фатальных аритмий.
2. Методы визуализации имеют большое значение для диагностики АДПЖ. При вентрикулографии и ЭхоКГ (в том числе контрастной) выявляют аномалии сократимости ПЖ. При выполнении МРТ выявляют повышенное содержание жировой ткани в миокарде. В ряде случаев эта методика может заменить ангиографию и, возможно, биопсию в диагностике этой патологии.
3. Эндомиокардиальная биопсия. С её помощью можно выявить достоверные диагностические признаки АДПЖ. Биопсию выполняют в области межжелудочковой перегородки и свободной стенки ПЖ. Чувствительность метода составляет около 20%, так как не всегда удаётся взять биопсию именно из поражённого участка.
Дифференциальный диагноз[править]
На поздних стадиях у больных может возникнуть недостаточность кровообращения, что вызывает серьёзные трудности при дифференциальной диагностике АДПЖ с ДКМП (Дилатационная кардиомиопатия).
Другие кардиомиопатии: Лечение[править]
Цели лечения
Заболевание имеет неуклонно прогрессирующий характер, однако, при своевременном выявлении и адекватном лечении можно существенно улучшить прогноз. Терапия при АДПЖ направлена на предупреждение ВСС и лечение сердечной недостаточности.
Показания к госпитализации
Пациентов с подозрением на АДПЖ для уточнения диагноза госпитализируют в специализированные кардиологические и кардиохирургические учреждения. При установленном диагнозе АДПЖ повторные госпитализации необходимы при рецидивирующих нарушениях ритма, а также при декомпенсации сердечной недостаточности.
Немедикаментозное лечение
Пациентам с признаками сердечной недостаточности необходимо ограничить потребление поваренной соли и жидкости. Всем пациентам с АДПЖ необходимо исключить интенсивные физические нагрузки.
Медикаментозное лечение
Лечение ХСН при АДПЖ предполагает назначение стандартной терапии: диуретиков, ингибиторов АПФ, дигоксина, при наличии показаний используют антикоагулянты.
Среди антиаритмиков наибольший опыт накоплен в отношении амиодарона и соталола. Последний имеет наибольшую эффективность, поэтому с целью лечения желудочковых аритмий и профилактики ВСС рекомендуют назначать, в первую очередь, соталола.
Хирургическое лечение
При неэффективности антиаритмической терапии следует использовать хирургические методы, в частности, имплантацию кардиовертера-дефибриллятора. Проведение радиочастотной абляции имеет низкую эффективность, так как развиваются рецидивы аритмий, вызванные активизацией новых очагов. Пациентам, рефрактерным к консервативной терапии, показана трансплантация сердца.
Информация для пациентов
Пациенту необходимо разъяснить характер заболевания, дать рекомендации по диете, потреблению жидкости, режиму физической активности. Важно предупреждать больных о возможности прогрессирования заболевания, а также информировать о симптомах, требующих обращения за медицинской помощью. Необходимо профилактическое обследование родственников пациента для исключения семейных форм АДПЖ.
Прогноз
АДПЖ — прогрессирующе заболевание, и при отсутствии лечения высока вероятность ВСС (внезапная сердечная смерть). Данные о долгосрочном прогнозе АДПЖ отсутствуют. Пятилетняя летальность, по разным данным, составляет от 4 до 19%.
Профилактика[править]
Не разработана.
Прочее[править]
Кардиомиопатия такоцубо
Синонимы: синдром тако-цубо, ампуллярная кардиомиопатия, апикальный баллонный синдром,
баллонная кардиомиопатия, синдром разбитого сердца, синдром такоцубо, транзиторный апикальный баллонный синдром левого желудочка, стрессовая кардиомиопатия, TAKO-TSUBO
Определение и общие сведения
Кардиомиопатия такоцубо представляет собой недавно описанный острый сердечный синдром, который имитирует острый инфаркт миокарда и характеризуется ишемическими симптомами, повышением сегмента ST на электрокардиограмме и повышенным уровнем сердечных маркеров.
Синдром такоцубо был первоначально был описан в японской популяции, но недавно был зарегистрирован в США и Европе. Кардиомиопатия такоцубо чаще всего встречается у женщин в постменопаузе в возрасте от 55 до 75 лет, с оценкой заболеваемости в общей популяции 1/36 000.
Этиология и патогенез
Хотя точная причина остается неизвестной, синдром обычно провоцируется острым эмоциональным или физическим стрессом.
Клинические проявления
Пациенты, обычно обнаруживают ишемическую боль в грудной клетке, одышку, повышение сегмента ST и продление интервала QT на ЭКГ, незначительное повышение уровней сердечных ферментов и биомаркеров, а также транзиторное «шаровидное (баллонное)» расширение верхушки и среднего отдела левого желудочка. В отличие от острых коронарных артериальных синдромов, у пациентов с кардиомиопатией такоцубо не наблюдается ангиографически подтвержденной обструкции коронарных артерий. Наиболее распространенными осложнениями синдрома такоцубо являются кардиогенный шок и затруднение оттока из левого желудочка, инсульт и образование апикального тромба.
Диагностика
Диагноз подтверждается коронарной артериографией, вентрикулографией и эхокардиографией левого желудочка.
Дифференциальный диагноз
Дифференциальный диагноз включает острый коронарный артериальный синдром и другие типы транзиторной желудочковой дисфункции.
Лечение
Пациентов следует контролировать и шоспитализировать при предсердных и желудочковых аритмиях, сердечной недостаточности и механических осложнениях. Ведение состоит из поддерживающей и симптоматической терапии бета-блокаторами, ингибиторами АПФ, ацетилсалицилвой кислотой и диуретиками.
Прогноз
Краткосрочный прогноз благоприятный, характеризуется клиническим выздоровлением в течение нескольких недель, когда принимаются соответствующие меры во период острой фазы заболевания. Течение синдрома такоцубо может быть осложнено разрывом левого желудочка, что делает синдром одной из причин внезапной смерти.
Источники (ссылки)[править]
Кардиология [Электронный ресурс] / под ред. Ю. Н. Беленкова, Р. Г. Оганова — М. : ГЭОТАР-Медиа, 2011. — https://www.rosmedlib.ru/book/ISBN9785970427675.html
https://www.orpha.net
Дополнительная литература (рекомендуемая)[править]
Действующие вещества[править]
Источник
