Для синдрома паллистера w характерны
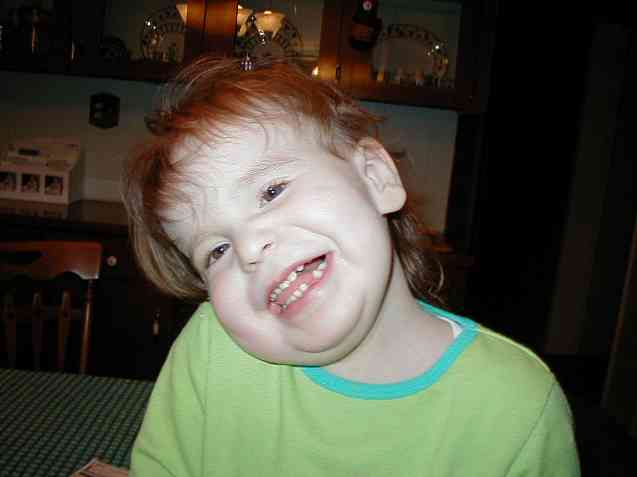
Синдром Паллистера-Киллиана (SPK), также известный под именем тетрасомия 12, это редкое заболевание генетического происхождения, характеризующееся широким спектром участия многих органов.
На клиническом уровне эта патология определяется умственной отсталостью, психомоторной отсталостью, мышечной гипотонией, атипичным лицевым фенотипом, пигментными аномалиями кожи и алопецией (Толедо-Браво-де-ла-Лагуна, Кампо-Казанеллы, Сантана-Рогригес, Сантана -Артилис, Себастьян-Гарсануа, Кабрера-Лопес, 2014).
Кроме того, могут возникать и другие виды медицинских осложнений, связанные с пороками развития в различных системах организма или судорожными эпизодами (Толедо-Браво-де-ла-Лагуна и др., 2014)..
Этиологическое происхождение этого заболевания связано с генетическим изменением, распространенным в мозаике. В частности, это связано с наличием дополнительной хромосомы 12 в некоторых клетках организма (Понимание хромосомных нарушений, 2016).
Диагноз синдрома Паллистера-Киллиама может быть поставлен как на дородовой, так и на постнатальной стадии. Основной целью является выявление клинических характеристик и использование подтверждающего генетического исследования (Мендес, Родригес, Болуарте, Картолин, Вальдес и Матеус, 2013).
Этот синдром имеет высокий уровень смертности (Рамирес Ферандес, Гарсия Кавасос, Санчес Мартинес, 2007). Тем не менее, медицинский фармакологический подход и реабилитационное лечение могут обеспечить важные преимущества в качестве жизни и клиническом статусе пострадавших (Méndez et al., 2013).
Характеристика синдрома Паллистера-Киллиама
Синдром Pallister-Killiam (SPK) — это тип мозаичного генетического заболевания. В этом случае изменение хромосомы затрагивает только некоторые клетки организма..
Некоторые учреждения, такие как Genectis Home Reference (2016), классифицируют эту патологию в рамках так называемых нарушений развития.
На общем уровне нарушения развития или нарушения развития в их международном термине, как правило, относятся к широкому набору физических и когнитивных изменений и аномалий. Все это приводит к отклонению или значительной задержке развития относительно нормальных или ожидаемых паттернов (Национальный институт неврологических расстройств и инсульт, 2015).
При синдроме Pallister-Killiam выявлено широкое поражение различных систем организма и организмов (Genectis Home Reference, 2016)
Он в основном характеризуется умственной отсталостью, мышечной гипотонией, развитием отличительных черт лица, изменением пигментации кожи или ростом волос, среди других врожденных изменений (Genectis Home Reference, 2016).
Кроме того, синдром Pallister-Kiliam является редким врожденным заболеванием (Turleau, 2009), которое может получить большое количество имен в медицинской литературе (Национальная организация по редким заболеваниям, 2016):
- Синдром мозаики Паллистера-Киллиама.
- Синдром ишромосомы 12р.
- Синдром Киллиама.
- Синдром Никола-Тешлера
- Синдром паллистерной мозаики.
- Тетрасомия 12р.
- Синдром Киллиама-Тешелера-Никола.
Это заболевание было впервые описано Паллистером в 1977 году (Толедо-Браво-де-ла-Лагуна и др., 2014).
В первых публикациях указывалось на два случая взрослых пациентов, течение которых характеризовалось различными признаками: судороги, мышечная гипотония, интеллектуальный дефицит, костно-мышечные и органические пороки развития, грубая конфигурация лица и изменения цвета кожи (Méndez et al. al., 2013).
Параллельно Teschler-Nicola и Killiam в 1981 году описали эту же клиническую картину у трехлетней девочки (Méndez et al., 2013).
Поэтому в первых клинических отчетах была сделана общая ссылка на медицинское состояние, характеризующееся сочетанием судорог, умственной отсталости и характерного физического фенотипа (Толедо-Браво-де-ла-Лагуна и др., 2014)..
Кроме того, уже в 1985 году Гильгенкрац смог выявить в первом случае на этапе беременности, что часто встречается в настоящее время благодаря современным методам диагностики (Méndez et al., 2013).
статистика
Показатели распространенности синдрома Паллистера-Киллиама точно не известны. Было поставлено не так много точных диагнозов, и большинство из них не были опубликованы в медицинской литературе (Понимание хромосомных расстройств, 2016).
Таким образом, все авторы и учреждения определяют этот синдром как редкую или редкую генетическую патологию в общей популяции (EuRed, 2016).
Около 15 лет назад синдром Паллистера-Киллиама был выявлен только в 100 случаях во всем мире. В настоящее время эта цифра превысила 200 пострадавших (Понимание хромосомных расстройств, 2016).
Эпидемиологические исследования позволили оценить частоту этого заболевания примерно в 5,1 случая на миллион новорожденных детей (Понимание хромосомных расстройств, 2016), хотя такие авторы, как Толедо-Браво-де-ла-Лагуна и сотрудники (2014), считают, что 25000.
Более высокой распространенности, связанной с социально-демографическими характеристиками пострадавших, выявлено не было. Синдром Паллистера-Киллиана может проявляться в любой половой, технической и / или расовой группе..
Признаки и симптомы
В клиническом течении синдрома Паллистера-Киллиана могут быть выявлены самые разнообразные признаки и симптомы. Все они связаны с аномалиями черепно-лицевой и / или скелетных мышц и когнитивными изменениями.
Настройки лица
Развитие черепно-лицевых пороков развития от фазы беременности к постнатальному и младенческому росту является одним из наиболее характерных медицинских признаков синдрома Паллистер-Киллиама.
Наиболее распространенные признаки и симптомы включают нарушения в различных черепных и лицевых структурах, которые приводят к грубому и нетипичному внешнему виду (Toledo-Bravo de la Laguna et al., 2014; Понимание хромосомных нарушений, 2016):
- брахицефалия: этот термин относится к черепной конфигурации, которая приводит к увеличению ширины головы и уплощению затылочной и задней областей.
- Фронтальная черепная конфигурация: Передняя и лобная области головы имеют тенденцию развиваться чаще, чем обычно. Видный или выпуклый лоб можно увидеть.
- Задняя черепная конфигурация: самая задняя часть головы звучит, чтобы представить недоразвитое состояние. Плоский затылок можно увидеть.
- hipertelorismo: глаза должны быть расположены на большем расстоянии, чем обычно. На визуальном уровне глаза очень разделены.
- Носовая конфигурация: Нос обычно имеет большой объем, с корнем или широким мостом. Ноздри должны быть ориентированы вперед (ноздри).
- Орально-челюстная конфигурация: оральные структуры должны иметь аномальные размеры. Челюсть меньше обычной (микрогнатия). Верхняя губа приобретает тонкий и уменьшенный вид, а нижняя — толстая. Язык больше, чем ожидалось, и длинная носогубная борозда.
- Слуховые павильоны: уши находятся в низком положении и повернуты назад.
- алопеция: Рост волос ненормальный в разных областях. Наиболее распространенным является наблюдение небольших участков облысения в бровях, ресницах или голове.
- Акромовые и гиперхомные пятна: Можно выявить развитие небольших пятен на лицевых участках. Они характеризуются потерей цвета или темного внешнего вида.
Костно-мышечные пороки развития
Несмотря на то, что изменения являются менее значимыми, чем изменения лица, очень часто можно наблюдать несколько скелетно-мышечных нарушений у пациентов, страдающих синдромом Паллистера (Понимание хромосомных расстройств, 2016):
- шея: Расстояние между головой и туловищем тела обычно уменьшается. На визуальном уровне мы можем увидеть короткую шею или меньше, чем обычно.
- Позвоночник: Несмотря на то, что выявление заболеваний позвоночника не очень распространено, возможно, что появляются расщелина позвоночника, крестцовый аппендикс, сколиоз или кифоз..
- советы: на руках и ногах также наблюдается аномальный рост, который меньше ожидаемого для пола и биологического возраста больного.
- полидактилия: также могут появиться изменения, связанные с количеством пальцев рук и ног. Наиболее распространенным является наблюдать больше пальцев на руках
Мышечная гипотония и психомоторная отсталость
Нарушения, связанные с мышечной структурой и подвижностью, являются еще одним из основных клинических признаков синдрома Паллистера-Киллиана (Понимание хромосомных расстройств, 2016):
Мышечная гипотония относится к выявлению аномально сниженного мышечного тонуса или напряжения. На визуальном уровне вялость и лабильность могут наблюдаться в разных группах мышц, особенно в конечностях..
Таким образом, мышечная и скелетная патология вызовет значительную задержку в приобретении различных двигательных навыков, как у новорожденных, так и у детей..
Хотя периоды разработки варьируются среди затронутых, наиболее распространенный календарь включает в себя следующие этапы:
- sedestation: способность приобретать позы самостоятельно, сидеть или вращаться с собственным телом может начать развиваться с 3 месяцев. Однако у людей, страдающих этим синдромом, его можно отложить до 8 лет..
- Первые шагиОбычно дети начинают делать свои первые шаги примерно через 12 месяцев, однако при этой патологии этот этап эволюции может быть отложен до 9 лет. Кроме того, во многих случаях необходимы некоторые компенсационные методы, такие как шина или специальная обувь..
Неврологические изменения
Еще одна область, сильно пострадавшая — это нервная система. В большинстве случаев признаки и симптомы в основном связаны с судорогами и умственной отсталостью (Толедо-Браво-де-ла-Лагуна и др., 2014; Понимание хромосомных расстройств, 2016):
- Судороги: Наличие и развитие необычной, измененной и дезорганизованной электрической активности нейронов может привести к наличию повторяющихся событий, определяемых мышечными спазмами, двигательным возбуждением или отсутствием сознания. Структура мозга сильно нарушена, что приводит к значительному ухудшению когнитивных функций и тканей.
- Интеллектуальная инвалидность: Хотя уровень когнитивных нарушений варьируется, в большинстве случаев выявляется низкий или пограничный интеллектуальный коэффициент. Наиболее затронутыми областями являются психомоторная и лингвистическая, при этом клинические критерии расстройства аутистического спектра соответствуют одному из затронутых критериев..
- Обобщенная задержка в развитии: ритм обучения различным повседневным и академическим навыкам, как правило, медленный у значительной части пострадавших. Требуется адаптация и поддержка специализированных школ.
Другие аномалии
Хотя они встречаются реже, могут возникать и другие виды медицинских осложнений (Национальная организация по редким заболеваниям, 2016 г.) (Толедо-Браво-де-ла-Лагуна и др., 2014 г.):
- Нарушения и пороки развития сердца, желудочно-кишечного тракта, почек и половых органов.
- Слуховой стеноз.
- Легочная гипоплазия.
- Косоглазие и катаракта.
- Снижение остроты зрения и слуха.
причины
Происхождение синдрома Pallister-Killian связано с генетической аномалией в мозаике на хромосоме 12. Он влияет только на генетический материал некоторых клеток организма (Inage et al., 2010).
Хромосомы являются частью ядра всех клеток, найденных в организме человека. Они состоят из широкого спектра биохимических компонентов и содержат генетическую информацию каждого человека (Национальная организация по редким заболеваниям, 2016 г.).
У людей есть 46 различных хромосом, организованных парами и пронумерованных от 1 до 23. Кроме того, на индивидуальном уровне каждая хромосома имеет участок или короткое плечо, называемое «p», и еще одно длинное, называемое «q» (Национальная организация по редким расстройствам, 2016).
Аномалия влияет на хромосому 12 и приводит к наличию хромосомы с аномальной структурой, называемой изокромосома (Genetics Home Reference, 2016).
Таким образом, эта хромосома имеет тенденцию иметь два коротких плеча вместо одного из каждой конфигурации p (короткий) и длинный (q) (Genetics Home Reference, 2016).
Как следствие, наличие дополнительного и / или аномального генетического материала изменит нормальный и эффективный ход физического и когнитивного развития больного человека, приводя к клиническим характеристикам синдрома Паллистер-Киллиана (Genetics Home Reference, 2016).
диагностика
Синдром Pallister-Killian может быть идентифицирован во время беременности или в постнатальном периоде, основываясь на клинических характеристиках и результатах различных лабораторных тестов (Turleau, 2009).
Во время беременности чаще всего используются ультразвуковые исследования, амниоцентез или ворсин хориона (Turleau, 2009)..
В этом смысле анализ генетического материала зародыша может предложить нам подтверждение этой патологии путем выявления совместимых аномалий (Turleau, 2009)..
С другой стороны, если диагноз ставится после рождения, он имеет основополагающее значение (Понимание хромосомных расстройств, 2016):
- Кожная биопсия.
- Анализ крови.
- Исследование лимфоцитов крови.
- Флуоресцентная гибридизация in situ.
- Сравнительная геномная гибридизация.
лечение
Для лечения людей с синдромом Паллистера-Киллиана не было разработано никаких специальных методов лечения (Национальная организация по редким заболеваниям, 2016).
Синдром Pallister-Killian обычно ассоциируется с плохим прогнозом и высоким уровнем смертности (Рамирес Ферандес, Гарсия Кавасос, Санчес Мартинес, 2007).
Однако реабилитационное лечение, специальное образование и трудотерапия могут дать хороший функциональный прогноз и повысить качество жизни пострадавших..
Например, Мендес и его команда (2013) описывают случай реабилитационного лечения, который характеризуется:
- Улучшение психомоторных навыков: контроль головы, самостоятельное сидение и стояние.
- Улучшение уровня бдительности, внимания, поведенческой регуляции.
- Улучшение мелкой моторики, такой как ручное давление.
- Излучение звуков и контекстная улыбка.
- Визуальное отслеживание, фиксация и различение слуховых раздражителей.
ссылки
- Ecured. (2016). Синдром Паллистера-Киллиана. Получено от Ecured.
- Генетика Главная Справочник. (2016). Синдром Паллистера-Киллиана. Получено от Genetics Home Reference.
- Inage et al. (2010). Фенотипическое перекрытие трисомии 12p и синдром PallistereKillian. Европейский журнал медицинской генетики, 159-161.
- Мендес М., Родригес М., Буларте А., Картолин Р., Вальдес Г. и Матеус Ф. (2013). Синдром Киллиана-Паллистера. Сообщение о случае в междисциплинарной реабилитационной терапии. Преподобный Мед Херед.
- NORD. (2016). Синдром мозаики Паллистер Киллиан. Получено от Национальной организации по редким заболеваниям.
- Рамирес-Фернандес, М., Гарсия Кавасос, Р. и Санчес-Мартинес, Х. (2007). Синдром Паллистера-Киллиама. Связь случая. Гинекол и препятствие Мекс, 414-18.
- Толедо-Браво-де-ла-Лагуна, Л., Кампо-Казанеллес, М., Сантана-Родригес, А., Сантана-Артилес, А., Себастьян-Гарсия, И., & Кабрера-Лопес, Дж. (2014). Представление трех случаев синдрома Pallister-Killiam. Преподобный Нейрол, 63-68.
- Turleau, C. (2009). Тетрасомы 12р. Получено от Orphanet.
- Понимание хромосомных расстройств. (2016). Синдром Паллистера-Киллиама. Понимание хромосомных расстройств.
- Исходное изображение.
Источник
Синдром Паллистера – Холла
Синдром Паллистера – Холла (Pallister-Hall syndrome, PHS, МКБ-10 — Q87.8) — редкое
наследственное заболевание, которое характеризуется наличием гипоталамической
гамартомы (редкое объемное доброкачественное образование гипоталамуса) и
проявляется задержкой интеллектуального и психомоторного развития, полидактилией и
аномалиями развития внутренних органов. На сегодняшний день специфического лечения
синдрома Паллистера – Холла не существует. Симптоматическое лечение включает в себя
хирургическую коррекцию аномалий развития внутренних органов, а также удаление
гипоталамической гамартомы.
Синдром Паллистера – Холла связан с мутациями гена GLI3.
Заболевание впервые описал J. G. Hall (Дж. Г. Холл) в 1980 г. на примере шести детей с
синдромом, который характеризовался наличием гипоталамической гамартомы,
полидактилией, аномалиями ануса, дисплазией почек, гипофункцией надпочечников,
врожденными пороками сердца и задержкой роста [1]. В 1989 г. П. Д. Паллистер (P. D.
Pallister) описал трёх пациентов со схожими клиническими симптомами [2].
Ген GLI3, связанный с развитием синдрома Паллистера – Холла, был картирован в 1990 г.
[3].
Распространенность и тип наследования
Заболевание является редким. Частота встречаемости не установлена. На сегодняшний
день в литературе зарегистрировано около 100 случаев.
Большинство случаев заболевания носят спорадический характер. Для семейных форм
заболевания характерен аутосомно-доминантный тип наследования: достаточно получить
от родителей хотя бы одну копию «дефектного» гена, чтобы проявилась патология [4].
Синдром Паллистера – Холла дебютирует в младенчестве и характеризуется наличием
гипоталамической гамартомы (редкое объемное доброкачественное образование
гипоталамуса, проявляющееся задержкой интеллектуального и психомоторного развития).
Заболевание также включает следующие симптомы: полидактилию (большее, чем в
норме, количество пальцев), неперфорированный анус, агенезию, дисплазию или
отсутствие почки, дисплазию ногтей, врожденные пороки сердца, гипофункцию
надпочечников и гипоспадию (отсутствие дистальной части мочеиспускательного канала
у мужчин или дефект задней стенки мочеиспускательного канала у женщин) [5].
Первичную диагностику заболевания проводит неонатолог или педиатр. Диагноз ставится
на основании клинической картины, МРТ головного мозга, рентгенографии скелета, УЗИ
почек и ЭКГ [6]. Диагноз подтверждается с помощью молекулярно-генетического анализа
гена GLI3. Для данного заболевания возможна пренатальная диагностика с помощью УЗИ,
а также биопсии ворсин хориона или амниоцентеза с последующим молекулярно-
генетическим анализом гена GLI3. [7].
На сегодняшний день специфического лечения синдрома Паллистера – Холла не
существует. Симптоматическое лечение включает в себя хирургическую коррекцию
аномалий развития внутренних органов и хирургические методы удаления
гипоталамической гамартомы [5].
Прогноз зависит от выраженности клинических симптомов и сопутствующих осложнений,
своевременности диагностики и степени адекватности назначенной терапии [5].
Синдром Паллистера – Холла связан с мутациями гена GLI3. Ген GLI3 кодирует белок,
представляющий собой транскрипционный фактор, который играет важную роль в
эмбриональном развитии. Мутации гена GLI3 приводят к нарушению эмбрионального
развития органов и тканей, а также к аномалиям развития опорно-двигательной системы.
- Ген GLI3: c.4431dup (p.Glu1478Ter)
- Ген GLI3: c.4395del (p.Ser1466fs)
- Ген GLI3: c.3904_3912delinsT (p.Asn1302fs)
- Hall, J. G., Pallister, P. D., Clarren, S. K., Beckwith, J. B., Wiglesworth, F. W., Fraser, F.
C., Cho, S., Benke, P. J., Reed, S. D. Congenital hypothalamic hamartoblastoma,
hypopituitarism, imperforate anus, and postaxial polydactyly—a new syndrome? Part I: clinical,
causal, and pathogenetic considerations. Am. J. Med. Genet. 7: 47-74, 1980 [PubMed: 7211952] - Pallister, P. D., Hecht, F., Herrman, J. Three additional cases of the congenital
hypothalamic ‘hamartoblastoma’ (Pallister-Hall) syndrome. (Letter) Am. J. Med. Genet. 33: 500-
501, 1989 [PubMed: 2596511] - Ruppert, J. M., Vogelstein, B., Arheden, K., Kinzler, K. W. GLI3 encodes a 190-
kilodalton protein with multiple regions of GLI similarity. Molec. Cell. Biol. 10: 5408-5415,
1990 [PubMed: 2118997] - Kletter, G. B., Biesecker, L. G. Male-to-male transmission of the Pallister-Hall
syndrome. (Abstract) Am. J. Hum. Genet. 51 (suppl.): A100 only, 1992. - Biesecker, L. G., Abbott, M., Allen, J., Clericuzio, C., Feuillan, P., Graham, J. M., Jr.,
Hall, J., Kang, S., Olney, A. H., Lefton, D., Neri, G., Peters, K., Verloes, A. Report from the
workshop on Pallister-Hall syndrome and related phenotypes. Am. J. Med. Genet. 65: 76-81,
1996 [PubMed: 8914745] - Iafolla, K., Fratkin, J. D., Spiegel, P. K., Cohen, M. M., Jr., Graham, J. M., Jr. Case
report and delineation of the congenital hypothalamic hamartoblastoma syndrome (Pallister-Hall
syndrome). Am. J. Med. Genet. 33: 489-499, 1989 [PubMed: 2688416] - Sills, I. N., Rapaport, R., Robinson, L. P., Lieber, C., Shih, L. Y., Horlick, M. N. B.,
Schwartz, M., Desposito, F. Familial Pallister-Hall syndrome: case report and hormonal
evaluation. Am. J. Med. Genet. 47: 321-325, 1993 [PubMed: 8135274] - Kang, S., Graham, J. M., Jr., Olney, A. H., Biesecker, L. G. GLI3 frameshift mutations
cause autosomal dominant Pallister-Hall syndrome. Nature Genet. 15: 266-268, 1997 [PubMed:
9054938]
Источник
