Дифференциальная диагностика заболеваний с синдромом тонзиллита

Смотри еще: Антибиотико- и химиотерапия инфекций у детей (В.К. Таточенко, Москва, 2008)
В отечественной медицине термином «острый тонзиллит» обозначают воспаление небных миндалин при наличии более или менее выраженных воспалительных изменений слизистой ротоглотки. Воспаление последней без преимущественного поражения миндалин обозначают как «фарингит». В зарубежной литературе применяют термин «фаринготонзиллит», по нашему мнению, неопределенный.
Острое воспаление небных миндалин чаще всего возникает при вирусных инфекциях (аденовирус, вирусы Эпштейна-Бара), особенно у детей первых лет жизни. Основной бактериальный возбудитель — БГСА, иногда стрептококки групп G и С, чаще вызывают тонзиллит у детей после 5 лет. Редкие возбудители — Neisseria gonorrhoeae, анаэробы, Franciscella tularensis, микоплазмы и хламидии.
Признаки острого тонзиллита
Острое начало, температура 39°С и выше, озноб, боль в горле, усиливающаяся при глотании, гиперемия, отечность миндалин, часто также язычка и слизистой глотки, гнойный детрит в лакунах, рыхлые налеты — не позволяют надежно дифференцировать вирусные и бактериальные тонзиллиты. Общие нарушения (артро- и миалгии, рвота, боли в животе), увеличение и болезненность лимфоузлов также не имеют специфичности. Отличительные признаки — см. ниже и в Табл. 2.4.
Стрептококковый тонзиллит
Стрептококковый тонзиллит (J03.3) отличается от вирусного отсутствием кашля и катарального синдрома, болезненностью лимфоузлов и падением температуры через 24-48 ч после назначения антибиотика (Рис. 2.1). Появление мелкоточечной сыпи при остром тонзиллите — скарлатина, делает диагноз БГСА-инфекции бесспорным.
Аденовирусный тонзиллит
Аденовирусный тонзиллит обычно сопровождается катаром — кашлем, ринитом, ринофарингитом со слизью на задней стенке глотки, покраснением конъюнктивы; последние 2 признака наиболее весомы в диагностике. Характерна высокая температура в течение 5-7 дней, после чего наступает выздоровление. Осложнения редки.
Инфекционный мононуклеоз
Инфекционный мононуклеоз (В27) по клиническим данным дифференцировать трудно; лимфаденопатия, гепатоспленомегалия наблюдаются далеко не всегда. Смотри Мононуклеоз — ангина, температура, отек лица, заложен нос, большие лимфоузлы, слабость.
Дифтерия зева
Дифтерия зева — Раздел 2.1. Анаэробная ангина протекает чаще с односторонней некротической язвой миндалины, иногда также неба и слизистой рта; облегчает диагноз гнилостный запах. Чаще наблюдается у лиц с иммунными дефектами. Подробнее смотри Дифтерийная палочка.
Герпангина
Герпангина — энтеровирусная инфекция, протекает при высокой температуре с характерными высыпаниями мелких (просовидных) пузырьков на передних дужках, больше в верхней их части, на границе с язычком. Гнойный выпот на миндалинах не характерен. Окончание инфекции на 3-5-й день иногда сопровождается высыпанием необильной сыпи.
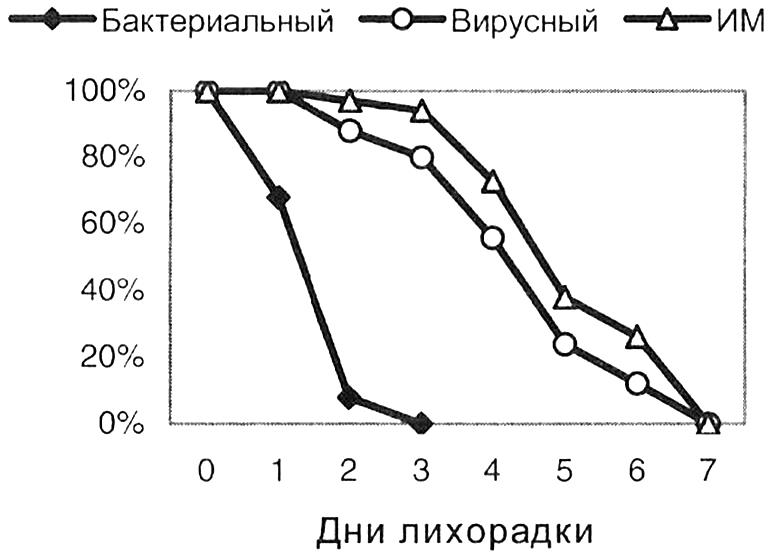
Рисунок 2.1. Длительность лихорадки при бактериальных, аденовирусных тонзиллитах и инфекционном мононуклеозе
 Синдром Маршалла
Синдром Маршалла
Синдром Маршалла — предположительно иммунопатологическое заболевание — сопровождается периодической высокой лихорадкой, тонзиллитом (часто с лакунарным выпотом), увеличением безболезненных шейных лимфоузлов (до 4-6 см), реже — появлением афт на слизистой рта. Начинается на 2-3-м году жизни и дает рецидивы с периодичностью 3-4 недели, реже 1-2 месяца. Большинству детей ставится диагноз хронического тонзиллита и проводятся повторные курсы антибиотиков, не оказывающих влияния ни на клинические проявления, ни на частоту рецидивирования. Подробнее смотри Синдром Маршала — это частые ангины у детей.
Обострение хронического тонзиллита
Обострение хронического тонзиллита (J35.0) могут быть связаны как с активацией микробной флоры (стрептококки групп А, С, G), так и с вирусной инфекцией, они обычно урежаются через год-два, особенно в пубертатном возрасте. Диагноз хронического тонзиллита оправдан лишь при наличии 3 из следующих 4 симптомов:
- гнойные фолликулы или детрит в ретротонзиллярных карманах вне обострения;
- рубцовое изменение миндалин, их сращение с дужками;
- стойкое увеличение регионарного лимфоузла вне обострения;
- частые обострения.
Таблица 2.4. Сравнительная частота симптомов при острых тонзиллитах разной этиологии
| БГСА | Аденовирус | Эпштейн-Бар | Дифтерия | Анаэробная ангина | Энтеровирус | Маршалла синдром | |
| Возраст, иммунитет | >5 лет | >6 мес | >1 года | Непривитые | Иммунный дефект | >6 мес | >1,5 лет |
| Налеты | +++ | +++ | +++ | +/- | язва | — | +++ |
| Гиперемия зева | +++ | +++ | +++ | тусклая | + | ++ | ++ |
| Назофарингит | — | +++ | ++ | — | — | — | — |
| Конъюнктивит | — | +++ | + | — | — | — | — |
| Увеличение лимфоузла | +++ Болезн. | ++ | +++ | ++ | + | — | +++ |
| Спленомегалия | — | +/- | ++ | — | — | — | — |
| Лейкоцитоз выше 15?109/л | +++ | ++ | ++ | — | — | — | +++ |
| СРБ | +++ | ++ | ++ | — | — | — | +++ |
| Прокальцитонин | +++ | + | + | — | — | — | + |
| Другие признаки | Посев+ АСЛО | Аденовирус РНИФ+ | Антитела IgM + | Посев + | Гнилостный запах | Герпангина | Рецидивы, афты |
| БГСА | Аденовирус | Эпштейн-Бар | Дифтерия | Анаэробная ангина | Энтеровирус | Маршалла синдром |
Дополнительные исследования при остром тонзиллите
Без лабораторного уточнения во всем мире врачи имеют тенденцию к перестраховке, так что процент необоснованного применения антибиотиков при тонзиллитах весьма значителен (50-80%).
Посевы мазка из зева на БГСА
Посевы мазка из зева на БГСА является наиболее важным методом. К сожалению, далеко не везде производятся посевы на БГСА, а экспресс-тесты на стрептококковый антиген имеют чувствительность всего около 60-70%. Хотя выявление в посеве БГСА не всегда говорит о его этиологической роли — посев будет положительным у носителя БГСА и в случае его заболевания вирусной ангиной — лечение подобных случаев не сильно повысит процент необоснованного применения антибиотиков.
Выделение аденовируса с помощью РНИФ
Выделение аденовируса с помощью РНИФ имеет диагностическое значение при наличии соответствующей клинической картины, выделение вируса Эпштейна-Бара с помощью ПЦР малонадежно ввиду частоты его носительства.
Серологические пробы
Антистрептолизин О (АСЛ-О) обычно повышается при БГСА — тонзиллите и ревматизме, так что 4-кратное повышение его титра в течение болезни делает диагноз стрептококкового тонзиллита бесспорным, -хотя и ретроспективным. Диагностическое значение имеет и выявление тигра ACЛ-O выше 166-250 Ед в остром периоде, однако, это наблюдается редко. Для диагностики инфекционного мононуклеоза тест Поля-Буннеля часто бывает отрицательным у детей 0-5 лет. Более надежно выявление антител против вирусного капсида (VCA) класса IgM, появляющихся рано, оно более специфично при отсутствии нуклеарных антител (EBNA) (Табл. 2.2).
Общий анализ крови
Картина крови специфична для инфекционного мононуклеоза при обнаружении более 10% атипичных лимфомоноцитов, что выявляется далеко не у всех больных.
Лейкоцитоз в пределах 10-15 х 109/л, часто с нейтрофилезом и сдвигом лейкоцитарной формулы влево наблюдается у 1/2 детей с бактериальным тонзиллитом, еще у 1/3 больных находят цифры 15-20 х 109/л. Но и при аденовирусном тонзиллите цифры 10-15 х 109/л наблюдаются у 40%, а 15-20 х 109/л — у 23% больных, также нередко с нейтрофилезом и сдвигом влево. При инфекции вирусом Эпштейна-Бара число лейкоцитов поднимается выше 15 х 109/л в половине случаев, обычно за счет лимфомоноцитов. При синдроме Маршалла лейкоцитоз выше 15 х 109/л (до 30 х 109/л) наблюдается постоянно.
Острофазные белки
Уровень СРБ при бактериальных тонзиллитах в 1/4 случаев находится в пределах 30-70 мг/л, в половине — выше 70 мг/л. При вирусных тонзиллитах в половине случаев уровень СРБ остается ниже 20 мг/л, а у 1/3 он превосходит 70 мг/л, так что положительное прогностическое значение уровня СРБ выше 30 и 70 мг/л для выявления бактериального тонзиллита не превышает 45%. При синдроме Маршалла уровень СРБ повышается практически во всех случаях, в половине до очень высоких цифр — параллельно с уровнем лейкоцитоза.
Уровень прокальцитонина выше 2 нг/мл наблюдается у 2/3 детей с бактериальным тонзиллитом и лишь у 1/4 детей с вирусными тонзиллитами и синдромом Маршалла. Этот уровень прокальцитонина имеет 67%-ное положительное и 84%-ное отрицательное предсказательное значение в отношении бактериального тонзиллита.
Когда надо назначить антибиотики при остром тонзиллите
Поскольку антибактериальная терапия показана, в основном, при стрептококковой этиологии, решение о ее проведении при острым тонзиллите следует базировать на следующих правилах:
- Стрептококковый тонзиллит вероятен у ребенка старше 4-5 лет, без катара и кашля, с увеличенным болезненным лимфоузлом, особенно в весенне-летний сезон — назначение антибиотика до получения результатов посева и АСЛ-О оправдано.
- Стрептококковый тонзиллит возможен у ребенка старше 4-5 лет, с незначительными катаральными явлениями, увеличенным безболезненным подчелюстным лимфоузлом — антибиотик может быть назначен при наличии в крови нейтрофильного лейкоцитоза выше 10 х 109/л и отсутствии атипичных лимфоцитов. Если результаты посева и АСЛ-О отрицательные — антибиотик отменяют.
- Аденовирусный тонзиллит вероятен у ребенка 0-5 лет с катаром (кашель, назофарингит, слизь на задней стенке глотки, конъюнктивит), в т.ч. при высоком лейкоцитозе — антибиотик не назначают, если только не получат в посеве БГСА и/или высокие цифры АСЛО.
- Инфекционный мононуклеоз (вирус Эпштейна-Барра) возможен у ребенка с лимфаденопатией, гепатоспленомегалией. Назначение антибиотика не оправдано. Диагноз подтверждают характерная формула крови и/или данные серологии, при выявлении БГСА и/или повышенном АСЛО проводят антибактериальное лечение.
- Энтеровирусная инфекция вероятна у ребенка с картиной герпангины — антибиотик не назначают. Появление сыпи на 3-5 день при падении температуры наблюдается часто и подтверждает диагноз.
- Анаэробная ангина вероятна у ребенка с картиной язвенного тонзиллита, особенно с дефектами иммунитета — показаны антибиотики.
- Синдром Маршалла вероятен у больного с регулярно рецидивирующими эпизодами высокой лихорадки с картиной тонзиллита, особенно с афтами и резким увеличением регионарного лимфоузла — антибиотик не показан, уместно провести пробу с кортикостероидами (см. ниже).
- Дифтерия возможна у ребенка с пленчатыми серыми налетами — взять мазок на BL. При наличии контакта с дифтерией, не полностью проведенными прививками, признаков токсичности вводят противодифтерийную сыворотку до получения результатов посева.
В случае назначения антибиотика с последующим снятием диагноза БГСА-тонзиллита антибиотик отменяют.
Выбор антибиотика при БГСА-тонзиллите
Выбор антибактериального препарата при БГСА-тонзиллите имеет целью снятие острых проявлений, предотвращение нагноений и эрадикацию БГСА как условие профилактики ревматизма. Последнее достигается при начале лечения в первые 5 и даже 7 дней от начала болезни, так что ожидание результатов посева на БГСА до начала лечения риска развития ревматизма не увеличивает. Основу составляют пенициллины (Табл. 2.5), длительность лечения — 10 дней, 5-дневные курсы эффективны для азитромицина и цефуроксима аксетила. Амоксициллин в сомнительных случаях БГСА-тонзиллита не желателен из-за риска сыпи, если это окажется инфекционный мононуклеоз. Скарлатину лечат по тем же правилам. Биопарокс не заменяют антибиотики.
При рецидивирующем БГСА-тонзиллите (при высеве БГСА и нарастании АСЛ-О при рецидивах после отрицательных посевов в ремиссии) используют защищенные пенициллины (преодоление ко-резистентности), макролиды, клиндамицин.
Носительство БГСА лечения не требует, кроме групповых, в т.ч. семейных вспышек ревматизма, гломерулонефрита или БГСА-тонзиллита, ревматизме в семейном анамнез.
Таблица 2.5. Антибактериальное лечение стрептококкового тонзиллита
| Антибиотик | Режим дозирования | Курс | Принимать |
| Феноксиметилпенициллин (Оспен) | Вес менее 25 кг — 500 мг/сут, более 25 кг — 1 г/сут в 2 приёма | 10 дней | За 1 ч до еды 1 |
| Бензатина бензилпенициллина | В/м: вес до 25 кг — 600000 ЕД, более 25 кг —1200000 ЕД | Однократно | |
| Цефалексин | 45 мг/кг/сут в 3 приёма | 10 дней | Независимо от еды |
| Цефуроксим | 30 мг/кг/сут в 2 приёма | 5 дней | Во время еды |
| Эритромицин | 40 мг/кг/сут в 3 приёма | 10 дней | За 1 час до еды |
| Азитромицин | 12 мг/кг/сут в 1 приём | 5 дней | За 1 час до еды |
| Кларитромицин | 15 мг/кг/сут в 2 приёма | 10 дней | Независимо от еды |
| Рокситромицин | 5 мг/кг/сут в 2 приёма | 10 дней | До еды |
| Джозамицин | 50 мг/кг/сут в 2-3 приема | 10 дней | Независимо от еды |
| Мидекамицин | 50 мг/кг/сут в 2 приёма | 10 дней | За 15 мин до еды |
| Спирамицин | 3 000 000 ЕД/сут в 2 приёма | 10 дней | Независимо от еды |
| Клиндамицин | 20 мг/кг/сут в 3 приёма | 10 дней | Запивать водой |
Лечение вирусных тонзиллитов
Аденовирусный тонзиллит, инфекционный мононуклеоз, герпангина не отвечают на антибактериальное лечение. Данных об эффективности интерферонов нет. Эффективность ацикловира при мононуклеозе не доказана, его используют у детей на фоне иммуносупрессии; в тяжелых случаях (резкие боли в горле, нарушение глотания и дыхания из-за увеличения миндалин) показан преднизолон (1 мг/кг/сут, макс. 30 мг/сут) 5-7 дней. Анаэробную ангину лечат защищенными пенициллинами, клиндамицином. Динамика лихорадки при вирусных тонзиллитах не зависит от назначения антибиотиков.
Лечение синдрома Маршалла
При синдроме Маршалла неэффективность антибиотика имеет диагностическое значение. Температуру обрывают системные стероиды (преднизолон 1 мг/кг 1-3 дозы), но они не предотвращают рецидивы в обычные сроки. Тонзиллэктомия, по данным ретроспективных наблюдений, в 75% прекращает приступы.
Лечение обострения хронического тонзиллита
Обострение хронического тонзиллита требуют повторных курсов антибиотиков (лучше по данным посева), полоскания содой, марганцевокислым калием 1:10000. Используют Имудон, пидотимод (Имунорикс). Тонзиллэктомию проводят, согласно международным стандартам, при минимум 7 острых эпизодах в течение 1 года, 5 эпизодах в год последние 2 года или 3 эпизодах в год последние 3 года, но не ранее, чем через 6-12 мес. энергичного лечения.
Смотри еще: Антибиотико- и химиотерапия инфекций у детей (В.К. Таточенко, Москва, 2008)
Источник
Дифференциальную диагностику ангины следует осуществлять с заболеваниями, протекающими с синдромом тонзиллита:
а) локализованные формы дифтерии (островчатая и пленчатая) — отличаются от ангины постепенным началом заболевания, специфическими проявлениями общей интоксикации в виде бледности кожи лица, умеренной адинамии и вялости (озноб, ломота в теле, боли в мышцах и суставах, характерные только для ангины), несоответствием объективных и субъективных проявлений болезни (незначительная боль в горле при глотании при наличии выраженных воспалительных изменений со стороны миндалин), особенностями воспалительного процесса в ротоглотке, характеризующегося застойно-синюшным цветом гиперемии и выраженным отеком миндалин с наличием на их поверхности пленчатого трудно снимаемого налета, оставляющего после себя дефект ткани. При атипичном течении дифтерии, что наблюдается у половины взрослых больных, налет снимается легко, не оставляя дефекта ткани. Однако и в этих случаях сохраняются остальные характерные для дифтерии зева признаки.
б) ангина Симановского-Венсана (фузоспирохетоз)— характеризуется незначительно выраженными общими проявлениями (кратковременная субфебрильная температура тела, отсутствие общей слабости, головной боли и др.),поражением лишь одной миндалины в виде язвы размером 5-10 мм, покрытой легко снимающимся желтовато-белым или беловато-серым налетом, наличием в препаратах из отделяемого язвы, окрашенных по Романовскому-Гимза, веретенообразных палочек и спирохет. Регионарный лимфаденит не выражен.
в) скарлатина — отличается от ангины появлением в первые сутки болезни по всему телу, кроме носогубного треугольника, обильной точечной сыпи, расположенной на гиперемированном фоне, сгущающейся на шее, боковых поверхностях грудной клетки и в треугольнике Симона и особенно выраженной в естественных складках кожи (симптом Пастия), а также характерными проявлениями тонзиллита в виде ярко-красного цвета гиперемии миндалин, небных дужек, язычка и мягкого неба («пылающий зев»).
г) инфекционный мононуклеоз — характерны, кроме тонзиллита (гнойно-некротического или фибринозного), полиаденит, увеличение печени и селезенки, лимфомоноцитоз с одновременным появлением атипичных мононуклеаров и плазматических клеток, а также положительная реакция ХД/ПБД.
д) ангинозная форма туляремии — отличается от ангины сравнительно поздним появлением (на 3-5-е сутки) одностороннего катарального или некротического тонзиллита, выраженным увеличением регионарных к пораженной миндалине лимфатических узлов, которые продолжают увеличиваться и после исчезновения тонзиллита (туляремийный бубон).
е) для лейкозов и агранулоцитоза типично сравнительно позднее (на 3-6-е сутки болезни) появление некротического тонзиллита с распространением некротических изменений на слизистую оболочку небных дужек, язычка, щек; наличие септической лихорадки, гепатолиенального синдрома и характерных изменений гемограммы (hiatus leucemicus — при лейкозах и резкое снижение количества нейтрофилов при агранулоцитозе).
ж) герпангина — наблюдаются, наряду с лихорадкой и интоксикацией, местные изменения в виде гиперемии слизистой оболочки ротоглотки и наличия на небных дужках, язычке, мягком небе, а иногда — на миндалинах и языке отдельных папул размером 2-4 мм в диаметре, быстро превращающихся в пузырьки бело-серого цвета, а затем эрозии.
з) кандидоз ротоглотки — протекает с нормальной или субфебрильной температурой тела, хорошим самочувствием больных, наличием на поверхности миндалин, язычка, небных дужек, а иногда и на задней стенке глотки крошкообразного налета белого цвета в виде легко снимающихся островков размером 2-3 мм в диаметре. В анамнезе имеются указания на более или менее длительное применение антибиотиков широкого спектра действия или их комбинаций.
и) обострение хронического тонзиллита — отличается от повторной ангины постепенным началом, вялым и относительно продолжительным течением заболевания с непостоянной субфебрильной температурой тела, отсутствием выраженной интоксикации, умеренными болями и неприятными ощущениями в горле при глотании, застойным характером гиперемии рубцово измененных и спаянных с небными дужками миндалин, наличием казеозного содержимого в лакунах, увеличением углочелюстных лимфатических узлов, характеризующихся плотной консистенцией и умеренной болезненностью, нормальными показателями количества нейтрофилов в крови или незначительно выраженным нейтрофильным лейкоцитозом.
Источник
Хронический тонзиллит (ХТ) является одним из наиболее распространенных заболеваний в практике врача-оториноларинголога. Высокая распространенность ХТ заставляет искать новые, более совершенные методы диагностики и лечения, а также совершенствовать уже имеющиеся методы лечения данной патологии. Анализируя данные литературы, а также назначения отдельных специалистов, приходится констатировать, что зачастую небным миндалинам (НМ) совершенно необоснованно приписывается какая-то особая, уникальная роль в синтезе иммуноактивных веществ, которая осуществляется даже в условиях развития в организме пациента токсико-аллергических реакций при Х.Т. Все это ошибочно убеждает многих врачей, в том числе и оториноларингологов, в необходимости сохранять НМ с очагом инфекции и проводить консервативное лечение у пациентов такого рода [1]. Подобные представления о терапии ХТ, а также патоморфоз биологических свойств основного возбудителя ХТ — β-гемолитического стрептококка (БГСА) в современных условиях явились причиной роста как местных, так и системных осложнений, развивающихся при данном заболевании. Благодаря обширным анатомо-топографическим и гуморальным связям НМ, патогенез ХТ как постоянно действующей хронической инфекции характеризуется влиянием тонзиллярной интоксикации на жизненно важные органы. При этом функция НМ как иммунного органа полностью прекращается, однако появляется способность к выработке иммунопатологических антител [2].
По результатам большинства современных исследований [3—5], системные осложнения ХТ в настоящее время часто протекают латентно, что во многих случаях является причиной поздней диагностики этих состояний. Стоит отметить, что основными мишенями иммунокомплексного воспаления, сформировавшегося в НМ, являются органы сердечно-сосудистой, выделительной и костно-мышечной систем, при этом патологические изменения в вышеназванных органах и системах обычно приводят к снижению качества жизни, часто к инвалидизации и даже к смерти [6]. Поражение этих органов и систем является следствием гомологичной антигенной структуры белков соединительной ткани, кардиомиоцитов и клубочков почечной ткани и молекулы M-протеина БГСА [3].
Кроме того, некоторые исследователи данной проблемы [5, 7] подчеркивают, что у лиц с семейным анамнезом по аутоиммунным заболеваниям почек, сердца и суставов имеется более высокий риск развития данных состояний, в среднем в 5—6 раз выше среднепопуляционного. Это свидетельствует о наличии общих генетических закономерностей развития указанных заболеваний. Рассматривая эти состояния в контексте возможного развития системных осложнений хронической инфекции, персистирующей в НМ, важно уделять особое внимание своевременной диагностике и элиминации тонзиллярной патологии у людей, родственники которых страдают заболеваниями сердца, суставов и почек.
Необходимо подчеркнуть, что течение и клинические проявления поражений внутренних органов при ХТ должны быть известны не только врачам терапевтических специальностей, занимающихся диагностикой и лечением этих состояний, но и врачам-оториноларингологам для правильного выявления связи патогенеза ХТ и общего заболевания (или интоксикации), что позволит назначить адекватное лечение.
Учитывая вышеизложенное, цель нашей работы — выявление объективных диагностических критериев для дифференциации различных форм хронического тонзиллита (по классификации Б.С. Преображенского — В.Т. Пальчуна) на основании результатов клинических, бактериологических и серологических методов исследования с применением методов математического анализа для установления достоверно значимых критериев.
Нами были обследованы 113 пациентов (44 мужчины и 69 женщин, средний возраст которых составил 26,51±1,10 года), направленных на плановое стационарное лечение — тонзиллэктомию (ТЭ), а также находившихся на обследовании и лечении в оториноларингологическом отделении КДЦ и ревматологическом центре при ГКБ № 1 им. Н.И. Пирогова.
На основании жалоб больных и данных анамнеза все пациенты были объединены в 3 группы в зависимости от формы ХТ: 1-ю группу составили 20 (18%) больных с диагнозом ХТ, простая форма; 2-ю группу — 50 (45%) пациентов с ХТ токсико-аллергической формы (ТАФ) I; 3-ю группу — 43 (37%) пациента с ХТ ТАФ II.
Критерием отнесения пациентов в 3-ю группу являлось наличие сопряженной патологии с Х.Т. Так, 8 (19%) больных ранее перенесли паратонзиллярный абсцесс (ПТА) и были направлены на ТЭ в плановом порядке. 6 (14%) человек находились на стационарном лечении в ревматологическом отделении ГКБ № 1 им. Н.И. Пирогова с диагнозом: ревматоидный артрит (РА), хронический тонзиллит, ТАФ II. Этим пациентам была рекомендована ТЭ в плановом порядке после достижения ремиссии по ревматологическому заболеванию. 6 (14%) человек были направлены на ТЭ вследствие наличия патологии почек, 3 (7%) пациента перенесли постстрептококковый гломерулонефрит (ПГН), 3 (7%) — болезнь Берже (IgA — ассоциированная нефропатия). 22 (51%) человека перенесли острую ревматическую лихорадку (ОРЛ) в различных проявлениях. У 1 (2%) больной левосторонний ПТА осложнился развитием ПГН. Структура сопряженной патологии представлена на рисунке.
 Структура сопряженной патологии у больных хроническим тонзиллитом ТАФ II (n=43).
Структура сопряженной патологии у больных хроническим тонзиллитом ТАФ II (n=43).
Всем пациентам было произведено стандартное обследование: выяснение жалоб, сбор анамнеза настоящего заболевания и жизни. Обязательным условием сбора анамнеза явилось уточнение наличия перенесенных ревматологических и нефрологических заболеваний у родственников пациентов. Осмотр ЛОР-органов проводили по общепринятой методике. Также всем пациентам было проведено стандартное лабораторное обследование, включавшее определение показателей белков острой фазы воспаления: ревматоидного фактора (РФ) и С-реактивного белка (СРБ), которые исследовали в лаборатории ревмоцентра ГКБ № 1 им. Н.И. Пирогова на анализаторе AU 2700 OLYMPUS (Япония).
При необходимости, для исключения негнойных осложнений стрептококковой инфекции (СИ) проводили рентгенологическое исследование суставов, ЭХО-кардиографию и, по показаниям, пациентов консультировали нефролог и ревматолог.
Все микробиологические исследования проводили на базе лабораторий кафедры микробиологии и вирусологии ГБОУ ВПО РНИМУ им. Н.И. Пирогова. Материал из ротоглотки забирали стерильным ватным тампоном, увлажненным стерильным физиологическим раствором, а также аспирацией стерильного физиологического раствора, который вводился посредством стерильной канюли тонзиллярного шприца для промывания лакун НМ непосредственно в полость тонзиллярных лакун. Сразу после взятия материала ватный тампон или физиологический раствор, полученный при аспирации из лакуны, погружали на транспортную среду для доставки материала в лабораторию. Время от забора материала до доставки в лабораторию составляло не более 40 мин, после чего производили предварительную инкубацию в термостате в течение 3 ч и рассеивали на плотные питательные среды с последующей инкубацией в течение 24—72 ч при температуре 37˚С. Далее выделяли собственно чистую культуру микроорганизмов на скошенном агаре и проводили идентификацию выделенных микроорганизмов с помощью систем API. Выделенные чистые культуры микроорганизмов исследовали на антибиотикочувствительность к различным антибактериальным препаратам диско-диффузионным методом со стандартными концентрациями на среде Mueller Hinton 2 («Becton Dickinson», США). Оценку результатов производили путем измерения диаметра зоны задержки роста вокруг диска.
Все серологические исследования проводили на базе лаборатории по изучению стрептококковых инфекций кафедры эпидемиологии и доказательной медицины ГБОУ ВПО Первый МГМУ им. И.М. Сеченова путем определения антител к нескольким группам антигенов: экстрацеллюлярным антигенам: О-стрептолизину (О-СЛ) и дезоксирибонуклеазе-В (ДНКаза-В), а также к оболочечному антигену клеточной стенки — группоспецифичному полисахариду, А (ПСХ-А) стрептококка методом иммуноферментного анализа.
Статистический анализ проводили при помощи программы, которая была разработана на кафедре медицинской кибернетики и информатики ГБОУ ВПО РНИМУ им. Н.И. Пирогова для персонального компьютера, производящей сравнение групп данных, сформированных пользователем, с использованием статистических непараметрических критериев, не зависящих от характера распределения — точного критерия Фишера и критерия χ2, на основании которых определяли достоверную значимость исследуемых клинических и лабораторных признаков Х.Т. Каждому выявленному признаку на основании его важности для дифференциации форм ХТ присваивали числовой коэффициент. С помощью математического анализа числовые коэффициенты были преобразованы в значимые диагностические критерии, по сумме которых в соответствии с разработанной шкалой мы предлагаем дифференцировать различные формы ХТ.
При детальном сборе анамнеза у пациентов 2-й группы с ХТ ТАФ I установлено, что у 9 (18%) пациентов имеется семейный анамнез по хроническому ГН, а у 14 (28%) больных — по ревматологическим заболеваниям (6, 12% — ревматоидный артрит; 8, 16% — последствия ОРЛ).
При лабораторном обследовании пациентов с ХТ, родственники которых страдают хроническим ГН, мы обнаружили признаки микрогематурии у 7 из 9 больных, что достоверно отличало этих пациентов от больных ХТ, родственники которых не страдали ГН (p=0,04). Однако ни один из этих пациентов никогда не отмечал изменения цвета мочи, отеков и повышения артериального давления.
Также у 4 из 6 больных, страдавших ХТ ТАФ I с семейным анамнезом по РА, мы выявили надпороговые значения (более 30 ед./л) уровня РФ, что достоверно отличало указанных пациентов по данному показателю от больных ХТ, родственники которых не страдали РА (p=0,04). Необходимо отметить, что ни один из этих пациентов не отмечал субъективного ощущения скованности и деформации мелких суставов.
При проведении серологического исследования у 8 пациентов 2-й группы с ХТ ТАФ I, родственники которых перенесли ОРЛ, нами отмечены достоверно более высокие уровни стрептококковых антител (табл. 1).
 Таблица 1. Показатели противострептококкового иммунитета у больных 2-й группы (n=50)
Таблица 1. Показатели противострептококкового иммунитета у больных 2-й группы (n=50)
Таким образом, мы рекомендуем врачам-оториноларингологам при наблюдении больных ХТ, родственники которых страдают аутоиммунными заболеваниями сердца, суставов и почек, для профилактики вышеуказанных заболеваний расценивать это состояние как II степень токсико-аллергических проявлений ХТ, вследствие чего необходимо выполнять раннюю хирургическую санацию очага хронической инфекции, персистирующей в НМ.
Следующим этапом исследования стало сравнение лабораторных (общеклинических и серологических) показателей у пациентов с различными формами ХТ.
По результатам проведенных лабораторных исследований обнаружены достоверно значимые различия между группами пациентов при оценке показателей мочи по уровню эритроцитов, белка и цилиндров. Так, ни один из вышеперечисленных показателей не встречался у пациентов с простой и ТАФ I формами Х.Т. Указанные данные свидетельствуют о локализованном характере течения инфекционного процесса в НМ без признаков выраженного воздействия на организм в целом.
Абсолютно иные результаты были получены нами у 9 (20,2%) больных 3-й группы, у которых были выявлены признаки гематурии, признаки протеинурии — у 4 (8,89%) и цилиндрурии — у 5 (12,1%). При этом при проведении статистического анализа значимости этих лабораторных находок было установлено, что данные показатели были достоверны при p=0,006; p=0,01 и p=0,04 соответственно. Таким образом, данные показатели могут являться одним из скрининговых факторов оценки иммунокомплексного поражения клубочкового аппарата почек и свидетельствуют о вовлечении почечной ткани в токсико-аллергические реакции, инициированные БГСА, персистирующим в НМ в условиях хронического воспаления. Всем указанным пациентам была выполнена тонзиллэктомия, после чего (через 3 мес) достигнута нормализация показателей общего анализа мочи.
Помимо этого нами выявлены достоверные различия между пациентами всех трех групп по уровню Р.Ф. Так, ни у одного пациента 1-й группы не было зафиксировано повышение уровня РФ более 30 ед./л (норма менее 30 ед./мл), при этом у 6 (11,3%) пациентов 2-й группы и у 15 (35,6%) больных 3-й группы мы определили надпороговый уровень РФ (при p=0,03 и p=0,00008 соответственно). Учитывая, что РФ по своей молекулярной структуре является Ig M к Fc-фрагменту структуры Ig G, повышение этого показателя, на наш взгляд, может являться признаком нарастания сенсибилизации организма в условиях сформировавшегося хронического тонзиллярного очага инфекции. Необходимо отметить, что нормализация данного показателя наступала через 6 мес после хирургического лечения и отмечена нами у всех прооперированных больных, что лишний раз доказывает значимость ТЭ как единственно эффективного способа, приводящего к санации очага хронической тонзиллярной инфекции и, соответственно, купированию аутоиммунных процессов, возникающих в макроорганизме на фоне данной патологии.
Параллельно с этим по мере нарастания степени выраженности токсико-аллергических проявлений отмечено повышение уровня скорости оседания эритроцитов (СОЭ) более 20 мм в час. Так, повышенный уровень СОЭ (норма менее 20 мм в ч) был выявлен у 3 (15%) пациентов 1-й группы, у 10 (20,8%) пациентов 2-й группы и у 27 (63,6%) больных 3-й группы (p=0,04; p=0,003 и p=0,00003 соответственно). Необходимо отметить, что СОЭ, являющийся показателем изменения соотношения белковых фракций сыворотки, опосредованно является критерием выраженности иммунокомлексного системного воспалительного процесса, в том числе и при осложненном течении ХТ.
Помимо этого были отмечены различия в длительности интервалов сердечного цикла при ЭКГ-исследовании у пациентов с различными формами Х.Т. По результатам статистической обработки данных длительность интервалов PQ (норма 0,12—0,2 с) и QRS (норма 0,08 с) у всех больных 1-й и 2-й групп находилась в пределах допустимых значений. Однако у 15 (36%) пациентов 3-й группы мы отметили удлинение интервала PQ более 0,2 с, что достоверно отличало пациентов данной группы от больных ХТ простой формы и ТАФ I (p=0,05). Кроме того, у 6 (14%) пациентов 3-й группы мы выявили расширение и деформацию комплекса QRS, что также достоверно отличало пациентов этой группы (p=0,03). Патологические находки, обнаруживаемые на ЭКГ у больных ХТ ТАФ II, могут свидетельствовать об аутоиммунном характере поражения сердца или отражать дистрофические изменения проводящей системы сердца — развитие кардиосклероза в сердечной мышце вследствие иммунокомплексного поражения стрептококковыми антителами.
По данным бактериологического исследования нами было установлено, что в этиологии ХТ преобладает Streptococcus pyogenes, причем частота его выделения увеличивалась по мере нарастания степени выраженности клинических проявлений токсико-аллергических реакций. Так, данный микроорганизм был высеян у 5 (27%), 18 (35%) и 24 (52%) пациентов в 1-й, 2-й и 3-й группах соответственно. При этом 15 (35%) пациентов 3-й группы составили лица молодого возраста. Кроме того, нами было выявлено увеличение удельного веса анаэробных патогенов (4% составили бактерии родов Bacteroides и 3% — Fusobacterium) у пациентов с ХТ ТАФ II, что является предрасполагающим фактором развития местных осложнений хронической тонзиллярной патологии вследствие способности этих микроорганизмов персистироват
