Дексаметазоновая проба и синдром кушинга
Главная
Библиотека
Заболевания гипофиза
Дифференциальная диагностика болезни Иценко-Кушинга
Дифференциальную диагностику болезни Иценко-Кушинга проводят с вторичным симптоматическим гиперкортицизмом. Гиперкортицивм, обусловленный первичной гиперфункцией надпочечников или гипоталамо-гипофизарной системы, и вторичный симптоматический гиперкортицизм можно отдифференцировать в амбулаторных условиях с помощью малых дексаметазоновых проб. Смысл проб заключается в том, что больные с первичным гиперкортицизмом не реагируют на малые дозы дексаметазона, а при его вторичных формах сохранение механизма обратной связи обеспечивает положительный ответ на дексаметазон.
Существует несколько вариантов малой дексаметазоновой пробы. При использовании в качестве гормонального критерия уровня кортизола в крови практикуется вариант с разовым приемом 1 мг дексаметазона.
Оценивают уровень кортизола в крови в 8 ч утра после предварительного приема дексаметазона в 23-24 ч, а также разницу в базальных уровнях гормона до и после проведения пробы. При отсутствии гиперкортицизма или вторичном его характере утреннее содержние кортизола в крови после приема дексаметазона не превышает 80-140 нмоль/л, а при болезни или синдроме Иценко-Кушинга остается или повышенным, или отмечаются пределы нормальных его колебаний. Некоторые клиницисты приравнивают диагностическую эффективность этой пробы к 100 %.
Если в качестве критерия диагностики гиперкортицизма используют содержание 17-ОКС в суточной моче, рекомендуется вариант пробы с применением 0,5 мг дексаметазона через каждых 6 ч в течение 2 суток. При отсутствии болезни или синдрома Иценко-Кушинга после приема дексаметазона суточная секреция 17-ОКС уменьшается до 11 мкмоль и ниже.
Наличие у больного симптоматики гиперкортицизма и повышение глюкокортикоидной активности надпочечников при отрицательной малой дексаметазоновой пробе дают основание считать гиперкортицизм первичным. В таких случаях проводят дифференциальную диагностику между болезнью Иценко-Кушинга и опухолью коркового вещества надпочечников (синдром Иценко-Кушинга). Клиническая картина этих заболеваний практически идентична. Для опухолей характерно быстрое развитие и меньший полиморфизм симптоматики, более выраженный гирсутизм и повышение экскреции 17-КС у женщин, а также наличие локальных признаков опухоли и общей интоксикации.
Для дифференциальной диагностики болезни и синдрома Иценко-Кушинга применяется ряд функциональных проб, основанных на особенностях нарушения механизма обратной связи при этих заболеваниях. Наибольшее распространение получила большая дексаметазоновая проба. При болезни Иценко-Кушинга ответная реакция на большие дозы дексаметазона у большинства больных сохранена (так как механизм обратной связи нарушен неполностью, сохранен его длительный, зависящий от уровня кортизола, компонент). В то же время большинство опухолей обладают автономностью секреции кортизола и не реагируют на дексаметазон. При проведении пробы назначают дексаметазон по 2 мг через 6 ч в течение 2 сут. Пробу оценивают по динамике суточной экскреции суммарных 17-ОКС и считают положительной при уменьшении содержания гормонов в моче на 40-45 %. Для болезни Иценко-Кушинга характерна положительная дексаметазоновая проба, для опухолей коркового вещества надпочечников — отрицательная.
Необходимо отметить, что этот тест не отличается абсолютной достоверностью. При тяжелых формах болезни Иценко-Кушинга с высоким уровнем кортизола в крови большая дексаметазоновая проба может быть отрицательной, а у 25-30 % больных с аденомами коркового вещества надпочечников — положительной. В целом значение этой пробы исключительно вспомогательное, окончательное установление диагноза на основании ее результатов недопустимо.
Информативным дифференциально-диагностическим критерием при гиперкортицизме является уровень кортикотропина в крови. При болезни Иценко-Кушинга базальное содержание кортикотропина в крови повышено или нормально, при опухолях коркового вещества надпочечников — снижено. Вместе с тем, оценивая кортикотропинемию при гиперкортицизме, следует помнить, что, помимо типичных вариантов болезни и синдрома Иценко-Кушинга, существуют первичная гиперплазия или аденоматоз надпочечников с низким или нормальным уровнем кортикотропина, кортикотропинзависимые аденомы надпочечников с нормальной или повышенной кортикотропинемией, кортикотропинпроду-цирующие опухоли внегипофизарной локализации (эктопический АКТГ-синдром) с выраженной гиперкортикотропинемией.
Окончательная идентификация клинической формы гиперкортицизма возможна только в условиях специализированной эндокринной клиники на основании визуализации надпочечников. В этом плане широкое распространение получила рентгенография надпочечников в условиях пневморетроперитонеума, с помощью которой правильный топографический диагноз можно установить у 75-80 % больных. В некоторых клиниках пневморетроперитонеографию дополняют внутривенной пиелографией. В затруднительных случаях при большой массе околопочечной жировой ткани, наличии аденом небольших размеров ценным диагностическим приемом является ангиография надпочечников с селективным забором крови на различных уровнях для исследования кортизолемии. В качестве первого этапа топографической диагностики может быть использовано ультразвуковое исследование надпочечников.
В течение последних лет с целью определения характера поражений надпочечников успешно применяются новые методы исследования — компьютерная томография и сцинтиграфия.
Лишь после безоговорочного установления диагноза можно обсудить вопрос о выборе метода и тактики лечения болезни Иценко-Кушинга.
А.Ефимов, Н.Скробонская, A.Чебан
«Дифференциальная диагностика болезни Иценко-Кушинга» — статья из раздела Заболевания гипофиза
Читайте также в этом разделе:
- Диагностика болезни Иценко-Кушинга
- Методы лечения болезни Иценко-Кушинга
- Вся информация по этому вопросу
Сегодня 24.05.2020
с 10:00 до 19:00 на звонки
отвечает врач.
Источник
Масимов Э.Н., к.б.н., ветеринарный врач ИВЦ МВА, г.Москва
Устойчивое длительное повышение уровня кортизола в крови, сопровождаемое нарушением ряда клинических функций называется синдромом Кушинга (гиперадренокортицизм). Гиперадренокортицизм ассоциирован с излишней продукцией или экзогенным введением глюкокортикоидов, и является одной из наиболее часто диагностируемой эндокринопатией у собак.
В гуманной медицине можно встретить такое понятие как «синдром Иценко-Кушинга», «болезнь Иценко-Кушинга». Эти два определения имеют довольно четкие различия. Так, например, болезнь Иценко-Кушинга, нейроэндокринное заболевание. Синдромом Иценко-Кушинга принято обозначать новообразование надпочечника, доброкачественного или злокачественного характера.
В ветеринарной медицине, как правило, таких строгих разграничений нет. Под термином «синдром Кушинга» принято подразумевать и новообразование надпочечника, так и новообразование гипофиза, так и ятрогенную форму заболевания.
Надпочечник, или адреналовая железа – парный инкреторный орган, который располагается у краниального конца почки, соединяясь с ней жировой тканью и кровеносными сосудами. В формировании надпочечников учувствуют мезодерма в виде межпочечной ткани, являющейся производным метамерно расположенных утолщений перитонеального эпителия, и супреренальной, или хромаффинной ткани, развивающейся из зачатков симпатических нервных узлов. Из-за срастания двух типов железистой ткани образуются две части надпочечника – кора и мозговое вещество, каждая из которых вырабатывает «свои гормоны». Кортикостероиды вырабатывает кора надпочечников, а норадреналин и адреналин – мозговое вещество. Из особенности строения у собак можно отметить его длину – 1-2см, удлиненно-овальную форму, а также характерный желтоватый оттенок1.
В основе гиперадренокортицизма собак лежат множественные патофизиологические нарушения, но все они сводятся к хроническому избытку кортизола в организме.
Патофизиологическая классификация причин синдрома Кушинга собак включает:
- Гипофизарные опухоли, продуцирующие и секретирующие избыточное количество АКТГ, сочетающееся с вторичной гиперплазией надпочечников.
- Ятрогенные факторы вследствие передозировки экзогенного АКТГ или избыточной терапии глюкокортикоидами.
- Первичный избыток кортизола, который автономно секретируется аденомой или карциномой надпочечников5.
У 80-85% собак со спонтанно развившимся синдромом Кушинга имеют гиперкортицизм, зависимый от гипофиза, т.е. избыточную секрецию АКТГ гипофизом, которая вызывает двустороннюю гиперплазию коры надпочечников и повышенную концентрацию глюкокортикоидов в плазме крови. Почти у всех собак с гипофизарным гиперадренокортицизмом имеется гипофизарная аденома, чаще всего локализованная в передней доле.
Первичные опухоли коры надпочеников, как аденомы, так и карциномы, по-видимому, развиваются автономно5. Процессы, приводящие к образованию опухолей коры надпочечников, изучены недостаточно. Секреция кортизола в данных случаях носит неупорядоченный, эпизодический характер.
Стоит также отметить, что двусторонние опухоли коры надпочечников и по литературным данным, и по личному наблюдению автора, встречаются у собак редко. В исследовании Hoerauf, Reusch в 1999г у 15 исследованных собак с синдромом Кушинга, который был вызван активными опухолями коры надпочечников, у трех собак опухоли имелись в обоих железах.
Гиперадренокортицизм встречается у собак среднего или старого возраста, с возрастным диапазоном от 2 до 16 лет и средним возрастом 7-9 лет. По данным ряда авторов, патология надпочечникового происхождения встречается у более пожилых собак, чей средний возраст 11-12 лет. Породной предрасположенности нет. Из практики автора чаще всего данное заболевание диагностируется у собак пород такса, пинчер, пудель. Половая предрасположенность также отсутствует.

Рис.1 Собака пинчер, 7 лет, сука, новообразование надпочечника.
Клинические признаки гиперадренокортицизма весьма разнообразны. Самый частый симптомокомплекс это полиурия/полидипсия. Полидипсия – состояние, когда потребление воды свыше 100 мл/кг веса тела в течения дня, и полиурия, определяемая как продукция мочи свыше 50 мл/кг веса тела в течение дня, наблюдаются в большинстве случаев гиперадренокортицизма.
Далее, из симптомов, можно выделить полифагию, отвисший живот, алопеции, медленный рост шерсти, мышечная атрофия, одышка, у сук встречается анэструс, неврологические симптомы.
Также одним из «показательных» симптомов являются именно дерматологические признаки заболевания. Кожа, особенно на вентральной стороне живота, истончается и теряет эластичность. Вены живота выступают и легко заметны через тонкую кожу. Имеется повышенное образование поверхностных чешуек, и наблюдаются комедоны, вызванные закупоркой фолликулов, особенно вокруг молочных желез3.
Избыточное выделение кортизола негативно влияет на один из циклов роста волоса – анаген. Происходит истончение шерстного покрова, приводящее к билатеральной симметричной алопеции. Голова, лапы и хвост обычно поражаются последними.
Гиперадренокортицизм начинается незаметно для владельцев собаки и медленно прогрессирует в течение месяцев.
На текущее время диагностика синдрома Кушинга разнообразна. Для постановки диагноза можно использовать различные лабораторные методы, визуальную диагностику, а также проводить диагностические тесты.
Ультразвуковая диагностика применима только в случае дифференциации ГАК надпочечникового происхождения от патологии гипофиза.
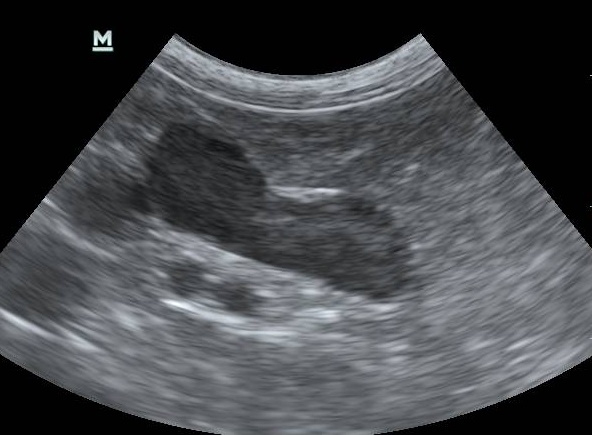
Рис.2 Патологический надпочечник.
Особое внимание стоит уделить гематологическим и биохимическим исследованиям крови. У собак, с предварительным диагнозом ГАК можно выделить следующие особенности лабораторных исследований.
Клинический анализ крови: нейтрофилия, лейкоцитоз, лимфопения, эозинопения. В биохимическом исследовании наблюдается повышение уровня триглицеридов и холестерина, снижение уровня мочевины, повышение щелочной фосфатазы.
Стоит уделить внимание и анализу мочи, в результатах которого отмечается снижение удельного веса.

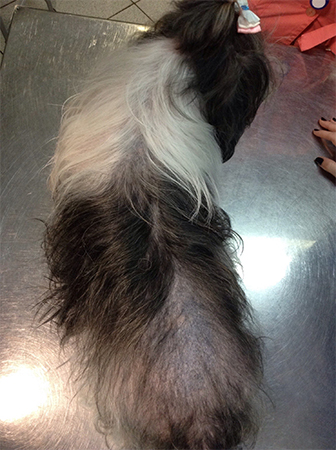
Рис.3 Собака шитцу, 9 лет, гипофизарная форма ГАК.
Редко проводимое исследование при подозрении на ГАК – радиография. При данном исследовании отмечают признаки остеопороза, минерализации надпочечников. Адреномегалия является крайне редкой находкой при рентгенографии брюшной полости, все же большое увеличение предполагает, но не диагностирует, наличие карциномы надпочечников.
Компьютерная томография – дорогостоящий вид исследования, в последнее время все чаще применяемый для визуализации новообразования гипофиза, опухолей надпочечников, гиперплазии надпочечников.
Диагностические тесты, применяемые в практике, являются подтверждением или полным опровержением диагноза. Скрининг-тесты – АКТГ-стимулирующий тест, а также проба с низкими уровнями дексаметазона. В арсенале ветеринарного врача также имеется тест на соотношение кортизол/креатинин в моче. У всех исследований есть и свои преимущества, и свои недостатки.
Из личного опыта автора, соотношение кортизол/креатинин в моче, не является тестом, на который можно полагаться при постановке окончательного диагноза. Данный тест используется в практике крайне редко. Данное соотношение является идеальным для исключения гиперадренокортицизма (если результат в норме), но не подтверждает наличие заболевания. В данном случае моча должна быть собрана дома, утром, при спонтанном мочеиспускании, без стресса. Чувствительность данного теста приближается к 98%3.
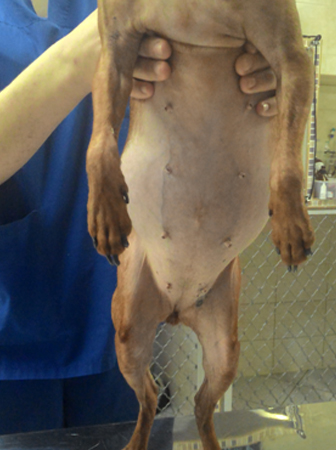
Рис.4 Собака пинчер, 7 лет, сука, новообразование надпочечника.
Дексаметазоновая проба (проба с низкими уровнями дексаметазона) – у пациента собирают около 3 мл плазмы или сыворотки для определения концентрации кортизола; далее, вводят внутривенно дексаметазон из расчета 0,01мг/кг; далее, собирают вторую пробу для определения концентрации кортизола через 3-4 часа и третью пробу через 8 часов после введения дексаметазона.
Супрессивная проба низкими дозами дексаметазона не подходит для определения ятрогенного гиперадренокортицизма. Также она довольно длительна по продолжительности – 8 часов. Тем не менее, она более надежна для подтверждения гиперадренокортицизма, так как позволяет диагностировать у собак все случаи гиперадренокортицизма надпочечникового происхождения и в 90-95 % случаях гипофизарный гиперадренокортицизм. Концентрация кортизола более 40 нмоль/л через 8 часов предполагает подтверждение диагноза гиперадренокортицизм.
Стимулирующая проба с АКТГ является лучшим выбором для дифференциации спонтанного и ятрогенного гиперадренокортицизма. Проба с АКТГ является незаменимой для мониторинга лечения синдрома Кушинга.
Техника проведения данного теста: Взятие пробы крови для определения базального уровня кортизола. Далее, введение 0,25 мг синтетического АКТГ внутривенно или внутримышечно. Собакам весом менее 5кг – 0,125мг. Взятие второго образца крови через 30-60 мин после введения АКТГ внутривенно и 60-90 мин, — после внутримышечного введения. Результаты теста считаются позитивными, если после стимуляции АКТГ уровень кортизола вырос> 600 нмоль/л у собак с характерными клиническими признаками. Уровень кортизола <450нмоль/л после стимуляции считается нормой для животного, у которого нет гиперадренокортицизма.
Лечение синдрома Кушинга (ГАК) имеет несколько вариантов в зависимости от причины заболевания – это хирургический метод, или медикаментозный.
В случае, если ГАК является ятрогенным, то животному осторожно уменьшают дозу, а затем прекращают терапию глюкокортикоидами3.
Хирургическое лечение применимо в случае с гиперадренокортицизмом надпочечникового происхождения имеет лучший прогноз, если опухоль может быть полностью удалена хирургическим путем. Односторонняя адреналэктомия требует большого опыта и экспертной оценки, из-за сложной анатомии. Техника хорошо описана с использованием паракостального, бокового доступа. Во время проведения операции и после нее требуется дополнительное введение глюкокортикоидов и минералокортикоидов, так как кора противоположного надпочечника будет атрофирована и не способна адекватно отвечать на стресс.
Хирургическое лечение применимо и в случае с гипофизарным происхождением ГАК. Но хирургическое вмешательство, в данном случае, технически сложная и ассоциирована с высокой заболеваемостью и смертностью. Частыми осложнениями являются кровотечение и неполная визуализация и удаление большего поражения. Может развиться транзиторный несахарный диабет.
Медикаментозное лечение применяется довольно широко. Даже несмотря на официальную недоступность на территории России таких препаратов как Трилостан или Митотан, их применение является по сути единственным лечением ГАК.
Назначение в виде лечения препаратов с содержанием кетоконазола или L-дипренила является малоэффективным и практически не используется. Альтернативная терапия имеет или минимальный эффект, либо эффект отсутствует вовсе. Мелатонин, метапирон, бромокриптин – все эти препараты не имеют доказанной эффективности при лечении ГАК2.
Препаратом выбора, на взгляд автора, является Трилостан («Веторил»). Трилостан — обратимый конкурентный ингибитор 3β- гидроксистероиддегидрогеназы, блокирующий синтез стероидов в надпочечниках. Дозировки, применяемые для животных – от 2,5 до 5мг/кг, 1 раз в день. Контроль лечения: первая проба с АКТГ – через 7-14 дней лечения, тест проводится через 4-6 часов после дачи препарата. Целью является уровень кортизола 50-120 (250) нмоль/л. Контроль лечения: первая проба с АКТГ – через 7-14 дней лечения, тест проводится через 4-6 часов после дачи препарата. Целью является уровень кортизола 50-120 (250) нмоль/л7.
Митотан эффективный и относительно безопасный препарат для применения у собак с гиперадренокортицизмом надпочечникового происхождения. Однако собаки с опухолью надпочечников склонны быть более устойчивыми к митотану, чем собаки с гипофизарным гиперадренокортицизмом. Митотан назначают внутрь в дозе 50 мг/кг/день. Его следует давать вместе с кормом, так как это жирорастворимый препарат. Лечение митотаном относительно безопасно, а побочные эффекты, которые возникают наиболее часто, например, анорексия, рвота или диарея, редко серьезны, при условии, что их рано заметили, так что лечение митотаном может быть приостановлено.
Подводя итог данному обзору, можно отметить широкие возможности диагностики синдрома Кушинга, а также распространенные методы лечения данного заболевания. Продолжительность жизни собаки с ГАК, в среднем, 30 месяцев. Так, например, пациент бостон-терьер «Тема», являющийся пациентом автора, на текущий момент имеет продолжительность жизни после постановки диагноза 18 месяцев.
Также необходимо отметить факт, что в 80-85% случаев диагностируется гипофизарный гиперадренокортицизм.
Список литературы:
- Акаевский А.И., Юдичев Ю.Ф., Селезнев С.Б., «Анатомия домашних животных», 5-е издание, Москва, 2005, Аквариум
- Small animal dermatology 2nd ed, Karen Helton Rhodes, Alexander H.Werner, 2011, Blackwell
- Материалы II международного ветеринарного дерматологического симпозиума, 2013г., Спб
- Руководство по эндокринологии мелких домашних животных, под редакцией Эндрю Дж. Торранс и Кармел Т. Муни, 1998, Аквариум
- Эндокринология и репродукция собак и кошек, Э.Фелдмен, Р.Нельсон., 2008, Софион
- Canine and Feline Endocrinology, Mooney C. T., Peterson M. E., BSAVA, 2004
- Игнатенко Н.А., «Гиперадренокортицизм: диагностика и лечение у собак», журнал Vetpharma №6-2012, Москва
Вернуться к списку
Источник
